Что значит повышает абсорбцию
Что значит повышает абсорбцию
Путь введения может ограничить доступ лекарства в системный кровоток. Как было указано ранее, поступление лекарственного вещества в кровоток зависит от пути введения. Например:
• лекарство в форме глазных капель действует в основном местно, хотя могут возникать и системные эффекты, вызванные веществом, абсорбированным через слезные протоки;
• пенициллин G нестабилен в кислой среде желудка, и при пероральном приеме необходимы большие дозы, чтобы компенсировать разрушение антибиотика в желудке;
• нитроглицерин принимают сублингвально, чтобы обеспечить быструю системную абсорбцию и избежать предсистемной элиминации в печени при пероральном приеме.
Скорость абсорбции лекарства при пероральном приеме может зависеть от скорости опорожнения желудка. Скорость абсорбции из ЖКТ может быть замедлена вследствие задержки кислого лекарства в желудке или повышена в результате быстрого перехода основного лекарства в тонкую кишку. Так, стакан воды, выпитой вместе с приемом лекарства на пустой желудок, ускоряет опорожнение желудка и переход лекарства в верхний отдел кишечника с более высоким рН и значительно большей площадью абсорбирующей поверхности. Опорожнение желудка можно ускорить фармакологически. Метоклопрамид повышает сократительную активность желудка и ускоряет его опорожнение. Наоборот, жирная пища, кислые напитки или лекарства с антихолинергическим действием замедляют опорожнение желудка.
Распределение лекарств в организме
Лекарственное вещество, поступающее в системный кровоток, распределяется по различным частям тела со скоростью, которая зависит от ряда факторов, включая метаболизм, экскрецию и перераспределение в организме. Чтобы попасть в ткани, лекарство должно покинуть кровоток. Как было указано ранее, большинство лекарственных веществ имеет небольшую молекулярную массу, вследствие чего они легко покидают кровоток при фильтрации через стенку капилляров. Однако скорость фильтрации может изменяться в зависимости от степени связывания лекарства с белками плазмы, такими как альбумин и альфа-кислый гликопротеин.
Ожирение может влиять на распределение лекарства. Независимо от пути введения лекарственный препарат достигает тканей со скоростью, прямо пропорциональной кровотоку. В состоянии покоя кровоснабжение жировой и мышечной ткани (в мл/кг/мин) сходно. При физической нагрузке кровоток в мышцах резко возрастает. В зависимости от растворимости в липидах лекарства накапливаются в жировой и мышечной тканях в различном количестве и с разной скоростью. Таким образом, различия в соотношении между жировой и мышечной тканями у тучных и худощавых людей при одинаковой массе тела могут осложнить подбор точной дозы некоторых лекарств, если учитывать только общую массу, поскольку указанное соотношение может повлиять на уровень лекарства в плазме.
Концентрация свободного лекарства в жидкости различных компартментов организма зависит от рКа лекарства и рН жидкости. В основу расчета концентрации лекарства в тканях при состоянии равновесия положен принцип, согласно которому концентрация свободных неионизированных молекул одинакова по обе стороны клеточной мембраны. На рисунке изображено распределение между двумя биологическими средами кислого лекарства (напроксен) и основного лекарства (морфин) при состоянии равновесия. Видно, что:
• кислые лекарства концентрируются в плазме крови;
• основные лекарства концентрируются в тканях.
Следует отметить, что эти примеры относятся только к несвязанной фракции лекарств, растворенных в специфической биологической жидкости или ткани, и представлены в крайне упрощенном виде, особенно при сравнении с организмом как единым целым в условиях отсутствия равновесия.
Биодоступность железа и влияние ионов кальция на ее эффективность
Содержание железа в организме человека составляет в среднем 4,2 г. Около 75% от его общего количества входит в состав гемоглобина эритроцитов, которые переносят кислород от легких к тканям
Содержание железа в организме человека составляет в среднем 4,2 г. Около 75% от его общего количества входит в состав гемоглобина эритроцитов, которые переносят кислород от легких к тканям, 20% железа является резервным (костный мозг, печень, макрофаги), 4% входит в состав миоглобина, около 1% содержится в дыхательных ферментах, катализирующих процессы дыхания в клетках и тканях, а также в других ферментативных структурах. Железо осуществляет свою биологическую функцию, находясь в составе биологически активных соединений, преимущественно ферментов. Железосодержащие ферменты выполняют следующие основные функции:
Железо обладает несколькими особыми свойствами, которые отличают его от других биологически активных ионов и веществ.
В организме человека нет никаких специальных механизмов для выведения железа. В основном железо выделяется через кожу и кишечник (I. Guinote et al., 2006). Кроме этого, оно теряется также с волосами, ногтями, мочой и потом. Общее количество выделяемого железа у здорового человека (мужчины) составляет около 1 мг в сутки. Такое же количество в норме усваивается из потребляемой пищи (Linder, 1991). Отличие составляет менструальный период, когда потребление должно составлять около 4 мг железа в день. Таким образом, концентрация элемента в сыворотке крови зависит от его всасывания в желудочно-кишечном тракте, от накопления в селезенке, костном мозге и скелетных мышцах (миоглобин), а также от синтеза и распада гемоглобина и выделения его из организма. В пище железо может присутствовать в двух видах — гемовое и негемовое, которые характеризуются разными механизмами всасывания. Гемовое железо (порфириновое кольцо с атомом железа в центре, связанное с 4 атомами азота) в желудочно-кишечном тракте освобождается от белковых цепей и в виде металлопорфирина всасывается энтероцитами кишечника. Там происходит неспецифическое эндосомальное проникновение гема в клетку с последующим его разрушением. Далее, с помощью белковой транспортной системы IREG1, ионы железа окисляются до трехвалентного железа, связываются с трансферрином и покидают энтероцит, выходя в ток крови (Linder et al., 2006). В плазме крови железо перемещается в соединении с этим же белком, который выполняет как функцию депо, так и функцию переносчика. Наличие свободных ионов железа в крови не характерно и является патологией. Всасывание гемового железа происходит в пределах 15–50% (в среднем 20–30%).
В литературе описывается несколько механизмов транспортировки железа внутри энтероцита, основанные главным образом на экспериментах, проведенных на культуре ткани Caco2 (M. Linder et al., 2006). Согласно первой теории, двухвалентное железо, поступившее в энтероцит с помощью транспортера DMT1, доставляется посредством везикул с трансферрином (некоторые отводят ему роль внутриклеточного рецептора) или в свободном состоянии к базолатеральной мембране энтероцита, где присутствует другой транспортер — IREGI/ferroportin/MTP1 (Donovan et al., 2000). Этот транспортер окисляет двухвалентное железо до трехвалентного и транспортирует в кровь, где он соединяется с плазменным трансферрином. Согласно второй теории, внутри энтероцита железо транспортируется, по-видимому, в везикулах вместе с апотрансферрином, который путем эндоцитоза попадает из тока крови в энтероцит (эндо-/экзоцитоз) (Ma et al., 2002). Во время этой транспортировки двухвалентное железо окисляется до трехвалентного и путем экзоцитоза поступает через базилярную мембрану энтероцита в кровь. В этом процессе возможно участие уже упоминавшейся системы IREG. Согласно литературным данным, именно механизм транспорта железа через базолатеральную мембрану энтероцита в кровь является лимитирующим в процессе адсорбции железа (Roy and Enns, 2000). Усвоение неорганического двухвалентного железа обычно происходит в пределах 6–15%.
Негемовое трехвалентное железо может быть восстановлено с помощью ферриредуктазы до двухвалентного железа и усвоено с помощью DMT1. Восстановление трехвалентного железа сильно зависит от кислотности желудочного сока. Невосстановленное железо может всасываться с помощью специфической интегрин-мобифериновой системы IMP. Усвоение трехвалентного железа происходит наименее полно и редко превосходит 4%.
Количество железа, поступающего в эффекторную клетку, куда оно транспортируется с кровью, прямо пропорционально числу мембранных рецепторов. В клетке происходит высвобождение железа из трансферрина. Затем плазменный апотрансферрин возвращается в циркуляцию. Повышение потребности клеток в железе при их быстром росте или синтезе гемоглобина ведет к индукции биосинтеза рецепторов трансферрина и, напротив, при повышении запасов железа в клетке число рецепторов на ее поверхности снижается. Железо, высвободившееся из трансферрина внутри клетки, связывается с ферритином, который доставляет микроэлемент в митохондрии, где он включается в состав гема. Помимо синтеза гема, двухвалентное железо используется в митохондриях для синтеза железосерных центров. В организме человека происходит постоянное перераспределение железа. В количественном отношении наибольшее значение имеет метаболический цикл: плазма — красный костный мозг — эритроциты — плазма. Обычно 70% плазменного железа поступает в костный мозг. За счет распада гемоглобина в сутки высвобождается около 21–24 мг железа, что во много раз превышает поступление железа из пищеварительного тракта (1–2 мг/сут).
Существует выраженная обратная зависимость между обеспеченностью организма железом и его всасыванием в пищеварительном тракте. В основном всасывание железа происходит в двенадцатиперстной кишке и проксимальных отделах тощей кишки и отсутствует в подвздошной кишке.
Всасывание железа зависит от следующих причин: возраста, обеспеченности организма железом, состояния желудочно-кишечного тракта, количества и химических форм поступающего железа и прочих компонентов пищи. Для оптимального всасывания железа необходима нормальная секреция желудочного сока. Прием соляной кислоты способствует усвоению железа при ахлоргидрии. В таблице приведены основные вещества, содержащиеся в продуктах питания человека, которые могут активизировать или уменьшать всасывание железа, содержащегося в этих продуктах или мультивитаминной таблетке. Аскорбиновая кислота, восстанавливающая железо и образующая с ним хелатные комплексы, повышает доступность этого элемента так же, как и другие органические кислоты. Она является одним из наиболее сильных стимуляторов всасывания железа. Другим компонентом пищи, повышающим всасывание железа, является «фактор животного белка», в котором содержится миоглобин и гемоглобин. Улучшают всасывание железа простые углеводы: лактоза, фруктоза, сорбит, а также такие аминокислоты, как гистидин, лизин, цистеин, образующие с железом легковсасываемые хелаты.
Самыми сильными ингибиторами, блокирующими всасывание железа, являются фитаты и полифенолы. Фитаты представляют собой форму хранения фосфатов и минералов, присутствующих в зернах злаковых растений, овощах, семенах и орехах. Они активно тормозят всасывание железа, действуя при этом в прямой зависимости от дозы. Всасывание железа снижают такие напитки, как чай, содержащий таннин, а также другие полифенольные соединения, которые прочно связывают этот элемент. Феноловые соединения существуют почти во всех растениях и являются частью системы защиты против насекомых и животных. Поэтому чай применяют для профилактики повышенного усвоения железа у больных талассемией. Большое влияние на усвоение железа оказывают различные заболевания. Оно усиливается при недостаточности железа, при анемиях (гемолитической, апластической, пернициозной), гиповитаминозе В6 и гемохроматозе, что объясняется повышением эритропоэза, истощением запасов железа и гипоксией.
Из перечисленных веществ, которые могут уменьшать всасывание железа, особое внимание обращает на себя ион кальция. Кальций обладает высокой биологической активностью, в значительном количестве содержится в основных продуктах питания и, как правило, присутствует в одной мультивитаминной таблетке с железом.
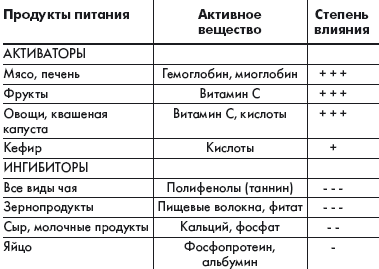 |
| Таблица. Активаторы и ингибиторы всасывания железа, содержащиеся в пищевом рационе человека |
В связи с этим вопрос о возможном влиянии кальция на биодоступность железа изучается длительное время как в экспериментах на животных, так и в исследованиях на людях.
Необходимо отметить, что клеточные механизмы всасывания, т. е. поступления ионов железа и кальция из просвета кишечника в ток крови через энтероциты кишечника, различны. Многочисленными работами было показано, что в этом процессе участвуют различные клеточные транспортеры (J. Hoenderop et al., 2005). Кроме того, имеются данные о том, что кальций уменьшает поступление в организм как гемового (L. Hallberg, 1991), так и негемового железа. Все вместе указывает на то, что кальций может влиять на биодоступность железа, оказывая ингибирующее влияние либо на транспорт его в желудочно-кишечном тракте, либо на связывание с рецепторами, расположенными на апикальной мембране энтероцитов.
В экспериментах на изолированный кишечной петле в условиях in vivo на крысах было показано уменьшение всасывания железа из раствора FeCl2, вводимого непосредственно в петлю при добавлении кальция. Причем эффект зависел от абсолютной концентрации кальция в двенадцатиперстной кишке, а не от молярного соотношения Ca/Fe (Barton et al., 1983). Изучение влияния на клеточный транспорт железа различных солей, содержащих кальций, показало, что наибольший ингибирующий эффект вызывает СаСО3, в то время как эффекты СаSO4 и Na2CO3 присутствуют, но в меньшей степени (Prather, 1992). Эта кальциевая соль, добавленная в количестве 500 мг, способна уменьшить всасывание негемового железа, содержащегося в пищевых продуктах на 32% в случае потребления пищи, не содержащей дополнительные ингибирующие вещества, и на 42% при потреблении продуктов в сочетании с яйцами, кофе и др. (Сook et al., 1991). СaCO3 уменьшает также всасывание железа при совместном использовании их в одной таблетке. В этом случае 300 мг кальциевой соли при совместном употреблении с 37 мг железа, присутствующего в виде FeSO4, уменьшает всасывание железа на 15% (Seligman et al., 1983; Cook et al., 1991).
930 мг кальция в день). Это привело к снижению абсорбции железа на 30–50% (Hallberg, 1995). На основании полученных данных авторы предполагают, что ингибирование всасывания железа происходит на этапе «просвет кишечника — энтероцит».
В исследованиях на людях также изучалось влияние искусственных минеральных добавок: сульфата железа, цитрата и фосфата кальция и др. Работа была проведена на 61 здоровом испытуемом. Для оценки всасывания использовался также двойной радиоизотопный метод. При употреблении цитрата кальция (600 мг) абсорбция железа снижалась на 49%, фосфата — на 62% (Cook et al., 1991). Интересно, что в этом исследовании эффект от применения кальциевых добавок отмечался только на фоне употребления пищи. Вероятно, конкуренция между катионами возникала при заполненном кишечнике. Теоретически возможно, что высокие концентрации кальция могут изменять реологические свойства пищевого комка в просвете верхней части тонкого кишечника (Conrad et al., 1993). На людях также изучалось различие во влиянии кальция на потребление гемового и негемового железа. Так, в исследованиях на 27 добровольцах с применением полного промывания кишечника для измерения степени усвоения железа при использовании кальциевых добавок (450 мг) было показано снижение абсорбции только гемового железа на 20%. В этой работе добавление кальция не влияло на абсорбцию негемового железа (Z. K. Roughead, 2005). В другом исследовании, проведенном на 44 мужчинах и 81 женщине, наблюдали снижение всасывания гемового железа из рациона при добавлении кальция в дозах от 40 до 300 мг. Максимальное снижение наблюдалось при дозе 300 мг и составило 74%. Дальнейшее увеличение содержания кальция до 600 мг не приводило к возрастанию ингибирования иона железа (L. Hallberg et al., 1991). Противоречивые результаты, получаемые в разных работах, связаны, по-видимому, со сложностью воспроизведения точности методических подходов, проводимых на людях.
Во всех приведенных выше исследованиях было показано в той или иной мере уменьшение абсорбции железа в желудочно-кишечном тракте на 20–60% при совместном употреблении с кальцийсодержащими продуктами в ходе однократного приема пищи или таблетированных препаратов. Характерно, что использованные дозы кальция не превышали дневную норму взрослого человека (во всех описанных случаях суммарное поступление кальция за сутки было меньше 1000 мг). Однако непосредственный механизм антагонистического влияния кальция на всасывание железа остается неясным.
Серия исследований, проведенных на добровольцах при длительном совместном приеме пищи, содержащей определенное количество железа и кальция, не позволила получить однозначного ответа о влиянии иона кальция на биодоступность железа, а главное — на уровень гемоглобина у этих испытуемых. Часто эффект выявлялся (ингибирование составляет 19%), но был статистически недостоверен (Reddy et al., 1997). По-видимому, длительные исследования на людях осложняются контролем над соблюдением диеты и составлением диеты для контрольной группы (S. R. Lynch, 2000).
Анализ литературы позволяет заключить, что экспериментальные исследования на животных и работы, проведенные на испытуемых, подтвердили, что ионы кальция способны уменьшать уровень всасывания железа. Степень выявления эффекта зависела от используемых методических подходов, которые в разных работах отличались друг от друга, и это затрудняет интерпретацию результатов. Однако возможность таких взаимодействий может быть наиболее актуальна и должна безусловно учитываться для людей, страдающих железодефицитными состояниями (анемии) или входящих в группу риска по этому состоянию (дети, беременные и т. д.). Для лечения и профилактики таких состояний необходимо увеличить потребление железа, как за счет соблюдения соответствующей диеты, так и с помощью минеральных добавок. Но следует помнить, что эффективность этих мер может значительно снижаться на фоне потребления диетического кальция или кальцийсодержащих витаминных комплексов. Ограничивать потребление кальция не желательно, поскольку во многих случаях (беременность, возраст 12–18 лет) существует повышенная потребность в обоих элементах. Выходом из ситуации может служить раздельное применение кальция и железа. Экспериментальные данные показали, что интервал между приемом кальция и железа даже в 4 ч исключает эффект ингибирования (A. Gleeprup et al., 1993). Помимо этого, во время приема препарата железа стоит воздержаться от употребления любых продуктов, содержащих кальций, т. е. требуется исключить весь спектр молочной продукции, а также зеленые части растений.
В данном случае удобно применять витаминно-минеральные комплексы, которые заранее предусматривают раздельное употребление железа и кальция. И это не единственное сочетание жизненно важных микронутриентов, проявляющих антагонистические свойства. Таким образом, грамотное разделение компонентов витаминно-минеральных комплексов по времени приема является необходимым условием эффективности их применения.
Литература
Н. А. Медведева, доктор биологических наук, профессор
МГУ, Москва
Особенности минерального обмена
Минеральные вещества наряду с белками, жирами, углеводами и витаминами являются жизненно важными компонентами пищи человека, необходимыми для построения структур живых тканей и осуществления биохимических и физиологических процессов, лежащих в основе жизнедеятельности организма. В данной статье речь пойдет о макроэлементах — кальции, фосфоре, магнии, их метаболизме в организме человека, биологической роли, клинических признаках их недостаточности, основных пищевых источниках, а также способах коррекции нарушений минерального обмена. Важно помнить, что содержание минеральных веществ в плазме крови не всегда коррелирует с их запасами в организме, поэтому выявить дефицит минеральных компонентов можно лишь с учетом клинической картины.
КАЛЬЦИЙ
Строительный материал
Роль кальция как структурного материала известна в течение столетий. Доисторический человек тоже страдал от остеопороза. Несмотря на прогресс, достигнутый в изучении этого заболевания, все еще требует уточнения роль потребления кальция как причинного, профилактического и лечебного фактора.
Кроме структурной функции кальций влияет на проницаемость клеточных мембран, действуя как вторичный мессенджер, инициируя ответы клеток на различные стимулы. Перемещение кальция из внутриклеточного пространства во внеклеточную среду обеспечивает такие события, как дифференцировка клетки, сокращение, секреция и перистальтика. Множество ферментов, включая те, что участвуют в системе свертывания крови, зависят от кальция. Он влияет на функцию эндокринных желез (особенно паращитовидных), оказывает противовоспалительное и десенсибилизирующее действие, находится в биологическом антагонизме с ионами натрия и калия.
Хранилище кальция
Приблизительно из 800 мг кальция, потребляемых ежедневно, 25–50 % абсорбируются и поступают в обновляемый кальциевый пул. Этот пул состоит из небольшого количества кальция в биологических жидкостях и составляет 1 % от общего количества кальция в организме. Остальные 99 % кальция находятся в костях и зубах.
У взрослого человека внеклеточный пул кальция обновляется 20–30 раз в сутки, тогда как кость обновляет его каждые 5–6 лет. Почки фильтруют приблизительно 8,6 г/сут, почти все количество его повторно абсорбируется и лишь от 100 до 200 мг экскретируется с мочой. Всасывание кальция кишечником, реабсорбция почкой и обновление в кости непосредственно регулируется гормоном паращитовидной железы, кальцитонином и витамином D. Уровень кальция сыворотки тщательно регулируется (составляет около 2,5 ммоль/л), чтобы сохранить внеклеточную концентрацию кальция и, таким образом, обеспечить нормальную нейромышечную и гормональную функцию.
Условия всасываемости кальция
Абсорбция кальция зависит от его взаимодействия с другими компонентами пищи и таких факторов, как действие кальций-регулирующих гормонов и физиологическое состояние организма.
Растворимость солей кальция увеличивается в кислой среде желудка, но растворенные ионы до некоторой степени повторно связываются и преципитируются в тощей и подвздошной кишке, где pH ближе к нейтральному. В желудочно-кишечном трактате компоненты пищи, такие как глюкоза, жирные кислоты, фосфор и оксалаты, связываются с кальцием, образуя комплексы. Желудочная кислотность оказывает небольшой эффект на абсорбционную способность кальция, применяемого с пищей.
Вообще всасывание кальциевых добавок, особенно менее растворимых, улучшается, если они принимаются вместе с пищей. Возможно, это происходит потому, что пища стимулирует желудочную секрецию и моторику и пищевые источники кальция становятся более измельченными и растворимыми.
Абсорбция кальция
Есть два пути всасывания кальция в кишечнике. Один — активный, трансцеллюлярный процесс, который происходит главным образом в дуоденуме и проксимальном отделе тощей кишки. Он регулируется витамином D. На активное всасывание кальция воздействует физиологическое состояние организма (в т. ч. беременность и кормление грудью), гиповитаминоз D, возраст. Другой путь всасывания кальция — пассивный — независим от витамина D и происходит на всем протяжении тонкой кишки. В этом случае количество абсорбируемого кальция зависит от его содержания в рационе.
Большая часть абсорбции кальция происходит в подвздошной кишке, где пища остается на наиболее длительный период. Приблизительно 4 % кальция (8 мг/сут) всасывается в толстой кишке.
Поскольку основная часть кальция организма находится в кости, скелет — главное депо кальция. Вначале отрицательный баланс кальция приводит к безопасной мобилизации его из кости. В дальнейшем хроническое истощение скелетного кальция приводит к неблагоприятным эффектам.
Сколько в граммах?
Организм новорожденного содержит 30 г кальция, который увеличивается к периоду взрослой жизни к 1000–1200 г. Чтобы накопить это количество, ежедневно в течение детства от рациона должно оставаться приблизительно от 100 до 150 мг кальция. Пик достигается к половой зрелости: 200 мг для женщин и 280 мг для мужчин. Затем происходит снижение до 10–30 мг/сут (в период зрелости). Способность удерживать определенный уровень кальция теряется (становится отрицательной) у женщин после менопаузы и у мужчин к 65-летнему возрасту. Баланс кальция положителен во время беременности и отрицателен в период кормления грудью.
Имеются данные, что остеопороз является следствием повышения экскреции кальция с мочой при сниженной абсорбции. Кроме того, вторичный гиперпаратиреоидизм ведет к увеличенному обмену веществ в кости и возрастной потере костной массы.
Существуют дискуссии относительно того, увеличивается ли потребность кальция при старении.
Причины потери кальция
Хотя паратгормон, кальцитонин, и витамин D — основные кальций- регулирующие гормоны, другие гормоны также влияют на обмен веществ кости и метаболизм кальция. Это глюкокортикоиды, гормоны щитовидной железы, гормон роста, инсулин и эстрогены.
Избыток глюкокортикостероидов (ГКС) (при болезни Кушинга или когда они используются в терапии) приводит к потере кости, особенно трабекулярной, приводя к остеопорозу. Главный эффект ГКС — подавление остеобластной деятельности, хотя функцию остеокластов они также нарушают. ГКС также мешают транспорту кальция через энтероциты.
Гормоны щитовидной железы стимулируют резорбцию кости. И компактная, и трабекулярная кость разрушаются при гипертиреоидизме. Гипотиреоидизм мешает эффекту паратгормона по мобилизации кости, ведя к вторичному гиперпаратиреоидизму. При этом увеличивается и абсорбция кальция в кишке, и его почечная реабсорбция. Гормон роста стимулирует рост хряща и кости посредством факторов роста. Это также стимулирует активный транспорт кальция в кишке. Инсулин стимулирует остеобластную продукцию коллагена и непосредственно уменьшает почечную реабсорбцию кальция и натрия.
Есть обратная взаимосвязь между потреблением с пищей фосфора и содержанием кальция в моче. Фосфор увеличивает синтез паратгормона (уменьшающего уровень кальция в моче) и оказывает непосредственное влияние на почечный канальцевый транспорт кальция. Изменения содержания кальция в моче обычно сопровождаются аналогичными изменениями содержания натрия, и наоборот. Эти два элемента сообща участвуют в механизмах реабсорбции в проксимальном отделе канальца. Если к диете здоровых женщин, находящихся в постменопаузе, ежедневно на протяжении десяти лет добавлять 3 и 6 г хлорида натрия, то это привело бы к мобилизации 7,5 и 10 % соответственно скелетного кальция и явилось бы фактором риска развития остеопороза.
Кофеин также увеличивает потерю кальция с мочой. Инфузия аминокислот и глюкозы пациентам, получающим полное парентеральное питание, приводит к потере кальция с мочой и отрицательному балансу кальция, который может быть оптимизирован назначением дополнительного фосфора в растворах.
Нормальные уровни эстрогена сыворотки необходимы для обеспечения оптимального баланса кости. Снижение уровня эстрогенов у постклимактерических женщин — главный фактор в развитии резорбции кости и остеопороза. В кости были идентифицированы рецепторы эстрогена. Лечение эстрогенами уменьшает резорбцию кости в течение недель без изменений в сыворотке паратгормона, кальцитонина или метаболитов витамина D. Однако более пролонгированная терапия эстрогенами приводит к увеличению синтеза паратгормона и метаболита витамина D, что может объяснять наблюдаемые улучшения кишечной абсорбции и почечной реабсорбции кальция. Тестостерон также ингибирует резорбцию кости. Остеопороз наблюдается у взрослых мужчин с гипогонадизмом.
Кальций экскретируется приблизительно в равных количествах с мочой и кишечным секретом. Потеря кальция через кожу составляет лишь около 15 мг/сут, хотя она существенно увеличивается при выраженном потоотделении. Приблизительно 150 мг/сут кальция поступает в просвет кишки при секреции кишечного сока и с желчью, но приблизительно 30 % абсорбируется, так что минимальная фекальная экскреция кальция составляет 100 мг/сут. Экскреция кальция с мочой составляет от 100 до 240 мг/сут и очень изменчива у здоровых людей. 99,8 % его подвергаются реабсорбции. У одного и того же человека есть большие дневные колебания в уровне кальция в моче, главным образом благодаря кальцийуретическому эффекту пищевых продуктов.
Усвоенные углеводы и белок имеют кальцийуретический эффект, который линейно связан с потреблением этих веществ, но относительно независим от потребления кальция. На каждые дополнительные 50 г белка рациона теряются с мочой 60 мг кальция. Высокий уровень содержания фосфора в некоторых белках снижает, но не устраняет его кальцийуретический эффект. Кальцийуретический эффект белка приводит к снижению почечной реабсорбции кальция, что не компенсируется увеличением его абсорбции в кишке. Следовательно, богатая белками диета у взрослых приводит к отрицательному балансу кальция.
Инсулин может ухудшать почечную реабсорбцию кальция.
Дефицит кальция и его коррекция
Количество абсорбируемого из пищи кальция недостаточно, чтобы восполнить потери с калом и мочой. Некоторые исследования баланса кальция у взрослых женщин показывают, что в среднем ежедневно необходимо 550 мг, чтобы предотвратить отрицательный баланс кальция. Люди пожилого возраста нуждаются даже в более высоком его поступлении, так как у них может быть нарушена абсорбция.
Потребление кальция в течение жизни может иметь существенное влияние на минеральную плотность кости в зрелом, тем более в пожилом и старческом, возрасте. Высокое содержание минерала в кости задерживает наступление времени, когда развиваются симптомы остеопороза, но не изменяют степени потери костью кальция.
Проводилось множество клинических испытаний, но не все они показали, что добавки кальция замедляют потерю кости у женщин в постменопаузе. Известно, что добавки карбоната кальция, обеспечивая 2000 мг кальция в день, в большей степени замедляют скорость потери кортикальной кости (пример — проксимальный отдел предплечья), чем трабекулярной (поясничный отдел позвоночника). К сожалению, большинство переломов происходит в трабекулярной кости. Пищевые добавки кальция могут защищать от деминерализации кости тех женщин, чья обычная диета содержит мало кальция. Добавки эффективны при поддержании скелетного кальция у женщин, находившихся более шести лет в постменопаузе и не получавших эстрогены. Исследования показывают, что кальция цитрат-малат более эффективен, чем карбонат кальция. Но никакая пищевая добавка не изменяет скорости потери минерала кости у тех женщин, которые исходно получали оптимальный уровень кальция с пищей, от 400 до 650 мг/сут.
Нарушение метаболизма кальция
Заболевания, связанные с нарушением метаболизма кальция, могут быть классифицированы следующим образом:
Кишечная мальабсорбция
Многие расстройства функции кишечника характеризуются мальабсорбцией кальция, так же как и дефицитом витамина D и остеомаляцией. Они включают желудочно-кишечные заболевания, такие как болезнь Крона и целиакия, резекцию тонкой кишки или наложение обходного анастомоза. Истощение кальция и витамина D объясняется мальабсорбцией, стеатореей, неадекватным пероральным потреблением или комбинацией этих причин.
Идиопатическая гиперкальциурия и кальциевый нефролитиаз.
У большинства пациентов с кальциевыми камнями в почке имеется идиопатическая гиперкальциурия. Приблизительно в 90 % случаев она характеризуется повышением активной абсорбции кальция, нормальным содержанием кальция и паратгормона в сыворотке и повышением в сыворотке метаболитов витамина D. Повышение уровня производных витамина D может быть первичным дефектом, и связано оно с усиленной фильтрацией фосфата почками. По причинам, которые полностью не поняты, при кальциевом нефролитиазе наблюдается более низкое содержание минерала в кости. Возможные объяснения — гипофосфатемия, гиперкальциурия и нарушение метаболизма витамина D, сопровождающееся низким потреблением кальция. Лечение мочекаменной болезни диетой с низким содержанием кальция не предупреждает камнеобразование и способствует остеопорозу.
Нарушение кишечной абсорбции
Чрезмерное кишечное всасывание и гиперкальциемия наблюдаются при саркоидозе и при первичном гиперпаратиреоидизме (из-за увеличенной экстраренальной продукции метаболита витамина D). Ухудшение всасывания кальция вызвано редуцированным синтезом метаболитов витамина D при хронической почечной недостаточности и гипопаратиреоидизме.
Гипертензия
Адекватное потребление кальция обратно пропорционально связано с давлением крови. Низкий ренин плазмы, чувствительность к пищевой соли и измененный метаболизм кальция — предикторы гипотензивного ответа на дополнительное поступление кальция. Ренин-альдостероновая система и кальций- регулируемые гормоны, особенно метаболиты витамина D, работают скоординированно через изменение распределения кальция между внутриклеточным и внеклеточным пространствами. Предполагаются также другие механизмы, включая прямой эффект кальций-регулируемых гормонов на транспорт кальция в клетках гладкой мускулатуры сосудов и редуцирование симпатического ответа мозга.
Рак толстой кишки
Данные большого количества эпидемиологических обзоров свидетельствуют, что потребление кальция в количестве, равном норме или слегка превышающем ее, защищает от рака толстой кишки. Однако комплексность рациона человека препятствует подтверждению правильности этой гипотезы. Например, более высокое потребление кальция из молочных продуктов обычно сочетается с большим количеством жира, белка, витамина D (молоко насыщено этим витамином), фосфора и рибофлавина. Однако несколько клинических испытаний показали сокращение пролиферации клеток в слизистой оболочке толстой кишки у лиц с риском развития рака толстой кишки, получавших добавки кальция. Считают, что кальциевые добавки увеличивают внутрипросветную концентрацию ионов кальция (и фосфата кальция), которые могут преципитировать желчные или жирные кислоты. А те могут стимулировать пролиферацию эпителиальных клеток толстой кишки.
Потребность в кальции
Рекомендуемые потребности основаны на количестве диетического кальция, необходимого для восполнения потерь с кишечным секретом, мочой и потом, учитывая эффективность кишечного всасывания. Суточная потребность составляет у взрослых 0,8–1 г/сут.
Потребность в кальции повышается у беременных и кормящих грудью женщин, спортсменов, при работе, связанной с профессиональными вредностями (фторсодержащая пыль, пыль от фосфатных удобрений и др.), обильном потоотделении, лечении ГКС и анаболическими стероидами. У лиц с остеопорозом потребность в дополнительном кальции оценивается в ходе их лечения.
Пищевые источники
Более половины количества потребляемого кальция население получает с молочными продуктами. Другими источниками являются некоторые зеленые овощи (брокколи), орехи, соевый творог, осажденный кальцием, костная мука.
Существенным вкладом в потребление кальция у некоторых людей могут быть обогащенные кальцием пищевые продукты (соки и мука) и антациды, содержащие кальций. В продуктах питания кальций содержится главным образом в виде труднорастворимых солей (фосфатов, карбонатов, оксалатов и др.). Биодоступность кальция из ряда немолочных источников недостаточна.
Увеличение биодоступности
К составным компонентам пищи, стимулирующим биодоступность кальция, относится лактоза. Она увеличивает всасывание кальция. Повышается абсорбция и после добавления лактазы, что может быть объяснено тем фактом, что наиболее метаболизированный сахар увеличивает всасывание кальция. Эти данные получены для младенцев. Неясно, улучшает ли лактоза абсорбцию кальция из молочных продуктов у взрослых.
Более высокая распространенность остеопороза у людей с непереносимостью лактозы скорее связана с низким потреблением молочных продуктов, а не с эффектом лактозы на всасывание кальция.
Уменьшение биодоступности
Пищевая клетчатка снижает всасывание кальция. Замена белой муки (22 г пищевых волокон в день) мукой из цельной пшеницы (53 г пищевых волокон в день) в обычном рационе служит причиной отрицательного баланса кальция даже при его потреблении, превышающем норму.
Аналогично влияют на абсорбцию кальция пищевые волокна фруктов и овощей. Несколько составных частей волокон связывают кальций. Уроновые кислоты прочно связывают кальций in vitro. Вероятно, поэтому гемицеллюлоза подавляет всасывание кальция. 80 % уроновых кислот пектина подвергается метилированию и не может связывать кальций. Поэтому пектин не влияет на абсорбцию кальция. Теоретически типичная вегетарианская диета содержит достаточное количество уроновых кислот, чтобы связать 360 мг кальция, но большинство этих кислот усваивается в дистальных отделах кишечника, поэтому часть кальция все же абсорбируется.
Фитиновая кислота — другая составная часть растений, которая связывает кальций. Высокое содержание фитинов в пшеничных отрубях объясняет их неблагоприятные эффекты на абсорбцию кальция. Интересно, что добавление кальция к пшеничному тесту уменьшает деградацию фитинов на 50 % в течение брожения и выпечки. Пшеничные отруби препятствуют всасыванию кальция в такой степени, что это использовалось в терапевтических целях при гиперкальциуриях.
Темно-зеленые покрытые листвой овощи зачастую имеют относительно высокое содержание кальция. Но всасыванию кальция из большинства их препятствует щавелевая кислота. Продукты с низким содержанием щавелевой кислоты (белокочанная капуста, брокколи, репа) — хорошие источники кальция. Например, всасывание из капусты кальция столь же высоко, как из молока.
Жир пищи не оказывает влияния на баланс кальция у здоровых лиц. Но при наличии мальабсорбции жира (стеатореи — повышенного содержания в кале нейтрального жира, жирных кислот или их солей) кальций преципитируется с жирными кислотами, формируя нерастворимые мыла в просвете кишечника.
Хотя индуцированная диетой (богатой белком) кальциурия служит причиной отрицательного баланса кальция, удивительно, что она не приводит к компенсаторному увеличению эффективности абсорбции кальция в кишке.
Взаимодействие с нутриентами
Ни уровень фосфора в пище, ни соотношение кальция с фосфором не влияет на всасывание кальция у людей. Напротив, длительное непрерывное поступление с пищей большего количества фосфора приводит к гиперпаратиреоидизму и вторичной резорбции костей.
Поскольку и кальций, и железо обычно рекомендуется женщинам, интересны взаимодействия между этими добавками. В одном исследовании добавка карбоната кальция и гидроксиапатита уменьшала абсорбцию железа примерно до 50 % у постклимактерических женщин. В другом исследовании кальций молока ингибировал всасывание железа на 30 %. В случае дополнительного приема с пищей кальций ингибирует всасывание железа из его препаратов (сульфата железа), пищевого негемового и гемового железа. Но если карбонат кальция принимался без пищи, то он даже в высоких дозах не ингибировал всасывание железа из сульфата железа. Таким образом, использование добавки кальция с пищей существенно влияет на всасывание железа. Кальций, вероятно, затрагивает внутриклеточную передачу железа энтероцитом.
Не выявлено влияние кальциевых добавок на абсорбцию магния и цинка.
Кальций для пожилых людей
Работами многих авторских коллективов (Wood R. еt al., 1995; Russel R., 1997; Evans W., Cyr-Campbell D., 2001 и др.) проводились исследования, имеющие цель ответить на вопрос, нуждаются ли пожилые люди в дополнительном введении кальция. Действительно, в стареющем организме происходит накопление минеральных веществ, особенно солей кальция, наблюдаются отложения его в стенках сосудов, хрящах и других тканях. Отмеченные явления нередко сочетаются с явным дефицитом минерала в костной ткани, особенно у женщин. Было установлено, что по ряду причин, связанных с расстройством ферментных систем пищеварения, всасывание кальция в тонкой кишке существенно снижено и, соответственно, усвоение данного макроэлемента не способно обеспечить метаболические нужды организма. В этом заключается одна из нередких причин остеопороза у пожилого человека. Несомненно, данная категория пациентов нуждается в повышенных дополнительных количествах пищевого кальция.
Тканевые потребности в кальции увеличиваются у людей старших возрастов при развитии у них эндокринопатий, особенно скрыто протекающих (например, гипопродукции эстрогенов), при нарушениях минерального обмена, проявляющегося желчнокаменной или мочекаменной болезнью, при расстройствах витаминной (особенно витамина D), минеральной (особенно Mg) обеспеченности.
Кальций для женщин
Сформулированы рекомендации о ежедневном дополнительном обеспечении кальцием в количестве 1000 мг женщин в менопаузе, не получающих эстрогены, и 1500 мг женщин в менопаузе, принимающих дополнительно эстрогены. Использование замещающих эстрогенов и другой фармакологической терапии привлекает повышенное внимание к предупреждению и лечению остеопороза. Ежедневное употребление стандартных поливитаминов с минералами (в первую очередь Ca), определенно, рекомендуется тем, у кого потребление неадекватно, нарушено всасывание или повышены тканевые потребности.
Хотите больше новой информации по вопросам диетологии?
Оформите подписку на информационно-практический журнал «Практическая диетология»!
ФОСФОР
Энергия организма
Высшие организмы используют органический фосфор, получая его из растительных источников с пищей. Скорее фосфат, чем фосфор, является центром внимания нутриционной биохимии.
Фосфорная кислота (H3PO4) — сильная кислота. Моновалентные катионы (натрий, калий и аммоний) могут формировать высокорастворимые соли фосфата, а двухвалентные (кальций и магний) образуют относительно нерастворимые его соединения.
Живая материя имеет огромную потребность в фосфоре. ДНК и РНК — это полимеры, основанные на мономерах сложных эфиров фосфата; высокоэнергетичная связь фосфата АТФ — основная энергия живущих организмов. Мембраны клетки состоят в значительной степени из фосфолипидов. Неорганические компоненты кости — это прежде всего фосфат кальция и гидроксиапатит. Разнообразие его ферментных функций определяется чередованием фосфорилирования и дефосфорилирования белков клеточными киназами и фосфатазами. Метаболизм всего главного метаболического субстрата зависит от функционирования фосфора как кофактора разнообразных ферментов и как основного резервуара для метаболической энергии в форме АТФ, креатин фосфата и фосфоэнолпирувата.
Другая важная роль фосфора заключается в том, что нейтральные молекулы являются растворимыми в липидах и проходят через мембраны. Так как фосфаты ионизированы в физиологическом pH, они могут осуществлять перемещение фосфорилированных молекул в пределах клеток. Наконец, фосфор соединяется с кальцием, образуя гидроксиапатит — основное неорганическое соединение кости.
Фосфор во внеклеточных жидкостях составляет лишь 1 % от общего фосфора организма. Большая часть (70 %) общего фосфора в плазме обнаружена как составная часть органических фосфолипидов. Однако клинически полезной фракцией в плазме является неорганический фосфор, 10 % которого связано с белком, 5 % составляют комплексы с кальцием или магнием, и большая часть неорганического фосфора плазмы представлена двумя фракциями ортофосфата. Фосфор обнаружен во всех клетках организма. Основные места, содержащие его, — это гидроксиапатит кости и скелетная мускулатура. Общее содержание фосфора составляет приблизительно 500 г у мужчин и 400 г у женщин.
Метаболизм фосфора
Метаболизм фосфора в организме представляет сложное взаимодействие между различными факторами, которые могут затрагивать пищеварение, его абсорбцию, распределение и экскрецию.
Нерастворимые минеральные соли фосфата образуются при повышенном pH. Кислая среда желудка (pH — 2) и большей части проксимального отдела тонкой кишки (pH — 5) может играть важную роль в поддержании растворимости и биодоступности неорганического фосфора. В этом отношении важны потенциальные эффекты гипохлоргидрии (у пожилых и получающих антисекреторную терапию пациентов) на растворимость и биодоступность фосфора.
Приблизительно 60–70 % фосфора абсорбируется из обычной смешанной диеты. Показано, что всасывание фосфора находится в диапазоне от 4 до 30 мг/кг массы тела в сутки и связано с его потреблением. Физиологические состояния, характеризующиеся увеличением потребности в фосфоре (рост, беременность и кормление грудью), сопровождаются соответствующим усилением его абсорбции. У людей старших возрастных групп происходят изменения в экскреции фосфора и адаптации к фосфору пищи. Показано, что, несмотря на потребление рекомендуемой нормы фосфора, отрицательный его баланс наблюдается у пациентов в возрасте старше 65 лет, за счет потери фосфора с мочой.
Клеточный и молекулярный механизм всасывания фосфора кишкой до конца не изучен. Транспорт фосфора через кишечную клетку — это активный, натрий-зависимый путь. Внутриклеточные уровни фосфора относительно высоки. Паратгормон напрямую не регулирует абсорбцию фосфора в кишечнике. Назначение активного метаболита витамина D приводит к увеличению всасывания фосфора и у здоровых, и у пациентов с уремией. Регуляция общего уровня фосфора в организме требует скоординированных усилий почки и кишечника. В условиях низкого потребления фосфора с пищей кишечник увеличивает его всасывание, а почка — почечный транспорт, чтобы минимизировать его мочевые потери. Эта адаптация обеспечивается изменениями в уровне активного метаболита витамина D и паратгормона в плазме. Если эти адаптивные меры не в состоянии скомпенсировать низкое потребление фосфора, то фосфор кости может перераспределяться в мягкие ткани. Однако эти компенсаторные возможности не безграничны.
Фекальные потери фосфора составляют 0,9–4 мг/кг в день. Основная экскреция происходит через почки. Экскреция фосфора имеет широкий диапазон (0,1–20,0 %). Следовательно, почки обладают способностью эффективно регулировать фосфор плазмы. Скорость почечной реабсорбции регулируется его концентрацией в плазме. Это саморегулируемый процесс.
Гормональный регулятор почечной реабсорбции фосфора — гормон паращитовидной железы и нефрогенный цАМФ. Концентрация паратгормона плазмы положительно коррелирует с уровнем экскреции фосфора с мочой. Главные признаки потери фосфора с мочой — увеличение абсорбции фосфора и повышение его уровня в плазме. Состояния, которые приводят к гиперфосфатурии, — гиперпаратиреоидизм, острый дыхательный или метаболический ацидоз, мочегонные средства и увеличение внеклеточной массы фосфора. Уменьшение выделения фосфора с мочой связано с диетическим ограничением фосфора, увеличением в плазме инсулина, гормона щитовидной железы, роста или глюкагона, алкалозом, гипокалиемией и внеклеточным снижением массы фосфора.
Дефицит фосфора
Признаки хронического дефицита фосфора у лабораторных животных — потеря аппетита, развитие тугоподвижности в суставах, хрупкость костей и восприимчивость к инфекциям. У здоровых людей существует малая вероятность развития дефицита фосфора вследствие его широкой представленности в рационах. Однако недоношенные новорожденные часто склонны к развитию рахита из-за неадекватной поставки фосфора и кальция. Витамин D-независимый гипофосфатемический рахит был впервые описан в 1937 г.
Классическое изучение дефицита фосфора у людей проводилось Лотцем в 1968 г. При этом дефицит индуцировался применением у здоровых лиц диеты с низким содержанием фосфора. Показано, что явные симптомы дефицита фосфора (анорексия, слабость, боли в костях) не развивались до снижения уровня фосфора сыворотки ⅓ фосфора в молоке; 20 % приходится на соединения сложных эфиров с аминокислотами казеина; 40 % — на казеиновые. Неорганические фосфаты в молоке представлены солями кальция, магния и калия. Относительная биодоступность фосфора в молоке составляет 65–90 % у младенцев. Однако весь фосфор в казеине молока (20 % от общего) восстановлен фосфопептидом, который является стойким к ферментному расщеплению трипсином и поэтому менее биодоступен. Более низкое содержание казеина в женском молоке, по сравнению с коровьим молоком, может быть причиной более высокой биодоступности фосфора из женского молока.
Растительная пища
В пшенице, рисе и кукурузе более чем 80 % общего фосфора найдено в виде фитиновой (инозитгексафосфорной) кислоты, и 35 % ее обнаружено в зрелых картофельных клубнях.
У людей нет фермента фитазы, необходимого для расщепления фитатов и освобождения фосфора. Но прокариоты (дрожжи и бактерии) содержат фитазу. Это любопытное свойство природы важно для пищевого фосфора по двум причинам. Вначале традиционное использование дрожжей в производстве хлеба приводит к разложению фитата из-за гидролитического действия дрожжей до выпечки. Далее кишечные бактерии способны разложить некоторое количество пищевого фитата. Фитат плохо переваривается в желудочно-кишечном трактате человека. Но впитывание воды может эффективно удалять фитат из некоторых пищевых продуктов. Например, 99,6 % фитата в бобах может быть извлечено при пропитывании их водой. Размалывание зерна удаляет внешние оболочки, которые содержат существенные количества фитата в некоторых хлебных злаках. Но такая обработка уменьшает содержание и фосфора, и других минералов.
Взаимодействие между нутриентами
Высокий уровень фосфора в молочных смесях, используемых для кормления недоношенных новорожденных, может уменьшать абсорбцию магния. Показано, что фосфор уменьшает всасывание свинца у людей.
Известно, что диета, содержащая ежедневно 2 г кальция, не влияет на всасывание фосфора. Однако высокое содержание в пище кальция и тем самым пищевое подавление абсорбции может быть полезным в терапевтических целях для улучшения состояния гиперфосфатемии у пациентов с хронической почечной недостаточностью. Прием с пищей 1000 мг кальция при содержании в ней 372 мг фосфора уменьшает всасывание фосфора до 70–31 %. То есть избыточное потребление добавки кальция может оказывать неблагоприятный эффект на баланс фосфора.
Безрецептурные алюминий- или магний-содержащие антациды связывают фосфор в желудочно- кишечном трактате и уменьшают его всасывание. 3 г гидроксида алюминия (25 ммоль алюминия), поступаемые с пищей, уменьшают всасывание фосфора до 70–35 %.
Насущная проблема — адаптация к диетам с высоким содержанием фитатов. Известно, что наблюдаются ингибирующие эффекты фитатов на абсорбцию железа у людей, потребляющих в течение многих лет пищу с высоким их содержанием (например, у вегетарианцев).
Хотите больше новой информации по вопросам диетологии?
Оформите подписку на информационно-практический журнал «Практическая диетология»!
МАГНИЙ
Энергетик клетки
Магний играет эссенциальную роль во многих фундаментальных клеточных реакциях, поэтому его дефицит может приводить к серьезным биохимическим и клиническим изменениям. Экспериментальные и клинические наблюдения показали важные взаимосвязи этого эссенциального иона с другими электролитами, вторичными мессенджерами, гормонами и факторами роста, их мембранными рецепторами, сигнальными путями, ионными каналами, секрецией и действием гормона паращитовидной железы, метаболизмом витамина D и функцией кости. Несмотря на то что рационы, используемые здоровыми европейцами, по всей вероятности, не ведут к клинически значимой гипомагниемии, были выявлены симптомы, обусловленные его дефицитом.
Место в организме
Магний участвует в следующих реакциях: в синтезе жирных кислот, активации аминокислот, синтезе белка, фосфорилировании глюкозы и ее производных по гликолитическому пути, окислительном декарбоксилировании цитрата. Хорошо известны протеинкиназы — ферменты, которые катализируют передачу фосфата к белковому субстрату. Из них магний аденозин-трифосфат — один из огромного семейства, насчитывающего более чем 100 ферментов. Магний требуется для формирования циклического аденозин монофосфата (цАМФ).
Более половины общего количества магния находится в кости, почти вся остальная часть — в мягких тканях. Это катион с высокой концентрацией в клетках. В количественном отношении он является вторым после калия. Большая часть внутриклеточного магния существует в связанной форме. Магний, как и кальций, формирует комплексы с фосфолипидами мембран клетки и нуклеотидами.
Абсорбция магния
Процент абсорбции магния регулируется его концентрацией в пище и присутствием ингибирующих или способствующих абсорбции компонентов рациона. Магний абсорбируется и в тощей, и в подвздошной кишке. Увеличение потребления кальция незначительно влияет на всасывание магния. В случаях, когда абсорбция магния увеличивалась, не наблюдалось повышение его уровня в крови, из-за повышения экскреции с мочой. Увеличение перорального поступления магния приводит к уменьшению абсорбции фосфата. При различных синдромах мальабсорбции, как правило, уменьшается всасывание магния в кишке.
Клинически значимая мальабсорбция магния может наблюдаться:
Почки играют ключевую роль в гомеостазе магния. Приблизительно 75 % магния сыворотки фильтруется в почечных клубочках. Нарушение фильтрации уменьшает количество магния, поступающего в канальцы. Серьезное снижение функции клубочков служит причиной повышения магния в сыворотке. Восходящая часть петли Генле — главный участок реабсорбции магния, регулирующий экскрецию. Здоровая почка при среднем потреблении магния повторно абсорбирует приблизительно 95 % профильтрованного ею количества.
Когда потребление магния строго ограничено у людей с нормальной функцией почек, выделение магния становится небольшим — менее 0,25 ммоль/сут. Увеличение потребления магния до нормы повышает мочевую экскрецию без изменения уровня магния сыворотки при условии, что функция почек нормальна и вводимое количество не превышает максимальную клубочковую фильтрацию.
Дефицит магния
Симптомы дефицита магния: парестезии, скрытая или явная тетания. Состояния, при которых может развиться гипомагниемия, указаны в таблице 1.
Таблица 1. Клинические состояния, способствующие истощению запасов магния
Воспалительные заболевания кишки
Глютеновая энтеропатия; спру
Кишечная фистула, обходной анастомоз или резекция
Состояние недостатка желчи, например дисфункция слепой кишки со стеатореей
Иммунные заболевания с атрофией ворсинок
Радиационный энтерит Лимфангиоэктазия; другие дефекты абсорбции жира
Первичная идиопатическая гипомагниемия Желудочно-кишечные инфекции
Гиперпаратиреоидизм с гиперкальциемией
Постпаратиреоидэктомия (синдром «голодных костей»)
Первичная идиопатическая гипомагниемия
Синдром теряющей почки
Синдром Барттера Младенцы,рожденные от матерей, страдающих диабетом или гиперпаратиреоидизмом
Преходящая неонатальная гипомагниемия, гипокальциемия
Недостаточное потребление белковых калорий (обычно с инфекцией)
Пролонгированная инфузия или прием пищи с низким содержанием магния в растворах или рационе
Состояние повышенного катаболизма (ожоги, травмы)
Гипермагниемия
Нормальная почка способна к выделению больших количеств магния, абсорбируемого или экскретируемого настолько быстро, что уровень сывороточного магния обычно не достигает опасного. Повышение его может происходить при приеме содержащих магний антацидов или слабительных у больных с хронической почечной недостаточностью. Поскольку 20 % или более количества Mg2+ из различных солей может абсорбироваться, ухудшение почечной фильтрации может привести к существенному повышению магния в сыворотке. При острой почечной недостаточности с олигурией, особенно в сочетании с метаболическим ацидозом, может иметь место гипермагниемия. Инфузия кальция может противодействовать токсичности магния.
Потребность в магнии
В 1989 г. норма для взрослых принята равной 4,5 г/кг. Это составляет в среднем для мужчины и женщины 350 и 280 мг/сут соответственно.
Пищевые источники
Магний широко распространен в продуктах растительного и животного происхождения. Наиболее богаты им хлеб из муки грубого помола, крупы, бобовые, зеленые овощи. Источники магния из различных групп пищи представлены в таблице 2.
Таблица 2. Количество магния в различных пищевых продуктах (в % от ежедневного потребления)