Что такое per os в медицине простыми словами
per os
Смотреть что такое «per os» в других словарях:
per — per·acetic; per·acid; per·act; per·acute; per·alkaline; per·aluminous; per·am·bu·lant; per·am·bu·late; per·am·bu·la·tion; per·am·bu·la·tor; per·am·bu·la·to·ry; per·a·na·kan; per·bend; per·borate; per·bromide; Per·bu·nan; per·ca; per·cale;… … English syllables
per — pér prep. FO 1a. introduce determinazioni di spazio, spec. di moto per luogo, o indica un movimento entro uno spazio circoscritto; anche fig.: il treno passerà per Bologna, ho passeggiato a lungo per il parco, ha vagabondato tutto il giorno per… … Dizionario italiano
Per — ist ein skandinavischer männlicher Vorname[1], abgeleitet vom griechischen Namen Petros (deutsch Peter). Weiteres zu Herkunft und Bedeutung des Namens siehe hier. Andere Formen des Namens sind Pär und Peer. Namensträger Per Ahlmark (* 1939),… … Deutsch Wikipedia
per-2 — per 2 English meaning: to go over; over Deutsche Übersetzung: “das Hinausfũhren about” Material: A. Dient as preposition, preverb and Adverb: a. per, peri (locative of Wurzelnomens) “vorwärts, in Hinausgehen, Hinũbergehen about … Proto-Indo-European etymological dictionary
per se — 1 /pər sā, ˌper ; pər sē/ adv [Latin, by, of, or in itself] 1: inherently, strictly, or by operation of statute, constitutional provision or doctrine, or case law the transaction was illegal per se see also negligence per se at negligence; … Law dictionary
per — /per/ prep. [lat. per ]. 1. [per indicare attraversamento di un luogo (compl. di moto per luogo): l aria penetra p. le fessure ; il corteo passerà per via Nazionale ] ▶◀ attraverso, da, in, lungo. 2. [per indicare il luogo entro il quale avviene… … Enciclopedia Italiana
per- — ♦ Préfixe exprimant un excès de la quantité normale d un élément dans un composé chimique : peracide, peroxyde, persulfate, etc. per CHIM Préfixe qui servait à désigner les composés au degré d oxydation le plus élevé ou contenant le plus d… … Encyclopédie Universelle
Per — Per, prep. [L. Cf.
per — prep. (Termen comercial folosit în legătură cu preţul unei mărfi raportat la o unitate de măsură) Pentru, de fiecare. – Din it., germ. per. Trimis de ana zecheru, 13.09.2007. Sursa: DEX 98 PER prep. (termen comercial; instrumental modal) pe,… … Dicționar Român
Пероральный приём лекарственных средств
Перора́льный приём лекарственных средств — приём лекарства через рот (лат. per os, oris ), путём проглатывания лекарства.
Содержание
Применение
Преимущественно приём лекарственных средств данным способом назначают для лекарств, которые хорошо всасываются слизистой оболочкой желудка или кишечника. При лечении заболеваний органов пищеварения в некоторых случаях, напротив, применяются плохо всасывающиеся лекарственные препараты, что позволяет достичь их высокой концентрации в желудочно-кишечном тракте и получить хороший местный эффект без побочных реакций.
Недостатки
Лекарственные формы для перорального применения
Основными лекарственными формами для перорального применения являются растворы, порошки, таблетки, капсулы и пилюли. Также существуют лекарственные формы (например, таблетки с многослойными оболочками), при приёме которых действующий препарат высвобождается дольше обычного (по сравнению с обычными лекарственными формами), что позволяет продлить терапевтический эффект.
Большинство лекарственных препаратов при пероральном применении следует запивать большим количеством жидкости. При приёме некоторых лекарств в лежачем положении они могут задерживаться в пищеводе и вызывать изъязвление, поэтому необходимо запивать таблетки и капсулы водой.
Литература
См. также
Полезное
Смотреть что такое «Пероральный приём лекарственных средств» в других словарях:
Приём — многозначное слово Может означать: Действие по значению глагола принимать, взятие, получение какого либо передаваемого объекта Приём посуды Приём информации Приём почтовых отправлений Приём (введение) лекарственных средств Сублингвальный приём… … Википедия
Трансбуккальный приём препаратов — (лат. buccalis, «щёчный») фармакологический термин, означающий приём определённого лекарства путём размещения его между верхней губой и десной или в полости рта до полного рассасывания. При этом лекарство направляется в… … Википедия
Трансбуккальный приём — препаратов (лат. buccalis щёчный) фармакологический термин, означающий приём определённого лекарства путём размещения его между верхней губой и десной или в полости рта до полного рассасывания. При этом лекарство направляется в… … Википедия
Варфарин — … Википедия
Прокаинамид — (Procainamide) … Википедия
Merck — (Мерк) Компания Merck, история компании, деятельность компании Компания Merck, история компании, деятельность компании, руководство компании Содержание Содержание Обозначение Собственники и руководство Деятельность KGaA в Соединение… … Энциклопедия инвестора
Туберкулёз о́рганов дыха́ния — Туберкулез органов дыхания. Органы дыхания при туберкулезе (Туберкулёз органов дыхания) поражаются наиболее часто. В соответствии с принятой в нашей стране клинической классификацией туберкулеза различают следующие формы Т. о. д.: первичный… … Медицинская энциклопедия
Ципролет — Ципрофлоксацин (Ciprofloxacinum) Химическое соединение ИЮПАК 1 циклопропил 6 фтор 4 оксо 7 пиперазин 1 ил хинолин 3 карбоновая кислота Брутто ф … Википедия
Ципрофлоксацин — (Ciprofloxacinum) Химическое соединение … Википедия
Бетаципрол — Ципрофлоксацин (Ciprofloxacinum) Химическое соединение ИЮПАК 1 циклопропил 6 фтор 4 оксо 7 пиперазин 1 ил хинолин 3 карбоновая кислота Брутто ф … Википедия
Новый препарат per os в лечении язвенного колита
Кроме того, 89% пациентов испытали некоторую степень улучшения своих показателей по шкале Мэйо, 61% улучшения в отношении слизистой оболочки и 33% достигли ее заживления.
О побочных эффектах, связанных с общим подавлением иммунитета, не сообщалось.
По словам исследователей, ни один из пациентов не прекратил исследование из-за побочных эффектов.
Однако в целом у 15 пациентов было зарегистрировано 40 нежелательных явлений; 95% из них были от легкой до умеренной степени тяжести, а 40% были связаны с лечением.
Никаких различий в побочных эффектах, связанных с двумя дозами, не наблюдалось.
Заключение
Гибридный белок на растительной основе безопасен и эффективен для благоприятной иммунной модуляции у пациентов с язвенным колитом легкой и средней степени тяжести, при этом не было получено данных о побочных эффектах подавления иммунитета.
Исследование OPRX-106 фазы 1 на здоровых добровольцах показало безопасность и иммуномодулирующий эффект при дозах 2, 8 или 16 мг / день.
Доказательством системного противовоспалительного эффекта было снижение уровней провоспалительных цитокинов интерлейкина-6 и гамма-интерферона в сыворотке крови, что коррелировало с клиническим ответом, отметили исследователи.
Точно так же увеличение CD3 + CD4 + CD25 + Foxp3 + супрессорных лимфоцитов коррелировало с клиническим ответом.
Доступные в настоящее время антагонисты TNF вводятся внутривенно или подкожно и несут риск инфекционных осложнений, поэтому разработка агента, который можно вводить перорально с меньшими побочными эффектами, имеет большое значение.
Для подтверждения полученных результатов необходимы более масштабные рандомизированные плацебо-контролируемые исследования.
Инсулин per os
Существующий способ лечения сахарного диабета путем ежедневных инъекций инсулина является далеко не идеальным. Поэтому появление инсулина в таблетках стало бы настоящим событием для больных сахарным диабетом. Не только потому, что жизненно необходимые ежедневные инъекции инсулина не всегда удобны для больных диабетом, особенно детей, но еще и потому, что новый препарат позволил бы оттянуть момент перехода на уколы, что немаловажно для больных, которые не хотят становиться зависимыми от инъекций.
Между тем инсулин в таблетках был разработан еще более 10 лет назад и ни где-нибудь, а в России. Препарат даже получил название «РАНСУЛИН» – инсулин Российской академии наук. Однако, как это часто бывает, до массового производства уникального лекарства дело так и не дошло. Между тем, недавно немецкие ученые протестировали инсулин в капсулах и подтвердили, что пероральная форма имеет явные преимущества перед инъекционной. Так дождутся ли больные диабетом всего мира появления в продаже инсулиновых таблеток?
Об этом корреспондент zdorovieinfo беседует с одним из создателей чудо-таблеток, доктором химических наук Львом Ивановичем Валуевым.
Милена Сигаева / «Здоровье-инфо»
Роль инсулина в регуляции содержания сахара крови и его связь с диабетом была открыта учеными Бестом и Бентингом в 1922 году.
После этого ученые во всем мире работали над созданием такой формы инсулина, которую можно было применять перорально (в том числе в виде назальных спреев и таблеток). Еще в 50-ых годах XX века в журнале Nature появилась статья американского профессора Ласковский, который описал принцип перорального введения инсулина. Ему не хватило совсем немного для того, чтобы полностью завершить работу.
В 90-ых годах группа российских ученых в институте нефтехимического синтеза им.
А.В. Топчиева РАН, возглавляемая академиком Платэ Николаем Альфредовичем в рамках программы Президиума Российской академии наук «Фундаментальные науки – медицине» создала препарат инсулина в таблетированной форме.
Почему таблетки лучше?
Еще великий среднеазиатский философ и врач Авиценна обратил внимание на роль печени в системе распределения продуктов пищеварения в человеческом организме.
После еды, в крови человека появляется глюкоза. В ответ на повышение концентрации глюкозы поджелудочная железа начинает вырабатывать инсулин, который попадает в печень через кровеносные сосуды одновременно с продуктами пищеварения. Печень, в свою очередь, контролирует количество инсулина, достигающего другие органы и ткани. Когда же больной сахарным диабетом делает инъекцию инсулином, который попадает сразу в кровь, то печень из этого процесса исключается. Отсутствие контроля со стороны печени приводит к тому, что у больных сахарным диабетом развиваются такие осложнения, как сердечно-сосудистые заболевания, расстройство функций головного мозга и т.д.
По некоторым оценкам, сегодня в мире насчитывается более 70 миллионов человек больных диабетом. И их число неуклонно увеличивается.
Поэтому наиболее безопасным считается пероральное введение инсулина. При этом не следует забывать и моральные аспекты этой проблемы. Необходимость ежедневных инъекций инсулина травмирует психику больных, особенно детей, и причиняет им физические и моральные страдания.
Один из авторов актуального исследования, эндокринолог Кристоф Капица из Профильного института метаболических исследований города Нейсса в Германии, сказал: «Инсулин в капсулах, комбинированный с носителем лекарственного вещества, продемонстрировал видимое превосходство над своим инъекционный аналогом. Он действует и распадается гораздо быстрее, что поможет лучше контролировать сахар крови у пациентов с диабетом 2 типа».
Механизм действия перорального инсулина
Инсулин – это белковый гормон, вырабатываемый поджелудочной железой. А белок при пероральном применении организм воспринимает не как лекарство, а как простую белковую еду, и соответственно разлагает его до составляющих его аминокислот. Именно защита инсулина от разрушающего действия пищеварительных ферментов и былаглавной проблемой в создании пероральной формы инсулина, над решением которой и стала работать группа российских ученых.
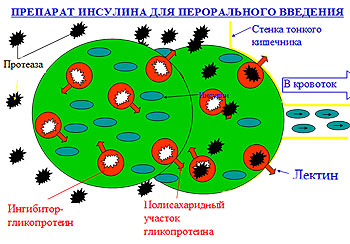
Переваривание белков начинается в желудке в кислой среде, дальше пища поступает в тонкий кишечник, где переваривание заканчивается в нейтральной среде и там же происходит всасывание веществ в организм. Белки разрушаются до составляющих их аминокислот, которые и всасываются в кровоток. Проблема предотвращения разрушения инсулина в желудке решалась достаточно просто. Его надо было поместить в капсулу из полимера, который не растворялся бы в кислой среде желудка, но растворялся бы в нейтральной среде тонкого кишечника. Подобные разработки существовали уже давно.
Гораздо сложнее оказалось решить другую проблему – предотвратить разрушение инсулина в тонком кишечнике. Полностью убивая ферменты, переваривающие белки, можно сохранить инсулин, однако тогда замедлялся бы процесс переваривания пищи. Именно это и поставило крест на возможности клинического применения предложенной еще в 50-ых годах профессором М. Ласковски смеси инсулина и ингибиторов ферментов.
Российские ученые предложили принципиально иной способ использования ингибитора ферментов – молекулы ингибитора химически связали с полимерным гидрогелем. Кроме того, в состав гидрогеля ввели полисахариды – соединения, способные взаимодействовать с находящимися на стенках тонкого кишечника лектинами. В этот гидрогель водили уже не связанный с ним инсулин, и все это помещали в желудочнонерастворимую полимерную капсулу.
Во время экспериментов, проведенных российскими учеными с больными диабетом 2 типа, был проверено действие инсулина в капсулах с гидрогелем. У больных, принимавших двойную (по сравнению с инъекционной) дозу инсулина в капсулах, сахар в крови понижался несколько в меньшей степени, чем при уколах. А когда дозу перорально вводимого инсулина увеличивали в 4 раза, уровень сахара в крови снижался даже в большей степени, чем у тех, кто делал уколы инсулина. «Большое количество инсулина – абсолютно не страшно, – уверяет Валуев, – ведь в кровоток попадает ровно столько же инсулина, как при инъекции, а остальная его часть просто погибает».
В последнем исследовании немецкие ученые предложили половине участников своего эксперимента по две капсулы со 150 единицами комбинированного перорального препарата, а другим сделали инъекции по 15 единиц обычного гормона. В течение всей ночи специалисты контролировали содержание глюкозы и инсулина в крови людей. При использовании капсул концентрация нужного количества инсулина была достигнута быстрее. Был и еще один плюс – пероральный инсулин быстрее удалялся из крови, чем его инъекционная форма, а значит, снижалась вероятность передозировки. Но при этом требовалось в 20 раз больше инсулина.
Другие способы введения инсулина
Профессор Валуев уверяет, что существует и еще один простой способ перорального введения инсулина.
В толстый кишечник человека ежедневно поступает до 5 литров воды. Если прохождение пищи по желудку занимает практически сутки, то вода проходит по нему быстро и не всасывается. Около 5% поглощенной воды поступает в толстый кишечник, остальная остается в тонком кишечнике, где и всасывается в кровь также, как и продукты разрушения белков.
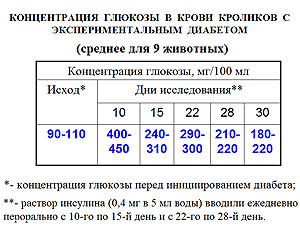
Если мы выпьем воду, то значительная ее часть появится в крови уже через 3 минуты, поскольку она очень быстро проходит в тонкий кишечник. И Лев Иванович предложил растворить инсулин в воде до такой концентрации, чтобы желудок не успел почувствовать появление инсулина и начать его разрушать. И вот что получилось – когда кроликам с диабетом 2 типа вводили раствор инсулина в воде концентрации 1 мг/мл, то концентрация глюкозы в их крови практически не менялась. Чем в большем количестве воды растворяли инсулин, тем быстрее он начинал действовать. В ходе эксперимента выяснилось, что идеальная концентрация инсулина в обычной воде составляет 1 мг в 10-12 мл.
Назальный спрей
Способ назального введения лекарства не нашел распространения в мире по нескольким причинам. Самой важной из них является то, что количество лекарства, которое распыляется с помощью аэрозоля на слизистую оболочку носа, очень трудно точно дозировать.
На все вышеперечисленные формы перорального инсулина российские ученые получили патенты. И диабетики всего мира уже давно бы пользовались ими, но от процесса изобретения лекарства до его изготовления проходят годы, даже при обоюдном желании фармацевтических компаний и изобретателей. А с этими изобретениями сложилась парадоксальная ситуация. Пероральные формы инсулина уже прошли все медико-биологические испытания на животных и начальные стадии клинических испытаний, но нужно еще довольно много денег и усилий, чтобы довести лекарства до массового производства. К сожалению, в России недооценили важности этой разработки. И на настоящий момент может получиться так, что новейшие и улучшенные формы перорального инсулина Россия будет вынуждена закупать за рубежом.
Отечно-асцитический синдром: практический алгоритм
Каждый пункт рекомендаций базируется на данных рандомизированных клинических исследований и имеет соответствующий уровень доказательности (табл. 1–3).
Отметим, что при определении степени рекомендации нет прямой связи между уровнем доказательности данных и степенью рекомендации. Например, отсутствие доказательств высокого уровня не исключает возможность дать рекомендации уровня А, если имеется богатый клинический опыт и достигнут консенсус. При определении степени рекомендаций качество научных доказательств, лежащих в их основе, является важным фактором, но его необходимо соотнести с преимуществами и недостатками, полезностью и стоимостью.
Данные рекомендации разработаны для применения у взрослых пациентов (старше 18 лет), у которых развитие отечно-асцитического синдрома связано с циррозом печени.
1.1. Определение асцита
Асцит – патологическое скопление жидкости в брюшной полости (рис. 1).
Самая распространенная причина развития асцита – цирроз печени (81% случаев) [3], далее следуют онкологические заболевания, затем смешанные причины, как правило цирроз печени с трансформацией в гепатоцеллюлярную карциному (ГЦК). Такие причины асцита, как сердечная недостаточность, туберкулез, заболевания поджелудочной железы, не превышают по частоте встречаемости 5% (рис. 2).
1.2. Классификация причин асцита по системам и органам
Если асцит рассматривать в отношении конкретных органов, доминировать будут печень и ее сосуды – до 90% всех причин развития асцита (табл. 4).
Как видно из представленных данных, несмотря на то что подавляющее большинство случаев асцита развивается на фоне патологии печени, существует ряд заболеваний, требующих дифференциальной диагностики.
1.3. Медико-социальная значимость асцита
Вопрос развития отечно-асцитического синдрома стоит остро. Дело в том, что данное осложнение цирроза печени развивается у 60% пациентов в течение десяти лет с момента выявления компенсированного цирроза печени [4, 5] и является маркером неблагоприятного исхода: в течение первого года от момента появления асцита доля летального исхода составляет 40%, пятилетняя выживаемость не превышает 50% [1, 5, 6].
1.4. Клиническая классификация асцита
В практическом применении наиболее удобна классификация, разработанная в 2003 г. IAC (International Ascitic Club). В ней учтены выраженность асцита и терапевтические мероприятия в зависимости от его степени (табл. 5).
Так, асцит 1-й степени визуально не диагностируется. К способам его определения можно отнести сонографические и/или лучевые методы исследования. Такой асцит не требует назначения терапии. Асцит 2-й степени может быть определен методами перкуссии и, как правило, сопровождается явлениями флуктуации. Терапевтическая тактика при данном варианте асцита включает ограничение потребления соли с пищей, назначение адекватной диуретической терапии. Асцит 3-й степени обычно характеризуется наличием напряженной передней брюшной стенки (рис. 3), требует проведения объемных парацентезов, ограничения потребления соли с пищей, назначения адекватной диуретической терапии.
2. Методы диагностики асцита
Основными жалобами пациентов с циррозом печени при наличии асцита являются увеличение живота в объеме, увеличение веса, отеки ног и т.п. При физикальном осмотре можно верифицировать наличие асцита перкуторным методом, в положении лежа и стоя.
Инструментальными методами, подтверждающими наличие асцита, могут служить ультразвуковое исследование, магнитно-резонансная и компьютерная томография.
Основными специфическими методами диагностики пациентов с асцитом считаются проведение диагностического парацентеза с анализом асцитической жидкости, сопоставление лабораторных результатов диагностики асцитической жидкости и сыворотки.
2.1. Диагностический парацентез: общие положения
(А1) Диагностический парацентез должен быть проведен всем больным:
при впервые выявленном асците;
при асците 2–3-й степени;
при наличии признаков ухудшения общего состояния больного и/или осложнений цирроза печени.
2.2. Диагностический парацентез: частные вопросы
Осложнения при циррозе печени, требующие проведения диагностического парацентеза:
прогрессирование печеночной энцефалопатии (ПЭ);
наличие признаков кровотечения из варикозно расширенных вен (пищевода, желудка, прямой кишки);
признаки системной воспалительной реакции (лихорадка, озноб, лейкоцитоз, сдвиг лейкоцитарной формулы влево, повышение уровня С-реактивного белка, увеличение скорости оседания эритроцитов, положительный результат прокальцитонинового теста, положительный рост культуры сыворотки);
признаки развития гепаторенального синдрома (ГРС).
2.3. Диагностика спонтанного бактериального перитонита
(А1) При проведении диагностического парацентеза должна быть осуществлена диагностика на предмет исключения спонтанного бактериального перитонита (СБП). СБП устанавливается при наличии следующих критериев:
абсолютное число нейтрофильных лейкоцитов > 250/мм 3 ;
определение положительного роста культуры при посеве асцитической жидкости;
снижение уровня белка в асцитической жидкости 0,4 свидетельствует в пользу панкреатического генеза асцита, наличия перфорации полого органа);
билирубина (дифференциальная диагностика с перфорацией билиарного тракта);
триглицеридов (травма лимфатического протока);
лактатдегидрогеназы (дифференциальная диагностика с воспалительным процессом в брюшной полости, онкопатологией).
3. Лечение пациентов с циррозом печени при наличии асцита
3.1. (В1) Наличие асцита 2–3-й степени требует обсуждения хирургической тактики
Все пациенты с асцитом 2–3-й степени рассматриваются для проведения трансъюгулярного шунтирования (transjugular intrahepatic portosystemic shunt – TIPS) как метода хирургического симптоматического лечения. Донорская или ортотопическая трансплантация – радикальный метод лечения пациентов данной категории. Поскольку асцит резко ухудшает прогноз, следует объективно оценивать состояние больного и предпринимаемые консервативные методы лечения. При неэффективности терапии пациент должен получать лечение в условиях палаты/отделения интенсивной терапии, а также быть поставлен в лист ожидания трансплантации печени.
3.2. (В1) Ограничение потребления соли
У пациентов с циррозом печени, осложненным асцитом, ограничивают потребление соли до 6,9 г/сут. Данное количество рассматривается в качестве эквивалента неупотребления соли как нутритивного компонента.
3.3. Терапия, которая должна быть назначена пациенту с циррозом печени, осложненным асцитом
3.3.1. Адекватная диуретическая терапия
При подборе схемы диуретической терапии должны быть учтены степень асцита, наличие признаков диуретико-ассоциированных осложнений.
3.3.2. Адекватная антибиотикотерапия
Профилактически антибиотики должны быть назначены всем пациентам с асцитом при отсутствии признаков СБП и пациентам с купированными признаками СБП. Препаратом выбора является норфлоксацин 400 мг/сут. Альтернативными препаратами считаются ципрофлоксацин 750 мг 1 раз/нед или ко-тримоксазол (сульфаметоксазол 800 мг/сут + триметоприм 160 мг/сут).
В случае подтверждения СБП эмпирическая антибиотикотерапия назначается незамедлительно. Препаратами выбора являются цефалоспорины третьего и четвертого поколения в дозе 4 г/сут с обязательным проведением повторного диагностического парацентеза через 48 часов и на пятые сутки применения антибиотиков с целью контроля эффективности антибиотикотерапии. При неэффективности применяемых препаратов антибиотик меняют в соответствии с принятыми терапевтическими канонами.
В случае низкого содержания белка в асцитической жидкости ( 2 кг в течение недели, но 2 кг в течение недели, но 6 ммоль/л).
При неэффективности первой линии терапии показано применение второй линии диуретической терапии.
3.3.8.5. (А1) Вторая линия диуретической терапии – добавление к максимальной дозе спиронолактона (400 мг/сут) препарата фуросемид:
начальная доза фуросемида – 40 мг утром;
пошаговое увеличение дозы фуросемида на 40 мг один раз в неделю;
максимальная доза фуросемида – 160 мг/сут.
3.3.8.6. (А1) Признаки эффективности диуретической терапии второй линии:
снижение массы тела > 2 кг в течение недели, но 2 кг в течение недели, но 2 кг в течение недели, но 2 кг в течение недели, но 5 л) при условии показателя МНО 40 000/мкл;
обязательное условие: замещение альбумином (8 г альбумина/1 л эвакуированной асцитической жидкости);
доза диуретиков в день проведения одноэтапного лечебного парацентеза должна быть минимальной, в дальнейшем корректируется в зависимости от степени асцита.
3.3.8.13. (В1) Цель диуретической терапии – купирование асцита на минимальной дозе диуретических препаратов.
3.3.9. Диуретическая терапия: правила отмены
Диуретическая терапия верошпироном должна быть прекращена при повышении калия сыворотки > 6 ммоль/л.
Диуретическая терапия фуросемидом должна быть прекращена при снижении калия сыворотки 6 ммоль/л).
Асцит – практически неминуемое осложнение при естественном течении цирроза печени. Это указывает на неблагоприятный прогноз основного заболевания. Медико-социальная значимость асцита очевидна в силу высокой вероятности летального исхода у пациентов с циррозом печени. Именно поэтому в основу разработки национального руководства по ведению больных с этим заболеванием легли принципы доказательной медицины, предусматривающие наиболее эффективные методы диагностики и лечения. В течение последних лет cтановление практических рекомендаций для врачей претерпело множество правок, и данные, приведенные в этой статье, сводят воедино принципы дифференциальной диагностики, правила назначения терапии, критерии эффективности применяемого лечения и вопросы, связанные с неэффективностью консервативных мероприятий. Учитывая существующие реалии, врачам, курирующим пациентов с декомпенсированными заболеваниями печени, видимо, следует решать вопрос о постановке больного в лист ожидания трансплантации в РФ сразу после диагностирования первого эпизода асцита.