Что такое cl2 в химии
Физические свойства
6,5 г/л); х. р. в неполярных органических растворителях. В свободном виде встречается только в вулканических газах.
Способы получения
Промышленный
Лабораторные
Окисление конц. HCI различными окислителями:
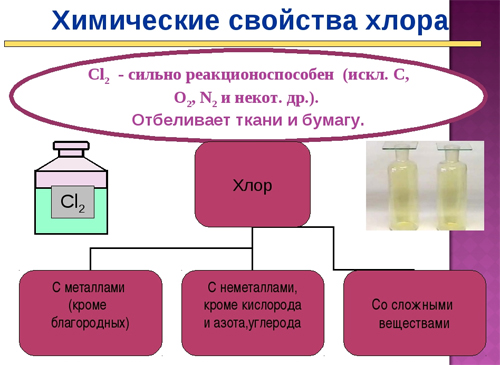
Химические свойства
Реакции с металлами
Активные металлы в атмосфере сухого газообразного хлора воспламеняются и сгорают; при этом образуются хлориды металлов.
Малоактивные металлы легче окисляются влажным хлором или его водными растворами:
Реакции с неметаллами
Хлор непосредственно не взаимодействует только с O2, N2, С. С остальными неметаллами реакции протекают при различных условиях.
Образуются галогениды неметаллов. Наиболее важной является реакция взаимодействия с водородом.
Вытеснение свободных неметаллов (Вr2, I2, N2, S) из их соединений
Диспропорционирование хлора в воде и водных растворах щелочей
Cl2 + Н2O = HCl + НClO хлорноватистая к-та
Эти реакции имеют важное значение, поскольку приводят к получению кислородных соединений хлора:
Взаимодействие хлора с органическими веществами
а) замещение атомов водорода в молекулах ОВ
б) присоединение молекул Cl2 по месту разрыва кратных углерод-углеродных связей
Хлороводород и соляная кислота
Газообразный хлороводород
Физические и химические свойства
Газообразный HCl широко используется в органическом синтезе (реакции гидрохлорирования).
Способы получения
1. Синтез из простых веществ:
2. Образуется как побочный продукт при хлорировании УВ:
3. В лаборатории получают действием конц. H2SO4 на хлориды:
H2SО4(конц.) + NaCl = 2HCl↑ + NaHSО4 (при слабом нагревании)
H2SО4(конц.) + 2NaCl = 2HCl↑ + Na2SО4 (при очень сильном нагревании)
HCl очень хорошо растворяется в воде: при об. Т в 1 л Н2O растворяется
450 л газа (растворение сопровождается выделением значительного количества тепла). Насыщенный раствор имеет массовую долю HCl, равную 36-37 %. Такой раствор имеет очень резкий, удушающий запах.
Молекулы HCl в воде практически полностью распадаются на ионы, т. е. водный раствор HCl является сильной кислотой.
Химические свойства соляной кислоты
1. Растворенный в воде HCl проявляет все общие свойства кислот, обусловленные присутствием ионов Н +
а) с металлами (до Н):
б) с основными и амфотерными оксидами:
в) с основаниями и амфотерными гидроксидами:
г) с солями более слабых кислот:
Уравнения реакция см. «Получение хлора». Особое значение имеет ОВР между соляной и азотной кислотами:
Реакции с органическими соединениями
а) с аминами (как органическими основаниями)
б) с аминокислотами (как амфотерными соедимнеиями)
Оксиды и оксокислоты хлора
Основные сведения о хлоре как химическом элементе
История открытия хлора
Хлор — химический элемент с атомным номером 17. Принадлежит к 17-й группе периодической таблицы химических элементов, находится в третьем периоде таблицы. Обозначается символом Cl. Активный неметалл. Галоген. Молекула хлора состоит из двух атомов. Кристаллическая решетка хлора ромбическая. Молярная масса хлора (M (Cl)) составляет 35,446-35,457 г/моль.
Ковалентная связь хлора:
В 1772 году Джозеф Пристли впервые получил первое соединение с хлором — газообразный хлороводород.
В 1774 году хлор был получен шведским ученым Вильгельмом Шееле, который описал выделение хлора при взаимодействии пиролюзита с соляной кислотой: 4 H C l + M n O 2 = C l 2 + M n C l 2 + 2 H 2 O
Шееле вывел хлор со следующими характеристиками:
Однако Вильгельм, используя теорию флогистона, сделал предположение о том, что хлор состоит из дефлогистированной муриевой (соляной) кислоты.
В 1810 году Г. Дэви с помощью процесса электролиза разложил поваренную соль на хлор и натрий, тем самым доказав элементарную природу хлора. В 1811 году ученый предложил новое название для элемента — «хлорин». А спустя год Ж. Гей-Люссак доработал окончательное название, которое мы используем по сей день — хлор. В 1811 также Иоганн Швейгер хотел предложить для хлора название галоген, но вскоре для всей 17 группы элементов закрепился этот термин.
В 1826 году химиком Йёнсом Якобом Берцелиусом была определена точная атомная масса хлора 35,446. 35,457 а. е. м
Физические и химические свойства
К физическим свойствам хлора относят:
К химическим свойствам относят:
C l 2 + 2 H B r → B r 2 + 2 H C l — при таких реакциях хлор вытесняет бром из соединений с водородом или металлом;
2 N a + C l 2 → 2 N a C l — при взаимодействии натрия и хлора мы получаем хлорид натрия;
2 F e + 3 C l 2 → 2 F e C l 3 — при взаимодействии железа и хлора мы получим хлорид железа(III);
C l 2 + H 2 O ⇄ H C l + H C l O
C l 2 + 2 N a O H → N a C l + N a C l O + H 2 O ;
H 2 + C l 2 → 2 H C l ;
Строение электронной оболочки
Электронная оболочка — совокупность всех электронов в атоме, которые окружают ядро.
На валентном уровне атома хлора содержится 1 неспаренный электрон: 1s2 2s2 2p6 3s2 3p5. За счет присутствия в атоме хлора незанятой орбитали d-подуровня, атом хлора может проявлять и прочие степени окисления.
Обратимся к схеме возбужденных состояний атомов хлора:
| Валентность | Возможные степени окисления | Электронное состояние валентного уровня | Пример соединений |
|---|---|---|---|
| I | +1, −1, 0 | 3s2 3p5 | NaCl, NaClO, Cl2 |
| III | +3 | 3s2 3p4 3d1 | NaClO2 |
| V | +5 | 3s2 3p3 3d2 | KClO3 |
| VII | +7 | 3s1 3p3 3d3 | KClO4 |
Нахождение в природе
Биологическая роль хлора
Ионы хлора жизненно необходимы растениям, потому что они участвуют в энергетическом обмене у растений. Человек потребляет 5-10 г NaCl в сутки. Каждый день с пищей человек получает 3-6 г хлора, что абсолютно покрывает потребность в этом элементе откуда-либо из внешней среды.
Хлорные каналы присутствуют во многих типах митохондриальных мембран, скелетных мышцах и клетках. Эти каналы выполняют исключительные функции в нормализации объема жидкости, участвуют в поддержании кислотно-щелочного баланса — рН клеток. Всасывание хлора происходит в толстой кишке.
Получение и применение хлора
Получение хлора в химии
Хлор, который производят, хранится в специальных «танках» или закачивается в стальные баллоны высокого давления. Баллоны с жидким хлором под давлением имеют специальную окраску — болотный цвет.
В настоящее время химические методы получения хлора не используют, так как они являются очень ресурсозатратными и малоэффективными.
Метод Дикона
В 1867 году ученым химиком Диконом был разработан метод получения хлора каталитическим окислением хлороводорода кислородом воздуха: 4 H C l + O 2 → 2 H 2 O + 2 C l 2 ↑
Современные лабораторные методы
На данный момент хлор используется в лабораториях в баллонах.
Для того чтобы получить небольшое количество хлора, обычно используют процессы, основанные на окислении хлороводорода более сильными окислителями. Чаще всего это перманганат калия или диоксид марганца: 2 K M n O 4 + 16 H C l → 2 K C l + 2 M n C l 2 + 5 C l 2 ↑ + 8 H 2 O
Электрохимические методы
При невозможности использования сжиженного хлора в баллонах, используют электрохимические методы.
В промышленности применяются три варианта электрохимического метода: два из них — электролиз с твердым катодом, третий — электролиз с жидким ртутным катодом (ртутный метод производства). При таких методах качество получаемого хлора почти не отличается.
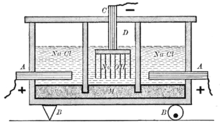
Мембранный метод
Мембранный метод производства хлора наиболее энергоэффективен, но при этом довольно сложен в организации и эксплуатации.
В мембранном методе катодное и анодное пространства полностью разделены непроницаемой для анионов катионообменной мембраной. Поэтому в мембранном электролизере два потока.
В анодное пространство поступает поток раствора соли. А в катодное — деионизированная вода. Все потоки предварительно очищаются от всевозможных примесей.
Применение хлора
Реакции с органическими веществами
Замещение атомов водорода в молекулах О В :
Ароматические соединения замещают атом водорода на хлор в присутствии катализаторов: C 6 H 6 + C l 2 → C 6 H 5 C l + H C l
Особенности работы с хлором
Хлор (Cl, Chlorine)
История хлора
В 1774 году Карл Шееле, химик из Швеции, впервые получил хлор, но считалось, что это не отдельный элемент, а разновидность соляной кислоты (calorizator). Элементарный хлор был получен в начале XIX века Г. Дэви, который разложил поваренную соль на хлор и натрий путём электролиза.
Общая характеристика хлора
Хлор (от греческого χλωρός – зелёный) является элементом XVII группы периодической таблицы химических элементов Д.И. Менделеева, имеет атомный номер 17 и атомную массу 35,452. Принятое обозначение Cl ( от латинского Chlorum).
Нахождение в природе
Хлор является самым распространённым в земной коре галогеном, чаще всего в виде двух изотопов. В силу химической активности встречается лишь в виде соединений многих минералов.
Физические и химические свойства
Хлор является ядовитым жёлто-зелёным газом, имеет резкий неприятный запах и сладковатый вкус. Именно хлор после его открытия предложили называть галогеном, в одноимённую группу он входит как один из самых химически активных неметаллов.
Суточная потребность в хлоре
В норме взрослый здоровый человек должен получать в сутки 4-6 г хлора, потребность в нём возрастает при активных физических нагрузках или жаркой погоде (при повышенном потоотделении). Обычно суточную норму организм получает из продуктов питания при сбалансированном рационе.
Продукты питания богатые хлором
Основным поставщиком хлора в организм является поваренная соль – особенно, если она не подвергается термической обработке, поэтому лучше солить уже готовые блюда. Также хлор содержат яйца, морепродукты, мясо, горох, фасоль и чечевица, гречка и рис, оливки.
Взаимодействие с другими
Кислотно-щелочной и водный баланс организма регулируется калием, натрием и хлором.
Признаки нехватки хлора
Нехватка хлора вызвана процессами, приводящими к обезвоживанию организма – сильное потоотделение в жару или при физических нагрузках, рвота, диарея и некоторые заболевания моче-выделительной системы. Признаками недостатка хлора являются вялость и сонливость, слабость в мышцах, явная сухость во рту, потеря вкусовых ощущений, отсутствие аппетита.
Признаки избытка хлора
Признаками избытка хлора в организме являются: повышение кровяного давления, сухой кашель, боль в голове и в груди, резь в глазах, слезотечение, расстройства деятельности желудочно-кишечного тракта. Как правило, переизбыток хлора может быть вызван употреблением обычной воды из-под крана, которая проходит процесс дезинфекции хлором и случается у работников тех отраслей промышленности, которые напрямую связаны с использованием хлора.
Полезные свойства хлора и его влияние на организм
Хлор в организме человека:
Применение хлора в жизни
Основное применение хлора – химическая промышленность, где с его помощью изготавливают поливинилхлорид, пенопласт, материалы для упаковки, также боевые отравляющие вещества и удобрения для растений. Обеззараживание питьевой воды хлором – практически единственный доступный способ очистки воды.
Что такое cl2 в химии
Хлор / Chlorum (Cl), 17
3,214 г/л;
(жид. при −35 °C) 1,557;
(тв. при −105 °C) 1,9 г/см³
172,2 K ( Ошибка выражения: неопознанный символ пунктуации « »°C)
238,6 K ( Ошибка выражения: неопознанный символ пунктуации « »°C)
Простое вещество хлор (CAS-номер: 7782-50-5) при нормальных условиях — ядовитый газ желтовато-зелёного цвета тяжелее воздуха, с резким запахом. Молекула хлора двухатомная (формула Cl2).
Содержание
История открытия хлора
Соединение с водородом — газообразный хлороводород — было впервые получено Джозефом Пристли в 1772 г. Хлор был получен в 1774 г. шведским химиком Карлом Вильгельмом Шееле, описавшим его выделение при взаимодействии пиролюзита с соляной кислотой в своём трактате о пиролюзите:
Шееле отметил запах хлора, схожий с запахом царской водки, его способность взаимодействовать с золотом и киноварью, а также его отбеливающие свойства. Однако Шееле, в соответствии с господствовавшей в химии того времени теории флогистона, предположил, что хлор представляет собой дефлогистированную муриевую (соляную) кислоту. Бертолле и Лавуазье в рамках кислородной теории кислот обосновали, что новое вещество должно быть оксидом гипотетического элемента мурия. Однако попытки его выделения оставались безуспешными вплоть до работ Дэви, которому электролизом удалось разложить поваренную соль на натрий и хлор, доказав элементарную природу последнего.
Распространение в природе
В природе встречаются два изотопа хлора 35 Cl и 37 Cl. В земной коре хлор самый распространённый галоген. Хлор очень активен — он непосредственно соединяется почти со всеми элементами периодической системы. Поэтому в природе он встречается только в виде соединений в составе минералов: галита NaCl, сильвина KCl, сильвинита KCl · NaCl, бишофита MgCl2 · 6Н2О, карналлита KCl · MgCl2 · 6Н2O, каинита KCl · MgSO4 · 3Н2О. Самые большие запасы хлора содержатся в составе солей вод морей и океанов (содержание в морской воде 19 г/л [4] ). На долю хлора приходится 0,025 % от общего числа атомов земной коры; кларковое число хлора — 0,017 %. Человеческий организм содержит 0,25 % ионов хлора по массе. В организме человека и животных хлор содержится в основном в межклеточных жидкостях (в том числе в крови) и играет важную роль в регуляции осмотических процессов, а также в процессах, связанных с работой нервных клеток.
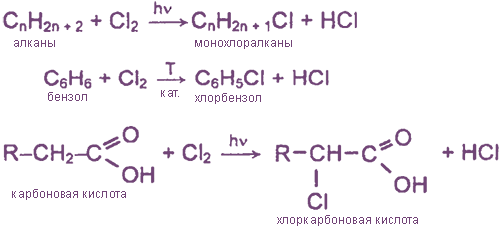
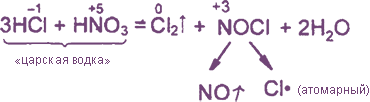































 — основной процесс
— основной процесс 
 Катод:
Катод:  — основной процесс
— основной процесс 






