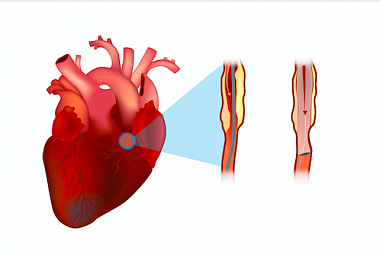
Чем опасно стентирование сосудов сердца
Что делать после стентирования
В сосудистой хирургии все чаще используют малотравматичные рентгеноэндоваскулярные методики. Благодаря таким методам удалось сократить восстановительный период для пациентов, но больные часто забывают, что любое хирургическое вмешательство меняет жизнь. Очень важно не отказываться от госпитализации и соблюдать все врачебные рекомендации в постреабилитационный период. Досрочная выписка и игнорирование схемы лечения после сердечно-сосудистых операций увеличивают риск инфаркта в два раза. Сегодня мы поговорим о том, что нельзя делать после стентирования сосудов сердца и какой образ жизни показан прооперированным.
Как проводят стентирование сосудов сердца
Стент — это крошечная ячеистая конструкция, состоящая из различных металлов и сплавов, совместимых с человеческим организмом. По этой причине трубка не отторгается иммунной системой и хорошо приживается, со временем образуя с сосудом единое целое. До операции стенты в сложенном виде располагаются в баллонах. Стентирование совмещается с ангиопластикой.
Во время ангиопластики введенный в сосуд баллон устраняет атеросклеротическую бляшку, после чего происходит стентирование – размещение в нужном месте сосуда сетчатой конструкции. Операция не требует разрезов: катетер с баллоном вводится через прокол артерии.
Стенты отличаются не только материалами изготовления, но и моделями, размерами, диаметром, а также покрытием. Некоторые модели покрыты фармакологическим препаратом, который высвобождается в течение некоторого времени, предотвращая риск роста внутренней оболочки сосуда, следовательно, и рецидива стеноза. Если вам провели стентирование, придерживайтесь рекомендаций врача — от действий пациента во многом зависит прогноз выздоровления. В 95 % случаев наблюдаются успешные результаты операции.
Что делать после стентирования
Для профилактики осложнений пациент остается несколько дней под наблюдением врачей, а затем выписывается. Стоит помнить: операция не дает гарантий, что сосуд снова не сузится. По этой причине больные обязательно должны наблюдаться у кардиолога.
Что делать после стентирования сосудов сердца:
Чаще всего после операции давление у больных повышается, но бывает и обратная ситуация. Что делать, если после стентирования низкое давление? В первую очередь, таким больным необходим покой, в том числе эмоциональный. Для нормализации АД можно выпить крепкий чай. Пропуск или отмена лекарств могут сказаться на динамике выздоровления, поэтому при гипотонии нужно записаться на прием к лечащему кардиологу и скорректировать терапию.
Что нельзя делать после стентирования:
МРТ делают после того, как конструкция приживется. Стент содержит металлы, а аппарат МРТ— это большой магнит. Из-за магнитного поля стент может смеситься. По прошествии полугода исследование не представляет опасности и даже показано для контроля состояния конструкции. Однако рентгенолога необходимо предупредить о наличии других металлических протезов в организме. Поскольку модели имеют отличия, в инструкции к каждой указано, по истечении какого срока можно проходить МРТ. Клиника, проводящая операцию, должна выдать пациенту документ с указанием, какой стент был установлен. Многих пациентов интересует, можно ли делать КТ после стентирования. Компьютерная томография, как и МРТ, разрешена через время после хирургического вмешательства.
Что нельзя делать после стентирования сосудов
Один из факторов риска после операции — сгущение крови. Поэтому нужно избегать ситуаций, провоцирующих такое состояние. Не стоит посещать баню, усиленно тренироваться и простужаться (высокая температура влияет на показатели крови).
Многие прооперированные первое время ощущают слабость и сонливость. Но это не повод отказываться от активности. Чтобы вернуться к привычному образу жизни, необходимо увеличить физические нагрузки до разумного предела: заниматься скандинавской ходьбой, плавать, ездить на велосипеде. Нагрузки тренируют сердечную мышцу, помогают стабилизировать АД и, в целом, положительно сказываются на общем самочувствии. Травмоопасных видов спорта лучше избегать, а умеренные нагрузки показаны до 5 раз в неделю.
Пациентам придется навсегда отказаться от курения, снизить количество соли в пище, избегать жирной и копченой еды, кофеина. Диета — одна из составляющих ЗОЖ и важна не меньше физических упражнений.
Установка стентов – не чудесное исцеление
Простота и безболезненность эндоваскулярной методики, быстрое восстановление и разительное улучшение самочувствия создают у пациентов иллюзию полнейшего выздоровления. Однако стентирование — это процедура, направления на устранение симптомов. Основную болезнь, вызвавшую закупорку сосудов, необходимо грамотно лечить и чаще всего пожизненно. Атеросклероз и ИБС без должной терапии продолжают прогрессировать и создавать новые риски, в том числе опасность рестеноза. Необходимо помнить, что объем лекарств после операции не уменьшится, дополнительно добавится антитромбоцитарная терапия.
Чтобы получить квалифицированную медицинскую помощь и рекомендации о том, что нельзя делать после стентирования сосудов сердца, обращайтесь в «Октябрьским сосудистый центр» республики Башкортостан. Здесь операции выполняют опытные сосудистые хирурги, а после хирургического вмешательства все пациенты получают план лекарственной терапии и консультации по правильному образу жизни во время и после реабилитации.
Влияние стентирования коронарных артерий на электрическую нестабильность у больных с острым инфарктом миокарда
В данной статье рассмотрены результаты исследования влияния стентирования коронарных артерий на электрическую нестабильность миокарда с помощью оценки вариабельности сердечного ритма и дисперсионного картирования.
Электрическая нестабильность миокарда – физиологическое понятие характеризующее патофизиологический механизм возникновения нарушений сердечного ритма манифестирующийся различными аритмиями (суправентрикулярные и желудочковые экстрасистолы).
Поиск новых методов оценки нарушений сердечного ритма и/или их предикторов является научной и практической задачей в современной кардиологии [1, 2].
Анализ ВСР является методом оценки состояния механизмов регуляции физиологических функций в организме человека и животных. В общей активности регуляторных механизмов, нейрогуморальной регуляции сердца, соотношения между симпатическим и парасимпатическим отделами вегетативной нервной системы является одной из причин нарушений сердечного ритма [1, 2, 3].
Текущая активность симпатического и парасимпатического отделов является результатом реакции многоконтурной и многоуровневой системы регуляции кровообращения, изменяющей во времени свои параметры для достижения оптимального приспособительного ответа, который отражает адаптационную реакцию целостного организма.
Адаптационные реакции индивидуальны и реализуются у разных лиц с различной степенью участия функциональных систем, которые обладают в свою очередь обратной связью, изменяющейся во времени и имеющей переменную функциональную организацию. Метод основан на распознавании и измерении временных интервалов между R-зубцами ЭКГ (R-R–интервалы), построении динамических рядов кардиоинтервалов и последующего анализа полученных числовых рядов различными математическими методами. Динамический ряд кардиоинтервалов называют кардиоинтервалограммой (КИГ) [4, 5].
Динамический ряд кардиоинтервалов может быть отнесен к числу стационарных или нестационарных. Стационарными называют случайные процессы, протекающие приблизительно однородно и имеющие вид непрерывных колебаний вокруг некоторого среднего значения. Стационарные процессы характеризуются эргодичностью, т. е. усреднение по времени соответствует усреднению по множеству реализаций. Иными словами на любом участке времени мы должны получать одни и те же характеристики. Нестационарные ( или переходные) процессы имеют определенную тенденцию развития во времени и их характеристики зависят от в начала отсчета. Практически в каждой кардиоинтервалограмме содержатся элементы нестационарности (фрактальные компоненты). В данных методических рекомендациях кардиоинтервалограмма рассматривается как стационарный случайный процесс с соответствующей интерпретацией получаемых в результате ее анализа данных. Для оценки фрактальных компонентов кардиоинтервалограммы в последние годы активно развиваются методы нелинейной динамики [6].
Материал и методы исследования
С целью оценки влияния стентирования коронарных артерий на изменение электрической нестабильности миокарда было проанализировано 32 пациента. Все пациенты разделены на группы: основная – 19 пациентов перенесших острый инфаркт миокарда, которым было выполнено стентирование коронарных артерий, контрольная группа – 13 пациентов изначально здоровых мужчин. Возраст больных был от 43 до 92 лет. В основном пострадавшие были мужчины 14 человек и 5 женщин. Использовался контингент больных находящихся на лечении в отделении ОРИТ «Клинической Больницы №1» УД Президента РФ (Волынская). В отделении больные инфарктом миокарда в первые сутки болезни выполнено ЧКВ, исследование ритма сердца проводилось при поступлении в стационар и сразу после выполненного стентирования коронарных артерий. В последующем отдаленные результаты оценивались через 7 дней. Рентгенэндоваскулярное вмешательство проводилось под руководством профессора Закаряна Н. В. [4, 9].
Для анализа вариабельности сердечного ритма (ВСР) и дисперсионного картирования электрокардиограммы впервые использовался аппаратно-программный комплекс «Кардиовизор-06с». Для оценки ВСР использовались 5-минутные записи R-R интервалов ритма сердца.
Результаты исследований и их обсуждения
Электрофизиологические показатели вариабельности сердечного ритма у исследуемых
Поздние осложнения чрескожных коронарных вмешательств
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
По данным Всемирной организации здравоохранения, сердечно-сосудистые заболевания занимают первое место в мире в структуре причин смертности. В настоящее время стандартом интервенционного лечения пациентов с атеросклеротическим поражением коронарных артерий является чрескожное коронарное вмешательство (ЧКВ). Внедрение в клиническую практику стентов второго поколения с лекарственным покрытием (СЛП) позволило увеличить эффективность и безопасность ЧКВ за счет уменьшения выраженности воспалительных изменений, а также увеличения скорости заживления и эндотелизации артерии в месте имплантации стента. Однако техника и технология вмешательства сами по себе препятствуют полному восстановлению структуры и функции сосудов и сопряжены с риском отсроченного нарушения функции стента. У пациентов, перенесших ЧКВ с имплантацией СЛП, сохраняется риск поздних осложнений стентирования (тромбоза стента, рестеноза, неоатеросклероза и кровотечения), информация о которых представлена в настоящем обзоре. Важную роль в патогенезе острого коронарного синдрома после стентирования, а также в рецидивировании клинических симптомов после ЧКВ играет неоатеросклероз. Расширенная коронарная визуализация и длительная двойная антитромбоцитарная терапия, возможно, будут иметь фундаментальное значение для дальнейшего понимания и лечения этого процесса.
Ключевые слова: ишемическая болезнь сердца, чрескожное коронарное вмешательство, стент с лекарственным покрытием, рестеноз коронарных артерий, тромбоз стента, кровотечение.
Для цитирования: Шумаков Д.В., Шехян Г.Г., Зыбин Д.И. и др. Поздние осложнения чрескожных коронарных вмешательств. РМЖ. 2020;10:25-28.
Late complications of percutaneous coronary interventions
D.V. Shumakov, G.G. Shekhyan, D.I. Zybin, A.A. Yalymov, E.V. Stepina, M.A. Popov
Moscow Regional Clinical Research Institute named after M.F. Vladimirsky, Moscow
According to the World Health Organization, cardiovascular diseases occupy first place in the world as the causes of fatal outcomes. At present, percutaneous coronary intervention (PCI) is the standard treatment regimen of patients with atherosclerotic lesions of the coronary arteries. The introduction of second-drug-eluting stents (SDES) into clinical practice has increased the efficacy and safety of PCI by reducing the severity of inflammatory changes, as well as increasing the rate of regeneration and endothelization of the artery at the stent implantation site. However, the technique and technology of intervention itself prevent the complete regeneration of vascular structure and function and are associated with the risk of late stent dysfunction. Patients who have undergone PCI with SDES implantation remain at risk of late stenting complications (stent thrombosis, restenosis, neoa therosclerosis and bleeding), which are described in this review. Neoatherosclerosis plays an important role in the pathogenesis of acute coronary syndrome after stenting, as well as the recurrence of clinical symptoms after PCI. Advanced cardiac imaging and long-term dual antiplatelet therapy may be of fundamental importance for further understanding and treatment of this pathological process.
Keywords: coronary heart disease, percutaneous coronary intervention, drug-eluting stents, restenosis, stent thrombosis, bleeding.
For citation: Shumakov D.V., Shekhyan G.G., Zybin D.I. et al. Late complications of percutaneous coronary interventions. RMJ. 2020;10:25–28.
Введение
По данным Всемирной организации здравоохранения, сердечно-сосудистые заболевания занимают первое место в мире в структуре причин смертности [1]. В Российской Федерации ишемическая болезнь сердца (ИБС) встречается у 13,5% населения [2], при этом 44,9% случаев смерти от всех причин у женщин и 55,4% у мужчин приходится именно на пациентов с ИБС (14% у лиц трудоспособного возраста) [3]. В настоящее время в лечении ИБС одно из ведущих мест занимает чрескожное коронарное вмешательство (ЧКВ) с имплантацией стента, которое ежегодно выполняется не менее чем у 5 млн пациентов во всем мире [4]. Внедрение в повседневную клиническую практику стентов с лекарственным покрытием (СЛП) второго поколения, которые в значительной степени заменили голометаллические стенты (ГМС), способствовало уменьшению выраженности воспалительных изменений, а также увеличению скорости заживления и эндотелизации артерии в месте имплантации стента [5]. Как следствие, при использовании СЛП наблюдалось снижение частоты осложнений, связанных со стентированием, что способствовало расширению показаний к ЧКВ. Однако проблема безопасности вмешательства остается актуальной. Настоящий обзор посвящен наиболее часто встречающимся поздним осложнениям стентирования: тромбоз стента (ТС), рестеноз, неоатеросклероз и кровотечение.
Тромбоз стента
Под ТС подразумевается его тромботическая окклюзия [6]. ТС относится к большим осложнениям ЧКВ и ассоциирован с высоким риском заболеваемости и смертности. В отличие от рестеноза, на фоне которого могут возникать симптомы, характерные для стабильной стенокардии, ТС является острым процессом, который обычно манифестирует в виде острого коронарного синдрома (ОКС). Определение и классификация ТС представлены в таблице 1 [7].
По данным ранних публикаций [8, 9], ТС после ЧКВ отмечался в 16% случаев, при этом показатель 30-дневной смертности составлял 15–30%. По крайней мере отчасти, подобные результаты были обусловлены низкоэффективными схемами профилактики ТС (препараты ацетилсалициловой кислоты, дипиридамол, декстран). С совершенствованием методов стентирования и внедрением двойной антитромбоцитарной терапии (ДАТ) в клиническую практику наблюдалось выраженное снижение частоты ТС до 0,7% в течение 1 года и 0,2–0,6% в течение последующего наблюдения [10–12]. Распространенность ТС при плановом ЧКВ составляет 0,3–0,5% и увеличивается до 3,4% при ОКС. Не получено статистически значимых различий в отношении частоты ТС при использовании ГМС и СЛП. Однако для ГМС по сравнению с СЛП характерно более раннее развитие тромбоза (первые 30 дней с момента вмешательства по сравнению с 3 мес. и более) [13].
В крупных рандомизированных исследованиях и регистрах были идентифицированы факторы, ассоциированные с ТС. Так, в исследовании CHAMPION-PHOENIX инфаркт миокарда с подъемом и без подъема сегмента ST на момент поступления, ангиографические характеристики тромботических поражений и длина стента являлись независимыми предикторами острого ТС [14]. В исследовании ACUITY была установлена ассоциация между сахарным диабетом (СД), почечной недостаточностью, количеством баллов по шкале Duke Jeopardy score, минимальным диаметром просвета стента, назначением тиенопиридинов в предоперационном периоде, исходным уровнем гемоглобина, протяженностью поражений коронарных артерий и ранним ТС [15]. В субанализе HORIZONS-AMI при использовании внутрисосудистого ультразвукового исследования (ВСУЗИ) были идентифицированы следующие предикторы ТС: площадь поперечного сечения менее 5 мм, некорректное позиционирование стента, пролапс или протрузия атеросклеротической бляшки, краевая диссекция, резидуальный стеноз и бифуркационное стентирование [16]. В исследовании Triton-TIMI 38 инфаркт миокарда с подъемом сегмента ST был ассоциирован с более высоким риском ТС, который снижался на 50% при использовании некоторых антитромбоцитарных препаратов [17].
В настоящее время особое внимание уделяется позднему и очень позднему ТС. Если при развитии острого и подострого ТС основную роль, по-видимому, играют анатомические особенности коронарного русла, а также техники и технологии стентирования, то механизм отсроченных тромботических явлений представляется более сложным [18, 19]. В исследованиях идентифицированы следующие факторы риска позднего и очень позднего ТС: СД, ОКС во время исходной процедуры, почечная недостаточность, пожилой возраст, снижение фракции выброса левого желудочка, сердечно-сосудистые осложнения в течение 30 дней после исходной процедуры. Особенности ангиопластики (малый размер сосуда, бифуркационное стентирование, многососудистое поражение, наличие кальцификаций и окклюзий, использование длинных стентов), скорее всего, ассоциированы с поздним ТС как для ГМС, так и для СЛП. Риск ТС увеличивается при нарушениях, связанных с ДАТ: несоблюдение режима приема препаратов, субоптимальная дозировка, лекарственные взаимодействия, коморбидный фон, генетический полиморфизм. К позднему ТС также могут приводить неоатеросклероз (НА) в стенте и поздние реакции гиперчувствительности.
Рестеноз
Применение коронарных стентов позволило улучшить прогноз при ЧКВ по сравнению с изолированной баллонной ангиопластикой, которая сопровождалась как механическими осложнениями (окклюзия, диссекция и т. д.), так и высокой частотой рестенозов (до 40–50%). К концу 1990-х гг. до 70% ЧКВ выполнялись с имплантацией ГМС [20]. Несмотря на совершенствование технологий вмешательства и медикаментозной терапии, риск рестеноза после имплантации ГМС оставался достаточно высоким и составлял около 20%, и внедрение в клиническую практику СЛП позволило дополнительно снизить частоту рестенозов [21, 22].
Одним из наиболее важных предикторов рестенозов является СД (табл. 2). Так, у пациентов с СД, перенесших имплантацию ГМС, риск развития рестеноза увеличивается на 30–50% [23]. При этом применение СЛП у больных с СД также не позволяет полностью предотвратить данное осложнение. Механизм формирования рестеноза при СД, вероятно, является комплексным и включает в себя как системные (например, вариабельность воспалительного ответа), так и анатомические (например, стентирование сосудов малого диаметра; протяженность и диффузный характер поражений) факторы [24]. Также на распространенность рестенозов независимо влияют диаметр сосуда и протяженность поражения [22]. Кроме того, при длине стента свыше 35 мм (по сравнению с длиной менее 20 мм) наблюдалось практически двукратное увеличение частоты рестеноза. Немаловажную роль играет минимальный диаметр просвета стента [25].
Неоатеросклероз
НА называют процесс трансформации нормального слоя интимы в атерогенную неоинтиму внутри стента. Процесс опосредован накоплением липидных макрофагов и в некоторых случаях сопровождается кальцификацией в области стентирования [26]. В отличие от атеросклероза в нативных коронарных артериях, прогрессирующего в течение десятилетий, формирование неоинтимы после ЧКВ происходит в течение нескольких месяцев — нескольких лет [27].
НА в стенте проявляется инфильтрацией и апоптозом макрофагов и последующим образованием некротического ядра [28]. Точная причина высокой скорости процесса в настоящее время не установлена, однако предложено несколько механизмов, в т. ч. неполное эндотелиальное покрытие, приводящее к эндотелиальной дисфункции. На фоне данного процесса, преимущественно после имплантации СЛП, нарушается формирование клеточных соединений, снижаются экспрессия антитромботических молекул и продукция оксида азота. Кроме того, при НА имеет место проникновение липопротеинов высокой плотности и протеогликанов в субэндотелиальное пространство [29].
В исследовании [29] изучалась распространенность НА у 142 пациентов с ГМС и 157 со СЛП. Было установлено, что частота возникновения НА была выше в группе СЛП, чем в группе ГМС (31% и 16% соответственно; р Литература
Только для зарегистрированных пользователей
Чем опасно стентирование сосудов сердца
Таким образом, минимальная цена коронарного стентирвоания в Клинике инновационной хирургии составляет всего 75000 рублей.
Экстренная помощь больным с острым инфарктом миокарда или нестабильной стенокардией, доставляемым в клинику бригадами скорой помощи, коронарография и коронарное стентирвоание выполняется бесплатно по полису ОМС.
Видео о стентировании сосудов сердца
Центр спасения конечностей от гангрены
Московская область, город Клин, улица Победы влад. 2
Записаться на прием
Вопросы-ответы
Здравствуйте, уважаемый доктор. Обращаюсь к Вам по вопросу спасения конечностей стопы моего отца, сейчас он находится в больнице ему уже ампутиповали больше пол стопы. Обратился своевременно и даже подозреваю, что.
Ответ: Пришлите на почту [email protected] фотографию стопы и данные исследований сосудов.
Ответ: Боюсь, что это очень надолго. Когда была операция?
Ответ: Приезжайте на консультацию. Мы этим занимаемся и спасаем ноги в большинстве случаев.
Добрый день! Отец мужа 6 раз оперировался в городской больнице. Ногу спасти не удалось и недавно ампутировали выше колена. Рана не заживает, гноится. А в больнице просто выписывают и толком ничего.
Ответ: Вам надо прислать фотографию культи и выписку из больницы (последнюю)
Ответ: Все рекомендации корректны и при их исполнении должны вам помочь.
Здравствуйте. Скажите пожалуйста делают ли повторные операции шунтирование артерии на ноге.
Ответ: Конечно, если есть необходимость и условия для этого.
Здравствуйте. У деда некроз 4 пальца и отёк уже стопы. На снимках видны сосуды до колена. Палец не удалили объяснив что дальше ещё быстрее пойдёт. Если удалять, то сказали надо.
Ответ: Я советую обратиться к компетентным сосудистым хирургам, занимающимся проблемой критической ишемии.
где и когда можно прооперировать ногу?? мы из Армении согласны приехать.. врач посоветовал обратиться к вам.. далее присылаю эпикриз врача
Ответ: Пришлите данные обследований и фотографии ноги на почту [email protected]
Добрый день! Мне после КТ с контрастом поставили диагноз \»Стеноз Чревного ствола 70%\» и сказали, что нужна операция. На сколько это серьёзно и если необходимо делать операцию, то как срочно.
Ответ: Любая операция имеет риски. Но стентирование чревного ствола не очень опасно. Нужна очная консультация, чтобы точно определить показания к операции.
Я повредил руку сорвал кожу при подении на гравии и ржавчина рука за два часа опухла что делать
Ответ: К хирургу на прием.
© 2007-2021. Инновационный сосудистый центр — сосудистая хирургия нового уровня
Контактная информация:
7 главных вопросов о стентировании
Стентирование — отличный пример медицины будущего. То, с чем раньше эскулапы бессильно боролись таблетками, а потом лечили с помощью большой и сложной операции аортокоронарного шунтирования, сегодня дело получаса и незаметной дырочки на предплечье.
Эта процедура сегодня доступна не только жителям мегаполисов или хорошо обеспеченных граждан – стентирование проводят по скорой помощи почти в любом уголке нашей страны. Операции выполняют бесплатно, ведь на коронарографию и стентирование распространяется программа ОМС и выделяются квоты ВТМП (высокотехнологичной медицинской помощи). К сожалению, многие не осведомлены о новых методах лечения, и нередко пациенты даже на фоне инфаркта отказываются от госпитализации в сосудистый центр.
Самые частые мифы о стентировании
Как проводится экстренное стентирование «по инфаркту»? Чем оно лучше консервативного лечения?
По сути – коронарография и операция ЧТКА со стентированием это единственная возможность точно верифицировать артерию, которая стала причиной инфаркта, и восстановить ее проходимость.
Для того, чтобы выполнить это процедуру, у врачей есть «120 золотых минут» – от момента начала приступа до попадания на операционный стол. Если в это время восстановить кровоток по артерии, то повреждение миокарда будет минимальным, и рубец либо не сформируется совсем, либо будет небольшим. Можно сказать, что инфаркта и не было.
Моему мужу успели сделать коронарографию и установить стент «по инфаркту». Но сужение в другой артерии трогать не стали, сказав, что это ситуация для планового стентирования. Насколько это оправданно?
Такая тактика абсолютно оправданна. В острой ситуации врачи обнаружили тромбированную артерию, восстановили по ней кровоток, имплантировали на место тромбированной бляшки стент. Но не стоит забывать, что операция проводится не в спокойном, плановом режиме, а на фоне острой ситуации, угрожающей жизни больного. Справившись с ней, более разумно не утяжелять операцию, а отложить решение вопроса со стабильной бляшкой на ближайшее будущее.
Чем отличаются обычные стенты от стентов с «лекарственным покрытием»?
Обычные или голометалические стенты представляют собой сетчатый каркас из специального сплава. Они широко применяются в мире и хорошо себя зарекомендовали, однако внимание разработчиков было направлено на то, чтобы снизить риск повторных стенозов – сужения, повторно возникающего непосредственно в стенте. Для этого ученые придумали покрывать поверхность стентов специальным веществом которое в течение многих месяцев постепенно выделяется и препятствует нарастанию неотинтимы и сужению стента.
Стенты с лекарственным покрытием показаны для людей, страдающих сахарным диабетом, для стентирования некоторых участков артерий (ствол левой коронарной артерии, проксимальная треть ПМЖВ), в других случаях больной может самостоятельно оплатить применение этих, более дорогих стентов.
Мне предложили установить не металлические, а биологические стенты, которые полностью рассасываются. Это новое поколение стентов?
Речь идёт о так называемых биодеградируемых стентах, которые в течение 1−2 лет полностью растворяются, оставляя после себя восстановленную структуру сосуда. Сегодня биодеградируемые стенты используют всё чаще, главное – четко соблюдать показания к их применению. В этом случае у нового поколения стентов очень хорошие ближайшие и отдаленные результаты.
В каких случаях рекомендовано проводить стентирование, а в каких – открытую операцию на сердце (аортокоронарное шунтирование)?
На этот счёт написаны десятки страниц клинических рекомендаций и стандартов. Обобщив информацию, можно сказать: стентирование показано при локальных атеросклеротических бляшках, одно- или двухсосудистом поражении. В последние годы специалисты берутся и за три сосуда, но, если бляшки расположены, что называется, «удобно».
Если же поражены все основные коронарные артерии, бляшки расположены не в одном участке артерии, а в разных, на всем ее протяжении, то лучшие отдаленные результаты у открытой операции на сердце. Наличие сахарного диабета также часто трактуется в пользу шунтирования.
Как долго после стентирования необходимо принимать разжижающие кровь лекарства?
Обычная практика — это двухкомпонентная (клопидогрель + аспирин) антиагрегантная терапия в течение 12 месяцев после стентирования. Но универсальных ситуаций не бывает, в случае «сложных» бляшек или сомнений в качестве стентирования у оператора, такое лечение может быть назначено пожизненно. Главное, что должны знать пациенты, прекращение приема лекарств антиагрегантов до года после стентирования недопустимо – это грозит развитием тромбоза стента и повторного инфаркта.
Появились ли в последние годы способы сделать стентирование еще более безопасным?
Методика стентирования постоянно совершенствуется. В последние годы процедуру все чаще проводят под контролем внутрисосудистого ультразвука (ВСУЗИ) или внутрисосудистой когерентной оптической компьютерной томографии (ОКТ). Эти методы позволяют оценить качество установки стента — насколько полно его удалось раздуть и плотно ли его край прилегает к внутренней стенке сосуда. Именно недостаточное раскрытие стента является одной из основных причин раннего и позднего тромбоза. Если стент раскрыт недостаточно, можно повторно раздуть баллон и добиться оптимальной позиции.
Онлайн консультации врачей
в мобильном приложении Доктис
Дежурный терапевт и педиатр консультируют бесплатно
© 2016-2021, ООО «Диджитал Медикэл Оперейшнс»
Лицензия на осуществление мед деятельности ЛО-76-01-002757.
Адрес: 121205, г. Москва, Территория Сколково Инновационного Центра, бульвар Большой, д. 42, стр. 1, эт. 4, пом. 1594, раб. 2
Филиал в г. Ярославль: 150062, Ярославская область, г. Ярославль, ул. 5-я Яковлевская, д.17