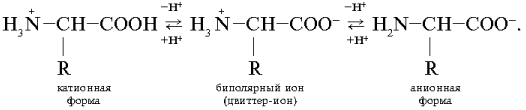
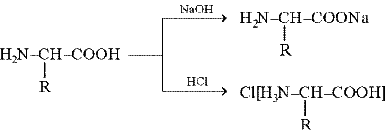
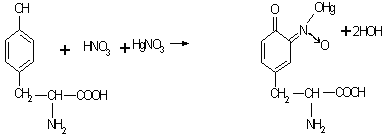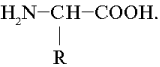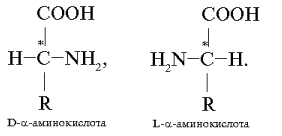Чем обусловлена реакция миллона
Чем обусловлена реакция миллона
Миллонова реакция
Реакция с реактивом Миллона возникает вследствие наличия у тирозина оксифенольного кольца. Эту реакцию дают также содержащие тирозин белки и многие фенолы и их производные. Поэтому она малоспецифична и ее лучше проводить с контролем, удаляя тирозин трихлоруксусной кислотой и фенолы 96%-ным спиртом.
Миллонова реакция высокочувствительна. В процессе реакции, по-видимому, образуется нестойкий комплекс фенола с ртутью. В дальнейшем, присоединяя нитрат, он превращается в относительно стойкое окрашенное соединение. Химизм этой реакции еще не вполне расшифрован.
Для получения постоянных препаратов с реакцией Миллона используют фиксированный в спирте или формалине материал. При этом рекомендуется максимально окрасившиеся в течение нескольких часов срезы промыть в 2%-ной азотной кислоте, затем быстро обезводить в спиртах (70%-ном и 100%-ном) и заключить в канадский бальзам.
Фиксированный материал окрашивается исключительно за счет тирозина белков, так как свободные аминокислоты теряются при фиксации (как и в случае с нингидриновой реакцией).
1) Реактив Миллона (нитрат ртути (I) ).
Приготовление реактива Миллона. Первый способ: 1 мл (13,6 г) ртути растворить в 9 мл концентрированной азотной кислоты (уд. вес 1,52) и разбавить водой (1:1). Второй способ: приготовить 4%-ную азотную кислоту и насытить ее кристаллами нитрата ртути, неоднократно встряхивая раствор в течение нескольких дней; полученный раствор профильтровать и к 400 мл его добавить 3 мл 40%-ной азотной кислоты и 1,4 г нитрата натрия. Последний способ приготовления реактива выгодно отличается от предыдущего, так как первый дает очень разнообразные химические соединения, осложняющие течение реакции.
2) 5%-ная трихлоруксусная кислота.
1. Поместить срез в каплю реактива Миллона на 10-15 мин, покрыв его покровным стеклом.
2. Наблюдать появление розовой или красновато-коричневой окраски в местах нахождения тирозина, содержащих тирозин белков и фенолов.
Как было сказано выше, миллонова реакция осуществляется не только с тирозином, но и с содержащими тирозин белками и фенолами. Для того чтобы определить, с какими из этих соединений прошла реакция, нужно повторно провести реакцию, предварительно удалив из одних срезов тирозин, из других фенолы. Сравнение интенсивности окраски этих срезов с окраской срезов, обработанных только реактивом Миллона, позволяет судить о наличии или отсутствии тирозина.
1. Поместить срез в 5%-ную трихлоруксусную кислоту в часовое стекло, сменить ее несколько раз в течение 5-15 мин.
2. Промыть срез водой.
3. Провести реакцию Миллона.
Если реакция станет отрицательной, значит, ее давала аминокислота тирозин. Если реакция останется положительной, следовательно, она возникает за счет содержащих тирозин белков или фенолов. Для выяснения вопроса о том, какие из этих веществ дают реакцию, следует провести ее еще раз, удалив фенолы.
1. Промыть срезы в часовом стекле 96%-ным спиртом, сменяя его 3-5 раз в течение 5-15 мин.
2. Промыть срезы водой.
3. Провести реакцию Миллона.
Если реакция останется положительной, значит, ее давали не фенолы, а белки. Если реакция станет отрицательной, следовательно, в препарате были фенолы.
Результаты реакции (табл. 12, 13)
В зерновке кукурузы окраска возникает главным образом за счет связанного в белках тирозина, свободного тирозина почти нет. Зародыш дает более яркую окраску, чем эндосперм.
Однако и компоненты эндосперма дают явное окрашивание, особенно алейроновый слой и прилежащие к нему клетки, а также клетки эндосперма, расположенные вдоль эпителия щитка. Это указывает на большое количество белка в зоне алейронового слоя и, возможно, на приток продуктов гидролиза белка к эпителию щитка. В зародыше реакция протекает наиболее интенсивно в почечке и корешке, что связано с наибольшей заполненностью белками и аминокислотами этой части зародыша, по и в щитке реакция происходит достаточно интенсивно.
РЕАКЦИЯ МИЛЛОНА



Реакция Миллона характерна для белков, содержащих ароматическую аминокислоту тирозин.
При взаимодействии белка с реактивом Миллона (р-р азотнокислой ртути в концентрированной НNO3) образуется осадок белка, который при нагревании окрашивается в красно-коричневый цвет.
Реакция вызвана присутствием в белке фенольной группы тирозина, после взаимодействия с реактивом Миллона образуется ртутная соль нитропроизводного.
Тирозин Ртутная соль нитротирозина
Реакцию Миллона дают все белки, за исключением тех, молекулы которых не содержат тирозина (желатин, клупеин и др.).
Реактив Миллона дает окрашивание почти со всеми фенолами.
Ход работы: К раствору белка 1-2 мл прилить 5-6 капель реактива Миллона. Осадок белка при нагревании окрашивается в красно-коричневый цвет, вследствие образования ртутной соли нитрозина. Следует избегать прибавления избытка реактива Миллона, поскольку он содержит азотную кислоту, которая при взаимодействии с белком может дать желтое окрашивание (ксантопротеиновую реакцию), маскирующее реакцию Миллона.
ЦВЕТНЫЕ И ИМЕННЫЕ КАЧЕСТВЕННЫЕ РЕАКЦИИ НА БЕЛКИ
История химии в школьном курсе
Белки – основа жизнедеятельности любого организма на Земле. Это сложные высокомолекулярные природные соединения. Мономерами белков являются аминокислоты. Умение определять аминокислоты важно и в теоретическом, и в практическом аспекте. Определение аминокислот сопровождается написанием уравнений качественных реакций, что способствует углублению знаний по органической химии. Это умение имеет большое значение при заболеваниях, связанных с ослаблением иммунной системы людей (аллергические заболевания, нарушение функционирования ферментативных систем и т. д.), при которых основную роль играют белки. В данной ситуации необходимо оперативно и грамотно определять аминокислоты (белки).
Мы постарались в этой работе выяснить химизм качественных реакций на аминокислоты, указать роль отдельных ученых, в том числе российских, в исследовании белков, а также:
1) изучить и систематизировать имеющиеся литературные данные по качественным реакциям на белковые аминокислоты, составить базу данных о качественных, в том числе цветных, реакциях на белки;
2) научиться практически осуществлять качественные реакции;
3) выделить качественные реакции на белковые аминокислоты, изучаемые в школьном курсе химии.
Для аминокислот, постоянно встречающихся в составе белков, разработано множество цветных (в том числе именных) реакций. Многие из них высокоспецифичны, что позволяет определять ничтожные количества той или иной аминокислоты.
Надо помнить, что все качественные реакции – это реакции не собственно на белки, а на определенные аминокислоты, входящие в их состав.
Большинство D-изомеров обладает сладким вкусом, а L-изомеры – горькие или безвкусные.
Описание опыта. К 2 мл 1%-го раствора триптофана приливают
1 мл концентрированной уксусной кислоты, встряхивают и по стенке пробирки осторожно добавляют
Реакция используется для количественного определения аминокислот по объему выделившегося газообразного азота.
Описание опыта. В пробирку наливают 1 мл 1%-го раствора глицина и равный объем 5%-го раствора нитрита натрия. Добавляют 0,5 мл концентрированной уксусной кислоты и осторожно взбалтывают смесь. Наблюдается выделение пузырьков газа:
Это реакция на аминокислоту тирозин. Реактив Миллона (раствор HgNO3 и Hg(NO2)2 в разбавленной HNO3, содержащей примесь HNO2) взаимодействует с тирозином с образованием ртутной соли нитропроизводного тирозина, окрашенной в розовато-красный цвет:
Описание опыта. К 2 мл концентрированного раствора тирозина прибавляют
Это реакция на аминокислоту триптофан.
Описание опыта. 1 мл 0,005%-го раствора триптофана смешивают с равным объемом глиоксиловой кислоты НС(О)СООН* и к смеси прибавляют 10 капель 0,04 М раствора сульфата меди(II). Затем небольшими порциями (по несколько капель) добавляют 2–3 мл концентрированной серной кислоты, охлаждая пробирку после приливания очередной порции кислоты током холодной воды (или в ванночке со льдом). Полученную смесь оставляют на 10 мин при комнатной температуре, после чего ставят на 5 мин в кипящую водяную баню. Наблюдается образование сине-фиолетового окрашивания.
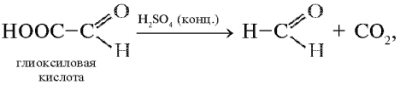
В этой реакции из глиоксиловой кислоты под действием концентрированной серной кислоты сначала получается формальдегид:
который затем конденсируется с триптофаном:
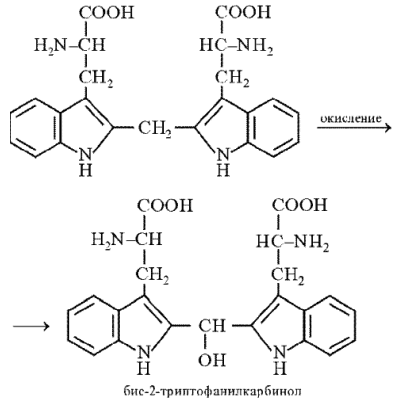
Продукт конденсации окисляется до бис-2-триптофанилкарбинола, который в присутствии минеральных кислот образует соли, окрашенные в сине-фиолетовый цвет:
Это реакция на аминокислоту метионин.
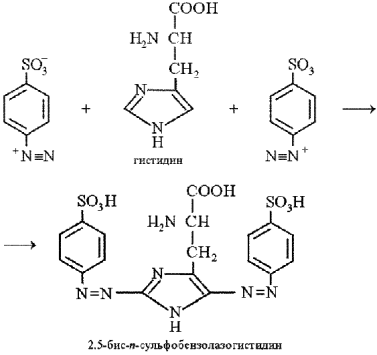
Эта реакция на аминокислоту гистидин основана на взаимодействии гистидина с диазобензолсульфоновой кислотой с образованием соединения вишнево-красного цвета.
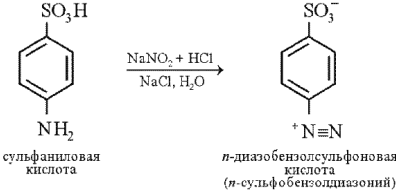
Реакцию диазотирования осуществляют при взаимодействии кислого раствора сульфаниловой кислоты с нитритом натрия. При этом образуется диазобензолсульфоновая кислота:
Эта кислота, взаимодействуя с гистидином, дает соединение вишнево-красного цвета:
Описание опыта. В пробирку наливают 1 мл 1%-го раствора сульфаниловой кислоты в 5%-м растворе соляной кислоты. Затем прибавляют 2 мл 0,5%-го раствора нитрита натрия, сильно встряхивают и немедленно приливают 2 мл 0,01%-го раствора гистидина. После перемешивания содержимого пробирки сразу приливают 6 мл 10%-го раствора соды. Появляется интенсивная вишнево-красная окраска.
Окончание следует
*К 2 г порошка магния (слегка увлажненного) прилить при охлаждении 50 мл (заранее охлажденного до 0 °С) насыщенного раствора щавелевой кислоты. Полученный осадок оксалата магния отфильтровывают и декантируют небольшим количеством воды. Фильтрат подкисляют уксусной кислотой и доводят до объема 200 мл (полученный раствор хранить в холодильнике!).
МИЛЛОНА РЕАКЦИЯ
Смотреть что такое «МИЛЛОНА РЕАКЦИЯ» в других словарях:
Миллона реакция — цветная реакция, применяемая для обнаружения белков (См. Белки); впервые её наблюдал в 1849 франц. химик О. Э. Миллон (А. Е. MilIon). При нагревании раствора белка с реактивом Миллона (раствор азотнокислой ртути в азотной кислоте,… … Большая советская энциклопедия
МИЛЛОНА РЕАКЦИЯ — цветная качеств. р ция на белки и фенолы. При добавлении к р ру белка реактива Миллона [р р HgNO3 и Hg(NO3)2 в разб. HNO3, содержащей примесь HNO2] образуется белый осадок денатурир. белка. При стоянии (быстрее при нагр. до 50 °С) осадок… … Химическая энциклопедия
Миллона реакция — (A. N. Е. Millon, 1812 1867, франц. химик) метод обнаружения тирозина и тирозин содержащих белков, основанный на появлении кирпично красного окрашивания при их нагревании со смесью нитратов и нитритов ртути … Большой медицинский словарь
МОЧА — (урина, urina), жидкость, отде ляемая почками и выделяемая из организ ма наружу через систему мочевыводящих путей. СМ. удаляются из организма почти все азотистые продукты обмена веществ (за исключением небольших количеств, поступающих в пот и в… … Большая медицинская энциклопедия
Ртуть * — (живое серебро, Hydrargirum, Quecksilber, mercure), Hg принадлежит к числу 7 металлов, известных в глубокой древности: золото, серебро, медь, железо, свинец, олово и Р. По сравнению с остальными 6 металлами человек, по всей вероятности,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Ртуть, её свойства, соединения и получение — (живое серебро, Hydrargirum, Quecksilber, mercure), Hg принадлежит к числу 7 металлов, известных в глубокой древности: золото, серебро, медь, железо, свинец, олово и Р. По сравнению с остальными 6 металлами человек, по всей вероятности,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Белковые вещества — Б. вещества составляют громадный класс органических, то есть углеродистых, а именно углеродисто азотистых соединений, неизбежно встречаемых в каждом организме до того, что каждая клетка растений содержит Б. вещества, а клетки животных организмов… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ГИСТОЛОГИЧЕСКАЯ ТЕХНИКА — ГИСТОЛОГИЧЕСКАЯ ТЕХНИКА. Содержание: Методика гистологич. исследований. 242 Теоретические основы Г. т. 246 Гистохимия. 253 Краски, употребляемые в Г. т. 258 Гистологическая техник а техника изучения… … Большая медицинская энциклопедия
Мочевина — (хим.; urée, urea, Harnstoff), карбамид, C2H4N2O = CO(NH2)2, впервые, как отдельная составная часть мочи, была выделена Круикшанком в 1797 г.; в 1799 г. это открытие нашло подтверждение в исследованиях Фуркруа и Вокелена, получивших М. в… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Лабораторная работа №1
Лабораторная работа №1
ХИМИЯ ПРОСТЫХ БЕЛКОВ.
ЦВЕТНЫЕ РЕАКЦИИ НА БЕЛКИ И АМИНОКИСЛОТЫ
Белки представляют собой высокомолекулярные полимерные органические соединения, построенные из остатков различных α-аминокислот, соединенных ковалентной пептидной связью.
Присутствие белка в растворах можно обнаружить с помощью цветных реакций, обусловленных наличием в белке аминокислот, их специфических групп и пептидных связей. Существуют универсальные цветные реакции, т. е. на все белки (биуретовая и нингидриновая), и специфические, т. е. на определенные аминокислоты (ксантопротеиновая, Миллона, Фоля и др.).
На основании некоторых цветных реакций разработаны методы количественного определения белков и аминокислот, которые широко используются в биохимических лабораториях.
Цель: Ознакомиться с универсальными цветными реакциями на белки и специфическими реакциями на отдельные аминокислоты, содержащиеся в белковых растворах.
Работа 1. Биуретовая реакция на пептидную связь (Пиотровского)
Биуретовая реакция обусловлена наличием в белке пептидных связей, которые в щелочной среде образуют с сернокислой медью комплексы фиолетового цвета с красным или синим оттенком. Группа, образующая пептидную связь, в щелочной среде присутствует в своей таутомерной енольной форме:
При избытке щелочи происходит диссоциация ОН-группы, появляется отрицательный заряд, с помощью которого кислород взаимодействует с медью. Возникает солеобразная связь. Кроме того, медь образует дополнительные координационные связи с атомами азота, участвующими в пептидной связи, путем использования их электронных пар. Возникающий таким образом комплекс очень стабилен. Интенсивность окраски комплекса зависит от концентрации белка и количества медной соли в растворе.
Исследуемый материал: раствор яичного белка, раствор растительного белка, 1% раствор желатина.
Реактивы: 10% раствор NaOH, 1% раствор CuSO4.
Оборудование: пробирки, капельницы.
Ход работы. К 5 каплям водного раствора белка добавляют 5 капель 10% раствора NaOH и 2 капли 1% раствора CuSO4. Содержимое перемешивают. Оно приобретает сине-фиолетовый цвет. Нельзя добавлять избыток CuSO4, так как синий осадок маскирует характерное фиолетовое окрашивание биуретового комплекса.
Работа 2. Нингидриновая реакция на α-аминокислоты
Белки, полипептиды и свободные α-аминокислоты дают синее или фиолетовое окрашивание с нингидрином. При нагревании белка с водным раствором нингидрина аминокислоты окисляются и распадаются, образуя СО2, NH3 и соответствующий альдегид. Нингидрин, являясь сильным окислителем, вызывает окислительное дезаминирование α-аминокислоты, приводящее к образованию аммиака, двуокиси углерода, соответствующего альдегида и восстановленной формы нингидрина. Нингидрин восстанавливается и связывается со второй молекулой нингидрина посредством молекулы аммиака, образуя продукты конденсации, окрашенные в синий, фиолетовый, красный, а в случае пролина – в желтый цвет.