Чем обусловлена биуретовая реакция
ЦВЕТНЫЕ И ИМЕННЫЕ КАЧЕСТВЕННЫЕ РЕАКЦИИ НА БЕЛКИ
История химии в школьном курсе
РЕАКЦИЯ ПИОТРОВСКОГО (БИУРЕТОВАЯ РЕАКЦИЯ)
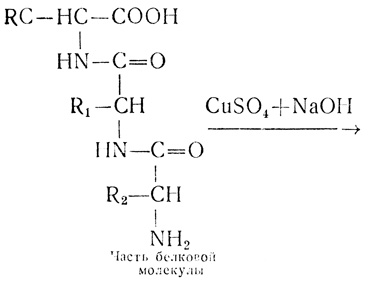
В белках аминокислоты связаны друг с другом по типу полипептидов и дикетопиперазинов. Образование полипептидов из аминокислот происходит путем отщепления молекулы воды от аминогруппы одной молекулы аминокислоты и карбоксильной группы другой молекулы:
Образующаяся группа –С(О)–NН– называется пептидной группой, связь С–N, соединяющая остатки млекул аминокислот, – пептидной связью.
При взаимодействии дипептида с новой молекулой аминокислоты получается трипептид и т. д.
Дикетопиперазины образуются при взаимодействии двух молекул аминокислот с отщеплением двух молекул воды:
Дикетопиперазины были выделены из белков Н.Д.Зелинским и В.С.Садиковым в 1923 г.
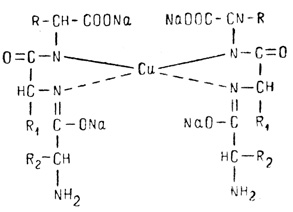
Наличие в белке повторяющихся пептидных групп подтверждается тем, что белки дают фиолетовое окрашивание при действии небольшого количества раствора медного купороса в присутствии щелочи (биуретовая реакция).
Реакция идет по схеме:
Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Описание опыта. В пробирку наливают 1 мл раствора цистина, прибавляют 0,5 мл 20%-го раствора гидроксида натрия. Смесь нагревают до кипения, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):
Описание опыта. В пробирку наливают 5 капель 1%-го раствора глицина и прибавляют 1 каплю индикатора метилового красного. Раствор окрашивается в желтый цвет (нейтральная среда). К полученной смеси добавляют равный объем 40%-го раствора формальдегида (формалин). Появляется красное окрашивание (кислая среда):
Это реакция на аминокислоту глицин.
В таких солях ион меди координационными связями соединен с аминогруппами.
Описание опыта. В пробирку наливают 3 мл 3%-го раствора сульфата меди(II), добавляют несколько капель 10%-го раствора гидроксида натрия до образования голубого осадка. К полученному осадку гидроксида меди(II) приливают 0,5 мл концентрированного раствора глицина. При этом образуется темно-синий раствор глицината меди:
Описание опыта. В пробирку наливают 1 мл раствора тирозина и добавляют 0,5 мл концентрированной азотной кислоты. Смесь нагревают до появления желтой окраски. После охлаждения добавляют 1–2 мл 20%-го раствора гидроксида натрия до появления оранжевой окраски раствора:
Описание опыта. В пробирку наливают около
0,5 мл раствора уксуснокислого свинца и прибавляют раствор едкого кали до растворения образовавшегося осадка гидроксида свинца. В другую пробирку наливают
Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. Например, с глиоксиловой кислотой (являющейся примесью к концентрированной уксусной кислоте) реакция протекает по уравнению:
По аналогичной схеме протекает и реакция триптофана с формальдегидом.
В ходе проведенного исследования мы выявили по литературным источникам имеющуюся информацию о цветных качественных реакциях на белковые аминокислоты; выполнили ряд перечисленных реакций и составили базу данных. Эта база может быть использована в школьной практике как в теоретическом плане, так и в практическом, т. к. мы приводим краткие, но подробные описания выполнения всех опытов.
Из предложенных 18 качественных реакций каждая практически осуществима в школьном курсе химии и имеет важное практическое значение. Сопровождение реакций химическими уравнениями конкретизирует и углубляет знания по биологической и органической химии, особенно знания учащихся специализированных биологических и химических классов.
Использованная литература
Ермаков А.Н., Арасимович В.В., Смирнова-Иконникова М.И., Мирри И.К. Методы биохимического исследования растений. М.,1952, 520 с.
Полянская А.С., Шевелева А.О. Методическая разработка по лабораторным работам: «Аминокислоты» и «Белки». Л., 1976, 37 с.
Пустовалова Л.М. Практикум по биохимии. 1999, 541 с.
Руководство к практическим занятиям по органической химии. Под ред. В.М.Родионова. М., 1954, 111 с.
Соловьев Н.А. Лабораторные работы по биологической химии. Методическая разработка. СПб., 1996, 70 с.
Филиппович Ю.Б., Егорова Т.А., Севастьянова Г.А. Практикум по общей биохимии. М., 1982, 311 с.
З.Саитов, С.В.Телешов, Б.Харитонцев,
секция «Юный химик» РХО им. Д.И.Менделеева (г. Тобольск)
БИУРЕТОВАЯ РЕАКЦИЯ
БИУРЕТОВАЯ РЕАКЦИЯ — реакция качественного и количественного определения в различных биологических жидкостях белков и продуктов их частичного гидролиза. Основана на образовании в щелочной среде окрашенного солеобразного комплекса веществами, имеющими 2 или более карбоксамидные группы. Окраска биуретового комплекса зависит от количества медной соли и от структуры вещества, с к-рыми координирован ион меди. Так, продукты распада белка — пептоны — образуют комплексное соединение красного оттенка, белки — сине-фиолетового. Реакция белков обусловлена наличием в их молекуле пептидных связей. Биуретовую реакцию могут давать биурет NH2—CO—NH—CO—NH2 (откуда возникло название этой реакции), оксамид, глицинамид, малонамид, некоторые аминокислоты (гистидин, серин, треонин) при достаточно большой концентрации их в растворе и др. Предложено несколько способов приготовления биуретового реактива, один из которых описывается ниже: 1,5 г сульфата меди и 6 г сегнетовой соли растворяют в 500 мл воды; добавляют 300 мл 10% раствора едкого натра, свободного от углекислого натрия, и 1 г йодистого калия для предотвращения самопроизвольного восстановления. Раствор доводят водой до 1 л.
Ход определения. К 1 мл исследуемого раствора, содержащего 1 — 10 мг белка, добавляют 4 мл биуретового реактива, перемешивают и оставляют на 30 мин. при комнатной температуре. Оптическую плотность раствора определяют с помощью фото-электроколориметра или спектрофотометра при длине волны 540— 560 нм. Контролем служит проба, содержащая 4 мл биуретового реактива и 1 мл воды или соответствующего солевого раствора. Концентрацию белка в исследуемом растворе определяют по калибровочной кривой, построенной с применением растворов казеина, сывороточного или яичного альбумина известных концентраций.
Определению белков с помощью Б. р. мешает присутствие солей аммония, препятствующих Б. р., т. к. они образуют с ионами меди биуретового реактива медноаммиачные комплексы.
В СССР с 1972 г. Б. р. предложена для обязательного применения во всех клинико-диагностических лабораториях в качестве метода количественного определения общего белка в сыворотке крови, в частности при циррозе печени, почечной недостаточности, миеломной болезни и др.
В норме содержание белка в сыворотке крови, определяемого с помощью Б. р., находится в пределах 6,5—8,5 г%.
Б. р. лежит также в основе широко применяемого в лабораторной практике метода определения белка в крови — Лаури метода (см.).
Библиография: Руководство по клиническим лабораторным исследованиям, под ред. Е. А. Кост и Л. Г. Смирновой, с. 197, М., 1964; Gornal 1 A. G., Bardawill С. J. a. David М. М. Determination of serum proteins by means of biuret reaction, J. biol. Chem., v. 177, p. 751, 1949; Weichselbaum Т. E. Accurate and rapid method for determination of proteins in small amounts of blood serum and plasma, Amer. J. clin. Path., v. 10, p. 40, 1946.
Лабораторная работа №1
Лабораторная работа №1
ХИМИЯ ПРОСТЫХ БЕЛКОВ.
ЦВЕТНЫЕ РЕАКЦИИ НА БЕЛКИ И АМИНОКИСЛОТЫ
Белки представляют собой высокомолекулярные полимерные органические соединения, построенные из остатков различных α-аминокислот, соединенных ковалентной пептидной связью.
Присутствие белка в растворах можно обнаружить с помощью цветных реакций, обусловленных наличием в белке аминокислот, их специфических групп и пептидных связей. Существуют универсальные цветные реакции, т. е. на все белки (биуретовая и нингидриновая), и специфические, т. е. на определенные аминокислоты (ксантопротеиновая, Миллона, Фоля и др.).
На основании некоторых цветных реакций разработаны методы количественного определения белков и аминокислот, которые широко используются в биохимических лабораториях.
Цель: Ознакомиться с универсальными цветными реакциями на белки и специфическими реакциями на отдельные аминокислоты, содержащиеся в белковых растворах.
Работа 1. Биуретовая реакция на пептидную связь (Пиотровского)
Биуретовая реакция обусловлена наличием в белке пептидных связей, которые в щелочной среде образуют с сернокислой медью комплексы фиолетового цвета с красным или синим оттенком. Группа, образующая пептидную связь, в щелочной среде присутствует в своей таутомерной енольной форме:
При избытке щелочи происходит диссоциация ОН-группы, появляется отрицательный заряд, с помощью которого кислород взаимодействует с медью. Возникает солеобразная связь. Кроме того, медь образует дополнительные координационные связи с атомами азота, участвующими в пептидной связи, путем использования их электронных пар. Возникающий таким образом комплекс очень стабилен. Интенсивность окраски комплекса зависит от концентрации белка и количества медной соли в растворе.
Исследуемый материал: раствор яичного белка, раствор растительного белка, 1% раствор желатина.
Реактивы: 10% раствор NaOH, 1% раствор CuSO4.
Оборудование: пробирки, капельницы.
Ход работы. К 5 каплям водного раствора белка добавляют 5 капель 10% раствора NaOH и 2 капли 1% раствора CuSO4. Содержимое перемешивают. Оно приобретает сине-фиолетовый цвет. Нельзя добавлять избыток CuSO4, так как синий осадок маскирует характерное фиолетовое окрашивание биуретового комплекса.
Работа 2. Нингидриновая реакция на α-аминокислоты
Белки, полипептиды и свободные α-аминокислоты дают синее или фиолетовое окрашивание с нингидрином. При нагревании белка с водным раствором нингидрина аминокислоты окисляются и распадаются, образуя СО2, NH3 и соответствующий альдегид. Нингидрин, являясь сильным окислителем, вызывает окислительное дезаминирование α-аминокислоты, приводящее к образованию аммиака, двуокиси углерода, соответствующего альдегида и восстановленной формы нингидрина. Нингидрин восстанавливается и связывается со второй молекулой нингидрина посредством молекулы аммиака, образуя продукты конденсации, окрашенные в синий, фиолетовый, красный, а в случае пролина – в желтый цвет.
Чем обусловлена биуретовая реакция
Биуретовая реакция
Биуретовая реакция служит для обнаружения пептидных связей. Пептидная связь наиболее характерна для белков, и в этом смысле биуретовая реакция являемся наиболее специфичной. В белках возможны и другие связи, например, сульфидная, эфирная, солевая, водородная. Для обнаружения этих связей биуретовая реакция негодна.
Биуретовая реакция основана на том, что в щелочной среде (в присутствии гидроокиси натрия) при добавлении солей меди (медного купороса) полипептиды и белки образуют окрашенные комплексные соединения с ионом меди.
Хотя отдельные аминокислоты этой реакции не дают, но, как исключение, она возникает в присутствии аспарагина и гистидина.
Отрицательной чертой биуретовой реакции является то, что она малочувствительна. Окрашивание особенно хорошо проявляется только там, где белков много (например, в меристематических клетках).
Проведение биуретовой реакции на свежем материале может дать ослабленное окрашивание из-за слабой проницаемости тканей. Фиксированный материал дает в этом отношении лучшие результаты; однако надо иметь в виду, что фиксация спиртом неприемлема для спирторастворимых белков (как, например, белки зерновых злаков).
1) 7%-ный раствор медного купороса.
2) 30-50%-ный раствор гидроокиси натрия (или калия).
1. Погрузить срез в раствор медного купороса на 5-30 мин в часовом стекле.
2. Тщательно отсосать этот раствор фильтровальной бумагой и промыть срез водой до удаления голубой окраски из промывной воды.
3. Перенести срез на предметное стекло и обработать раствором гидроокиси натрия (или калия) от 10-20 мин до 1 ч.
4. Наблюдать появление фиолетовой окраски (иногда розовой в присутствии низкомолекулярных белков или полипептидов).
Результаты реакции (табл. 17)
Реакция не идет в паренхиме листа капусты и проявляется неярко в тканях пучка.
Эндосперм зерновки кукурузы не дает реакции, не считая алейронового слоя, где она проявляется, хотя и очень незначительно. Зародыш окрашивается ярко.
Биуретовая реакция
Биуретовая реакция — качественная на все без исключения белки, а также продукты их неполного гидролиза, которые содержат не менее двух пептидных связей. Биуретовая реакция обусловлена присутствием в белках пептидных связей, которые в щелочной среде образуют с сульфатом меди (ІІ) окрашенные медные солеобразные комплексы. Биуретовую реакцию дают также некоторые небелковые вещества, например биурет (NH2-CO-NH-CO-NH2), оксамид (NH2CO-CO-NH2), ряд аминокислот (гистидин, серин, треонин, аспарагин).
Проведение
К 1 мл исследуемого раствора доливают 1 мл 10 % раствора гидроксида натрия (NaOH) и 2-3 капли 1 % раствора сульфата меди (CuSO4). При положительной реакции появляется фиолетовая окраска с красным либо синим оттенком.
Полезное
Смотреть что такое «Биуретовая реакция» в других словарях:
БИУРЕТОВАЯ РЕАКЦИЯ — БИУРЕТОВАЯ РЕАКЦИЯ, одна из наиболее характерных цветных реакций, к рую дают белки и высшие продукты их расщепления. К испытуемому раствору прибавляется треть объема крепкой натронной щелочи и небольшое количество сильно разведенного (1:500 или… … Большая медицинская энциклопедия
биуретовая реакция — biureto reakcija statusas T sritis chemija apibrėžtis Baltymų ir peptidų nustatymo reakcija. atitikmenys: angl. biuret reaction rus. биуретовая реакция … Chemijos terminų aiškinamasis žodynas
биуретовая реакция — метод качественного и количественного определения белков и продуктов их частичного гидролиза в крови, моче и других жидкостях, заключающийся в обнаружении и колориметрии фиолетового или красного окрашивания, появляющегося при добавлении к… … Большой медицинский словарь
БИУРЕТОВАЯ РЕАКЦИЯ — цветная р ция на биурет, к рую осуществляют, прибавляя к щелочному р ру последнего разб. водный р р соли Сu2+ (обычно CuSO4). При этом р р окрашивается в интенсивный фиолетовый цвет благодаря образованию комплексного соед. (ф ла I, М + катион… … Химическая энциклопедия
БЕЛКИ — БЕЛКИ, или протеины, высокомолекулярные коллоидальные органические вещества, построенные из остатков аминокислот. Б. по своему количественному содержанию в организме животных занимают среди твердых составных частей его одно из первых мест, а по… … Большая медицинская энциклопедия
Белки — I Белки (протеины) органические соединения, структурной основой которых служит полипептидная цепь, состоящая из аминокислотных остатков, соединенных пептидными связями ( СО NH2 ) в определенной последовательности. Белки являются главными… … Медицинская энциклопедия
Туберкулин — или так назыв. лимфа Коха в 1890 г. Robert ом Koch ом был предложен как диагностическое и терапевтическое средство при туберкулезе и встречен с небывалым энтузиазмом не только со стороны публики и ближайших сотрудников Коха, но и с большим… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Биурет — органическое соединение состава С2H5N3О2 + Н2О или, подробнее, CO (NH2)(NH CONH2), амид аллофановой кислоты (см. это сл.); открыт в 1847 г. Видеманом при нагревании мочевины до 150° 170°; реакция ведется на масляной бане до тех пор, пока взятая… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Биурет — Биурет … Википедия