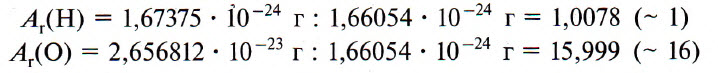Что значит относительная атомная масса
Что значит относительная атомная масса
Ключевые слова конспекта: атомная единица массы, относительная атомная масса химических элементов, относительная молекулярная масса.
Атомная единица массы — это 1/12 массы атома углерода, масса которого равна 12 а.е.м.
Обратите внимание! На Земле встречаются три разновидности атомов углерода, различающиеся только массой. Такие разновидности атомов одного и того же элемента называют изотопами. В данном случае речь идёт о разновидности, масса атомов которой в атомных единицах массы равна 12.
Разделив массу атома какого-либо химического элемента на 1/12 массы атома углерода, получают величину, которую называют относительной атомной массой и обозначают Аr (А — от слова «атом», r — от латинского слова relativus — относительный).
Например, относительную атомную массу водорода и кислорода вычисляют следующим образом:
Относительная атомная масса элемента (Аr) показывает, во сколько раз масса его атома больше 1/12 массы атома углерода, масса которого равна 12 а. е. м.
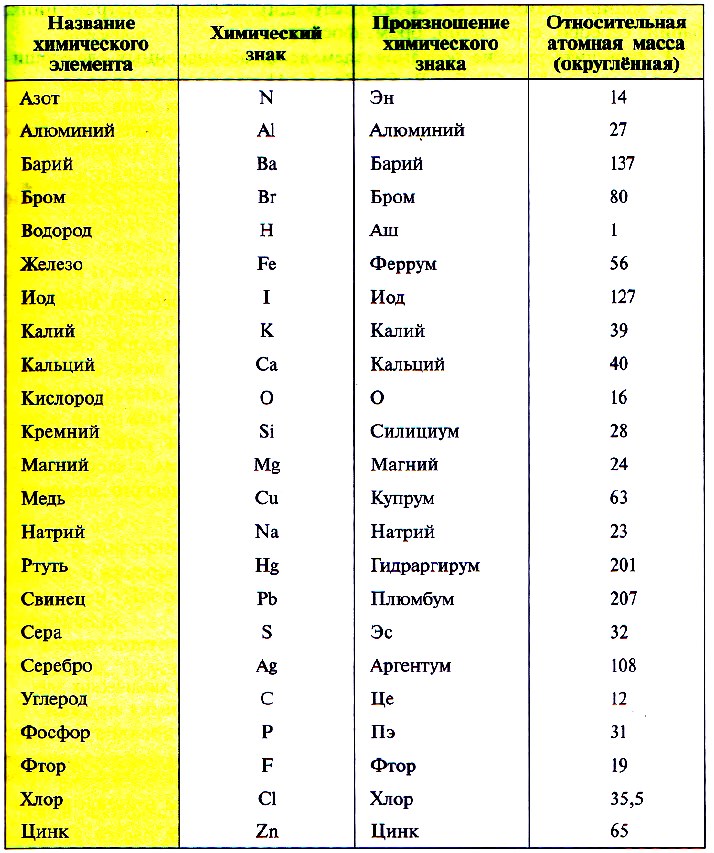
Так как первую таблицу относительных атомных масс ряда элементов составил английский учёный Джон Дальтон в 1803 г, то в память о его трудах химики иногда называют атомную единицу массы дальтоном (сокращённо Da). Значение относительной атомной массы каждого химического элемента приведено в периодической таблице Д. И. Менделеева. На практике эти значения обычно округляют до целых чисел.
Относительная молекулярная масса
Массу молекул, так же как массу атомов, принято выражать в атомных единицах массы. Разделив массу молекулы какого-либо вещества на 1/12 массы атома углерода, получают величину, которую называют относительной молекулярной массой вещества.
Относительная молекулярная масса вещества показывает, во сколько раз масса молекулы данного вещества больше 1/12 массы атома углерода, масса которого равна 12 а.е.м.
Относительная молекулярная масса Мr — безразмерная величина. Она складывается из относительных атомных масс элементов, составляющих молекулу, например:
Конец конспекта «Относительная атомная масса. Относительная молекулярная масса».
Атомная масса
А́томная ма́сса, относительная атомная масса (устаревшее название — атомный вес) — значение массы атома, выраженное в атомных единицах массы. В настоящее время атомная единица массы принята равной 1/12 массы нейтрального атома наиболее распространённого изотопа углерода 12 C, поэтому атомная масса этого изотопа по определению равна точно 12. Разность между атомной массой изотопа и его массовым числом называется избытком массы (обычно его выражают в МэВ). Он может быть как положительным, так и отрицательным; причина его возникновения — нелинейная зависимость энергии связи ядер от числа протонов и нейтронов, а также различие в массах протона и нейтрона.
Зависимость атомной массы изотопа от массового числа такова: избыток массы положителен у водорода-1, с ростом массового числа он уменьшается и становится отрицательным, пока не достигается минимум у железа-56, потом начинает расти и возрастает до положительных значений у тяжёлых нуклидов. Это соответствует тому, что деление ядер, более тяжёлых, чем железо, высвобождает энергию, тогда как деление лёгких ядер требует энергии. Напротив, слияние ядер легче железа высвобождает энергию, слияние же элементов тяжелее железа требует дополнительной энергии.
Атомная масса химического элемента (также «средняя атомная масса», «стандартная атомная масса») является средневзвешенной атомной массой всех стабильных изотопов данного химического элемента с учётом их природной распространённости в земной коре и атмосфере. Именно эта атомная масса представлена в периодической таблице Д. И. Менделеева, её используют в стехиометрических расчётах. Атомная масса элемента с нарушенным изотопным соотношением (например, обогащённого каким-либо изотопом) отличается от стандартной. Для моноизотопных элементов (таких как иод, золото и т. п.) атомная масса элемента совпадает с атомной массой его единственного представленного в природной смеси изотопа.
Молекулярной массой химического соединения называется сумма атомных масс элементов, составляющих её, умноженных на стехиометрические коэффициенты элементов по химической формуле соединения. Строго говоря, масса молекулы меньше массы составляющих её атомов на величину, равную энергии связи молекулы. Однако этот дефект массы на 9-10 порядков меньше массы молекулы, и им можно пренебречь.
Определение моля (и числа Авогадро) выбирается таким образом, чтобы масса одного моля вещества (молярная масса), выраженная в граммах, была численно равна атомной (или молекулярной) массе этого вещества. Например, атомная масса железа равна 55,847. Следовательно один моль железа (т. е. количество атомов железа, равное числу Авогадро, 6,022·10 23 ) имеет массу 55,847 г.
Прямое сравнение и измерение масс атомов и молекул выполняется с помощью масс-спектрометрических методов.
История
До 1960-х годов атомную массу определяли таким образом, чтобы нуклид кислород-16 имел атомную массу 16 (кислородная шкала). Однако соотношение кислорода-17 и кислорода-18 в природном кислороде, который также использовался в расчётах атомной массы, приводило к наличию двух разных таблиц атомных масс. Химики использовали шкалу, основанную на том, что естественная смесь изотопов кислорода должна была иметь атомную массу 16, тогда как физики присваивали то же число 16 атомной массе наиболее распространённого изотопа кислорода (имеющего восемь протонов и восемь нейтронов).
Относительная атомная масса
А́томная ма́сса, относительная атомная масса (устаревшее название — атомный вес) — значение массы атома, выраженное в атомных единицах массы. В настоящее время атомная единица массы принята равной 1/12 массы нейтрального атома наиболее распространённого изотопа углерода 12 C, поэтому атомная масса этого изотопа по определению равна точно 12. только для свинца изотопа атомная масса не является целым числом, хотя и близка к массовому числу данного изотопа (т. е. суммарному количеству нуклонов — протонов и нейтронов — в его ядре). Разность между атомной массой изотопа и его массовым числом называется избытком массы (обычно его выражают в МэВ). Он может быть как положительным, так и отрицательным; причина его возникновения — нелинейная зависимость энергии связи ядер от числа протонов и нейтронов, а также различие в массах протона и нейтрона.
Зависимость атомной массы от массового числа такова: избыток массы положителен у водорода-1, с ростом массового числа он уменьшается и становится отрицательным, пока не достигается минимум у железа-56, потом начинает расти и возрастает до положительных значений у тяжёлых нуклидов. Это соответствует тому, что деление ядер, более тяжёлых, чем железо, высвобождает энергию, тогда как деление лёгких ядер требует энергии. Напротив, слияние ядер легче железа высвобождает энергию, слияние же элементов тяжелее железа требует дополнительной энергии.
Атомная масса химического элемента (также «средняя атомная масса», «стандартная атомная масса») является средневзвешенной атомной массой всех стабильных изотопов данного химического элемента с учётом их природной распространённости в земной коре и атмосфере. Именно эта атомная масса представлена в периодической таблице, её используют в стехиометрических расчётах. Атомная масса элемента с нарушенным изотопным соотношением (например, обогащённого каким-либо изотопом) отличается от стандартной.
Молекулярной массой химического соединения называется сумма атомных масс элементов, составляющих её, умноженных на стехиометрические коэффициенты элементов по химической формуле соединения. Строго говоря, масса молекулы меньше массы составляющих её атомов на величину, равную энергии связи молекулы. Однако этот дефект массы на 9-10 порядков меньше массы молекулы, и им можно пренебречь.
Определение моля (и числа Авогадро) выбирается таким образом, чтобы масса одного моля вещества (молярная масса), выраженная в граммах, была численно равна атомной (или молекулярной) массе этого вещества. Например, атомная масса железа равна 55,847. Поэтому один моль атомов железа (т. е. их количество, равное числу Авогадро, 6,022·10 23 ) содержит 55,847 граммов.
Прямое сравнение и измерение масс атомов и молекул выполняется с помощью масс-спектрометрических методов.
История
До 1960-х годов атомную массу определяли таким образом, чтобы изотоп кислород-16 имел атомную массу 16 (кислородная шкала). Однако соотношение кислорода-17 и кислорода-18 в природном кислороде, который также использовался в расчётах атомной массы, приводило к наличию двух разных таблиц атомных масс. Химики использовали шкалу, основанную на том, что естественная смесь изотопов кислорода должна была иметь атомную массу 16, тогда как физики присваивали то же число 16 атомной массе наиболее распространённого изотопа кислорода (имеющего восемь протонов и восемь нейтронов).
Относительная атомная масса элемента
Абсолютные массы атомов Одним из фундаментальных свойств атомов, является их масса. Абсолютная (истинная) масса атома – величина чрезвычайно малая. Взвесить атомы на весах невозможно, поскольку таких точных весов не существует. Их массы были определены с помощью расчетов.
Например, масса одного атома водорода равна 0,000 000 000 000 000 000 000 001 663 грамма!
Масса атома урана – одного из самых тяжелых атомов, составляет приблизительно 0,000 000 000 000 000 000 000 4 грамма. Записывать и читать эти числа непросто; можно ошибиться, пропустив ноль или добавить лишний. Существует другой способ записи – в виде произведения: 4 ∙ 10−22 (22 – количество нулей в предыдущем числе).
Точное значение массы атома урана – 3,952 ∙ 10−22 г, а атома водорода, самого легкого среди всех атомов, – 1,673 ∙ 10−24 г. Производить расчеты с малыми числами неудобно. Поэтому вместо абсолютных масс атомов используют их относительные массы.
Относительная атомная масса
О массе любого атома можно судить, сравнивая ее с массой другого атома (находить отношение их масс). С момента определения относительных атомных масс элементов использовались различные атомы в качестве сравнения. Своеобразными эталонами для сравнения в свое время были атомы водорода и кислорода.
Единая шкала относительных атомных масс и новая единица атомной массы, принята Международным съездом физиков (1960) и унифицирована Международным съездом химиков (1961). По сегодняшний день эталоном для сравнения является 1/12 часть массы атома углерода. Данное значение называют атомной единицей массы, сокращенно а.е.м
Атомная единица массы (а.е.м.) – масса 1/12 части атома углерода
Сравним, во сколько раз отличается абсолютная масса атома водорода и урана от 1 а.е.м., для этого разделим эти числа одно на другое:
Полученные при расчетах значения и являются относительными атомными массами элементов – относительно 1/12 массы атома углерода.
Так, относительная атомная масса водорода приблизительно равна 1, а урана – 238. Обратите внимание, что относительная атомная масса не имеет единиц измерения, так как при делении единицы измерения абсолютных масс (граммы) сокращаются. Относительные атомные массы всех элементов указаны в Периодической Системе химических элементов Д.И. Менделеева. Символ, при помощи которого обозначают относительную атомную массу – Аr (буква r – сокращение от слова relative, что означает относительный).
Значения относительных атомных масс элементов используются во многих расчетах. Как правило, значения, приведенные в Периодической Системе, округляются до целых чисел. Обратите внимание, что элементы в Периодической Системе размещены в порядке увеличения относительных атомных масс. Например, при помощи Периодической Системы определим относительные атомные массы ряда элементов:
Ar(Na) = 23;
Относительную атомную массу хлора принято записывать равной 35,5!
Формула, используемая для преобразования:
Атомная масса атомов, ионов или атомных ядер немного меньше суммы масс составляющих их протонов, нейтронов и электронов из-за потери массы энергии связи (на E = mc 2 ).
СОДЕРЖАНИЕ
Относительная изотопная масса
Относительную изотопную массу (свойство отдельного атома) не следует путать со средней атомной массой (см. Выше), то есть средним значением для многих атомов в данном образце химического элемента.
Похожие термины для разных количеств
Атомная масса (относительная изотопная масса) определяется как масса отдельного атома, который может быть только одним изотопом (нуклидом) за раз, и не является средневзвешенным по содержанию, как в случае относительной атомной массы / атомной массы. масса. Следовательно, атомная масса или относительная изотопная масса каждого изотопа и нуклида химического элемента является числом, которое в принципе может быть измерено с высокой точностью, поскольку ожидается, что каждый образец такого нуклида будет точно идентичен любому другому образцу. поскольку ожидается, что все атомы данного типа в одном и том же энергетическом состоянии и каждый образец определенного нуклида будут точно идентичны по массе любому другому образцу этого нуклида. Например, ожидается, что каждый атом кислорода-16 будет иметь точно такую же атомную массу (относительную изотопную массу), что и любой другой атом кислорода-16.
В случае многих элементов, которые имеют один встречающийся в природе изотоп ( мононуклидные элементы ) или один доминирующий изотоп, разница между атомной массой наиболее распространенного изотопа и (стандартной) относительной атомной массой или (стандартной) атомной массой может быть небольшой. или даже nil, и не влияет на большинство массовых вычислений. Однако такая ошибка может существовать и даже быть важной при рассмотрении отдельных атомов для элементов, которые не являются мононуклидами.
Для немононуклидных элементов, которые имеют более одного общего изотопа, численное различие в относительной атомной массе (атомном весе) даже от наиболее распространенной относительной изотопной массы может составлять половину единицы массы или более (например, см. Случай хлора, где атомарный вес) масса и стандартная атомная масса около 35,45). Атомная масса (относительная изотопная масса) необычного изотопа может отличаться от относительной атомной массы, атомного веса или стандартного атомного веса на несколько единиц массы.
Относительные изотопные массы всегда близки к целым числам, но никогда (за исключением случая углерода-12) точно целым числам по двум причинам:
Отношение атомной массы к массовому числу (числу нуклонов) варьируется от 0,998 838 1346 (51) для 56 Fe до 1.007 825 031 898 (14) для 1 H.
Массовые дефекты в атомных массах
Вот некоторые значения отношения атомной массы к массовому числу:
| Нуклид | Отношение атомной массы к массовому числу |
|---|---|
| 1 ч | 1,007 825 031 898 (14) |
| 2 ч | 1,007 050 888 9220 (75) |
| 3 ч | 1,005 349 760 440 (27) |
| 3 Он | 1,005 343 107 322 (20) |
| 4 Он | 1.000 650 813 533 (40) |
| 6 Ли | 1,002 520 481 24 (26) |
| 12 С | 1 |
| 14 с.ш. | 1.000 219 571 732 (17) |
| 16 O | 0,999 682 163 704 (20) |
| 56 Fe | 0,998 838 1346 (51) |
| 210 По | 0,999 918 4461 (59) |
| 232 Чт | 1.000 164 0242 (66) |
| 238 U | 1.000 213 3905 (67) |
Измерение атомных масс
Связь между атомной и молекулярной массами
| Молярная масса of CH 4 | |||
|---|---|---|---|
| Стандартный атомный вес | Число | Общая молярная масса (г / моль) или молекулярная масса (Да или г / моль) | |
| C | 12,011 | 1 | 12,011 |
| ЧАС | 1,008 | 4 | 4,032 |
| CH 4 | 16,043 | ||
| Молекулярная масса 12 C 1 H 4 | |||
| Масса нуклида | Число | Общая молекулярная масса (Da или u) | |
| 12 С | 12.00 | 1 | 12.00 |
| 1 ч | 1,007825 | 4 | 4,0313 |
| CH 4 | 16.0313 | ||
История
В 1860-х годах Станислао Канниццаро уточнил относительные атомные массы, применив закон Авогадро (особенно на Конгрессе в Карлсруэ 1860 года). Он сформулировал закон для определения относительных атомных масс элементов: различные количества одного и того же элемента, содержащиеся в разных молекулах, являются целыми кратными атомному весу, и определил относительные атомные массы и молекулярные массы, сравнивая плотность пара в совокупности газов с молекулы, содержащие один или несколько рассматриваемых химических элементов.
В 20-м веке, до 1960-х годов, химики и физики использовали две разные шкалы атомных масс. Химики использовали шкалу «атомных единиц массы» (а.е.м.), так что естественная смесь изотопов кислорода имела атомную массу 16, в то время как физики присвоили то же число 16 только атомной массе наиболее распространенного изотопа кислорода ( 16 O, содержащий восемь протонов и восемь нейтронов). Однако, поскольку кислород-17 и кислород-18 также присутствуют в природном кислороде, это привело к двум различным таблицам атомных масс. Единая шкала, основанная на углероде-12, 12 C, удовлетворила потребность физиков основывать шкалу на чистом изотопе, будучи численно близкой к шкале химиков. Это было принято как «единая атомная единица массы». Текущая международная система единиц (СИ) рекомендует в качестве названия этой единицы использовать дальтон и символ «Да». Название «единая атомная единица массы» и символ «u» являются признанными названиями и символами для одной и той же единицы.
В 1979 году в качестве компромисса был введен термин «относительная атомная масса» как вторичный синоним атомного веса. Двадцать лет спустя приоритет этих синонимов изменился, и теперь термин «относительная атомная масса» стал предпочтительным.
Однако термин « стандартные атомные веса» (относящийся к стандартным ожидаемым атомным весам различных образцов) не был изменен, поскольку простая замена «атомного веса» на «относительную атомную массу» привела бы к термину «стандартный относительный атомный вес». масса «