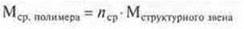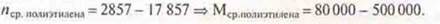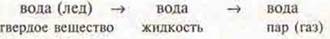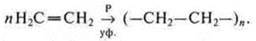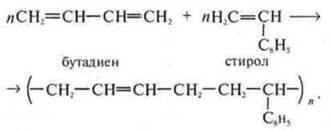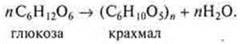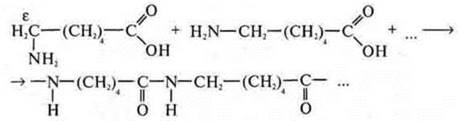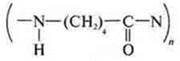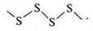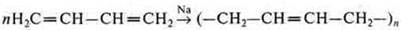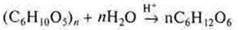Что значит непериодические полимеры
Белки – непериодические полимеры. Строение и свойства аминокислот
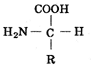 Схема строения аминокислоты Схема строения аминокислоты |
По своей химической природе белки являются непериодическими полимерами. Мономерами белковых молекул являются аминокислоты. Вообще аминокислотой можно назвать любое соединение, содержащее одновременно аминогруппу (–NH2) и группировку органических кислот – карбоксильную группу (–СООН). Число возможных аминокислот очень велико, но белки образуют только 20 так называемых золотых, или стандартных, аминокислот (8 из них являются незаменимыми, т.к. не синтезируются в организмах животных и человека). Именно сочетание этих 20 аминокислот и дает все многообразие белков. После того как молекула белка собрана, некоторые аминокислотные остатки в ее составе могут подвергаться химическим изменениям, так что в «зрелых» белках можно обнаружить до 30 различных аминокислотных остатков (но строятся все белки исходно все равно только из 20!).
В клетке находятся свободные аминокислоты, составляющие аминокислотный фонд, за счет которого происходит синтез новых белков. Этот фонд пополняется аминокислотами, постоянно поступающими в клетку вследствие расщепления пищеварительными ферментами белков пищи или распада собственных запасных белков. В зависимости от аминокислотного состава белки бывают полноценными, содержащими весь набор аминокислот, и неполноценными, в составе которых отсутствуют какие-то аминокислоты.
Общая формула аминокислот изображена на рисунке. В левой части формулы расположена аминогруппа –NH2 а в верхней – карбоксильная группа –СООН. Группа –NH2 имеет основные свойства, группа –СООН – кислотные свойства. Таким образом, аминокислоты – амфотерные соединения, совмещающие свойства кислоты и основания.
Аминокислоты отличаются своими радикалами (R), в роли которых могут быть самые разные соединения. Это обусловливает большое разнообразие аминокислот.
Амфотерными свойствами аминокислот обусловлена их способность взаимодействовать друг с другом. Две аминокислоты соединяются за счет реакции конденсации в одну молекулу путем установления связи между углеродом кислотной и азотом основной групп с выделением молекулы воды.
Образование пептидной связи
Связь, изображенная слева, называется пептидной (от греч. пепсис – пищеварение). Этот термин напоминает нам о том, что эта связь гидролизуется пищеварительным ферментом желудочного сока пепсином. По природе пептидная связь является ковалентной.
Соединение двух аминокислот называется дипептидом, трех – трипептидом и т.д. Примером трипептида может служить белок глютатион, состоящий из остатков глицина, цистеина и глютаминовой кислоты. Он содержится во всех живых клетках (особенно много его в зародыше пшеничного зерна и дрожжах) и активно участвует в обмене веществ.

В основном же белки, входящие в состав живых организмов, включают в себя сотни и тысячи аминокислот (чаще всего от 100 до 300), поэтому их называют полипептидами. Аминокислоты в составе белковой полипептидной цепи называют аминокислотными остатками.
Пептиды различаются числом (n), природой, порядком или последовательностью своих аминокислотных остатков. Их можно сравнить со словами разной длины, в написании которых использован алфавит, состоящий из 20 букв. Из 20 аминокислот можно теоретически получить 1020 возможных вариантов цепей, длиной каждая не менее чем 10 аминокислотных остатков. Белки же, выделенные из живых организмов, образованы сотнями, а иногда и тысячами аминокислотных остатков. В этом кроется источник бесконечного разнообразия белковых молекул, что является важной предпосылкой эволюционного процесса.
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.
Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим.
4.2.4. Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки.
Высокомолекулярными соединениями (ВМС) называют соединения с молекулярной массой более 10000.
Практически все высокомолекулярные вещества являются полимерами.
Полимеры — это вещества, молекулы которых состоят из огромного числа повторяющихся структурных звеньев, соединенных между собой химическими связями.
Полимеры могут быть получены с помощью реакций, которые можно разделить на два основных типа: это реакции полимеризации и реакции поликонденсации.
Реакции полимеризации
Реакции полимеризации — это реакции образования полимера путем объединения огромного числа молекул низкомолекулярного вещества (мономера).
Количество молекул мономера ( n ), объединяющихся в одну молекулу полимера, называют степенью полимеризации.
В реакцию полимеризации могут вступать соединения с кратными связями в молекулах. Если молекулы мономера одинаковы, то процесс называют гомополимеризацией, а если различны — сополимеризацией.
Примерами реакций гомополимеризации, в частности, является реакция образования полиэтилена из этилена:
Примером реакции сополимеризации является синтез бутадиен-стирольного каучука из бутадиена-1,3 и стирола:
Полимеры, получаемые реакцией полимеризации, и исходные мономеры
Мономер
Получаемый из него полимер
Структурная формула
Варианты названия
Структурная формула
Варианты названия
Реакции поликонденсации
Реакции поликонденсации — это реакции образования полимеров из мономеров, в ходе которых, помимо полимера, побочно образуется также низкомолекулярное вещество (чаще всего вода).
В реакции поликонденсации вступают соединения, в состав молекул которых входят какие-либо функциональные группы. При этом реакции поликонденсации по тому, один используется мономер или больше, аналогично реакциям полимеризации делятся на реакции гомополиконденсации и сополиконденсации.
К реакциям гомополиконденсации относятся:
* образование (в природе) молекул полисахарида (крахмала, целлюлозы) из молекул глюкозы:
* реакция образования капрона из ε-аминокапроновой кислоты:
К реакциям сополиконденсации относятся:
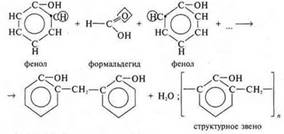
* реакция образования фенолформальдегидной смолы:
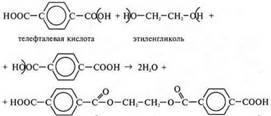
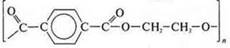
* реакция образования лавсана (полиэфирного волокна):
Материалы на основе полимеров
Пластмассы
Пластмассы — материалы на основе полимеров, которые способны под действием нагревания и давления формоваться и сохранять заданную форму после охлаждения.
Помимо высокомолекулярного вещества в состав пластмасс входят также и другие вещества, однако основным компонентом все же является полимер. Благодаря своим свойствам он связывает все компоненты в единую целую массу, в связи с чем его называют связующим.
Пластмассы в зависимости от их отношения к нагреванию делят на термопластичные полимеры (термопласты) и реактопласты.
Термопласты — вид пластмасс, способных многократно плавиться при нагревании и застывать при охлаждении, благодаря чему возможно многоразовое изменение их изначальной формы.
Реактопласты — пластмассы, молекулы которых при нагревании «сшиваются» в единую трехмерную сетчатую структуру, после чего изменить их форму уже нельзя.
Так, например, термопластами являются пластмассы на основе полиэтилена, полипропилена, поливинилхлорида (ПВХ) и т.д.
Реактопластами, в частности, являются пластмассы на основе фенолформальдегидных смол.
Каучуки
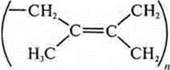
Каучуки — высокоэлластичные полимеры, углеродный скелет которых можно представить следующим образом:
Как мы видим, в молекулах каучуков имеются двойные C=C связи, т.е. каучуки являются непредельными соединениями.
Каучуки получают полимеризацией сопряженных диенов, т.е. соединений, у которых две двойные C=C связи, разделены друг от друга одной одинарной С-С связью.
Так например, особо зарекомендовавшими себя мономерами для получения каучуков являются:
В общем виде (с демонстрацией только углеродного скелета) полимеризация таких соединений с образованием каучуков может быть выражена схемой:
Таким образом, исходя из представленной схемы, уравнение полимеризации изопрена будет выглядеть следующим образом:
Весьма интересным является тот факт, что впервые с каучуком познакомились не самые продвинутые в плане прогресса страны, а племена индейцев, у которых промышленность и научно-технический прогресс отсутствовали как таковые. Естественно, индейцы не получали каучук искусственным путем, а пользовались тем, что давала им природа: в местности, где они проживали (Южная Америка), произрастало дерево гевея, сок которого содержит до 40-50% изопренового каучука. По этой причине изопреновый каучук называют также натуральным, однако он может быть получен и синтетическим путем.
Все остальные виды каучука (хлоропреновый, бутадиеновый) в природе не встречаются, поэтому всех их можно охарактеризовать как синтетические.
Однако каучук, не смотря на свои преимущества, имеет и ряд недостатков. Так, например, из-за того что каучук состоит из длинных, химически не связанных между собой молекул, его свойства делают его пригодным для использования только в узком интервале температур. На жаре каучук становится липким, даже немного текучим и неприятно пахнет, а при низких температурах подвержен затвердеванию и растрескиванию.
Технические характеристики каучука могут быть существенно улучшены его вулканизацией. Вулканизацией каучука называют процесс его нагревания с серой, в результате которого отдельные, изначально не связанные друг с другом, молекулы каучука «сшиваются» друг с другом цепочками из атомов серы (полисульфидными «мостиками»). Схему превращения каучуков в резину на примере синтетического бутадиенового каучука можно продемонстрировать следующим образом:
Волокна
Волокнами называют материалы на основе полимеров линейного строения, пригодные для изготовления нитей, жгутов, текстильных материалов.
Классификация волокон по их происхождению
Искусственные волокна (вискозу, ацетатное волокно) получают химической обработкой уже существующих природных волокон (хлопка и льна).
Синтетические волокна получаются преимущественно реакциями поликонденсации (лавсан, капрон, нейлон).
Введение в технологию переработки полимеров. Часть 2
1. Введение
1.1. Статистические данные
Рис. 1.1 Мировой рынок производства сырья.
Более 18000 различных видов полимеров, доступных сейчас на рынке США, могут быть разделены на 2 группы : термореактивные и термопластичные полимеры. Из более чем 31 миллиона тонн полимеров, произведенных в США в 1993 году 90% составили термопласты. Рисунки 1.2 и 1.3 показано процентное распределение производимых в США термопластов и термореактопластов соответственно. Каждый вид разделен на наиболее общие типы. Среди термопластов полиэтилен является наиболее широко используемым полимерным материалом, его производство в Америке составляет 41% от всех термоплатичных полимеров.
Табл. 1.1 Мировое потребление пластмасс на душу населения, кг.
| Область | 1980 | 2002 | 2010 | Ежегодное изменение % (2002-2010) |
| Во всем мире | 10 | 26 | 37 | 4.5 |
| США | 45 | 105 | 146 | 4.2 |
| Латинская Америка | 7.5 | 20.5 | 30.5 | 5.1 |
| Европа | 40 | 97 | 136 | 4.3 |
| Восточная Европа | 8.5 | 12.5 | 24 | 8.5 |
| Япония | 50 | 85 | 108 | 3.0 |
| Юго-Восточная Азия | 2 | 14.5 | 24 | 6.5 |
| Африка Ближний Восток | 3 | 8 | 10 | 2.8 |
Рис. 1.2 Соотношение производимых Соединенными Штатами термопластов.
Рис. 1.3 Соотношение производимых Соединенными Штатами термореактопластов
Рис. 1.4 Применение термопластов
Рис. 1.5 Применение термореактопластов
Табл. 1.2 Потребление пластмасс на душу населения в США.
| Рейтинг | Штат | Число рабочих, занятых в отрасли |
| 1 | Калифорния | 137,800 |
| 2 | Огайо | 112,100 |
| 3 | Мичиган | 95,300 |
| 4 | Техас | 94,900 |
| 5 | Иллинойс | 89,100 |
| 6 | Пенсильвания | 74,400 |
| 7 | Индиана | 70,000 |
| 8 | Нью-Йорк | 52,800 |
| 9 | Северная Королина | 51,700 |
| 10 | Висконсин | 50,900 |
Транспортный сектор является наиболее активно развивающейся областью применения как термопластичных, так и термореактивных материалов. В одних только Соединенных Штатах Америки на долю пластмасс в промышленности приходится 310 миллиардов долларов. Пластмассы обеспечивают работой 1,4 миллиона человек. В таблице 1.2 приведены 10 штатов США с наибольшим количеством персонала. На эту десятку лучших работает почти 60% всех занятых в пластмассовом производстве рабочих Америки.
1.2. Виды полимеров и пластмасс
Рис. 1.6 Классификация, подразделение и происхождение пластмасс
Та часть молекул полукристаллического полимера, которая не перешла в упорядоченное состояние образует небольшие аморфные участки. Эти участи теряют свою текучесть при температуре ниже температуры стеклования. Температура стеклования большинства полукристаллических полимеров меньше нуля, поэтому при комнатной температуре они ведут себя как резина или кожа. С другой стороны термореактопрасты могут затвердевать при химическом воздействии. При этом макромолекулы сшиваются, образуя сетку из молекул, которые не могут перемещаться относительно друг друга. Образование сеток приводит к потере материалом текучести даже при повторном нагревании. Высокая плотность сшивки молекул делает термореактивный материал жестким и ломким. Они также имеют температуру стеклования. В сравнении с треморективными материалами эластомеры лишь слегка сшиты, так что молекулы могут вытягиваться практически во всю длину. В то же время, связи молекул препятствуют их взаимному скольжению, делая даже большие деформации обратимыми. Общей характеристикой всех эластомеров является то, что их температура стеклования намного ниже комнатной температуры. И их способность течь теряется при вулканизации или сшивке.
При комнатной температуре, которая значительно выше температуры стеклования эластомеров, эти полимеры очень мягки и представляют собой очень податливый эластичный материал.
1.3. Сокращенные названия полимеров
В промышленности полимеры разделяют по химической природе и присваивают аббревиатуры, основанные на химическом строении. Однако часто специалисты используют для описания не стандартные сокращения, а названия торговых марок данных производителем, см табл.1.3
Таблица 1.4. Основные характеристики полимера и их обозначение.
| Символ | Характеристика материала |
| A | Аморфный |
| В | Блоксополимер |
| BO | Двухосно ориентированнный |
| С | Хлорированный |
| CO | Сополимер |
| E | Вспененный |
| G | Привитой сополимиризацией |
| H | Гомополимер |
| HC | Высококристаллический |
| HD | Высокой плотности |
| HI | High impact |
| HMW | Высокомолекулярный |
| I | Impact |
| LD | Низкой плотности |
| LLD | Линейный низкой плотности |
| (M) | Metallocene catalyzed |
| MD | Средней плотности |
| О | Ориентированный |
| P | Пластифицированный |
| R | Randomly polymerized |
| U | Непластифицированный |
| UHMW | Ультра высокомолекулярный |
| ULD | Крайне низкой плотности |
| VLD | Очень низкой плотности |
| X | Сшитый |
| XA | Сшитый пероксидными мостиками |
| XC | Electrically cross-linked |
В Табл. 1.5 представлены основные пластификаторы и их обозначение.
Таблица 1.5.основные пластификаторы и их обозначение
| Сокращение | Химическое название англ | Химическое название русское |
| DODP | Dioctyldecylphthalate | Диоктилдецилфталат |
| ASE | Alkylsulfone acid ester | Сложный эфир алкилсульфоновой кислоты |
| BBP | Benzylbutylphthalate | Бензилбутилфталат |
| DBA | Dibutyladipate | Дибутиловый эфир адипиновой кислоты |
| DBP | Dibutylphthalate | Дибутилфталат |
| DBS | Dibutylsebacate | Дибутилсебацинат |
| DCHP | Dicyclohexylphthalate | Дициклогаксилфталат |
| DEP | Diethylphthalate | Диэтилфталат |
| DHXP | Dihexylphthalate | Дигексилфталат |
| DD3P | Diisobutylphthalate | Диизобутилфталат |
| DIDP | Diisodecylphthalate | Диизодецилфталат |
| DINA | Diisononyladipate | Диизонаниладипат |
| DMP | Dimethylphthalate | Диметилфталат |
| DMS | Dimethylsebazate | Диэтилсебацилат |
| DNA | Dinonyladipate | Динониладипат |
| DNODP | Di-n-octyl-n-decylphthalate | Ди-н-октил-н-децилфталат |
2. Материаловедение полимеров
2.1. Структура полимеров
2.1.1. Химия
В таблице 2.1 представлена классификация полимеризации и конкретные примеры.
Полимеры.
Полимеры — высокомолекулярные соединения
Полимеры — вещества с очень большой молекулярной массой, содержащие многократно повторяющуюся группировку атомов.
По способу получения полимеры бывают:
природные — растительного происхождения (целлюлоза, крахмал), животного происхождения (белки, нуклеиновые кислоты, натуральный каучук), минеральные (минералы, горные породы, волокно асбест);
химические — химические полимеры, полученные переработкой природного полимера, называют искусственными (эфиры, целлюлозы), а химические полимеры, полученные синтезом, называют синтетическими (полиэтилен, полипропилен, капрон).
По свойствам и применению полимеры разделяют на пластмассы, эластомеры, волокна.
Какое строение имеют полимеры? Все полимеры синтезируются из мономеров.
Мономер — низкомолекулярное вещество, из которого в результате синтеза образуется ВМС.
Требования к мономеру:
1) наличие кратной связи одной или нескольких.
Пример. Н2С=СН2 — этилен, синтез полиэтилена.
2) наличие таких функциональных групп, которые взаимодействуют между собой.
Пример. 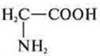
Функциональные группы —СООН и —NH2, способны взаимодействовать друг с другом. Синтез белка, капрона.
Структурное звено — группа атомов, многократно повторяющаяся в макромолекуле ВМС. Структурное звено сходно с мономером по составу, но различно по строению.
Пример: мономер полиэтилена Н2С=СН2.
Структурное звено полиэтилена —СН2—СH2—.
Степень полимеризации — число, которое показывает количество структурных звеньев в макромолекуле (сколько мономеров соединены в макромолекуле в полимерах) обозначается n, n— величина не постоянная, как правило средняя, поэтому молекулярная масса полимера средняя Мср.
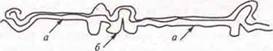
Геометрическая структура макромолекулы — форма макромолекулы — зависит от строения основной цепи и может быть:
а) линейной: 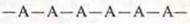
б) разветвленной: 
в) пространственной (сетчатой, сшитой):
Пример: резина, макромолекулы линейные «сшиты» между собой при помощи атомов серы.
Стереорегулярные полимеры образуются в том случае, если макромолекулы ВМС построены из структуры звеньев одинаковой пространственной конфигурации или структуры звеньев с разной пространственной конфигурацией, но чередующихся в цепи с определенной периодичностью.
Нестереорегулярные полимеры образуются, если структурные звенья с разной конфигурацией чередуются произвольно.
Полимеры могут иметь кристаллическое и аморфное строение.
Под кристалличностью полимера понимается упорядоченное (параллельное) расположение макромолекул.
Аморфное строение характеризуется отсутствием упорядоченности макромолекул. Следует отметить, что одни и те же молекулы проходят через кристаллические и аморфные области полимера. У полимера важной характеристикой является степень кристалличности.
Пример: полиэтилен высокого давления — 50—65%; полиэтилен низкого давления — 75—90%.
а — участок кристаллического строения полимера;
б — участок аморфного строения полимера.
Как правило, полимеры твердые, имеющие определенную степень кристалличности и аморфности, что в дальнейшем характеризует их свойства. ВМС не имеет определенной температуры плавления.
Пример: полиэтилен высокого давления от 105—108 °С;
полиэтилен низкого давления от 120—130°С.
При более высокой температуре полимер не перегоняется, а начинает разлагаться и гореть. Полиэтилен вначале размягчается, приобретает прозрачный цвет, затем при дальнейшем повышении температуры плавится, а затем разлагается, горит голубым пламенем, появляется запах горящей свечи, горение продолжается и вне пламени (линейная структура полиэтилена). Если у полимера пространственная структура, он при нагревании сразу разлагается, не переходя в вязкотекучее состояние, и начинают гореть продукты его разложения (пластмассы на основе феноло-формальдегидной смолы).
Вопрос. Почему полимеры не подвергаются перегонке?
Ответ. Чтобы вещество расплавилось и испарилось:
необходимо преодолеть силы межмолекулярного взаимодействия (водородные связи).
Вода — низкомолекулярное вещество при нагревании льда, разрушаются межмолекулярные водородные связи в кристаллах, вода становится жидкой, при дальнейшем нагревании разрушаются водородные связи в ассоциатах воды, она переходит в газообразное состояние.
ВМС межмолекулярные силы взаимодействия значительно сильнее, т.к. в отличие от низкомолекулярных веществ они притягиваются друг к другу огромным числом звеньев.
Когда полимер нагревают, он вначале размягчается, это значит, что силы взаимодействия между некоторыми макромолекулами уже ослаблены так, что вследствие теплового движения они могут перемещаться относительно друг друга. Более крупные макромолекулы вещества взаимодействуют между собой еще сильнее, и чтобы приобрести такую подвижность они требуют дальнейшего нагревания. В этом причина того, что полимеры не имеют определенной точки плавления. Для того чтобы осуществить перегонку вещества, необходимо его нагреть до более высокой температуры. Большие макромолекулы стали бы летучи при очень сильном нагревании. Но они не выдерживают этого, химические связи между атомами начинают рваться и разложение вещества наступает раньше, чем его перегонка.
Большинство полимеров трудно растворить в органических растворителях все по той же причине. Трудно разъединить макромолекулы низкомолекулярными растворителями. В полимерах линейной структуры это еще возможно. А вот если сетчатого пространственного строения ВМС, то молекулы растворителя могут только проникнуть в полимер, что приводит к его набуханию (резина). Все это связано с огромными силами межмолекулярного взаимодействия макромолекул.
Так же объясняется и высокая механическая прочность ВМС. Все полимеры инертны в агрессивных средах — кислотах, щелочах сильнейших окислителях, а также устойчивы к воздействию окружающей среды. Полимеры имеют невысокую плотность, их отличает легкость.
Для правильного обращения с полимерами необходимо знать отношение к нагреванию их макромолекул. Различают термопластичные и термореактивные полимеры.
Термопластичные полимеры при нагревании размягчаются и в этом состоянии легко изменяют форму. При охлаждении они снова затвердевают, сохраняя приданную форму. При следующем нагревании они снова размягчаются и им можно придать новую форму. Макромолекулы не претерпевают изменений при нагревании.
Пример: полиэтилен, полипропилен, капрон и т. д.
Термореактивные полимеры при нагревании становятся пластичными, но затем утрачивают пластичность, становятся неплавкими, нерастворимыми, т. к. происходит взаимодействие линейных макромолекул с образованием пространственной структуры полимера. Повторно переработать такое изделие уже невозможно.
Пример: полимеры на основе феноло-формальдегидной смолы.
Рассмотрим некоторые реакции синтеза полимеров.
Реакция полимеризации — процесс соединения множества молекул мономеров в крупные молекулы — макромолекулы, т. е. образование высокомолекулярного соединения. В реакции полимеризации участвуют мономеры с кратными связями, различают гомополимеризацию, А + А + А — участвуют мономеры одного вещества — и гетерополимеризацию А—В—А—В — участвуют мономеры разных веществ.
Пример: реакция гомополимеризации, синтез полиэтилена:
Пример: реакция гетерополимеризации (сополимеризации), синтез бутадиен-стирольного каучука:
Реакция поликонденсации — химический процесс соединения исходных молекул мономеров в макромолекуле, идущий с образованием побочного низкомолекулярного вещества (чаще воды).
Мономеры для реакции поликонденсации должны иметь функциональные группы, взаимодействующие между собой. Различают реакцию гомополиконденсации — синтез крахмала, капрона.
Пример: синтез крахмала.
Пример: синтез капрона из е-аминокапроновой кислоты.
Структурное звено капрона:
Синтез фенолоформальдегидной смолы, волокна лавсан.
Пример: синтез фенолоформальдегидной смолы:
Пример: синтез волокна лавсан:
Структурное звено:
Примером неорганического полимера может быть пластическая сера Sn; структурное звено — атом серы, главная цель макромолекулы — неорганическая:
Следует сделать вывод, что понятие полимер — универсальное.
Полимеры бывают не только органические, но и неорганические. Углерод образует соединения: алмаз, графит, карбин, фуллерен, кремний кристаллический. Все эти полимеры имеют атомную структуру. Но есть и сложные вещества с атомной структурой — полимеры: оксид кремния (SiO2) и его разновидности: кварц, кремнезем, горный хрусталь. Алюмосиликаты — два полимера вместе.
Следует отметить, что кремний — второй по распространенности элемент в природе (после кислорода) — 27,6 % от массы земной коры. Его соединения: силикаты, алюмосиликаты — составляют 75 % литосферы. К ним относятся около 500 минералов, в том числе породообразующие: полевые шпаты, слюды, пироксены (силикаты): песок, глина, асбест, тальк, изумруд, топаз.
К образованию неорганических полимеров наиболее склонны этилены III, IV групп главных подгрупп II, III периода В, Al, Si.
Неорганические полимеры могут иметь макромолекулы в виде гомо- и гетероцепей. Сами макромолекулы линейные, разветвленные, сетчатые.
Пример: алмаз, бор, фосфор горный, карбин (—С≡С—)n, поликумулен (=С=С=С=)n, пластическая сера, полимерное олово — гомоцепные.
Более устойчивые — гетероцепные полимеры, оксид бора содержит фрагменты 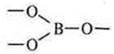
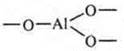
Известно множество элементоорганических полимеров. В основе таких полимеров кремний, фосфор, сера включены в основную или боковые цепи.
Пластмассы. Эластомеры. Волокна. Биополимеры
Пластмассы — конструкционные материалы, содержащие полимер, который при формировании изделия находится в вязкотекучем состоянии, а при его эксплуатации — стеклообразное. Кроме полимера в состав пластмассы входят компоненты: пластификаторы, стабилизаторы, красители, наполнители. При нагревании пластмассы приобретают заданную форму.
Наполнители — древесная мука, ткань, асбест, стекловолокно и др. Улучшают механическую прочность, снижают стоимость полимера.
Пластификаторы — высококипящие эфиры. Они повышают эластичность, устраняющие хрупкость.
Стабилизаторы — антиоксиданты, светостабилизаторы. Способствуют сокращению свойств полимеров в процессе их переработки и использования.
Красители сообщают материалу требуемую окраску, товарный вид.
Следует знать, является ли полимер термопластичным или термореактивным. На основе полимеров: полиэтилен, полистирол, поливинилхлорид, полипропилен, полиметилметакрилат — основано производство пластмасс.
Эластомеры (каучуки) — полимерные материалы, способные к высокоэластичным и обратимым деформациям в широком интервале температур.
а) натуральные; б) синтетические.
Каучук (от индейских слов «кау» — дерево, «учу» — плакать, течь) — так майя называли дерево гевея, которое при многократном надрезании коры «плакало» молочным соком — латексом (лат. «жидкость»). Название дерева было перенесено первооткрывателями на скоагулированную из латекса массу — каучук. Многие растения выделяют латекс: одуванчик, фикус.
Важные свойства каучука — эластичность и клеящая способность — лежат в основе его применения для производства резины. Известны и другие области применения каучука — производство непромокаемой ткани, т. к. каучук не пропускает воду и воздух. В 1823 г. К. Макинтош организовал в г. Глазго производство непромокаемой ткани для плащей, пропитанных каучуком. Их стали называть макинтошами. А еще 50 лет назад выяснили, что написанное карандашом легче стирать натуральным каучуком. Стали изготавливать стиральные резинки. Однако при низких температурах каучук становится хрупким, при повышении температуры размягчается. Эти недостатки сказывались на одежде, изготовленной из пропитанной каучуком ткани, она теряла износостойкость. В 1839 г. американец Ч. Гудьир разработал способ вулканизации каучука, в результате которого скрученные молекулы «сшиваются в структуру пространственного строения» — «объемную». Образуется резина. В отличие от каучука она в растворителях набухает, но при перепаде температуры не изменяется по свойствам.
Формула натурального каучука:
В 1910 г. С.В. Лебедев получил первый каучукоподобный полимер из дивинила.
Сырьем для дивинила явился этиловый спирт.
В начале 30-х годов создано промышленное производство синтетического каучука. На данный момент производят каучуки изопреновые, бутадиеновые, бутадиен-стирольные, хлоропреновые, полиуретановые, силиконовые, акриловые, этиленпропиленовые и т. д.
Многие из них применимы для изготовления имплантантов:
— кости и суставы — полиакрилаты; полиуретаны;
— суставы пальцев рук — полисилоксаны, полиэтилен;
— сердце и его части — полиуретаны; полисилоксаны и т.д.
— кровеносные сосуды — полипропилен, политетрафтор этилен. Учащиеся знакомятся с эластомерами из коллекции «Пластмассы», «Эластомеры»; описывают внешний вид.
Волокна — это гибкие и прочные ВМС ограниченной длины и малых поперечных размеров, пригодные для изготовления пряжи и текстильных изделий.
— растительного происхождения — хлопок, лен, конопля;
— животного происхождения — шерсть, шелк; и нереального происхождения — асбест;
— искусственные — ацетатное, вискозное;
— синтетические — капрон, лавсан, нитрон, полипропилен.
Учащиеся рассматривают ткани на основе волокон: хлопчатобумажного (хлопка); шерсти, ацетата, вискозы, лавсана. Описывают их внешний вид.
Биополимеры — ВМС живой природы.
а) полисахариды: крахмал, целлюлоза. Признак полисахаридов — подвергаются гидролизу:
Строение макромолекул обеспечивает свойства: линейные (целлюлоза) не растворяются в Н2О из-за прочного межмолекулярного взаимодействия; разветвленные (крахмал) не растворяются в воде, склонны к образованию гелей.
Полисахариды имеют огромную роль в клетке: энергетический резерв, опорная форма: биологически активные вещества, огромная пищевая ценность;
б) белки — ВМС, синтезируются в клетках. Мономерами являются аминокислоты. Известно, что полипептидная цепь белка (первичная структура) закручена в спираль (вторичная структура), эта спираль свернута в клубок (третичная структура). И если несколько третичных структур объединяются в одну крупную структуру — это четвертичная структура, обладающая биологической активностью.
Белковые молекулы бывают фибриллярные — волокноподобные и глобулярные — в виде шарика.
Молекулы фибриллярных белков вытянуты в длину, группируются одна возле другой, образуя за счет водородных связей супер-спирали, напоминающие канаты или кабели. Они не растворимы в воде, это конструкционный материал клеток (каротин волос, ногтей, перьев, коллаген сухожилий, мышц). Молекулы глобулярных белков соединены в компактные клубочки, растворимы в воде, в разбавленных кислотах, щелочах, солях, но осаждаются в концентрированных растворах. Они участвуют в регуляции жизненных процессов клетки (гемоглобин, фермент, гормоны).
Свойства белка: гидролиз до простых белков и до аминокислот, денатурация — разрушение их структур.
Цветные реакции: биуретовая — красно-фиолетовое окрашивание при приливании раствора щелочной Сu(ОН)2 в щелочной среде. Реакция на пентидную связь.
в) нуклеиновые кислоты — биополимеры, мономерами которых служат остатки нуклеотидов. Известны две нуклеиновые кислоты. ДНК — дезоксирибонуклеиновая кислота, носитель информации о структуре белка, в ядре клетки в хромосомах. РНК — рибонуклеиновая кислота и в ядре и в цитоплазме, отвечает за передачу информации о структуре белка с ДНК и РНК, транспортировку аминокислот Т—РНК, Р—РНК (рибосомальная).
ДНК — двойная спираль, азотистые основания; аденин—тимин, гуанин—цитозин, сахар—дезоксирибоза. Отвечает за хранение наследственной информации.
РНК — одна спираль, азотистые основания: аденин—урацил, гуанин—цитозин, сахар—рибоза.
Макромолекулы ДНК и РНК — это гигантские углеводно-фосфатные цепи с присоединенной к ним «бахромой» азотистых оснований. Постоянный состав и комплементарность цепей молекулы ДНК в ее спирали определяет ее уникальную и фундаментальную биохимическую роль — быть хранителем всей совокупности генетической информации в каждой клетке и организме в целом. Следует знать, что состав ДНК постоянен для всех клеток данного организма в любом возрасте и в любых физиологических условиях. Он заметно отличается для различных биологических видов. Последовательность и число азотистых оснований в полинуклеотидной цепи также носит индивидуальный характер для каждого организма.