Что такое no3 в химии
Нитрат
Устаревшее название — селитры — в настоящее время используется преимущественно в минералогии, как название для минералов, а также для удобрений в сельском хозяйстве.
Содержание
Общие химические свойства
Нитраты получают действием азотной кислоты HNO3 на металлы, оксиды, гидроксиды, соли. Практически все нитраты хорошо растворимы в воде.
Нитраты устойчивы при обычной температуре. Они обычно плавятся при относительно низких температурах (200—600°C), зачастую с разложением.
Нитраты щелочных металлов разлагаются до нитритов с выделением кислорода (а при длительном нагревании ступенчато разлагаются на оксид металла, молекулярные азот и кислород, ввиду чего являются хорошими окислителями).
Нитраты металлов средней активности разлагаются при нагревании до оксидов металлов с выделением диоксида азота и кислорода.
Нитраты самых малоактивных металлов (благородные металлы) разлагаются в основном до свободных металлов с выделением диоксида азота и кислорода.
Нитраты являются достаточно сильными окислителями в твёрдом состоянии (обычно в виде расплава), но практически не обладают окислительными свойствами в растворе, в отличие от азотной кислоты.
Применение
Биологическая роль
Соли азотной кислоты, которые являются элементом минеральных удобрений. Растение использует азот из соли для построения клеток организма, создания хлорофила. Для людей нитраты не ядовиты, но в организме первращаются в нитриты.
См. также
Полезное
Смотреть что такое «Нитрат» в других словарях:
НИТРАТ — НИТРАТ, нитрата, муж. (от греч. nitron селитра) (хим.). Соль азотной кислоты. Накопление нитратов в почве имеет большое значение для полевых культур. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
нитрат — нитрата, м. [от греч. nitron – селитра] (хим.). Соль азотной кислоты. Большой словарь иностранных слов. Издательство «ИДДК», 2007 … Словарь иностранных слов русского языка
нитрат — Соль или эфир азотной кислоты [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN nitrate … Справочник технического переводчика
нитрат — Природная соль азотной кислоты, хорошо растворимая в воде и широко представленная в почвах, образуется биогенным путем и в результате окисления азота атмосферы, используется как удобрение … Словарь по географии
нитрат — Азот кислотасы тозы. НИТРАТ КИСЛОТАСЫ – Азот кислотасы (HNO3) … Татар теленең аңлатмалы сүзлеге
нитрат — nitratai statusas T sritis ekologija ir aplinkotyra apibrėžtis Nitrato (azoto) rūgšties (HNO₃) druskos. Vandenyje gerai tirpstantys kristalai. Amonio nitratas, natrio nitratas, kalio nitratas ir kalcio nitratas vadinami salietromis ir naudojami… … Ekologijos terminų aiškinamasis žodynas
нитрат — нитрат, нитраты, нитрата, нитратов, нитрату, нитратам, нитрат, нитраты, нитратом, нитратами, нитрате, нитратах (Источник: «Полная акцентуированная парадигма по А. А. Зализняку») … Формы слов
нитрат — азотнокислая соль … Cловарь химических синонимов I
Нитраты
Устаревшее название — селитры — в настоящее время используется преимущественно в минералогии, как название для минералов, а также для удобрений в сельском хозяйстве.
Содержание
Общие химические свойства
Нитраты получают действием азотной кислоты HNO3 на металлы, оксиды, гидроксиды, соли. Практически все нитраты хорошо растворимы в воде.
Нитраты устойчивы при обычной температуре. Они обычно плавятся при относительно низких температурах (200—600 °C), зачастую с разложением.
Разложение нитратов (термолиз нитратов)
Соли азотной кислоты при нагревании разлагаются, причём продукты разложения зависят от положения солеобразующего металла в ряду стандартных электродных потенциалов:
Соли металлов, расположенные в ряду стандартных электродных потенциалов левее Mg (кроме Li)
При разложении образуют нитриты и кислород;
Например: Нитрат натрия при температуре 300 градусов по Цельсию разлагается:
Соли металлов, расположенные в ряду стандартных электродных потенциалов от Mg до Cu (включая Li)
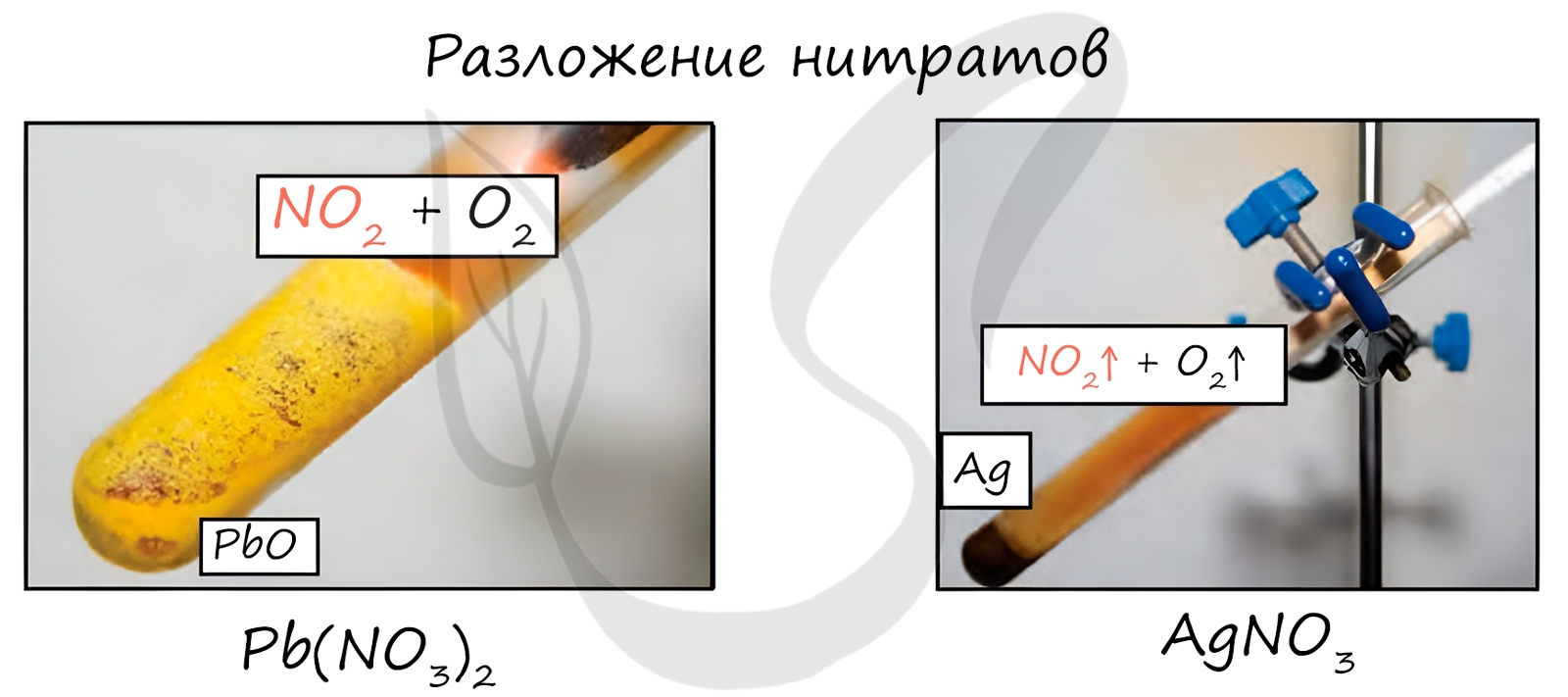
Дают при разложении оксид металла, NO2 и кислород.
Нитрат меди(II) при нагревании разлагается с образованием оксида меди(II) и диоксида азота: 
Соли металлов, расположенные в ряду стандартных электродных потенциалов после Cu
Образуют свободный металл, NO2 и кислород.
Нитрат серебра (аргентум нитрат), разлагается при температуре 170 градусов по Цельсию на свободный металл, диоксид азота и кислород. 
Разложение нитрата аммония (специфические реакции)
Термическое разложение нитрата аммония может происходить по-разному, в зависимости от температуры:
Нитраты являются достаточно сильными окислителями в твёрдом состоянии (обычно в виде расплава), но практически не обладают окислительными свойствами в растворе, в отличие от азотной кислоты.
Применение
Биологическая роль
Соли азотной кислоты, которые являются элементом минеральных удобрений. Растение использует азот из соли для построения клеток организма, создания хлорофилла. Для людей нитраты неядовиты, но в организме превращаются в нитриты.
См. также
Полезное
Смотреть что такое «Нитраты» в других словарях:
НИТРАТЫ — соли азотной кислоты с анионом (NO3), необходимый элемент питания растений. Широко используется в сельском хозяйстве в качестве удобрений и в пищевой промышленности в качестве добавки. Сами по себе нитраты относительно не токсичны, однако в… … Экологический словарь
НИТРАТЫ — НИТРАТЫ, соли азотной кислоты HNO3. Нитраты применяют как удобрения, компоненты ракетных топлив, пиротехнических составов, при крашении тканей, для травления и закаливания металлов и др. Токсичны. Предельно допустимая концентрация нитратов… … Современная энциклопедия
Нитраты — НИТРАТЫ, соли азотной кислоты HNO3. Нитраты применяют как удобрения, компоненты ракетных топлив, пиротехнических составов, при крашении тканей, для травления и закаливания металлов и др. Токсичны. Предельно допустимая концентрация нитратов… … Иллюстрированный энциклопедический словарь
НИТРАТЫ — НИТРАТЫ, ов (спец.). Соли и эфиры азотной кислоты, упор. в технике, медицине, а также (соли) как удобрение. | нитратный, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
Нитраты — соли и сложные эфиры азотной кислоты. Термин этот в русскойхимической номенклатуре обыкновенно не употребляется. П. Р … Энциклопедия Брокгауза и Ефрона
НИТРАТЫ — соли азотной кислоты, образующие в водном растворе при диссоциации аниона N03 ; широко применяются как удобрения (селитры KN03 и NaN03), в производстве взрывчатых веществ (аммониты), чёрного пороха и др … Большая политехническая энциклопедия
нитраты — ов; мн. (ед. нитрат, а; м.). [от греч. nitron селитра] 1. Хим. Соли и эфиры азотной кислоты (применяются в технике, в медицине). // Азотнокислые соли аммония и некоторых металлов; селитры (широко применяются в качестве минеральных удобрений). /… … Энциклопедический словарь
НИТРАТЫ — азотно кислые соли, соли азотной кислоты HNO3. аммония, щелочных и щелочно земельных металлов наз. также селитрами. Нитраты меди применяют в качестве катализатора карбамидно фурановых смол при изготовлении стержней по горячим ящикам … Металлургический словарь
Азотная кислота
Азотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы.
Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.
В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах.
Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты:
Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии выпадения осадка, выделения газа или образования слабого электролита.
При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в темном месте.
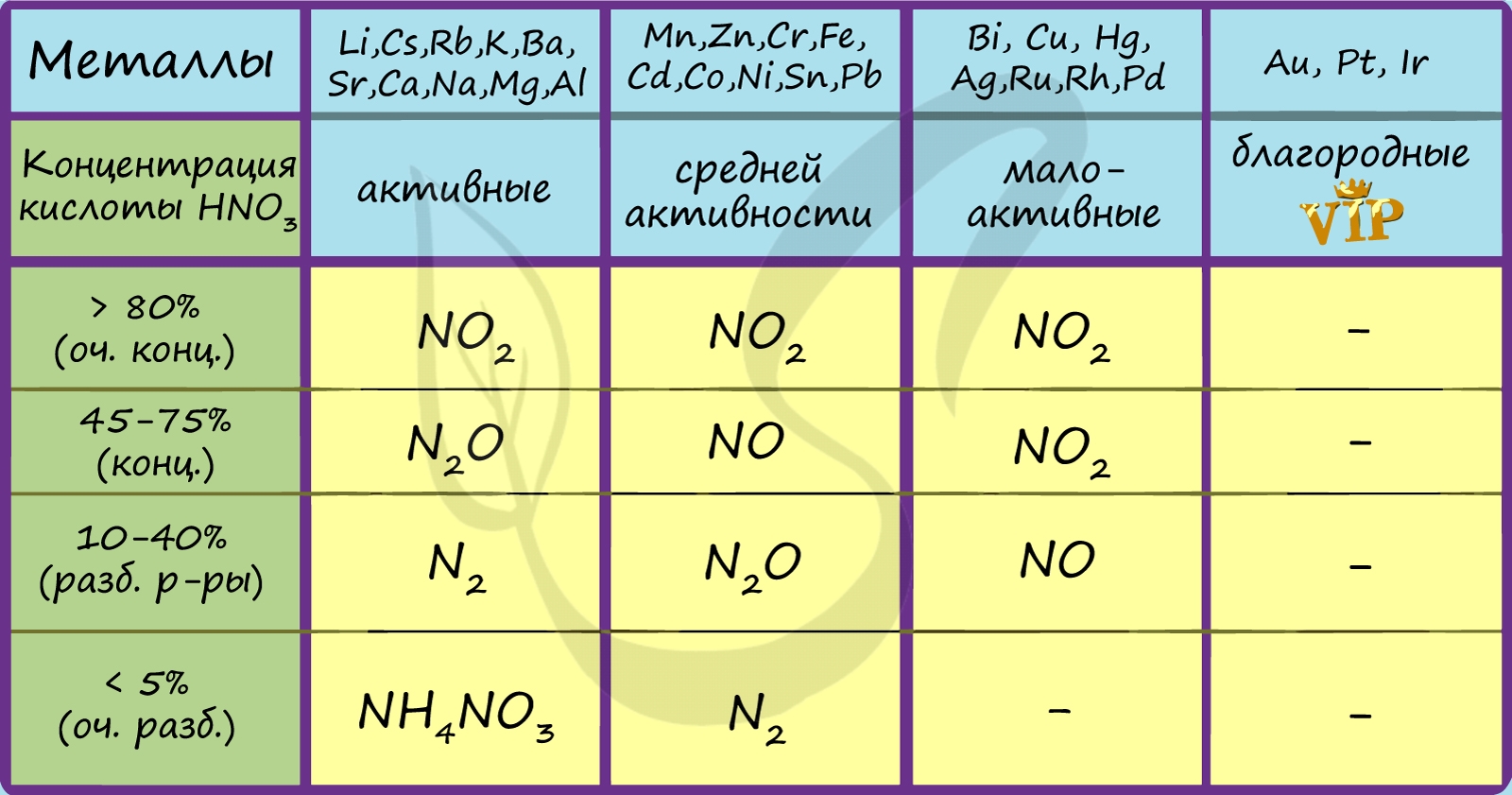
Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием нитрата и преимущественно NO2.
С разбавленной азотной кислотой газообразным продуктом преимущественно является NO.
В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2, NO, N2O, атмосферный газ N2, NH4NO3.
Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка с азотной кислотой в различных концентрациях.
Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности.
Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит за счет оксидной пленки, которой покрыты данные металлы.
Al + HNO3(конц.) ⇸ (реакция не идет)
При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так как оксидная пленка на поверхности металлов разрушается.
Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями.
В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется.
Нитрат аммония получают реакция аммиака с азотной кислотой.
Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).
Нитраты разлагаются в зависимости от активности металла, входящего в их состав.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Нитрат натрия: способы получения и химические свойства
Нитрат натрия NaNO3 — соль щелочного металла натрия и азотной кислоты. Белое вещество, весьма гигроскопичное, которое плавится без разложения, при дальнейшем нагревании разлагается.
Относительная молекулярная масса Mr = 84,99; относительная плотность для тв. и ж. состояния d = 2,266; tпл = 306,5º C;
Способ получения
1. Нитрат натрия можно получить путем взаимодействия гидроксида натрия и разбавленной азотной кислоты, образуется нитрат натрия и вода:
2. В результате взаимодействия горячего гидроксида натрия, оксида азота (IV) и кислорода образуется нитрат натрия и вода:
3. В результате реакции между горячим гидроксидом натрия, оксидом натрия (IV) и кислородом, происходит образование нитрата натрия и воды:
4. При комнатной температуре, в результате взаимодействия оксида азота (IV) и натрия образуется нитрат натрия и газ оксид азота (II):
2NO2 + Na = NO↑ + NaNO3
5. При смешивании горячего пероксида водорода и нитрита азота происходит образование нитрата натрия и воды:
Качественная реакция
Качественная реакция на нитрат натрия — взаимодействие с медью при нагревании в присутствии концентрированной кислоты:
1. При взаимодействии с серной кислотой и медью, нитрат натрия образует сульфат натрия, нитрат меди, газ оксид азота и воду:
Химические свойства
1. Hитрат натрия разлагается при температуре 380–500º С с образованием нитрита натрия и кислорода:
2. Н итрат натрия может реагировать с простыми веществами :
NaNO3 + Pb = NaNO2 + PbO
2.2. Нитрат натрия реагирует при комнатной температуре с цинком и разбавленной хлороводородной кислотой с образованием нитрита натрия и воды:
Нитрат натрия
| Нитрат натрия | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Нитрат натрия |
| Традиционные названия | Натриевая селитра |
| Химическая формула | NaNO3 |
| Физические свойства | |
| Отн. молек. масса | 84,99 а. е. м. |
| Плотность | 2,257 г/см³ |
| Термические свойства | |
| Температура плавления | 308 °C |
| Температура разложения | 380 °C |
| Безопасность | |
| Токсичность | соединение не токсично |
Нитрат натрия (NaNO3),натрий азотнокислотный, натриевая селитра) — натриевая соль азотной кислоты. Бесцветные кристаллы с ромбоэдрической или тригональной кристаллической решеткой без запаха. Соленый на вкус.
Содержание
Свойства
Физические свойства
Химические свойства
Реакция с серой проходит с большим выделением света и тепла, таким что стеклянный сосуд, в котором проводится опыт, может расплавиться.
Получение
В лаборатории нитрат натрия можно получить следующими способами:
Также вместо азотной кислоты можно использовать нитрат аммония:
Применение
Применяется как удобрение; в стекольной, металлообрабатывающей промышленности; для получения взрывчатых веществ, ракетного топлива и пиротехнических смесей для придания огню жёлтого цвета. Получается из природных залежей выщелачиванием горячей водой и кристаллизацией; абсорбцией раствором соды окислов азота; обменным разложением кальциевой или аммиачной селитры с сульфатом, хлоридом или карбонатом натрия.