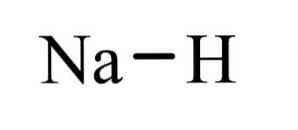Что такое nah в химии
Гидрид натрия: способы получения и химические свойства
Гидрид натрия NaH — неорганическое бинарное соединение щелочного металла натрия и водорода. Белый. При нагревании разлагается, под избыточным давлением H2 плавится без разложения.
Относительная молекулярная масса Mr = 24,00; d = 1,364; tпл = 638º C и избыточном давлении.
Способ получения
Гидрид натрия получают реакцией взаимодействия натрия и водорода:
2Na + H2 = 2NaH
Химические свойства
1. Гидрид натрия — сильный восстановитель. Поэтому он реагирует почти со всеми неметаллами.
1.1. При взаимодействии с кислородом при температуре выше 230º C гидрид натрия образует гидроксид натрия:
2NaH + O2 = 2NaOH
NaH + Cl2 = NaCl + HCl
1.3. Гидрид натрия реагирует с серой при температуре 350–400º C с образованием сульфида натрия и сероводорода:
2NaH + 2S = Na2S + H2S
1.4. Взаимодействуя с углеродом (графитом) гидрид натрия образует ацетиленид натрия и ацетилен, температура при этом должна быть 350º C:
2. Гидрид натрия взаимодействует со сложными веществами :
2.1. При взаимодействии с водой гидрид натрия образует гидроксид натрия и газ водород:
NaH + H2O = NaOH + H2↑
2.2. С разбавленной хлороводородной кислотой гидрид натрия реагирует образованием хлорида натрия и газа водорода:
NaH + HCl = NaCl + H2↑
2.3.1. Оксидом серы IV при температуре 200–250º C, образуя сульфат натрия и хлороводород:
2.4. Гидрид натрия реагирует с аммиаком при t = 350º C с образованием нитрида натрия и водорода:
2.5. Гидрид натрия может взаимодействовать с различными солями:
2.5.1. При взаимодействии с хлоридом алюминия в присутствии эфира, гидрид лития образует тетрагидроалюминат натрия и хлорид натрия:
4NaH + AlCl3 = Na[AlH4] + 3NaCl
2.5.2. Реагируя с хлоридом титана, гидрид натрия образует титан, хлорид натрия и хлороводородную кислоту:
2NaH + TiCl4 = Ti + 2NaCl + 2HCl
3. Гидрид натрия разлагается при температуре 430–500º C и вакууме, с образованием натрия и водорода:
2NaH = 2Na + H2
Гидрид натрия (NaH) свойства, реакционная способность, опасности и использование
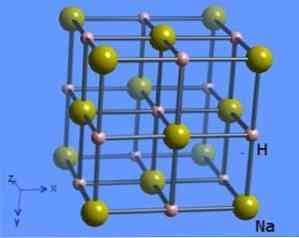
Кристаллическая структура имеет координационное число 6, где каждая молекула натрия окружена 8 ионами гидрида, имеющими октаэдрическую форму, и показана на рисунке 2 (Марк Уинтер [Университет Шеффилда и WebElements Ltd, 1993-2016).
Гидрид натрия продается коммерчески в виде 60% мас. / Мас. Дисперсии (процентное отношение массы к массе) в минеральном масле для безопасного обращения (SODIUM HYDRIDE, s.f.).
Физико-химические свойства гидрида натрия
Гидрид натрия представляет собой белое твердое вещество в чистом виде, хотя обычно его получают в сером или серебристом цвете. Его внешний вид показан на рисунке 3.
NaH имеет молекулярную массу 23,99771 г / моль, плотность 1,396 г / мл и температуру плавления 800 ° C (Royal Society of Chemistry, 2015). Он нерастворим в аммиаке, бензоле, четыреххлористом углероде и сероуглероде (Национальный центр биотехнологической информации, s.f.).
Соединение крайне нестабильно. Чистый NaH может легко воспламениться в воздухе. Когда он вступает в контакт с водой, присутствующей в воздухе, он выделяет легковоспламеняющийся водород.
Когда он открыт для воздуха и влаги, NaH также легко гидролизуется в сильное коррозионное основание гидроксида натрия (NaOH) в соответствии с реакцией:
NaH + H2O → NaOH + H2
В этой реакции можно наблюдать, что гидрид натрия ведет себя как основание. Это связано с электроотрицательностью.
Натрий обладает значительно более низкой электроотрицательностью (≈1,0), чем водород (≈2,1), что означает, что водород извлекает электронную плотность по направлению к себе, удаляясь от натрия, образуя катион натрия и анион гидрида.
Чтобы соединение было кислотой Бренстеда, оно должно отделять электронную плотность от водорода, то есть соединять его с электроотрицательным атомом, таким как кислород, фтор, азот и т. Д. Только тогда он может быть формально описан как H + и может быть диссоциирован как таковой..
Гидрид намного лучше описан как H- и имеет свободную пару электронов. Таким образом, это основание Бренстеда, а не кислота. Фактически, если вы расширите определение кислоты / основания Бренстеда так же, как это сделал Льюис, вы придете к выводу, что натрий (Na +) является кислотным видом здесь..
Продукт реакции кислоты Бренстеда с кислотой-основанием H-основания и H + кислоты превращается в H2. Поскольку кислотный водород извлекается непосредственно из воды, газообразный водород может пузыриться, смещая равновесие, даже если реакция не термодинамически благоприятна.
Можно оставить ионы ОН-, которые можно записать вместе с остальной частью катиона Na +, чтобы получить гидроксид натрия (почему на основе твердого гидрида натрия, а не кислоты при реакции с водой?, 2016).
Реактивность и опасности
Соединение является мощным восстановителем. Атакует SiO2 в стекле. Воспламеняется при контакте с газообразными F2, Cl2, Br2 и I2 (последний при температуре выше 100 ° C), особенно в присутствии влаги, с образованием HF, HCl, HBr и HI.
Он инициирует реакцию полимеризации в этил-2,2,3-трифторпропионате, так что сложный эфир сильно разлагается. Присутствие в реакции диэтилсукцината и этилтрифторацетата, вызвало взрывы (SODIUM HYDRIDE, 2016).
Гидрид натрия считается разъедающим для кожи или глаз из-за потенциальных побочных продуктов едких реакций с водой.
В случае попадания в глаза их следует промыть большим количеством воды под веками не менее 15 минут и немедленно обратиться к врачу..
В случае попадания на кожу, немедленно почистите щеткой и промойте пораженный участок водой. Обратиться к врачу, если раздражение не проходит.
Это вредно при проглатывании из-за реакции на воду. Не вызывайте рвоту. Вам следует немедленно обратиться за медицинской помощью и перевести пострадавшего в медицинский центр..
Дисперсия гидрида натрия в масле не является пылью. Однако материал, который реагирует, может испускать мелкий едкий туман. При вдыхании прополощите рот водой и перенесите пострадавшего в место со свежим воздухом. Следует обратиться за медицинской помощью (Rhom and Hass Inc., 2007).
приложений
Основное использование гидрида натрия заключается в проведении реакций конденсации и алкилирования, которые развиваются в результате образования карбаниона (катализируемого основанием)..
Гидрид натрия в масле напоминает алкоголяты натрия и металла по своей способности действовать в качестве депротонирующего агента в эфире ацетоуксусной кислоты, Кляйзена, Стоббе, Дикмана и других связанных реакциях. Он имеет заметные преимущества перед другими конденсирующими агентами в том, что:
Алкилирование ароматических и гетероциклических аминов, таких как 2-аминопиридин и фенотиазин, легко достигается с высоким выходом при использовании смесей толуол-метилформамид. Концентрация диметилформамида является переменной, используемой для контроля скорости реакции (HINCKLEY, 1957).
Было предложено использовать гидрид натрия для хранения водорода для использования в транспортных средствах на топливных элементах, причем гидрид заключен в пластиковые гранулы, которые измельчаются в присутствии воды для выделения водорода.
Гидрид натрия
| Гидрид натрия | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Гидрид натрия |
| Химическая формула | NaH |
| Эмпирическая формула | NaH |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 23,99777 г/моль |
| Плотность | 1.396 (20 °C) г/см³ |
| Термические свойства | |
| Температура плавления | 800 °C |
| Энтальпия образования (ст. усл.) | -56,4 кДж/моль |
| Классификация | |
| Рег. номер CAS | 7646-69-7 |
Гидри́д на́трия — сложное неорганическое вещество с химической формулой NaH.
Содержание
Описание
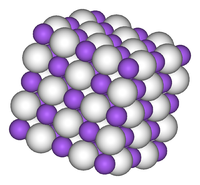
При стандартных условиях гидрид натрия NaH представляет собой бесцветные кубические кристаллы с кристаллической решёткой типа NaCl. Является сильным восстановителем. Воспламеняется в атмосфере некоторых галогенов: фтора, хлора, а также при 230 °C в кислороде. При нагревании до 300 °C в вакууме гидрид натрия NaH разлагается. Реагирует с водой, спиртами, жидким аммиаком, ацетиленом, трифторидом бора, оксидом углерода (IV).
Получение
Химические свойства
1. Взаимодействие с водой:
2. Разложение при сильном нагревании в вакууме:
Применение
Гидрид натрия NaH применяют для очистки железа от магнетита. В органической химии он используется в качестве конденсирующего и полимеризующего агента. Раствор гидрида натрия NaH в гидроксиде натрия NaOH применяют для снятия окалины с тугоплавких металлов и специальных сталей.
Примечания
См. также
Полезное
Смотреть что такое «Гидрид натрия» в других словарях:
гидрид натрия — водородистый натрий … Cловарь химических синонимов I
Гидрид алюминия — Гидрид алюминия … Википедия
Гидрид лития — Общие … Википедия
Гидрид кальция — Гидрид кальция … Википедия
Гидрид калия — K+ H− … Википедия
ГИДРИД — ГИДРИД, химическое соединение водорода с другим ЭЛЕМЕНТАМИ, особенно более электроположительными (которые теряют ЭЛЕКТРОНЫ и образуют положительные ионы). Гидриды электроположительных металлов, такие как гидрид лития (LiH) и гидрид натрия (NaH),… … Научно-технический энциклопедический словарь
Гидрид-ион — Эта статья или раздел нуждается в переработке. Пожалуйста, улучшите статью в соответствии с правилами написания статей. Гидрид ион, отрицательно заряженный ио … Википедия
Гидрид магния — Для улучшения этой статьи желательно?: Дополнить статью (статья слишком короткая либо содержит лишь словарное определение). Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждаю … Википедия
Натрия фосфаты — Известны следующие фосфаты натрия: Дигидрофосфат натрия NaH2PO4 Гидрофосфат натрия Na2HPO4 Ортофосфат натрия Na3PO4 Применение Употребляются для буферных растворов различного назначения, как эмульгаторы в пищевой промышленности … Википедия
Гидрид золота(I) — Общие Систематическое наименование Гидрид золота(I) Химическая формула AuH Физические свойства Состояние (ст. усл.) белый порошок … Википедия
Гидрид натрия — важный реактив для металлургии и химпрома
Гидрид натрия — бинарное неорганическое 
Получают реактив различными способами:
Выпускается химреактив в виде порошкового или гранулированного продукта или суспензии. Ее изготавливают из мелкодисперсионного вещества и жидкого углеводорода, например, минерального масла, вазелина, парафина, бензола, толуола, диметилформамида. Суспензия безопаснее и удобнее в применении. Она не воспламеняется на воздухе, легко дозируется, безопасно перекачивается насосами, долго сохраняет свою консистенцию (расслаивается очень медленно).
 |  |  |
| Бензол «хч» | Гидрид натрия | Диметилформамид «хч» |
Свойства
Кристаллический, очень гигроскопичный, не образующий пыли порошок белого цвета или с легким сероватым оттенком. Структура кристалла подобна структуре кристаллов хлорида натрия (поваренной соли), поэтому физические свойства NaCl и NaH похожи. Разлагается на натрий и водород при нагревании в инертной атмосфере.
Проявляет резко выраженные восстановительные свойства. Нейтрален к металлам, не реагирует с азотом. Бурно реагирует с водой, с выделением газообразного водорода и образованием гидроокиси натрия. Реакция сильно экзотермическая. Самовоспламеняется при взаимодействии с кислородом. Реакции с фторидом бора, фтором, хлором подобны процессу горения. Вступает в реакции со спиртами, аммиаком, окисью углерода, ацетиленом.
Меры предосторожности
Реактив опасен при использовании и требует очень осторожного обращения. Попадание на кожу и в глаза может вызвать химический и термический ожог, особенно если кожа влажная. При проведении опытов с реактивом в лабораториях следует следить, чтобы посуда, реактивы и аппараты были сухими. При взаимодействии с водой выделяется горючий водород и тепло, способствующее самовозгоранию гидрида натрия. Если возник пожар, то его категорически нельзя тушить водой.
При работе с соединением сотрудники должны строго соблюдать технику безопасности, использовать защитные костюмы, очки, лицевые маски и перчатки.
Хранят натрий гидрид в герметичной упаковке и герметично закрывающихся емкостях, в прохладных, хорошо проветриваемых помещениях, вдали от источников тепла и солнечного света. При перевозке транспорт помечается символом опасности F (огнеопасно) и знаком класса опасности 4.3 (не тушить водой, при контакте с водой образует горючие газы).
Водородные соединения: гидриды и их свойства
Способы завершения энергетического уровня
Помимо способов завершения энергетического уровня, существует классификация гидридов, в соответствии с их характером связи. Они подразделяются на 3 большие группы.
Типы гидридов
Стоит рассмотреть основные группы, поскольку побочные группы (полимерные, интерметаллические и комплексные) являются подвидами основных, а также имеют схожие с ними физические и химические свойства.
Ионные гидриды
Ионные (солеобразные) — соединения H2 с металлами IA и IIA (кроме магния), а также с алюминием. Их главное отличие от двух других видов в том, что они активно реагируют с H2O с образованием щёлочи и выделением H2 в виде газа. Самым ярким представителем ионных гидридов является гидрид натрия.
Физические свойства: белые твёрдые вещества с кристаллической решёткой, содержащей катион (плюс) металла и гидрид-анион (минус) Н–. Проводят электрический ток. Устойчивы при нормальных условиях (н.у.).
Как и любое вещество (химический элемент, простое вещество или химическое соединение), ионные гидриды обладают свойствами. Они проявляются в процессе реакции и влияют на неё. Химические свойства:
Применение: для получения металлов из их оксидов, удаления окалины с поверхности металлических изделий, как ракетное топливо.
Получение: при взаимодействии металлов с водородом при t 200-600°С:
Ковалентные соединения
Ковалентные — гидриды, образованные неметаллами IV, V, VI и VII групп, а также бором. Например, гидрид углерода/метан CH4, силан SiH4, гидрид серы/сероводород H2S.
Физические свойства: газообразные, легко воспламеняются на воздухе.
Ковалентные гидриды во многом отличаются от ионных и металлических. Если последние обладают химическими свойствами, схожими с металлами, то свойства ковалентных следует рассмотреть подробнее. Химические свойства:
Применение: для получения полупроводниковых пленочных покрытий, защитных покрытий на поверхности металлов.
Получение: термическое разложение, восстановление галогенидов.
Существуют многочисленные производные ковалентных гидридов, в которых часть атомов H2 замещена атомами галогенов или металлов.
Магний по своим свойствам и химической связи располагается между ионными и ковалентными гидридами. С водой и водными растворами MgH2 реагирует с выделением H2, но не так энергично, как ионные гидриды.
Соединения железа с водородом крайней неустойчивы и в чистом виде не обнаружены. Формула неустойчивого гидрида железа выглядит так: C5H5Fe.
Металлические соединения
Металлические — соединения переходных металлов. Фактически они являются твёрдым раствором H2 в металле, атомы водорода помещаются в кристаллическую решётку металла. Их образованию всегда способствует адсорбция водорода на поверхности металла.
Физические свойства: представляют собой кристаллические вещества с металлическим блеском. Обладают интенсивной окраской, проявляют металлические или полупроводниковые свойства. Устойчивы на воздухе. С кислородом и водой реагируют медленно. Магнитными, механическими, тепло- и электропроводными свойствами схожи с металлами.
Химическая связь очень прочная.
Применение: применяются в качестве источников водорода особой чистоты (который используется в топливных элементах), также для удаления водорода из газовых смесей.
Получение: реакция металла с водородом при обычной температуре или при нагревании: Ti + H2 = (150-200°С) TiH2.
При взаимодействии H2 с интерметаллическими соединениями, такими как TiFe, LaNi5, можно получить гидриды интерметаллидов TiFeH2, LaNi5H6, которые с высокой скоростью обратимо поглощают водород при атмосферном давлении.
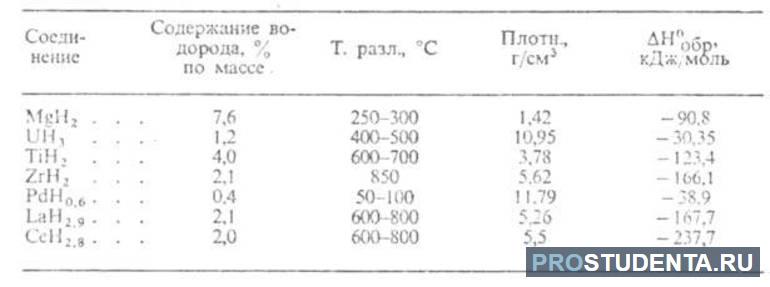
В прикрепленных таблицах указано содержание водорода, температура разложения, плотность и пр., что поможет в более глубоком понимании физических свойств водорода разных типов гидридов.
Особенности водородных соединений
Как и в любом разделе химии, водородные соединения имеют свои исключения. В их числе He, Ne, Ar, Kr, Pm, Os, Ir, Rn, Fr и Ra. Они не образуют бинарные соединения с водородом.
Информация, изложенная выше доказывает то, что химия интереснейший и увлекательный предмет, который стоит потраченного внимания и времени.