Что такое li2o в химии
Оксид лития: способы получения и химические свойства
Оксид лития — это белое, гигроскопичное, тугоплавкое вещество, при нагревании не разлагается.
Относительная молекулярная масса = 29,88; относительная плотность для тв. и ж. состояния = 2, 013; tпл = 1453º C; tкип ≈ 2600º C.
Способ получения
1. Оксид лития можно получить путем взаимодействия лития и кислорода :
2. Оксид лития получается при разложении гидроксида лития:
2LiOН → Li2O + Н2O
3. Путем термического разложения карбоната лития с образованием оксида лития и оксида углерода:
4. При термическом разложении нитрата лития образуется оксид лития, оксид азота и кислород:
Химические свойства
1. Литий вытесняется из оксида в результате взаимодействия с другими металлами :
1.1. Оксид лития взаимодействует с металлами и некоторыми неметаллами с образованием лития и оксида металла:
Li2O + Si = 4Li + SiO2
Li2O + Mg = 2Li + MgO
3Li2O + 2Al = 6Li + Al2O3
2. Оксид лития взаимодействует со сложными веществами:
Li2O + H2O = 2LiOH
2.3. При взаимодействии лития с оксидами образуются соли:
Оксид лития, характеристика, свойства и получение, химические реакции
Оксид лития, характеристика, свойства и получение, химические реакции.
Оксид лития – неорганическое вещество, имеет химическую формулу Li2O.
Краткая характеристика оксида лития:
Оксид лития – неорганическое вещество, без цвета.
Химическая формула оксида лития Li2O.
В воде не растворяется, а вступает в реакцию с ней.
Оксид лития – единственный среди оксидов щелочных металлов, образующийся в качестве основного продукта при нагревании металла выше 200 °C на воздухе (присутствуют только следы пероксида лития).
Физические свойства оксида лития:
| Наименование параметра: | Значение: |
| Химическая формула | Li2O |
| Синонимы и названия иностранном языке | lithium oxide (англ.) |
| Тип вещества | неорганическое |
| Внешний вид | бесцветные кубические кристаллы |
| Цвет | бесцветный |
| Вкус | —* |
| Запах | — |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м 3 | 2013 |
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см 3 | 2,013 |
| Температура кипения, °C | 2600 |
| Температура плавления, °C | 1570 |
| Гигроскопичность | гигроскопичен |
| Молярная масса, г/моль | 29,8774 |
Получение оксида лития:
Оксид лития получается в результате следующих химических реакций:
Химические свойства оксида лития. Химические реакции оксида лития:
1. реакция оксида лития с магнием:
Li2O + Mg → 2Li + MgO (t > 800 o C).
2. реакция оксида лития с магнием и водородом :
Li2O + Mg + H2 → 2LiH + MgO (t = 450-500 o C).
В результате реакции образуется оксид магния и гидрид лития.
3. реакция оксида лития с алюминием :
В результате реакции образуется оксид алюминия и литий.
4. реакция оксида лития с алюминием и водородом:
В результате реакции образуется оксид алюминия и гидрида лития.
5. реакция оксида лития с кремнием :
2Li2O + Si → 4Li + SiO2 (t = 1000 o C).
В результате реакции образуется оксид кремния и литий.
6. реакция оксида лития с водой:
7. реакция оксида лития с оксидом углерода (углекислым газом):
Оксид лития на воздухе реагирует с углекислым газом (являющийся кислотным оксидом), образуя соль – карбонат лития.
8. реакция оксида лития с оксидом кремния:
Оксид кремния также является кислотным оксидом. В результате реакции образуется соль – метасиликат лития.
9. реакция оксида лития с оксидом серы:
Оксид серы также является кислотным оксидом. В результате реакции образуется соль – сульфит лития.
10. реакция оксида лития с оксидом азота (IV) и оксидом азота (II):
В результате реакции образуются соль – нитрит лития.
11. реакция оксида лития с оксидом ванадия:
В результате реакции образуется диоксованадат лития.
12. реакция оксида лития с оксидом теллура:
В результате реакции образуется теллурит лития.
13. реакция оксида лития с оксидом марганца:
В результате реакции образуется оксид марганца-лития.
14. реакция оксида лития с йодоводородом:
15. реакция оксида лития с сероводородом:
16. реакция оксида лития с плавиковой кислотой:
В результате химической реакции получается соль – фторид лития и вода.
17. реакция оксида лития с азотной кислотой:
Аналогично проходят реакции оксида лития и с другими кислотами.
18. реакция оксида лития с бромистым водородом (бромоводородом):
Применение и использование оксида лития:
Примечание: © Фото //www.pexels.com, //pixabay.com
оксид лития реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие оксида лития
реакции с оксидом лития
Мировая экономика
Справочники
Востребованные технологии
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Классификация неорганических веществ
Среди простых веществ выделяют металлы и неметаллы. Среди сложных: оксиды, основания, кислоты и соли. Классификация неорганических веществ построена следующим образом:
Большинство химических свойств мы изучим по мере продвижения по периодической таблице Д.И. Менделеева. В этой статье мне хотелось бы подчеркнуть ряд принципиальных деталей, которые помогут в дальнейшем при изучении химии.
Оксиды
Все оксиды подразделяются на солеобразующие и несолеобразующие. Солеобразующие имеют соответствующие им основания и кислоты (в той же степени окисления (СО)!) и охотно вступают в реакции солеобразования. К ним относятся, например:
Солеобразующие оксиды, в свою очередь, делятся на основные, амфотерные и кислотные.
Основным оксидам соответствуют основания в той же СО. В химических реакциях основные оксиды проявляют основные свойства, образуются исключительно металлами. Примеры: Li2O, Na2O, K2O, Rb2O CaO, FeO, CrO, MnO.
Основные оксиды взаимодействуют с водой с образованием соответствующего основания (реакцию идет, если основание растворимо) и с кислотными оксидами и кислотами с образованием солей. Между собой основные оксиды не взаимодействуют.
Li2O + H2O → LiOH (основный оксид + вода → основание)
Здесь не происходит окисления/восстановления, поэтому сохраняйте исходные степени окисления атомов.
Эти оксиды действительно имеют двойственный характер: они проявляют как кислотные, так и основные свойства. Примеры: BeO, ZnO, Al2O3, Fe2O3, Cr2O3, MnO2, PbO, PbO2, Ga2O3.
С водой они не взаимодействуют, так как продукт реакции, основание, получается нерастворимым. Амфотерные оксиды реагируют как с кислотами и кислотными оксидами, так и с основаниями и основными оксидами.
ZnO + KOH + H2O → K2[Zn(OH)4] (амф. оксид + основание = комплексная соль)
ZnO + N2O5 → Zn(NO3)2 (амф. оксид + кисл. оксид = соль; СО азота сохраняется в ходе реакции)
Fe2O3 + HCl → FeCl3 + H2O (амф. оксид + кислота = соль + вода; обратите внимание на то, что СО Fe = +3 не меняется в ходе реакции)
Проявляют в ходе химических реакций кислотные свойства. Образованы металлами и неметаллами, чаще всего в высокой СО. Примеры: SO2, SO3, P2O5, N2O3, NO2, N2O5, SiO2, MnO3, Mn2O7.
Кислотные оксиды вступают в реакцию с основными и амфотерными, реагируют с основаниями. Реакции между кислотными оксидами не характерны.
SO2 + Na2O → Na2SO3 (кисл. оксид + осн. оксид = соль; сохраняем СО S = +4)
SO3 + Li2O → Li2SO4 (кисл. оксид + осн. оксид = соль; сохраняем СО S = +6)
P2O5 + NaOH → Na3PO4 + H2O (кисл. оксид + основание = соль + вода)
Реакции несолеобразующих оксидов с основаниями, кислотами и солеобразующими оксидов редки и не приводят к образованию солей. Некоторые из несолеобразующих оксидов используют в качестве восстановителей:
FeO + CO → Fe + CO2 (восстановление железа из его оксида)
Основания
Основания классифицируются по количеству гидроксид-ионов в молекуле на одно-, двух- и трехкислотные.
Так же, как и оксиды, основания различаются по свойствам. Все основания хорошо реагируют с кислотами, даже нерастворимые основания способны растворяться в кислотах. Также нерастворимые основания при нагревании легко разлагаются на воду и соответствующий оксид.
Mg(OH)2 → (t) MgO + H2O (при нагревании нерастворимые основания легко разлагаются)
Если в ходе реакции основания с солью выделяется газ, выпадает осадок или образуется слабый электролит (вода), то такая реакция идет. Нерастворимые основания с солями почти не реагируют.
Ba(OH)2 + NH4Cl → BaCl2 + NH3 + H2O (в ходе реакции образуется нестойкое основание NH4OH, которое распадается на NH3 и H2O)
KOH + BaCl2 ↛ реакция не идет, так как в продуктах нет газа/осадка/слабого электролита (воды)
В растворах щелочей pH > 7, поэтому лакмус окрашивает их в синий цвет.
Al(OH)3 + HCl → AlCl3 + H2O (амф. гидроксид + кислота = соль + вода)
Al(OH)3 + KOH → K[Al(OH)4] (амф. гидроксид + основание = комплексная соль)
При нагревании до высоких температур комплексные соли не образуются.
Кислоты
Кислоты отлично реагируют с основными оксидами, основаниями, растворяя даже те, которые выпали в осадок (реакция нейтрализации). Также кислоты способны вступать в реакцию с теми металлами, которые стоят в ряду напряжений до водорода (то есть способны вытеснить его из кислоты).
Zn + HCl → ZnCl2 + H2↑ (реакция идет, так как цинк стоил в ряду активности левее водорода и способен вытеснить его из кислоты)
Cu + HCl ↛ (реакция не идет, так как медь расположена в ряду активности правее водорода, менее активна и не способна вытеснить его из кислоты)
Все кислоты подразделяются на сильные и слабые. Напомню, что мы составили подробную таблицу сильных и слабых кислот (и оснований!) в теме гидролиз. В реакции из сильной кислоты (соляной) можно получить более слабую, например, сероводородную или угольную кислоту.
В завершении подтемы кислот предлагаю вам вспомнить названия основных кислот и их кислотных остатков.
Блиц-опрос по теме Классификация неорганических веществ
Формула оксида лития, свойства, риски и использование
оксид лития неорганическое химическое соединение формулы Li2Или это образуется вместе с небольшими количествами пероксида лития, когда металлический литий сжигается в воздухе и соединяется с кислородом.
До 1990-х годов на рынке металлов и лития доминировало производство в США из месторождений полезных ископаемых, но в начале 21-го века большая часть производства была получена из неамериканских источников; Австралия, Чили и Португалия были самыми важными поставщиками в мире. У Боливии есть половина месторождений лития в мире, но это не большой производитель.
Наиболее важной коммерческой формой является карбонат лития, Li2Колорадо3, производится из минералов или рассолов несколькими различными процессами.
Когда литий сжигается в воздухе, основным продуктом является белый оксид лития, Li2О. Кроме того, некоторое количество перекиси лития производится, Li2О2, также белый.
Это также можно сделать путем термического разложения гидроксида лития, LiOH или пероксида лития, Li2O2.
2LiOH (s) + тепло → Li2O (s) + H2O (г)
Физико-химические свойства
Оксид лития представляет собой белое твердое вещество, известное как лития, которому не хватает аромата и соленого вкуса. Его внешний вид показан на рисунке 2 (Национальный центр биотехнологической информации, 2017).
Рисунок 2: внешний вид оксида лития
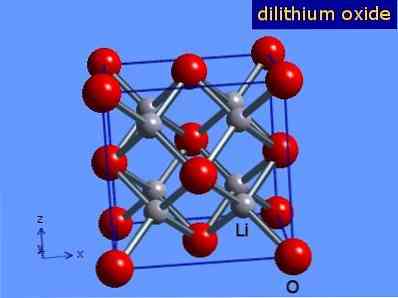
Рисунок 3: кристаллическая структура оксида лития.
Его молекулярная масса составляет 29,88 г / моль, его плотность составляет 2,013 г / мл, а температуры плавления и кипения составляют 1438 ° С и 2066 ° С соответственно. Это соединение очень хорошо растворяется в воде, спирте, эфире, пиридине и нитробензоле (Royal Society of Chemistry, 2015).
Оксид лития легко реагирует с водяным паром с образованием гидроксида и с диоксидом углерода с образованием карбоната; следовательно, он должен храниться и обрабатываться в чистой и сухой атмосфере.
Оксидные соединения не приводят к электричеству. Однако некоторые структурированные оксиды перовскита являются электронными проводниками, которые находят применение в катоде твердооксидных топливных элементов и системах генерации кислорода..
Они представляют собой соединения, которые содержат по меньшей мере один кислородный анион и один металлический катион (American Elements, S.F.).
Реактивность и опасности
Оксид лития является стабильным соединением, несовместимым с сильными кислотами, водой и углекислым газом. Насколько нам известно, химические, физические и токсикологические свойства оксида лития не были исследованы и подробно представлены.
Токсичность соединений лития зависит от их растворимости в воде. Ион лития обладает токсичностью для центральной нервной системы. Соединение обладает сильным коррозионным раздражающим действием при попадании в глаза или на кожу при вдыхании или проглатывании (ESPI METALS, 1993).
В случае попадания в глаза вам следует проверить, носите ли вы контактные линзы, и немедленно снять их. Глаза следует промыть проточной водой не менее 15 минут, держа веки открытыми. Вы можете использовать холодную воду. Мазь не следует использовать для глаз.
Если химическое вещество попало на одежду, удалите его как можно быстрее, защищая свои руки и тело. Поместите жертву под безопасный душ.
Если химическое вещество накапливается на незащищенной коже жертвы, например на руках, аккуратно и осторожно промойте кожу, загрязненную проточной водой и неабразивным мылом. Вы можете использовать холодную воду. Если раздражение не проходит, обратитесь к врачу. Выстирать загрязненную одежду перед повторным использованием.
В случае вдыхания пострадавшему должно быть разрешено отдыхать в хорошо проветриваемом помещении. Если вдыхание серьезное, пострадавшего следует как можно скорее эвакуировать в безопасное место..
Ослабьте тесную одежду, такую как воротник рубашки, ремни или галстук. Если пострадавшему трудно дышать, следует назначить кислород. Если пострадавший не дышит, проводится реанимация из уст в уста.
Всегда принимая во внимание, что человеку, оказывающему помощь в проведении реанимации изо рта в рот, может быть опасно, когда вдыхаемый материал токсичен, инфекционен или вызывает коррозию.
Во всех случаях вам следует немедленно обратиться к врачу (SIGMA-ALDRICH, 2010).
приложений
Оксид лития используется в качестве флюса в керамической глазури и создает синий с медью и розы с кобальтом. Оксид лития реагирует с водой и паром, образуя гидроксид лития и должен быть изолирован от них.
Оксид лития (Li2O) с его высоким потенциалом трития является привлекательным кандидатом на твердый культуральный материал термоядерной электростанции DT из-за его высокой плотности атомов лития (по сравнению с другими литиевыми или металлическими литиевыми керамиками) и его проводимости относительно высокая термическая (ОКСИД ЛИТИЯ (Li2O), SF).
Li2Или он будет подвергаться воздействию высоких температур под действием нейтронного излучения во время работы термоядерных покрытий. В этих условиях большое количество дефектов облучения будет происходить в Li2Или, например, вызванное гелием набухание, относительно высокое тепловое расширение, рост зерна, образование и осаждение LiOH (T) при низких температурах и перенос массы LiOH (T) при высоких температурах.
Кроме того, Ли2Или это будет предметом напряжений, возникающих из-за различий в тепловом расширении между Li2О и конструкционные материалы. Эти характеристики Ли2Или они приводят к сложным инженерным проблемам как при изготовлении, так и при проектировании одеял..
Литий: способы получения и химические свойства
Литий — это щелочной металл, серебристо-белого цвета. Самый легкий из металлов, мягкий, низкая температура плавления.
Литий получают в промышленности электролизом расплава хлорида лития в смеси с KCl или BaCl2 (эти соли служат для понижения температуры плавления смеси):
2LiCl = 2Li + Cl2
Качественная реакция
Химические свойства
Литий — активный металл; на воздухе реагирует с кислородом и азотом, и покрывается оксидно-нитридной пленкой. Воспламеняется при умеренном нагревании; окрашивает пламя газовой горелки в темно-красный цвет.
1.1. Литий легко реагирует с галогенами с образованием галогенидов:
2Li + I2 = 2LiI
1.2. Литий реагирует с серой с образованием сульфида лития:
2Li + S = Li2S
3Li + P = Li3P
2Li + H2 = 2LiH
1.4. С азотом литий реагирует при комнатной температуре с образованием нитрида:
1.5. Литий реагирует с углеродом с образованием карбида:
1.6. При взаимодействии с кислородом литий образует оксид.
2. Литий активно взаимодействует со сложными веществами:
2Li 0 + H2 + O = 2 Li + OH + H2 0
Видеоопыт: взаимодействие щелочных металлов с водой можно посмотреть здесь.
2.2. Литий взаимодействует с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой) со взрывом. При этом образуются соль и водород.
2Li + 2HCl = 2LiCl + H2↑
2.3. При взаимодействии лития с концентрированной серной кислотой выделяется сероводород.
2.4. Литий реагирует с азотной кислотой:
3Li + 4HNO3(разб.) = 3LiNO3 + NO↑ +2H2O
3Li + AlCl3 → 3LiCl + Al