Что такое fe2 so4 3 в химии
Сульфат железа(III)
| Сульфат железа(III) | |
 | |
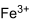   | |
| Общие | |
|---|---|
| Систематическое наименование | сульфат железа(III) |
| Традиционные названия | сернокислое железо(III), тетрасульфид(VI) железа(III) |
| Химическая формула | Fe2(SО4)3 |
| Эмпирическая формула | Fe2O12S3 |
| Физические свойства | |
| Состояние (ст. усл.) | безводный — светло-жёлтый порошок |
| Молярная масса | (безв.) 399.88 г/моль |
(пентагидрат) 489.96 г/моль
(безв.) растворим в разбавленной серной кислоте, ацетоне
15244-10-7 (для всех гидратов с формулой Fe2(SО4)3·nН2О (где n=1, 3, 4, 6, 7, 9, 10, 12)
Содержание
Физические свойства
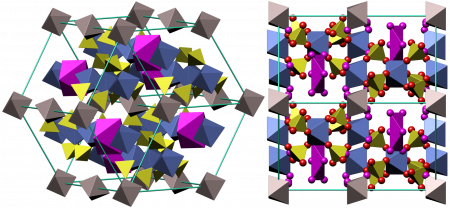
Безводный сульфат железа(III) — светло-желтые, парамагнитные, очень гигроскопичные кристаллы моноклинной сингонии, пространственная группа P21/m, параметры элементарной ячейки a = 0,8296 нм, b = 0,8515 нм,c = 1,160 нм, β = 90,5°, Z = 4. Есть данные, что безводный сульфат железа образовывает орторомбическую и гексагональную модификации. Растворим в воде и ацетоне, не растворяется в этаноле.
Из воды кристаллизуется в виде кристаллогидратов Fe2(SO4)3·n H2O, где n = 12, 10, 9, 7, 6, 3. Наиболее изученный кристаллогидрат — нонагидрат сульфата железа(III) Fe2(SO4)3·9H2O — жёлтые гексагональные кристаллы, параметры элементарной ячейки a = 1,085 нм, c = 1,703 нм, Z = 4. Хорошо растворяется в воде (440 г на 100 г воды) и этаноле, не растворяется в ацетоне. В водных растворах сульфат железа(III) из-за гидролиза приобретает красно-коричневый цвет.
При нагревании нонагидрат превращается при 98 °C в тетрагидрат, при 125 °C — в моногидрат и при 175 °C — в безводный Fe2(SO4)3, который выше 600 °C разлагается на Fe2O3 и SO3.
Нахождение в природе
Все перечисленные выше природные гидраты железа являются непрочными соединениями и в открытом состоянии быстро выветриваются.
Получение
В промышленности сульфат железа(III) получают прокаливанием пирита или марказита с NaCl на воздухе:
или растворяют оксид железа(III) в серной кислоте:
В лабораторной практике сульфат железа(III) можно получить из гидроокиси железа(III):
Препарат той же чистоты можно получить окислением сульфата железа(II) азотной кислотой:
также окисление можно провести кислородом или оксидом серы:

Концентрированные серная и азотная кислоты окисляют сульфид железа до сульфата железа(III):
Дисульфид железа можно окислить концентрированной серной кислотой:
Сульфат-аммоний железа(II) (соль Мора) также можно окислить дихроматом калия. Вследствие данной реакции выделятся сразу четыре сульфата — железа(III), хрома(III), аммиака и калия, и вода:

Сульфат железа(III) можно получить как один из продуктов термического разложения сульфата железа(II):
Ферраты с разбавленной серной кислотой восстанавливаются до сульфата железа(III):
Нагрев пентагидрат до температуры 70—175 °C получим безводный сульфат железа(III):
Сульфат железа(II) можно окислить таким экзотическим окислителем, как оксид ксенона(III):
Химические свойства
Сульфат железа(III) в водных растворах подвергается сильному гидролизу по катиону, при этом раствор окрашивается в красновато-коричневый цвет:


Горячая вода или пар разлагают сульфат железа(III):
Безводный сульфат железа(III) при нагревании разлагается:

Растворы щелочей разлагают сульфат железа(III), продукты реакции зависят от концентрации щёлочи:

Если с щёлочью взаимодействует эквимолярный раствор сульфатов железа(III) и железа(II), то в результате получится сложный оксид железа:
Активные металлы (такие как магний, цинк, кадмий, железо) восстанавливают сульфат железа(III):
Некоторые сульфиды металлов (например, меди, кальция, олова, свинца, ртути) в водном растворе восстанавливают сульфат железа(III):
С растворимыми солями ортофосфорной кислоты образует нерастворимый фосфат железа(III) (гетерозит):
Сульфат Железа
Химическое название
Железа(II) сульфат, сульфат железа (III).
Химические свойства
Двухвалентное сернокислое железо – неорганическое соединение, соль образованная серной кислотой и железом. Вещество не имеет запаха, не летуче. Безводная форма имеет вид бесцветных не прозрачных мелких гигрокопичных кристаллов. Кристаллогидраты имеют характерный зеленовато-голубой окрас, тетрагидраты зеленого цвета. Химическая формула Сульфата Железа 2: FeSO4, рацемическая: O4SFe. На вкус соединение вяжущее, с привкусом металла. Средство хорошо растворяется в воде. Молекулярная масса = 151,9 грамм на моль.
Вещество выделяется из железного купороса. Раствор сульфата Fe(2) под действием кислорода окисляется в переходит в Сульфат Железа 3. Разлагается при температуре выше 480 градусов Цельсия на оксиды.
Сульфат Железа 2 можно получить при воздействии разбавленной серной кислоты на обрезки железа; в виде побочного продукта реакции травления железных листов, при удалении окалины, при окислительном обжиге пирита.
Гидролиз Сульфата Железа 2 протекает по катиону в кислой среде. Первая ступень гидролиза: Fe2+ + SO42- + HOH ↔ FeOH+ + SO42- + H+; теоретически может протекать и вторая ступень гидролиза: FeOH+ + SO42- + HOH ↔ Fe(OH)2↓ + SO42- + H+.
Сернокислое железо 3 или тетрасульфид 6 железа 3 – это светло-желтые парамагнитные мелкие кристаллы. Вещество хорошо растворяется в воде, медленно – в этиловом спирте. Химическая формула Сульфата Железа 3: Fe2(SО4)3, рацемическая: Fe2O12S3. Вещество обладает способностью кристаллизоваться в форме кристаллогидратов Fe2(SO4)3•n H2O. Наибольшее значение имеет нонагидрат сульфата железа(III). Водные растворы приобретают красно-коричневую окраску из-за реакции гидролиза, протекающей по катиону. Соединение разлагается под действие горячей воды и высоких температур. При 98 градусах нонагидрат превращается в тетрагидрат, при температуре выше 125 градусов – в моногидрат и выше 175 – в безводный сульфат Fe, который при температуре более 600 градусов разлагается на оксиды серы и железа.
Фармакологическое действие
Противоанемическое, устраняющее железодефицит. Кровоостанавливающее (Сульфат Железа 3).
Фармакодинамика и фармакокинетика
Железо является основным микроэлементом, входящим в состав гемоглобина, миоглобина и прочих компонентов крови. Вещество принимает участие в окислительно-восстановительных реакциях, связывается и переносит молекулы кислорода по организму, стимулирует гемопоэз и эритропоэз. Сульфат Железа обеспечивает синтез всех железосодержащих метаболитов. После поступления Fe с пищей, оно усваивается в двенадцатиперстной кишке и переносится в депо тканей с помощью ферментов трансферетинов.
После приема лекарства внутрь, его активные компоненты полностью усваиваются организмом. Максимальная концентрация в крови наблюдается через 2-4 часа.
Показания к применению
Противопоказания
Сульфат Железа 2 противопоказан к приему:
Побочные действия
Побочные реакции во время лечения Сульфатом Железа возникают не часто.
Инструкция по применению (Способ и дозировка)
Лекарство назначают внутрь. Минимальная эффективная дозировка в пересчете на элементарное железо составляет 100 мг. Максимальное количество лекарства, которое можно принять – до 400 мг.
В профилактических целях назначают от 30 до 60 мг элементарного железа в сутки.
Передозировка
При передозировке усиливаются побочные реакции от приема лекарства. Возникают: диарея, тошнота, болезненные ощущения в животе, рвота, аритмия и рост ЧСС, повышается проницаемость капилляров, возможен сердечно-сосудистый коллапс. В качестве терапии промывают желудок, вводят дефероксамин для связывания ионов железа.
Взаимодействие
При сочетании с аскорбиновой кислотой улучшается всасывание препаратов железа.
Сочетанный прием сульфата и антацидных средств с магнием, алюминием, кальцием, пеницилламином и колестирамином замедляет всасывание железа.
Не рекомендуется сочетать лекарство с тетрациклиновыми антибиотиками, так как происходит взаимное снижение системной абсорбции обоих препаратов.
При сочетании лекарства с ГКС взаимно усиливается эритропоэз.
Условия хранения
Препараты хранят в сухом, темном, прохладном месте в оригинальной упаковке. Нельзя использовать лекарство после истечения срока годности.
Особые указания
Во время лечения Сульфатом Железа ii может наблюдаться окрашивание кала в черный цвет и потемнение эмали зубов.
При заболеваниях почек и печени железо может накапливаться в организме.
Особую осторожность соблюдают при лечении пациентов с язвенной болезнью желудка и 12-персной кишки, при язвенном колите и энтерите.
Вещество рекомендуется комбинировать с Фолиевой кислотой при железодефицитной анемии с дефицитом фол. к-ты.
При курсовом приеме лекарства рекомендуют периодически проводить контроль гемоглобина и уровня сывороточного железа.
При беременности и лактации
Лекарство можно использовать во время кормления грудью и при беременности по показаниям.
Препараты, в которых содержится (Аналоги)
Отзывы
Некоторые отзывы о применении препаратов Сульфата Железа:
Цена Сульфата Железа, где купить
Цена на лекарство варьирует в зависимости от производителя и лек. формы. Купить Сульфат Железа можно в любой аптеке. Например, стоимость таблеток пролонгированного действия Тардиферон составляет порядка 200 рублей за 30 штук.
Образование: Окончила Ровенский государственный базовый медицинский колледж по специальности «Фармация». Окончила Винницкий государственный медицинский университет им. М.И.Пирогова и интернатуру на его базе.
Опыт работы: С 2003 по 2013 г. – работала на должностях провизора и заведующего аптечным киоском. Награждена грамотами и знаками отличия за многолетний и добросовестный труд. Статьи на медицинскую тематику публиковались в местных изданиях (газеты) и на различных Интернет-порталах.
Сульфат железа (III)
| Сульфат железа (III) | |
|---|---|
 | |
| Систематическое наименование | сульфат железа (III) |
| Традиционные названия | сернокислое железо (III), тетрасульфид (VI) железа (III) |
| Хим. формула | Fe2(SO4)3 |
| Рац. формула | Fe2O12S3 |
| Состояние | безводный — светло-жёлтый порошок |
| Молярная масса | |
| • разложения | 600 |
| Мол. теплоёмк. | 271,75 Дж/(моль·К) |
| Энтальпия | |
| • образования | −2580 кДж/моль |
| Растворимость | |
| • в воде | (безв.) растворим(нонагидрат) 440 г/100 мл |
| • в этаноле | (нонагидрат) растворим |
| Рег. номер CAS | 15244-10-7 (для всех гидратов с формулой Fe2(SO4)3·nH2O (где n=1, 3, 4, 6, 7, 9, 10, 12) |
| RTECS | NO8505000 |
| ChEBI | 53438 |
| ChemSpider | 23211 и 21493902 |
| ЛД50 | (крысы, орально) 500 мг/кг |
| Пиктограммы ECB |  |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Содержание
Физические свойства
Безводный сульфат железа (III) — светло-жёлтые парамагнитные очень гигроскопичные кристаллы моноклинной сингонии, пространственная группа P21/m, параметры элементарной ячейки a = 0,8296 нм, b = 0,8515 нм, c = 1,160 нм, β = 90,5°, Z = 4. Есть данные, что безводный сульфат железа образовывает орторомбическую и гексагональную модификации. Растворим в воде, трудно растворим в этаноле.
Из воды кристаллизуется в виде кристаллогидратов Fe2(SO4)3·n H2O, где n = 12, 10, 9, 7, 6, 4, 3, 1. Наиболее изученный кристаллогидрат — нонагидрат сульфата железа (III) Fe2(SO4)3·9H2O — жёлтые гексагональные кристаллы, параметры элементарной ячейки a = 1,085 нм, c = 1,703 нм, Z = 4. Хорошо растворяется в воде (440 г на 100 г воды). В водных растворах сульфат железа(III) из-за гидролиза приобретает красно-коричневый цвет.
При нагревании нонагидрат превращается при 98 °C в тетрагидрат, при 125 °C — в моногидрат и при 175 °C — в безводный Fe2(SO4)3, который выше 600 °C разлагается на Fe2O3 и SO3.
Нахождение в природе
Все перечисленные выше природные гидраты железа на поверхности Земли нестабильны. Но их запасы постоянно пополняются благодаря окислению других минералов (в основном пирита и марказита).
Сульфат железа и ярозит были обнаружены двумя марсоходами: «Спирит» и «Оппортьюнити». Эти вещества являются признаком сильных окислительных условий на поверхности Марса. В мае 2009 года «Спирит» застрял, когда ехал по мягкому грунту планеты и наехал на залежи сульфата железа, скрытые под слоем обычного грунта. Вследствие того, что сульфат железа имеет очень низкую плотность, марсоход застрял настолько глубоко, что часть его корпуса коснулась поверхности планеты.
Получение
В промышленности сульфат железа (III) получают прокаливанием пирита или марказита с NaCl на воздухе:
или растворяют оксид железа (III) в серной кислоте:
В лабораторной практике сульфат железа (III) можно получить из гидроокиси железа (III):
Препарат той же чистоты можно получить окислением сульфата железа (II) азотной кислотой:
также окисление можно провести кислородом или оксидом серы:
Концентрированные серная и азотная кислоты окисляют сульфид железа до сульфата железа (III):
Дисульфид железа можно окислить концентрированной серной кислотой:
Сульфат-аммоний железа (II) (соль Мора) также можно окислить дихроматом калия. Вследствие данной реакции выделятся сразу четыре сульфата — железа (III), хрома (III), аммония и калия, и вода:
Сульфат железа (III) можно получить как один из продуктов термического разложения сульфата железа (II):
Ферраты с разбавленной серной кислотой восстанавливаются до сульфата железа (III):
При нагревании пентагидрата до температуры 70—175 °C получается безводный сульфат железа (III):
Сульфат железа (II) можно окислить триоксидом ксенона:
Химические свойства
Сульфат железа (III) в водных растворах подвергается сильному гидролизу по катиону, при этом раствор окрашивается в красновато-коричневый цвет:
Горячая вода или пар разлагают сульфат железа (III):
Безводный сульфат железа (III) при нагревании разлагается:
Растворы щелочей разлагают сульфат железа (III), продукты реакции зависят от концентрации щёлочи:
Если с щёлочью взаимодействует эквимолярный раствор сульфатов железа (III) и железа (II), то в результате получится сложный оксид железа:
Активные металлы (такие как магний, цинк, кадмий, железо) восстанавливают сульфат железа (III):
Некоторые сульфиды металлов (например, меди, кальция, олова, свинца, ртути) в водном растворе восстанавливают сульфат железа (III):
С растворимыми солями ортофосфорной кислоты образует нерастворимый фосфат железа (III) (гетерозит):
Формула сульфата железа 3
Определение и формула сульфата железа 3
Хорошо растворяется в воде (гидролизуется по катиону). Не растворяется в концентрированной серной кислоте. Разлагается горячей водой, щелочами, гидратом аммиака. В ОВР проявляет свойства слабого окислителя. Вступает в реакции обмена.
Рис. 1. Сульфат железа (III). Внешний вид.
Химическая формула сульфата железа 3
Химическая формула сульфата железа (III) Fe2(SO4)3. Она показывает, что в состав данной молекулы входят два атома железа (Ar = 56 а.е.м.), три атома серы (Ar = 32 а.е.м.) и двенадцать атомов кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу сульфата железа (III):
Mr(Fe2(SO4)3) = 2×56 + 3×32 + 12×16 = 112 + 96 + 192 = 400.
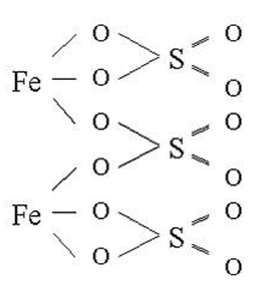
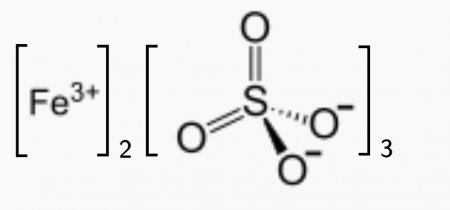
Графическая (структурная) формула сульфата железа 3
Структурная (графическая) формула сульфата железа (III) является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы:
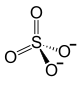
Ионная формула
Сульфат железа (III) является электролитом, т.е. в водном растворе диссоциирует на ионы согласно следующему уравнению:
Примеры решения задач
| Задание | При сжигании 24,6 г вещества образовалось 26,88 л углекислого газа (при н.у.), 9 г воды и 2,24 л азота (при н.у.). 1 литр паров этого вещества (н.у.) имеет массу 5,491 г. Установите молекулярную формулу органического вещества. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно: |
Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м., Ar(N) = 14 а.е.м.
Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr):
M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль;
M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль.
m(C) = [26,88 / 22,4]×12 = 14,4 г.
m(N) = 2×[2,24 / 22,4] = 1,28 г.
Определим химическую формулу соединения:
x:y:z:w = m(C)/Ar(C) : m(H)/Ar(H) : m(N)/Ar(N) : m(O)/Ar(O)
x:y:z:w= 14,4/12 : 1/1 : 1,28/14 : 6,4/16;
x:y:z:w= 1,2 : 1 : 0,09 : 0,4 = 13 : 11 : 1 : 4.
Значит простейшая формула соединения C13H11NO4и молярную массу 30 г/моль [M(C13H11NO4) = 13×Ar(C) + 11×Ar(H) +Ar(N) + 3× Ar(O) = 13×12 + 11×1 + 14 + 3×16 = 156 + 11 + 14 + 48 = 229 г/моль].
Найдем истинную молярную массу органического вещества:
Чтобы найти истинную формулу органического соединения найдем отношение истинной и полученной молярных масс:
Значит индексы атомов углерода, водорода и кислорода должны быть умножены на 0,5, т.е. формула вещества будет иметь вид C6H5NO2. Это нитробензол.
| Задание | Установите массовую формулу вещества, содержащего 33,3% натрия, 20,3% азота и 46,4% кислорода. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Обозначим количество моль элементов, входящих в состав соединения за «х» (натрий), «у» (азот) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел):
x:y:z = ω(Na)/Ar(Na) :ω(N)/Ar(N) : ω(O)/Ar(O);
x:y:z= 33,3/23 : 20,3/14 : 46,4/16;
x:y:z= 1,45 : 1,45:2,9 = 1 : 1: 2.
Значит формула соединения натрия, азота и кислорода будет иметь вид NaNO2. Это нитрит натрия.