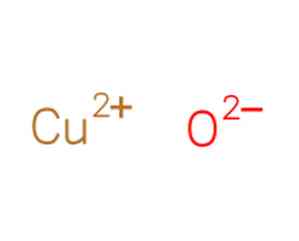Что такое cu2o в химии
Оксид меди (II)
Оксид меди (II)
| Оксид меди(II) | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Оксид меди(II)) |
| Химическая формула | CuO |
| Отн. молек. масса | 79.545 а. е. м. |
| Молярная масса | 79.545 г/моль |
| Физические свойства | |
| Плотность вещества | 6.31 г/мл г/см³ |
| Состояние (ст. усл.) | черный порошок |
| Термические свойства | |
| Температура плавления | 1447 [1] °C |
| Температура разложения | 1100 °C |
| Химические свойства | |
| Растворимость в воде | нерастоворим г/100 мл |
| Классификация | |
| номер CAS | [1317-38-0] |
Окси́д ме́ди(II) (окись меди) CuO — основный оксид двухвалентной меди. Кристаллы чёрного цвета, в обычных условиях довольно устойчивые, практически нерастворимые в воде. В природе встречается в виде минерала тенорита (мелаконита) чёрного цвета.
Содержание
Получение
Получить оксид меди(II) можно:
Химические свойства
Оксид меди(II) реагирует с кислотами с образованием соответствующих солей меди(II) и воды:
При сплавлении CuO со щелочами образуются купраты:
При нагревании до 1100 °C разлагается:
Оксиду меди(II) соответствует гидроксид меди(II) Cu(OH)2, который является очень слабым основанием. Он способен растворяться в концентрированных растворах щелочей с образованием комплексов (то есть обладает слабыми амфотерными свойствами):
Оксид меди(II) может быть восстановлен до металлической меди при помощи аммиака, монооксидом углерода или водородом:
Применение
CuO используют при производстве стекла и эмалей для придания им зелёной и синей окраски. Кроме того, оксид меди применяют в производстве медно-рубинового стекла.
В лабораториях применяют для обнаружения восстановительных свойств веществ. Вещество восстанавливает оксид до металлической меди, при этом цвет становится розовым.
Литература
Примечания
Полезное
Смотреть что такое «Оксид меди (II)» в других словарях:
Оксид меди(I) — Оксид меди(I) … Википедия
Оксид меди(II) — Оксид меди(II) … Википедия
ОКСИД МЕДИ — ОКСИД МЕДИ, химическое соединение меди и кислорода, существующее в двух формах: закиси (Сu2О), блестящий красный порошок, встречающийся в природе в виде минерала куприта, и окиси (СuО), черного цвета, которая разлагается на Сu2О и кислород при… … Научно-технический энциклопедический словарь
оксид меди — (CuO) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN copper oxidecupric oxidecuprous oxide … Справочник технического переводчика
Оксид меди (I) — Оксид меди(I) (закись меди) Cu2O твёрдое вещество красно бурого цвета, нерастворимое в воде и органических растворителях. Температура плавления 1235 °C. При нагревании до 1800 °C разлагается на металлическую медь и кислород. В природе оксид… … Википедия
Оксид меди — Известно три оксида меди: Оксид меди(I) Cu2O Оксид меди(II) CuO Оксид меди(III) Cu2O3 … Википедия
Оксид меди(III) — Общие Систематическое наименование Оксид меди(III) Традиционные названия Окисел медь Химическая формула Cu2O3 Физические свойства Состояни … Википедия
Оксид — (окисел, окись) соединение химического элемента с кислородом, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся… … Википедия
Меди оксиды — Известно три оксида меди: Оксид меди(I) Cu2O Оксид меди(II) CuO Оксид меди(III) Cu2O3 … Википедия
Оксид-сульфат титана — Общие Систематическое наименование Оксид сульфат титана Традиционные названия Основной сернокислый титан; оксосульфат титана; сульфат титанила Химическая формула TiOSO4 Физические свойства … Википедия
Оксид меди 2, химическая формула и свойства
Оксиды — широко распространённый в природе тип соединений, который можно наблюдать даже в повседневной жизни, в быту. Примером могут служить песок, вода, ржавчина, известь, углекислый газ, ряд природных красителей. Руда многих ценных металлов по своей природе является оксидом, вследствие чего представляет большой интерес для научных и производственных исследований.
Соединение химических элементов с кислородом называют оксидами. Как правило, образуются они при накаливании каких-либо веществ на воздухе. Различают кислотные и основные оксиды. Металлы образуют основные оксиды, в то время как неметаллы — кислотные. За исключением оксидов хрома и марганца, которые также являются кислотными. В данной статье рассматривается представитель основных оксидов — CuO (II).
CuO (II)
Медь, нагреваясь на воздухе при температуре 400–500 °C, постепенно покрывается налётом чёрного цвета, который химики называют оксид двухвалентной меди, или CuO(II). Описанное явление представлено в следующем уравнении:
2 Cu + О 2 → 2 CuO
Термин «двухвалентный» указывает на способность атома вступать в реакцию взаимодействия с другими элементами посредством двух химических связей.
Интересный факт! Медь, находясь в различных соединениях, может быть с разной валентностью и другим цветом. Например: оксиды меди имеют ярко-красную (Cu2O) и коричнево-чёрную (CuO) окраску. А гидроксиды меди приобретают жёлтый (CuOH) и синий (Cu(OH)2) цвета. Классический пример явления, когда количество переходит в качество.
Cu2O ещё иногда называют закись, оксид меди (I), а CuO — окись, оксид меди (II). Существует также оксид меди (III) — Cu2O3.
В геологии оксид двухвалентной (или бивалентной) меди принято называть тенорит, другое его название — мелаконит. Название тенорит произошло от фамилии выдающегося итальянского профессора ботаники Michele Tenore, (1780—1861). Мелаконит считается синонимом названия тенорит и переводится на русский язык, как медная чернь либо чёрная медная руда. В том или ином случае речь идёт о кристаллическом минерале коричнево-чёрного цвета, разлагающемся при прокаливании и плавящемся только при избыточном давлении кислорода, в воде нерастворимом, и не реагирующем с ней.
Акцентируем основные параметры названного минерала.
Химическая формула: CuO
Молекула его состоит из атома Cu с молекулярной массой 64 а. е. м. и атома O, молекулярная масса 16 а. е. м., где а. е. м. — атомная единица массы, она же дальтон, 1 а. е. м. = 1,660 540 2(10) × 10 −27 кг = 1,660 540 2(10) × 10 –24 г. Соответственно молекулярная масса соединения равняется: 64 + 16 = 80 а. е. м.
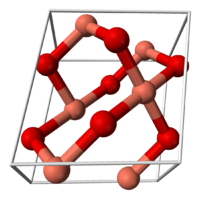
Кристаллическая решётка: моноклинная сингония. Что обозначает такой тип осей симметрии кристалла, когда две оси пересекаются под косым углом и имеют различную длину, а третья ось расположена по отношению к ним под углом 90°.
Плавится при температуре 1447 °C, под давлением кислорода.
Разлагается при накаливании до 1100 °C и преобразуется в оксид меди (I):
С водой не реагирует и не растворяется в ней.
Зато вступает в реакцию с водным раствором аммиака, с образованием гидроксида тетраамминмеди (II): CuO + 4NH3 + H2O = [Cu (NH3)4](OH) 2.
В кислотной среде образует сульфат и воду: CuO + H2SO4 = CuSO4 + H2O.
Реагируя со щёлочью, создаёт купрат: CuO + 2 NaOH → Na2CuO2 + H2O.
Реакция CuO NaOH
Образуется:
Токсичен. По степени неблагоприятного воздействия на человеческий организм причисляется к веществам второго класса опасности. Вызывает раздражение слизистых оболочек глаз, кожных покровов, дыхательных путей и желудочно-кишечной системы. При взаимодействии с ним обязательно использование таких средств защиты, как резиновые перчатки, респираторы, защитные очки, спецодежду.
Вещество взрывоопасно и легко воспламеняется.
Применяется в промышленности, как минеральная составляющая комбикормов, в пиротехнике, при получении катализаторов химических реакций, как красящий пигмент для стекла, эмалей, керамики.
Окислительные свойства оксида меди (II) наиболее часто применяются в лабораторных исследованиях, когда необходим элементарный анализ, связанный с изучением органических материалов на предмет наличия в них водорода и углерода.
Немаловажно, что CuO (II) достаточно широко распространён в природе, как минерал тенерит, другими словами — это природное соединение руды, из которого можно получить медь.
Латинское наименование Cuprum и соответствующий ему символ Cu происходит от названия острова Кипр. Именно оттуда, через Средиземное море вывозили этот ценный металл древние римляне и греки.
Медь входит в число семи наиболее распространённых в мире металлов и состоит на службе у человека с древних времён. Однако в первозданном, металлическом состоянии встречается довольно редко. Это мягкий, легко поддающийся обработке металл, отличающийся высокой плотностью, очень качественный проводник тока и тепла. По электрической проводимости уступает только серебру, в то время как является более дешёвым материалом. Широко используется в виде проволоки и тонкого листового проката.
Химические соединения меди отличаются повышенной биологической активностью. В животных и растительных организмах они участвуют в процессах синтеза хлорофилла, поэтому считаются очень ценным компонентом в составе минеральных удобрений.
Необходима медь и в рационе человека. Недостаток её в организме может привести к различным заболеваниям крови.
Видео
Из видео вы узнаете, что такое оксид меди.
Формула оксида меди, свойства, риски и использование
оксид меди, также называется оксидом меди (II), представляет собой химическое соединение формулы CuO. Его структура показана на рисунке 1 (EMBL-EBI, 2017).
Оксид меди встречается в природе как один из компонентов минералов, таких как тенорит и паралаконит. Он добывается из полезных ископаемых по всему миру, в основном в Южной Америке, в таких странах, как Перу, Боливия.
Некоторые химические соединения, такие как карбонат аммония и аммиак, используются для стимулирования добычи полезных ископаемых..
Оксид меди получают в основном путем извлечения в минералах, однако существует определенный процесс его промышленного производства..
В промышленности оксид меди получают реакцией воспламенения тригидрата нитрата меди (100-20 ° C), гидроксида меди (100 ° C) или карбоната меди (250 ° C):
Его также получают синтетическим путем, нагревая металлическую медь на воздухе приблизительно при 800 ° С (формула оксида меди, S.F.).
Физико-химические свойства оксида меди
Оксид меди (II). Представляется в виде тонкого черного порошка с ионной структурой. Его внешний вид показан на рисунке 3.
Молекула образована двухвалентной катионной медью Cu + 2 и анионным кислородом O-2. Молекулы образуют моноклинную кристаллическую систему, где каждый атом меди координируется 4 атомами кислорода..
Он тесно связан с другим оксидом меди: оксидом меди Cu2O (Национальный центр биотехнологической информации, 2005)..
Соединение нерастворим в воде, спирте, гидроксиде аммония, карбонате аммония и растворим в хлориде аммония и цианиде калия (Royal Society of Chemistry, 2015).
Оксид меди является амфотерным, поэтому он может растворяться в кислотах и щелочных растворах. В щелочном растворе реагирует с образованием других солей меди:
В кислотных растворах он также реагирует с образованием других солей меди:
Он взрывается при нагревании в контакте с алюминием, водородом или магнием. Кроме того, при нагревании образуются токсичные пары..
Реактивность и опасности
Оксид меди (II) чрезвычайно ядовит и токсичен при проглатывании. Вызывает повреждение центральной нервной системы и эндокринной системы (AZoM, 2013).
Это также раздражает глаза и кожу. Негорючий, стабильный и несовместимый с восстановителями, сероводородом, алюминием, щелочными металлами, тонкоизмельченными металлами (Fisher scientiffic, 2009).
В случае попадания в глаза, следует проверить, носите ли вы контактные линзы, и немедленно снять их..
Глаза следует промыть проточной водой не менее 15 минут, держа веки открытыми. Вы можете использовать холодную воду. Мазь не следует использовать для глаз.
Если химическое вещество попало на одежду, удалите его как можно быстрее, защищая свои руки и тело. Поместите жертву под безопасный душ.
Если химическое вещество накапливается на незащищенной коже жертвы, например на руках, аккуратно и осторожно промойте кожу, загрязненную проточной водой и неабразивным мылом..
Вы можете использовать холодную воду. Если раздражение не проходит, обратитесь к врачу. Выстирать загрязненную одежду перед повторным использованием.
Если контакт с кожей серьезный, его следует промыть дезинфицирующим мылом и покрыть кожу, загрязненную антибактериальным кремом..
В случае вдыхания пострадавшему должно быть разрешено отдыхать в хорошо проветриваемом помещении. Если вдыхание серьезное, пострадавшего следует как можно скорее эвакуировать в безопасное место..
Ослабьте тесную одежду, такую как воротник рубашки, ремни или галстук. Если пострадавшему трудно дышать, следует назначить кислород.
Если пострадавший не дышит, проводится реанимация из уст в уста. Всегда принимая во внимание, что человеку, оказывающему помощь в проведении реанимации изо рта в рот, может быть опасно, когда вдыхаемый материал токсичен, инфекционен или вызывает коррозию.
В случае проглатывания не вызывать рвоту. Ослабьте тесную одежду, такую как воротники рубашки, ремни или галстуки. Если пострадавший не дышит, проведите реанимацию из уст в уста.
Во всех случаях вам следует немедленно обратиться к врачу (паспорт безопасности материала Оксид меди, 2013 г.).
приложений
Оксид меди используется в качестве пигмента для кристаллов, фарфоровых эмалей и искусственных драгоценных камней. Оксид добавляет к таким материалам голубовато-зеленоватый оттенок.
Он также используется в качестве десульфурирующего агента для нефтяных газов и в качестве катализатора окисления и в гальванических электродах (Encyclopædia Britannica, 2017).
Оксид меди широко используется в химической и сельскохозяйственной химической промышленности для производства промежуточных продуктов в некоторых процессах..
Это широко используемый окислитель / восстановитель и регулятор процесса в химической реакции, особенно в производстве нефти..
Оксид меди используется для производства красок и покрытий, а также является компонентом некоторых продуктов по уходу за воздухом..
Редко используемый в качестве пищевой добавки у животных, он также имеет применение в качестве полупроводника p-типа из-за его узкой запрещенной зоны. Он используется в качестве альтернативы оксида железа в термитах.
Из-за своих фунгицидных и микробицидных свойств оксид меди (II) также находит применение в качестве инсектицида и фумиганта..
Когда эти организмы растут в корпусе корабля, они увеличивают трение, возникающее при прохождении корабля через воду, тем самым снижая его скорость..
Смесь также используется в качестве консерванта для древесины, для защиты столбов забора, стружки, настила, кровли, черепицы, морских стен и других пресноводных и морских сооружений от насекомых и грибков. (Томсон Гейл, 2006).
Оксид меди (I)
| Оксид меди (I) | |
|---|---|
 | |
| Традиционные названия | Закись меди, гемиоксид меди, оксид димеди |
| Хим. формула | Cu2O |
| Рац. формула | Cu2O |
| Внешний вид | Коричнево-красные кристаллы |
| Молярная масса | 143,09 г/моль |
| Плотность | 6,1 г/см³ |
| Твёрдость | 3,5 — 4 |
| Энтальпия | |
| • плавления | +64,22 кДж/моль |
| Растворимость | |
| • в воде | 2,4⋅10 −7 г/100 мл |
| Показатель преломления | 2,85 |
| Кристаллическая структура | кубическая |
| Рег. номер CAS | 1317-39-1 |
| PubChem | 10313194 |
| Рег. номер EINECS | 215-270-7 |
| SMILES | |
| RTECS | GL8050000 |
| ChEBI | 81908 |
| ChemSpider | 8488659 |
| ЛД50 | 470 мг/кг |
| Токсичность | средняя |
| Пиктограммы СГС |   |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Содержание
Нахождение в природе
Оксид меди (I) встречается в природе в виде минерала куприта (устаревшие названия: красная медная руда, стекловатая медная руда, рубиновая медь). Цвет минерала красный, коричнево-красный, пурпурно-красный или чёрный. Твёрдость по шкале Мооса 3,5 — 4.
Разновидность куприта с удлиненными нитевидными кристаллами называется халькотрихит (устаревшее название: плюшевая медная руда). Кирпично-красная смесь куприта с лимонитом носит название «черепичная руда».
Физические свойства
Оксид меди (I) при нормальных условиях — твёрдое вещество коричнево-красного цвета нерастворимое в воде и этаноле. Плавится без разложения при 1242 °C.
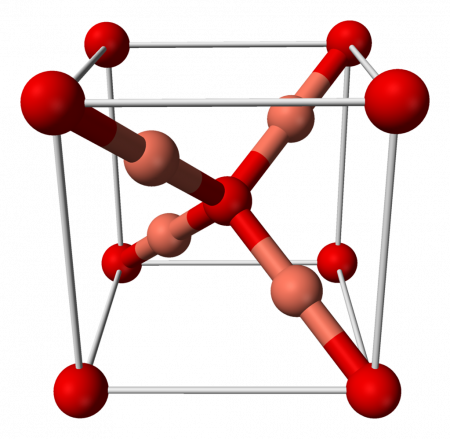
Оксид меди (I) имеет кубическую сингонию кристаллической решётки, пространственная группа P n3m, a = 0,4270 нм, Z = 2.
Химические свойства
Реакции в водных растворах
Оксид меди (I) не реагирует с водой. В очень малой степени (ПР = 1,2⋅10 −15 ) диссоциирует:
Оксид меди (I) переводится в раствор:
Также оксид меди (I) вступает в водных растворах в следующие реакции:
Реакции при высоких температурах
Оксид меди (I) восстанавливается до металлической меди в следующих реакциях:
Оксид меди (I) может быть окислен до соединений меди (II) в токе кислорода или хлора:
Также, при высоких температурах оксид меди (I) реагирует:
Прочие реакции
Оксид меди (I) реагирует с азидоводородом:
Получение
Оксид меди (I) может быть получен:
В лабораторных условиях оксид меди (I) может быть получен восстановлением гидроксида меди (II) (например, гидразином):
Также, оксид меди(I) образуется в реакциях ионного обмена солей меди (I) с щелочами, например:
Применение
Оксид меди (I) применяется как пигмент для окрашивания стекла, керамики, глазурей; как компонент красок, защищающих подводную часть судна от обрастания; в качестве фунгицида.
Обладает полупроводниковыми свойствами, используется в меднозакисных вентилях.
Токсичность
Оксид меди (I) — умеренно токсичное вещество: LD50 470 мг/кг (для крыс перорально). Вызывает раздражение глаз, может вызывать раздражение кожи и дыхательных путей.
Очень токсично для водной среды: LC50 для Daphnia magna составляет 0,5 мг/л в течение 48 ч.
Оксид меди (I, II, III): свойства, получение, применение
Как вам известно, в химии существует четыре класса неорганических соединений. Веществ, представляющих каждый из них, очень много, но лидирующее положение, несомненно, занимают оксиды. У одного химического элемента может быть сразу несколько разных бинарных соединений с кислородом. Такое свойство имеет и медь. У нее существует три оксида. Давайте рассмотрим их детальнее.
Оксид меди (I)
Свойства
Является кристаллическим веществом, имеющим коричнево-красный цвет. Этот оксид не растворяется в воде и этиловом спирте. Может плавиться, не разлагаясь, при температуре чуть больше 1240 о С. Данное вещество не взаимодействует с водой, но может переводиться в раствор, если участниками реакции с ним будут концентрированные хлоровородная кислота, щелочь, азотная кислота, гидрат аммиака, соли аммония, серная кислота.
Получение оксида меди (I)
Его можно получить, нагрев металлическую медь, или в такой среде, где кислород имеет малую концентрацию, а также в токе некоторых оксидов азота и вместе с оксидом меди (II). Кроме того, он может стать продуктом реакции термического разложения последнего. Оксид меди (I) получится и в том случае, если нагреть сульфид меди (I) в токе кислорода. Есть и другие, более сложные способы его получения (например, восстановление одного из гидроксидов меди, ионный обмен любой соли одновалентной меди с щелочью и т.п.), но их практикуют только в лабораториях.
Применение
Нужен в качестве пигмента, когда окрашивают керамику, стекло; компонента красок, которые защищают подводную часть судна от обрастания. Используется также как фунгицид. Без него не обходятся и меднозакисные вентили.
Оксид меди (II)
Свойства
Это высший оксид меди. Вещество имеет вид черных кристаллов, которые почти не растворяются в воде. Взаимодействует с кислотой и при этой реакции образует соответствующую соль двухвалентной меди, а также воду. При его сплавлении с щелочью продукты реакции представлены купратами. Разложение оксида меди (II) происходит при температуре около 1100 о С. Аммиак, монооксид углерода, водород и уголь способны извлекать из этого соединения металлическую медь.
Получение
Применение
С помощью данного оксида окрашивают в зеленый или синий цвет эмаль и стекло, а также производят медно-рубиновую разновидность последнего. В лаборатории этим оксидом обнаруживают восстановительные свойства веществ.
Оксид меди (III)
Свойства
Получение
Применение
Заключение
Вот и все оксиды меди. Их несколько из-за того, что медь имеет переменную валентность. Существуют и другие элементы, у которых есть по несколько оксидов, но о них поговорим в другой раз.