Чем отличаются молекулы воды и льда
Разница между водой и льдом
В ключевое отличие между водой и льдом заключается в том, что вода не имеет регулярного расположения молекул, тогда как лед имеет определенную кристаллическую структуру. С начальных этапов эволюции Зе
Содержание:
В ключевое отличие между водой и льдом заключается в том, что вода не имеет регулярного расположения молекул, тогда как лед имеет определенную кристаллическую структуру.
С начальных этапов эволюции Земли вода была основной частью Земли. На сегодняшний день вода покрывает более 70% поверхности земли. Отсюда большая часть воды находится в океанах и морях; что составляет около 97%. Реки, озера и пруды содержат 0,6% воды, и около 2% приходится на полярные ледяные шапки и ледники. Некоторое количество воды находится под землей, а незначительное количество находится в газовой форме в виде паров и облаков. Среди них менее 1% воды осталось для непосредственного использования человеком. Эта чистая вода также загрязняется день ото дня, и должен быть надлежащий план экономии воды.
Что такое вода?
Что такое лед?
Водородные связи важны для создания этой упорядоченной твердой структуры во льду. Водородные связи удерживают H2Молекулы O находятся на определенном расстоянии друг от друга, образуя кристаллическую структуру. При этом объем той же массы H2O расширяется (это означает, что при замерзании масса воды становится сравнительно большим, образуя лед). Поскольку при замерзании объем воды увеличивается, плотность льда ниже, чем у воды. Следовательно, он может плавать на воде. Это предотвращает замерзание воды на дне водоемов в зимний период, тем самым защищая водную жизнь.
В чем разница между водой и льдом?
Кроме того, мы можем определить разницу между водой и льдом по их объему и плотности. То есть; при той же массе объем воды сравнительно меньше льда. Потому что плотность воды выше, чем у льда. Приведенная ниже инфографика о разнице между водой и льдом показывает больше различий между ними.
ВОДА, ЛЕД И ПАР
ВОДА, ЛЕД И ПАР, соответственно жидкое, твердое и газообразное состояния химического соединения молекулярной формулы Н2О.
Историческая справка.
Идея древних философов о том, что все в природе образуют четыре элемента (стихии): земля, воздух, огонь и вода, просуществовала вплоть до Средних веков. В 1781 Г.Кавендиш сообщил о получении им воды при сжигании водорода, но не оценил в полной мере важности своего открытия. Позже (1783) А.Лавуазье доказал, что вода вовсе не элемент, а соединение водорода и кислорода. Й.Берцелиус и П.Дюлонг (1819), а также Ж.Дюма и Ж.Стас (1842) установили весовой состав воды, пропуская водород через оксид меди, взятый в строго определенном количестве, и взвешивая образовавшиеся медь и воду. Исходя из этих данных, они определили отношение Н:О для воды. Кроме того, в 1820-х годах Ж.Гей-Люссак измерил объемы газообразных водорода и кислорода, которые при взаимодействии давали воду: они соотносились между собой как 2:1, что, как мы теперь знаем, отвечает формуле Н2О.
Распространенность.
Вода покрывает 3/4 поверхности Земли. Тело человека состоит из воды примерно на 70%, яйцо – на 74%, а некоторые овощи – это почти одна вода. Так, в арбузе ее 92%, в спелых томатах – 95%.
Вода в природных резервуарах никогда не бывает однородной по составу: она проходит через горные породы, соприкасается с почвой и воздухом, а потому содержит растворенные газы и минеральные вещества. Более чистой является дистиллированная вода.
Морская вода.
Состав морской воды различается в разных регионах и зависит от притока пресных вод, скорости испарения, количества осадков, таяния айсбергов и т.д. См. также ОКЕАН.
Минеральная вода.
Минеральная вода образуется при просачивании обычной воды сквозь породы, содержащие соединения железа, лития, серы и других элементов.
Мягкая и жесткая вода.
Жесткая вода содержит в больших количествах соли кальция и магния. Они растворяются в воде при протекании по породам, сложенным гипсом (СaSO4), известняком (СаСО3) или доломитом (карбонаты Mg и Са). В мягкой воде этих солей мало. Если вода содержит сульфат кальция, то говорят, что она обладает постоянной (некарбонатной) жесткостью. Ее можно умягчить добавлением карбоната натрия; это приведет к осаждению кальция в виде карбоната, а в растворе останется сульфат натрия. Соли натрия не вступают в реакцию с мылом, и расход его будет меньше, чем в присутствии солей кальция и магния.
Вода, обладающая временной (карбонатной) жесткостью, содержит бикарбонаты кальция и магния; ее можно умягчить несколькими способами: 1) нагреванием, приводящим к разложению бикарбонатов на нерастворимые карбонаты; 2) добавлением известковой воды (гидроксида кальция), в результате чего бикарбонаты превращаются в нерастворимые карбонаты; 3) с помощью обменных реакций.
Вода, содержащая в большом количестве растворенный диоксид углерода, просачиваясь через известняковые породы, растворяет их, что приводит к образованию пещер. При повышении температуры начинается обратный процесс: бикарбонат разлагается и вновь образуется известняк. Именно из него состоят сталактиты и сталагмиты.
Молекулярная структура.
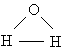
Анализ данных, полученных из спектров поглощения, показал, что три атома в молекуле воды образуют равнобедренный треугольник с двумя атомами водорода в основании и кислородом в вершине:
Физические свойства.
Благодаря сильному притяжению между молекулами у воды высокие температуры плавления (0 ° С) и кипения (100 ° С). Толстый слой воды имеет голубой цвет, что обусловливается не только ее физическими свойствами, но и присутствием взвешенных частиц примесей. Вода горных рек зеленоватая из-за содержащихся в ней взвешенных частиц карбоната кальция. Чистая вода – плохой проводник электричества, ее удельная электропроводность равна 1,5 Ч 10 –8 Ом –1 Ч см –1 при 0 ° С. Сжимаемость воды очень мала: 43 Ч 10 –6 см 3 на мегабар при 20 ° С. Плотность воды максимальна при 4 ° С; это объясняется свойствами водородных связей ее молекул.
Давление паров.
Если оставить воду в открытой емкости, то она постепенно испарится – все ее молекулы перейдут в воздух. В то же время вода, находящаяся в плотно закупоренном сосуде, испаряется лишь частично, т.е. при определенном давлении водяных паров между водой и воздухом, находящимся над ней, устанавливается равновесие. Давление паров в равновесии зависит от температуры и называется давлением насыщенного пара (или его упругостью). Когда давление насыщенного пара сравнивается с внешним давлением, вода закипает. При обычном давлении 760 мм рт.ст. вода кипит при 100 ° С, а на высоте 2900 м над уровнем моря атмосферное давление падает до 525 мм рт.ст. и температура кипения оказывается равной 90 ° С.
Испарение происходит даже с поверхности снега и льда, именно поэтому высыхает на морозе мокрое белье.
Вязкость воды с ростом температуры быстро уменьшается и при 100 ° С оказывается в 8 раз меньше, чем при 0 ° С.
Химические свойства.
Каталитическое действие.
Очень многие химические реакции протекают только в присутствии воды. Так, окисление кислородом не происходит в сухих газах, металлы не реагируют с хлором и т.д.
Гидраты.
Многие соединения всегда содержат определенное число молекул воды и называются поэтому гидратами. Природа образующихся при этом связей может быть разной. Например, в пентагидрате сульфата меди, или медном купоросе CuSO4 Ч 5H2O, четыре молекулы воды образуют координационные связи с ионом сульфата, разрушающиеся при 125 ° С; пятая же молекула воды связана так прочно, что отрывается лишь при температуре 250 ° С. Еще один стабильный гидрат – серная кислота; она существует в двух гидратных формах, SO3 Ч H2O и SO2(OH)2, между которыми устанавливается равновесие. Ионы в водных растворах тоже часто бывают гидратированы. Так, Н + всегда находится в виде иона гидроксония Н3О + или Н5О2 + ; ион лития – в виде Li (H2O)6 + и т.д. Элементы как таковые редко находятся в гидратированной форме. Исключение составляют бром и хлор, которые образуют гидраты Br2 Ч 10 H2O и Cl2 Ч 6H2О. Некоторые обычные гидраты содержат кристаллизационную воду, например хлорид бария BaCl2 Ч 2H2O, английская соль (сульфат магния) MgSO4 Ч 7H2O, питьевая сода (карбонат натрия) Na2CO3 Ч 10 H2O, глауберова соль (сульфат натрия) Na2SO4 Ч 10 H2O. Соли могут образовывать несколько гидратов; так, сульфат меди существует в виде CuSO4 Ч 5H2O, CuSO4 Ч 3H2O и CuSO4 Ч H2O. Если давление насыщенного пара гидрата больше, чем атмосферное давление, то соль будет терять воду. Этот процесс называется выцветанием (выветриванием). Процесс, при котором соль поглощает воду, называется расплыванием.
Гидролиз.
Гидролиз – это реакция двойного разложения, в которой одним из реагентов является вода; трихлорид фосфора PCl3 легко вступает в реакцию с водой:
Аналогичным образом гидролизуются жиры с образованием жирных кислот и глицерина.
Сольватация.
Вода – полярное соединение, а потому охотно вступает в электростатическое взаимодействие с частицами (ионами или молекулами) растворенных в ней веществ. Образовавшиеся в результате сольватации молекулярные группы называются сольватами. Слой молекул воды, связанный с центральной частицей сольвата силами притяжения, составляет сольватную оболочку. Впервые понятие сольватации было введено в 1891 И.А.Каблуковым.
Тяжелая вода.
В 1931 Г.Юри показал, что при испарении жидкого водорода его последние фракции оказываются тяжелее обычного водорода вследствие содержания в них в два раза более тяжелого изотопа. Этот изотоп называется дейтерием и обозначается символом D. По своим свойствам вода, содержащая вместо обычного водорода его тяжелый изотоп, существенно отличается от обычной воды.
В природе на каждые 5000 массовых частей Н2О приходится одна часть D2O. Это соотношение одинаково для речной, дождевой, болотной воды, подземных вод или кристаллизационной воды. Тяжелая вода используется в качестве метки при исследовании физиологических процессов. Так, в моче человека соотношение между Н и D тоже равно 5000:1. Если дать пациенту выпить воду с большим содержанием D2O, то, последовательно измеряя долю этой воды в моче, можно определить скорость выведения воды из организма. Оказалось, что около половины выпитой воды остается в организме даже спустя 15 сут. Тяжелая вода, вернее, входящий в ее состав дейтерий – важный участник реакций ядерного синтеза.
Лед, твердая фаза воды, используется в основном как хладагент. Он может находиться в равновесии с жидкой и газообразной фазами или только с газообразной фазой. Толстый слой льда имеет голубоватый цвет, что связано с особенностями преломления им света. Сжимаемость льда очень низка.
Лед при нормальном давлении существует только при температуре 0 ° С или ниже и обладает меньшей плотностью, чем холодная вода. Именно поэтому айсберги плавают в воде. При этом, поскольку отношение плотностей льда и воды при 0 ° С постоянно, лед всегда выступает из воды на определенную часть, а именно на 1/5 своего объема. См. также АЙСБЕРГИ.
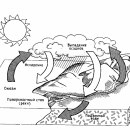
Пар – газообразная фаза воды. Вопреки общепринятому мнению, он невидим. Тот «пар», который вырывается из кипящего чайника, – это на самом деле множество мельчайших капелек воды. Пар обладает свойствами, очень важными для поддержания жизни на Земле. Хорошо известно, например, что под действием солнечного тепла вода с поверхности морей и океанов испаряется. Образующиеся водяные пары поднимаются в атмосферу и конденсируются, а затем выпадают на землю в виде дождя и снега. Без такого круговорота воды наша планета давно превратилась бы в пустыню.
Пар имеет множество применений. С одними мы хорошо знакомы, о других только слышали. Среди наиболее известных устройств и механизмов, работающих с применением пара, – утюги, паровозы, пароходы, паровые котлы. Пар вращает турбины генераторов на тепловых электростанциях. См. также КОТЕЛ ПАРОВОЙ; ДВИГАТЕЛЬ ТЕПЛОВОЙ; ТЕПЛОТА; ТЕРМОДИНАМИКА.
Эйзенберг Д., Кауцман В. Структура и свойства воды. Л., 1975
Зацепина Г.Н. Физические свойства и структура воды. М., 1987
Структура и свойства воды и льда
Карельский Государственный Педагогический университет
Структура и свойства воды и льда
Вступление
Пожалуй, на Земле нет более распространенного и в то же время более загадочного вещества, чем вода в жидкой и твердой фазах. Действительно, достаточно
вспомнить, что все живое вышло из воды и состоит из нее более чем на 50%, что 71% поверхности Земли покрыт водой и льдом, а значительная часть северных территорий суши представляет собой вечную мерзлоту.
Несмотря на многовековую историю изучения, простейший химический состав и исключительную важность для жизни на Земле, природа воды и льда таит в себе много
загадок из-за сложной динамической протонной и молекулярной структуры.
Основы современного понимания физикохимии воды заложили около 200 лет назад Генри Кавендиш и Антуан Лавуазье, обнаружившие, что вода – это не простой химический элемент, как считали средневековые алхимики, а соединение кислорода и водорода в определенном отношении. Собственно и название свое водород (hydrogene) – рождающий воду – получил только после этого открытия, и вода приобрела современное химическое обозначение H2O.
Водородная связь (Н-связь) – особый тип взаимодействия между реакционно-способными группами, при этом одна из групп содержит атом водорода, склонный к такому взаимодействию. В отличие от обычных химических связей, Н-связь появляется не в результате целенаправленного синтеза, а возникает в подходящих условиях сама и проявляется в виде межмолекулярных или внутримолекулярных взаимодействий.
Само понятие и термин «водородная связь» ввели В. Латимер и Р. Родебуш в 1920, для того, чтобы объяснить высокие температуры кипения воды, спиртов и др. соединений. Они выявили закономерность. Из этой закономерности следовало, что вода должна кипеть на 200° С ниже, чем наблюдаемое истинное значение.
Молекула воды

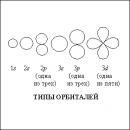
Для объяснения природы воды необходимо принять во внимание электронную структуру ее молекул. Как известно, на верхней оболочке у атома кислорода находятся четыре электрона, а у водорода имеется всего лишь один электрон. В образовании каждой ковалентной связи O–H участвуют по одному электрону от атомов кислорода и водорода. Два оставшихся у кислорода электрона получили название неподеленной пары, так как в изолированной молекуле воды они остаются свободными, не участвуя в образовании связей внутри молекулы H2O. Но при сближении с другими молекулами именно эти неподеленные электроны и играют решающую роль в образовании молекулярной структуры воды.

 Лед
Лед
С точки зрения обычного человека, лед более или менее одинаков независимо от того, где он образовывается: в атмосфере в виде градинок, на краях крыш в виде сосулек или в водоемах в виде пластин. С точки зрения физики имеется множество разновидностей льда, отличающихся своей молекулярной и мезоскопической структурой. Во льду, существующем при нормальном давлении, каждая молекула H2O окружена четырьмя другими, то есть координационное число структуры равно четырем (так называемый лед Ih ) Фрагмент структуры льда Ih. Молекулы воды, соединяющие их стержни – водородные связи (вся структура состоит из шестичленных колец); Характерной особенностью структуры льда является то, что в ней молекулы упакованы рыхло.
Соответствующая кристаллическая решетка (а) – гексагональная – не является плотноупакованной, поэтому плотность обычного льда (≈0,9 г/см ) ниже плотности воды (≈1 г/см ). Фиксированные положения в структуре льда занимают только атомы кислорода. Два атома водорода могут занимать различные положения на четырех связях молекулы H2O с другими соседями. Ввиду гексагональности решетки кристаллики, растущие в свободном состоянии (например, снежинки), имеют шестигранную форму.

Гексагональная фаза далеко не единственная форма существования льда. Точное число других кристаллических фаз – полиморфных форм льда – до сих пор неизвестно. Они образуются при высоких давлениях и низких температурах (рис. ). Одни исследователи считают точно установленным наличие 12 таких фаз, в то время как другие насчитывают их до 14. Количество различных фаз льда продолжают открывать и по сегодняшний день.
Римскими цифрами обозначены области существования стабильных фаз. Лед IV – метастабильная фаза, располагающаяся на диаграмме внутри области V.
Аномалии воды
Аномалия плотности


В последнее время много внимания уделяется изучению свойств переохлажденной воды, то есть остающейся в жидком состоянии ниже точки замерзания 0°С. (Переохладить воду можно либо в тонких капиллярах, либо – еще лучше – в виде эмульсии: маленьких капелек в неполярной среде – “масле”). Что же происходит с аномалией плотности при переохлаждении воды? Она ведет себя странно (см. рис.). С одной стороны, плотность воды сильно уменьшается по мере переохлаждения, но, с другой стороны, она приближается к плотности льда при понижении температуры (то есть вторая аномалия ослабевает). Чем ниже температура, тем ажурнее становится сетка, обусловливая уменьшение плотности при понижении температуры ниже 4°С.
 Аномалия сжимаемости
Аномалия сжимаемости

Аномалия теплоёмкости
Величина теплоемкости, как известно, показывает, сколько нужно затратить тепла, чтобы поднять температуру вещества на один градус. Для подавляющего числа веществ теплоемкость жидкости после плавления кристалла увеличивается незначительно – никак не более 10%. Другое дело – вода. При плавлении льда теплоемкость скачет от 9 до 18 кал/моль* град, то есть в два раза! Такого огромного скачка теплоемкости при 
Во льду энергия, подводимая для нагревания, тратится в основном на увеличение тепловой скорости молекул. Скачок теплоемкости после плавления означает, что чтобы деформировать сетку при изменении температуры, перестроить ее структуру, нужно затратить энергию; это и объясняет аномальный вклад в теплоемкость. Как видно на рис. сетка водородных связей в воде существует на всем интервале существования жидкости: с ростом температуры водородные связи не разрываются, а постепенно изменяют свою конфигурацию.
В переохлажденной воде рост теплоемкости также связан с изменением конфигурации водородных связей.
Свойства льда
Текучесть льда

Влияние скорости деформации на механические свойства монокристаллического льда хорошо иллюстрирует след. рис. Видно, что при увеличении скорости деформирования механические напряжения σ, необходимые для пластического течения, быстро нарастают и на зависимости относительной деформации Е от σ появляется гигантский зуб текучести.

Электрические свойства льда
Не менее замечательны и электрические свойства льда. Величина проводимости и ее экспоненциально быстрое возрастание с повышением температуры резко отличают лед от металлических проводников и ставят его в один ряд с полупроводниками. Обычно лед бывает очень чист химически, даже если растет из грязной воды или раствора (вспомните чистые прозрачные льдинки в грязной луже). Это обусловлено низкой растворимостью примесей в структуре льда. В результате при замерзании примеси оттесняются на фронте кристаллизации в жидкость и не входят в структуру льда. Поэтому рассчитывать на большую примесную проводимость во льду не приходится. Но в нем нет и свободных электронов, как в металлах. Лишь в 50-е годы XX века было установлено, что носителями заряда во льду являются неупорядоченные протоны, то есть лед является протонным полупроводником.

 Дефекты
Дефекты
а – пара ионных дефектов H3O+ и OH-; б – пара ориентационных дефектов Бьеррума
Рост кристаллов льда

Память воды
защитил диссертацию, посвященную памяти воды. До сих пор считалось, что вода не может образовывать долгоживущих структур. Однако его расчеты показали, что вода представляет собой иерархию правильных объемных структур, в основе которых лежит кристаллоподобный «квант воды», состоящий из 57 ее молекул. Эта структура энергетически выгодна и разрушается с освобождением свободных молекул воды лишь при высоких концентрациях спиртов и подобных им растворителей. «Кванты воды» могут взаимодействовать друг с другом за счет свободных водородных связей, что приводит к появлению структур второго порядка в виде шестигранников. Они состоят из 912 молекул воды, которые практически не способны к взаимодействию за счет образования водородных связей.

Кристаллы воды после «прослушивания» музыкальных произведений.
«Пасторали» Бетховена «Прощальной Песни» Шопена тяжелого металлического рока
Вывод
Вода, лед и их взаимные фазовые превращения еще таят в себе множество загадок. Их разгадывание представляет собой не только очень интересную физическую проблему, но и чрезвычайно важно для жизни на Земле, так как имеет прямое отношение к здоровью и благополучию человека. Возможно, они дают один из самых ярких примеров роли электронной и молекулярной структуры в формировании физических свойств при простейшем и хорошо известном химическом составе вещества.
Литература:
ВОДА И ЛЕД – ЗНАЕМ ЛИ МЫ О НИХ ДОСТАТОЧНО?
//Соросовский образовательный журнал, том 6, №9 2000 с.66-72
ЗАГАДКИ ВОДЫ. // Соросовский образовательный журнал, №5 1996, с. 41-48



 Лед
Лед Аномалия сжимаемости
Аномалия сжимаемости
 Дефекты
Дефекты

