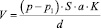Чем отличается воздух анатомического мертвого и альвеолярного пространства
Чем отличается воздух анатомического мертвого и альвеолярного пространства
Вентиляцией легких обозначают процесс обмена воздуха между легкими и атмосферой. Количественным показателем вентиляции легких служит минутный объем дыхания, определяемый как количество воздуха, которое проходит (или вентилируется) через легкие в 1 мин. В покое у человека минутный объем дыхания составляет 6—8 л/мин. Только часть воздуха, которым вентилируются легкие, достигает альвеолярного пространства и непосредственно участвует в газообмене с кровью. Эта часть вентиляции легких называется альвеолярной вентиляцией. В покое альвеолярная вентиляция равна в среднем 3,5—4,5 л/мин. Основная функция альвеолярной вентиляции заключается в поддержании необходимой для газообмена концентрации 02 и С02 в воздухе альвеол.
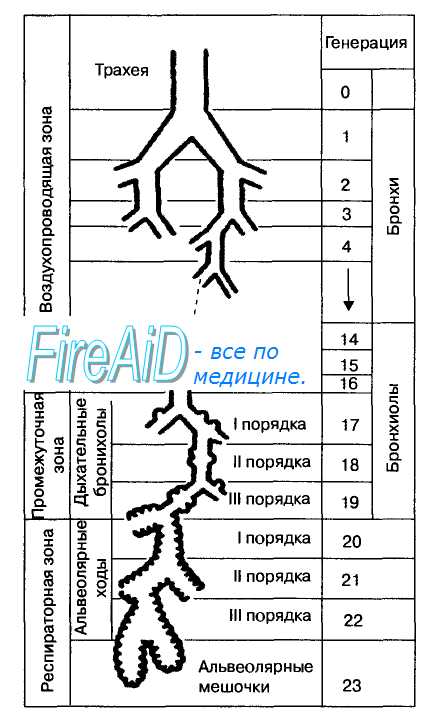
Легкие состоят из воздухопроводящей (дыхательные пути) и респираторной зон (альвеолы). Дыхательные пути, начиная от трахеи и до альвеол, делятся по типу дихотомии и образуют 23 генерации элементов дыхательного тракта (рис. 10.11). В воздухопроводящей или кондуктивной зонах легких (16 генераций) отсутствует газообмен между воздухом и кровью, поскольку в этих отделах дыхательные пути не имеют достаточной для этого процесса сосудистой сети, а стенки дыхательных путей, из-за их значительной толщины, препятствуют обмену газов через них. Этот отдел воздухоносных путей называется анатомическим мертвым пространством, объем которого составляет в среднем 175 мл. На рис. 10.12 показано, каким образом воздух, заполняющий анатомическое мертвое пространство в конце выдоха, смешивается с «полезным», т. е. атмосферным воздухом и вновь поступает в альвеолярное пространство легких.
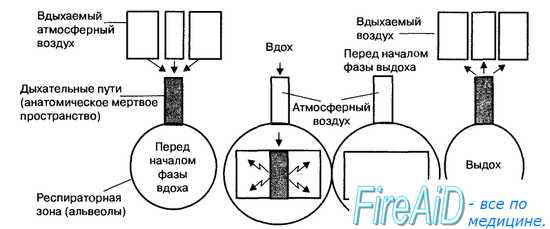
Дыхательные бронхиолы 17—19-й генераций относят к переходной (транзиторной) зоне, в которой начинается газообмен в малочисленных альвеолах (2 % от общего числа альвеол). Альвеолярные ходы и альвеолярные мешочки, непосредственно переходящие в альвеолы, образуют альвеолярное пространство, в области которого происходит в легких газообмен 02 и С02 с кровью. Однако у здоровых людей и, особенно, у пациентов с заболеваниями легких часть альвеолярного пространства может вентилироваться, но при этом не участвовать в газообмене, поскольку эти отделы легких не перфузируются кровью. Сумму объемов таких областей легких и анатомического мертвого пространства обозначают как физиологическое мертвое пространство. Увеличение физиологического мертвого пространства в легких приводит к недостаточному снабжению тканей организма кислородом и к увеличению содержания в крови углекислого газа, что нарушает в ней газовый гомеостазис.
Роль мертвого пространства в формировании и диагностике дыхательной недостаточности
Полный текст:
Аннотация
Об авторах
Список литературы
2. Шик Л. Л., Канаев Н. Н.(ред.) Руководство по клинической физиологии дыхания. Л.: Медицина; 1980.
3. Зильбер А. П., Шурыгин И. А.Высокочастотная вентиляция легких. Петрозаводск; 199
4. Корячкин В. А.Краткий толковый словарь врача анестезиолога-реаниматолога. СПб.; 2005.
5. Виницкая Р. С.Значение определения альвеоло-артериальной разницы респираторных газов в функциональной диагностике дыхания. Современные проблемы клинической физиологии дыхания. 1987; 95—102.
6. Левитэ Е. М.Краткий толковый словарь анестезиологов-реаниматологов. М.: Геотар-Медиа; 200
7. Левитэ Е. М.Введение в анестезиологию-реаниматологию. М.: Гео-тар-Медиа; 200
8. Wensel R., Georgiadou P., Francis D. P. et al.Differential contribution of dead space ventilation and low arterial pCO2 to exercise hyperpnea in patients with chronic heart failure secondary to ischemic or idiopathic dilated cardiomyopathy. Am. J Cardiol. 2004; 93 (3): 318—323.
9. Riou Y., Leclerc F., Neve V. et al.Reproducibility of the respiratory dead space measurements in mechanically ventilated children using the CO2SMO monitor. Intensive Care Med. 2004; 30 (7): 1461—1467.
10. Hedenstierna G., Sandhagen B.Assessing dead space. A meaningful variable Minerva Anestesiol.2006; 72 (6): 521—528.
11. Kallet R. H.Accuracy of physiologic dead space measurements in patients with acute respiratory distress syndrome using volumetric capnography: comparison with metabolic monitor method. Resp. Care. 2005; 50 (4): 462—467.
12. Verschuren F.Volumetric capnography: reliability and reproducibility in spontaneously breathing patients. Clin. Physiol. Funct. Imaging. 2005; 25 (5): 275—280.
13. Blanch L.Volumetric capnography in mechanically ventilated patients. Minerva Anestesiol. 2006; 72 (6): 577—585.
14. Wathanasormsiri A., Preutthipan A., Chantarojanasiri T.Dead space ventilation in volume controlled versus pressure controlled mode of mechanical ventilation. J. Med. Assoc. Thai. 2002; 85 (4): 1207—1212.
15. Hardman I, Aitkenhead A. Estimating alveolar dead space from the arterial to end-tidal CO2gradient: a modeling analysis. Anesth. Analg. 2003; 97 (6): 1846—1851.
Для цитирования:
For citation:
Чем отличается воздух анатомического мертвого и альвеолярного пространства
2.1. Дыхательные функции легких. Альвеолярное дыхание
Легкие играют важную роль не только в регуляции и обеспечении внешнего дыхания, но выполняют и ряд недыхательных функций. Недыхательные функции легких включают их участие в голосообразовании, регуляции теплоотдачи и кислотно-основного состояния организма, иммунных реакциях, в обеспечении тканевого фагоцитоза, регуляции метаболизма биологически активных прессорных и депрессорных субстанций, прокоагулянтных и антикоагулянтных факторов свертывания крови. В легких инактивируются пептиды, цикличесские нуклеотиды, простагландины, ксенобиотики, а также гистамин, серотонин.
Дыхательная функция легких определяется их участием в обеспечении альвеолярного дыхания, а также в регуляции внешнего дыхания за счет наличия мощных рефлексогенных зон.
Состояние легочной вентиляции определяется глубиной дыхания (дыхательным объемом) и частотой дыхательных движений.
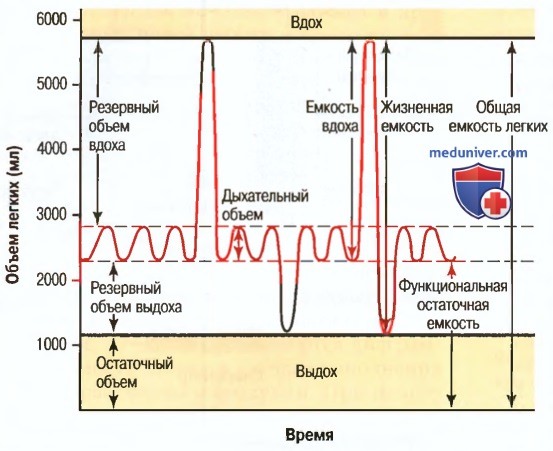
Различают следующие объемы дыхания:
Дыхательный объем – объем вдоха и выдоха при спокойном дыхании.
Резервный объем вдоха и выдоха – количество воздуха, которое человек может дополнительно вдохнуть или выдохнуть при нормальном дыхании.
Остаточный объем – количество воздуха, оставшегося в легких, после максимального выдоха.
Жизненная емкость легких (ЖЁЛ) – наибольшее количество воздуха, которое можно максимально выдохнуть после максимального вдоха (сумма дыхательного объема и резервных объемов вдоха и выдоха)
Функциональная остаточная емкость – количество воздуха, оставшееся в легких после спокойного выдоха.
Жизненную ёмкость легких можно вычислить по формуле ЖЁЛ (л)= 2,5*рост (в м).
ЖЁЛ зависит от роста, возраста человека, рода занятий, особенно велико у пловцов и гребцов (до 8 л).
Легкие плода и новорожденных, не совершивших первый вдох, не содержат воздуха.
Различают анатомическое и функциональное мертвое пространство.
Анатомическое мертвое пространство – это объем невентилируемых воздухоносных путей – трахеи, бронхов и бронхиол.
Функциональное мертвое пространство – более емкое понятие, оно включает не только анатомическое мертвое пространство, а также вентилируемые, но неперфузируемые альвеолы.
Минутный объем дыхания равен произведению дыхательного объема на частоту дыхательных движений. Частота дыхательных движений у детей различна: у новорожденных составляет 40-50 в мин, у грудных детей 30-40 в мин, в детском возрасте 20-30 в мин. У взрослого человека частота дыхательных движений составляет 14 – 18 в мин.
Следует отметить, что диффузионное давление для О2 составляет около 60 мм. рт.ст, а для СО2 около 6 мм.рт.ст. Однако, необходимо учесть, что СО2 значительно быстрее диффундирует через альвеолярно–капиллярную мембрану в связи с тем, что коэффициент его растворимости в биологической среде в 20 раз больше, чем у кислорода.
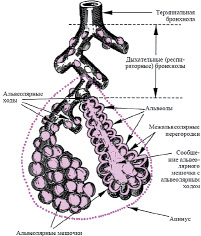
В легких взрослого человека содержится около 300 млн. альвеол, диаметр которых составляет около 0,2 мм. Две соседние альвеолы отделены друг от друга двумя слоями эндотелия и эпителия, расположенными на базальной мембране. Между этими слоями находится интерстициальное пространство. Альвеолярный эпителий и эндотелий капилляров образуют альвеолярно – капиллярную мембрану, через которую происходит диффузия газов; толщина мембраны составляет от 0,2 мкм до 2 мкм в местах скопления эластических и коллагеновых волокон. Площадь газообмена в легких находится в зависимости от возраста и колеблется от 40 до 140 м 2 (рис.4).
Рис.4. Схема строения альвеолярного дерева
Альвеолярно–капиллярная диффузия во многом зависит от эластичности легочной ткани, обеспечивается в значительной мере продукцией сурфактанта.
Различают два типа эпителия, выстилающего альвеолярные клетки. Клетки I типа – это плоский эпителий, занимает до 95 % площади альвеолярной поверхности, содержит небольшое количество органоидов. Клетки IIтипа крупные, имеют округлую форму, ядра и микроворсинки, синтезируют сурфактант.
Сурфактант легких – это смесь поверхностно-активных веществ (ПАВ), состоящая на 70 – 80% из фосфатидилхолина, фосфатидилглицерола, дипальмитолфосфатидилхолина и белков сурфактанта, продуцируемых альвеолоцитами II типа. Молекулы апопротеинов, фосфолипидов имеют гидрофильный и гидрофобные концы, обращенные соответственно в альвеолярную жидкость и альвеолярный воздух. Белки сурфактанта (SPA, SP-R, SP-C,SP-D) не только способствуют снижению поверхностного натяжения альвеол, обеспечиваемому фосфолипидами, но и обладают защитной функцией.
Система легочного сурфактанта играет многоплановую роль, обеспечивая антиателэктатическую функцию, способствует диффузии О2, участвует в регуляции водного обмена в легких, защищает организм от проникновения вредоносных мелкодисперсных аэрозолей, обладает свойствами антиоксиданта.
Сурфактант, как указывалось выше, уменьшает поверхностное натяжение альвеол в 2 – 10 раз, тем самым, предотвращая спадение альвеол. Сурфактант содержится не только на внутренней поверхности альвеол, но и на плевре, брюшине, перикарде, синовиальных оболочках, слизистой глазных яблок. Сурфактант обеспечивает раскрытое состояние мелких дыхательных путей, усиливает фагоцитирующую активность макрофагов, подавляет выделение медиаторов воспаления, обладает свойствами антиоксиданта, оказывает антибактериальное и противовирусное действие.
При дефиците сурфактанта некоторые альвеолы подвергаются ателектазу, другие – перерастягиваются, вентиляция легких становится негомогенной, нарушается вентиляционно – перфузионное отношение.
При спадении альвеолы концентрация сурфактанта на ее поверхности возрастает, возникает снижение поверхностного натяжения, что повышает их стабильность и препятствует дальнейшему спадению альвеол. Стабильность альвеол обеспечивается и так называемым феноменом «взаимозависимости» альвеол, т.е. их взаимной тяги. У недоношенных новорожденных недостаточность синтеза сурфактанта может быть причиной развития респираторного дистресс – синдрома, характеризующегося ригидными легкими.
Как известно, легкие в отличие от трахеи и бронхов являются мощной рефлексогенной зоной, обеспечивающей регуляцию внешнего дыхания в условиях нормы и патологии.
В паренхиме легких имеются различные высоко- и низкочувствительные рецепторы растяжения альвеол, медленно-адаптирующиеся и быстро-адаптирующиеся к структурным изменениям в легких. Медленно-адаптирующиеся рецепторы растяжения альвеол являются высокочувствительными, низкопороговыми механорецепторами, реагирующими на объем вдыхаемого воздуха. Эти рецепторы являются окончанием толстых миелинизированных волокон n.vagus. Афферентация с этих рецепторов при участии ретикулярной формации ствола мозга переключается на инспираторные нейроны дорзальной дыхательной группы продолговатого мозга, обеспечивая развитие рефлекса Геринга-Брейера. Рефлекс Геринга-Брейера участвует во время сна в смене фаз дыхательного цикла. В условиях патологии при участии этого рефлекса формируются испираторная, экспираторная и смешанная одышки.
Другой группой рецепторов паренхимы легких являются быстроадаптирующиеся рецепторы спадения альвеол и юкстакапилярные рецепторы, реагирующие соответственно на спадение альвеол и возрастание уровня тканевой жидкости. Импульсация с этих рецепторов проводится по мало– и немиелинизированным волокнам n.vagus в продолговатый мозг, вызывая развитие тахипное.
При раздражении С-волокон возникают брадикардия, тахи- и апное, гипер- и диссекреция слизи в воздухоносных путях.
2.2. Кровоснабжение и лимфоснабжение легких
Легкие получают кровь от системы легочных сосудов (малый круг кровообращения) и бронхиальных сосудов (большой круг кровообращения). Основной функцией малого круга кровообращения является оксигенация венозной крови и удаление из нее СО2.
Среднее время прохождения крови через малый круг составляет в среднем 4,5 – 5,0 сек.
В состоянии покоя в сосудах легких находится около 500 мл крови (10 % от общего объема). В условиях нагрузки объем крови в легких может возрастать в 5–6 раз, при этом происходит лишь незначительное увеличение давления в сосудах малого круга кровообращения за счет высокой растяжимости. Давление в артериолах легких составляет в среднем 9 – 15 мм. рт. ст.
В покое кровоток в легких неоднороден, большая часть его направлена в нижние зоны.
Система бронхиальных сосудов снабжает кровью дыхательные пути вплоть до терминальных бронхиол, составляя около 3% от величины легочного кровотока.
Гидродинамические параметры бронхиальных сосудов обеспечивают транспорт воды в интерстиций и последующее лимфообразование. В легких осуществляются анастомозы между сосудами большого и малого круга кровообращения.
Суммарно в легких отношение легочной вентиляции и легочной перфузии составляет примерно 0,8 – 1,0. При вертикальном положении человека снижается интенсивность кровотока у верхушек легких.
Лимфатические сосуды расположены в паренхиме легких и на поверхности висцеральной плевры, впадают в лимфатические узлы, расположенные вокруг крупных воздухоносных путей (ВП) и в средостении. Лимфоидная ткань находится в стенках воздухоносных путей. Терминальные мешки лимфатической системы расположены в субплевральной, перибронхиальной соединительной ткани, а затем поступают в собирательные лимфатические сосуды легких.
Регуляция легочного кровотока обеспечивается за счет влияния вегетативной нервной системы, а также ряда гуморальных факторов; в частности вазодилатирующих простагландина J2 – метаболита арахидоновой кислоты, оксида азота и вазоконстрикторных соединений: эндотелинов, тромбоксана.
Эндотелины продуцируются эндотелиальными клетками легочных сосудов и клетками бронхиального эпителия и вызывают вазоконстрикцию, являются медиаторами легочной гипоксической вазоконстрикции, вызывают сокращения гладкой мускулатуры воздухоносных путей.
Чем отличается воздух анатомического мертвого и альвеолярного пространства
а) Минутный объем дыхания равен частоте дыхания, умноженной на дыхательный объем. Общее количество нового воздуха, входящего в дыхательные пути за каждую минуту, называют минутным объемом дыхания. Он равняется произведению дыхательного объема на частоту дыхания в минуту. В покое дыхательный объем составляет около 500 мл и частота дыхания — около 12 раз в минуту, следовательно, минутный объем дыхания составляет в среднем около 6 л/мин. Человек в течение короткого периода времени может жить при минутном объеме дыхания около 1,5 л/мин и частоте дыхания 2-4 раза в минуту.
Иногда частота дыхания может вырасти до 40-50 раз в минуту, а дыхательный объем у молодого взрослого мужчины может достигать примерно 4600 мл. Минутный объем при этом может оказаться больше 200 л/мин, т.е. в 30 раз и более, чем в покое. Большинство людей не способны поддерживать эти показатели даже на уровне 1/2-2/3 приведенных значений в течение более 1 мин.
б) Альвеолярная вентиляция. Главной задачей легочной вентиляции является постоянное обновление воздуха в газообменных зонах легких, где воздух находится недалеко от легочных капилляров, наполненных кровью. К таким зонам относятся альвеолы, альвеолярные мешочки, альвеолярные протоки и бронхиолы. Количество нового воздуха, достигающего этих зон за минуту, называют альвеолярной вентиляцией.
в) Мертвое пространство и его влияние на альвеолярную вентиляцию. Некоторое количество вдыхаемого человеком воздуха не доходит до газообменных зон, а просто наполняет дыхательные пути — нос, носоглотку и трахею, где газообмена нет. Этот объем воздуха называют воздухом мертвого пространства, т.к. он не участвует в газообмене.
При выдохе воздух, наполняющий мертвое пространство, выдыхается первым — до того, как в атмосферу возвращается воздух из альвеол, поэтому мертвое пространство является дополнительным элементом при удалении выдыхаемого воздуха из легких.
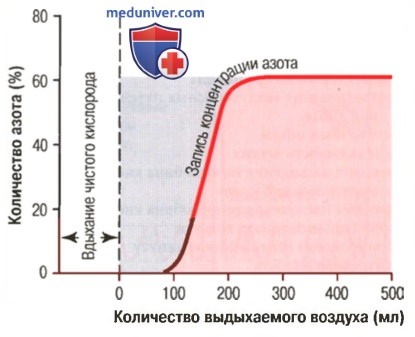
1. Измерение объема мертвого пространства. На рисунке выше показан простой способ измерения объема мертвого пространства. Испытуемый делает резкий глубокий вдох чистым кислородом, наполняя им все мертвое пространство. Кислород смешивается с альвеолярным воздухом, но не заменяет его полностью. После этого испытуемый делает выдох через нитрометр с быстрой записью (полученная при этом запись приведена на рисунке).
Первая порция выдыхаемого воздуха состоит из воздуха, который находился в мертвом пространстве дыхательных путей, где он был полностью заменен кислородом, поэтому в первой части записи присутствует только кислород и концентрация азота равна нулю. Когда до нитрометра начинает доходить альвеолярный воздух, концентрация азота резко возрастает, потому что содержащий большое количество азота альвеолярный воздух начинает смешиваться с воздухом из мертвого пространства.
С выходом все большего количества выдыхаемого воздуха из дыхательных путей вымывается весь воздух, находившийся в мертвом пространстве, и остается только альвеолярный воздух, поэтому концентрация азота на правой части записи вырисовывается как плато на уровне содержания его в альвеолярном воздухе. Серая область на рисунке представляет собой воздух, который не содержит азота и является мерой объема воздуха мертвого пространства.
Для точного измерения используют следующее уравнение:
Vd = (Серая область х Ve) / (Розовая область + Серая область),
где Vd — воздух мертвого пространства; Ve — общий объем выдыхаемого воздуха.
Мертвое пространство в этом случае равно 30 : (30 + 70) х 500 = 150 мл.
2. Нормальный объем мертвого пространства. Нормальный объем воздуха в мертвом пространстве у молодого взрослого мужчины составляет около 150 мл. С возрастом эта цифра немного увеличивается.
3. Анатомическое мертвое пространство и физиологическое мертвое пространство. Приведенный ранее способ измерения мертвого пространства позволяет измерить весь объем системы дыхания, кроме объема альвеол и расположенных около них зон газообмена, который называют анатомическим мертвым пространством. Но иногда некоторые из альвеол не функционируют или функционируют частично из-за отсутствия или уменьшения кровотока в близлежащих капиллярах. С функциональной точки зрения эти альвеолы также представляют собой мертвое пространство.
При включении альвеолярного мертвого пространства в общее мертвое пространство последнее называют не анатомическим, а физиологическим мертвым пространством. У здорового человека анатомическое и физиологическое пространства почти равны, но если у человека в некоторых участках легких часть альвеол не функционирует или функционирует только частично, объем физиологического мертвого пространства может оказаться в 10 раз больше анатомического, т.е. 1-2 л. Эти проблемы будут рассматриваться далее в связи с газообменом в легких и некоторыми болезнями легких.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Анализ газов во вдыхаемом и выдыхаемом воздухе
Капнометрия – это измерение концентрации или парциального давления углекислого газа в процессе дыхания во вдыхаемой и выдыхаемой газовой смеси.
На сегодняшний день в большинстве кабинетов функциональной диагностики из исследования внешнего дыхания проводится только спирометрия. Однако спирометрия выявляет преимущественно обструктивные нарушения и то лишь тогда, когда обструкция затрагивает бронхи среднего и крупного калибра. Сужение мелких (менее 2 мм в диаметре) дыхательных путей мало сказывается на бронхиальном сопротивлении и практически не ощущается пациентом. Хроническая обструктивная болезнь лёгких (ХОБЛ), как правило, начинается с дистальных дыхательных путей, длительно протекает без явных клинических проявлений (кашля, одышки) и достаточно долго может не проявляться обструктивными нарушениями, выявляемыми при спирометрии. В связи с этим, несомненный интерес представляют методы, оценивающие состояние респираторной зоны легких, включающей терминальные отделы воздухопроводящих путей и альвеолы.
Респираторная зона лёгких обеспечивает обмен газов в процессе дыхания, а её поражение в зависимости от его выраженности может сопровождаться тяжелой дыхательной недостаточностью, в т.ч. при незначительно сниженных или даже нормальных спирометрических показателях. Именно поражение респираторной зоны лёгких и объясняет выраженность дыхательной недостаточности при таких заболеваниях, как альвеолиты, бериллиоз, некоторые интерстициальные заболевания лёгких, вирусно-ассоциированные пневмонии.
Капнометрия как непрерывное измерение концентрации (парциального давления) углекислого газа при спокойном дыхании и при выполнении ряда дыхательных проб (задержки дыхания на вдохе, при глубоком выдохе и др.) является методом оценки состояния респираторной зоны лёгких, позволяет оценить неравномерность вентиляционно-перфузионных соотношений, эффективность газообмена в лёгких. Дыхание проводится в открытом контуре при непрерывном отборе части воздуха на газоанализатор, принцип действия которого основан на контроле поглощения углекислого газа в инфракрасной области.
Капнометрическое исследование, доступное в качестве опции в спирометрах МАС2-С, позволяет оценить:
– концентрацию углекислого газа в альвеолярном пространстве (через измерение PETCO2), позволяя соотнести адекватность альвеолярной вентиляции уровню метаболизма с возможностью выявления альвеолярной нормо-, гипо- или гипервентиляции;
– наклон альвеолярного плато, оценивая, тем самым, равномерность распределения вентиляции и кровотока (вентиляционно-перфузионные отношения) в легких;
– соотношение величины функционального мертвого пространства (МП), т.е. суммы анатомического и альвеолярного МП и дыхательного объема (Vd/Vt).;
– паттерн дыхания пациента, определяя его частоту и глубину, выявить состояние гиперкапнии, что широко используется в отделениях интенсивной терапии и в анестезиологический практике.
Наиболее частой причиной нарушения равномерности распределения вентиляции и кровотока в легких являются обструкция мелких дыхательных путей, выраженная в разной степени в разных участках легкого, нарушения эластических свойств легких, нарушения микроциркуляции в легких, очаговые воспалительные и фиброзные процессы в легочной ткани. При ХОБЛ нарушения на капнограмме могут обнаруживаться на ранней стадии (стадии предболезни), когда спирометрические показатели (ОФВ1, ОФВ1/ФЖЕЛ) снижены незначительно или находятся в пределах нормы.
Используются два подходa к расчету капнограммы: расчет по кривой зависимости концентрации (парциального давления) СО2 от времени и расчет по кривой зависимости концентрации (парциального давления) СО2 от объема выдохнутого воздуха (капноволюметрия). В первом случае оцениваются следующие показатели: РetСО2 – парциальное давление СО2 в конце спокойного выдоха, наклон альвеолярной фазы (ΔР/Δt), угол между восходящей частью кривой и альвеолярной фазой (угол α), угол между альвеолярной фазой и нисходящей частью кривой (угол β), индекс Tulou – разница РetСО2 в конце глубокого и спокойного выдоха. Рассчитывается также отношение объема мертвого пространства к дыхательному объему (Vd/Vt).
При капноволюметрии (требуется одновременная запись спирограммы и капнограммы), рассчитывают наклон альвеолярной фазы при спокойном и глубоком выдохе, величины альвеолярного и анатомического мертвого пространствах, и ряд других показателей.