Чем определяются свойства хим элементов
Периодический закон
Периодический закон был открыт Д.И. Менделеевым в 1868 году. Его современная формулировка: свойства химических элементов и образуемых ими соединений (простых и сложных) находятся в периодической зависимости от величины заряда атомного ядра.
Периодический закон лежит в основе современного учения о строении вещества. Периодическая система Д.И. Менделеева является наглядным отражением периодического закона.
Группой называют вертикальный ряд химических элементов в периодической таблице. Элементы собраны в группы на основе степени окисления в высшем оксиде. Каждая из восьми групп состоит из главной подгруппы (а) и побочной подгруппы (б).
Периодическая таблица Д.И. Менделеева содержит колоссальное число ответов на самые разные вопросы. При умелом ее использовании вы сможете предполагать строение и свойства веществ, успешно писать химические реакции и решать задачи.
Радиус атома
Радиусом атома называют расстояние между атомным ядром и самой дальней электронной орбиталью. Это не четкая, а условная граница, которая говорит о наиболее вероятном месте нахождения электрона.
В периоде радиус атома уменьшается с увеличением порядкового номера элементов («→» слева направо). Это связано с тем, что с увеличением номера группы увеличивается число электронов на внешнем уровне. Запомните, что для элементов главных подгрупп номер группы равен числу электронов на внешнем уровне.
С увеличением числа электронов они становятся более скученными, так как притягиваются друг к другу сильнее: это и есть причина маленького радиуса атома.
Чем меньше электронов, тем больше у них свободы и больше радиус атома, поэтому радиус увеличивается в периоде «←» справа налево.
Период, группа и электронная конфигурация
Правило составления электронной конфигурации, которое вы только что увидели, универсально. Если вы имеете дело с элементом главной подгруппы, то увидев номер группы вы знаете, сколько электронов у него на внешнем уровне. Посмотрев на период, знаете номер его внешнего уровня.
Длина связи
Убедимся в этом на наглядном примере, сравнив длину связей в четырех веществах: HF, HCl, HBr, HI.
Чем больше радиусы атомов, которые образуют химическую связь, тем больше между ними и длина связи. Радиус атома водорода неизменен во всех трех веществах, а в ряду F → Cl → Br → I происходит увеличение радиуса атома. Наибольшим радиусом обладает йод, поэтому самая длинная связь в молекуле HI.
Металлические и неметаллические свойства
Сравним металлические и неметаллические свойства Rb, Na, Al, S. Натрий, алюминий и сера находятся в одном периоде. Металлические свойства возрастают S → Al → Na. Натрий и рубидий находятся в одной группе, металлические свойства возрастают Na → Rb.
Основные и кислотные свойства
Замечу, что здесь есть одно важное исключение. Как и в общем случае: исключения только подтверждают правила. В ряду галогенводородных кислот HF → HCl → HBr → HI происходит усиление кислотных свойств (а не ослабление, как должно быть по логике нашего правила).
Восстановительные и окислительные свойства
Электроотрицательность (ЭО), энергия связи, ионизации и сродства к электрону
Для примера сравним ЭО-ость атомов Te, In, Al, P. Индий расположен в одной группе с алюминием, ЭО-ость In → Al возрастает (снизу вверх). Алюминий расположен в одном периоде с серой, ЭО-ость возрастает Al → S (слева направо). Сравнивая серу и теллур, мы видим, что сера расположена в группе выше теллура, значит и ее электроотрицательность тоже выше.
Энергия связи (а также ее прочность) возрастают с увеличением электроотрицательности атомов, образующих данную связь. Чем сильнее атом тянет на себя электроны (чем больше он ЭО-ый), тем прочнее получается связь, которую он образует.
Продемонстрирую на примере. Сравним энергию связи в трех молекулах: H2O, H2S, H2Se.
Высшие оксиды и летучие водородные соединения (ЛВС)
В периодической таблице Д.И. Менделеева ниже 7 периода находится строка, в которой для каждой группы указаны соответствующие высшие оксиды, ниже строка с летучими водородными соединениями.
Для элементов главных подгрупп начиная с IV группы (в большинстве случае) максимальная степень окисления (СО) определяется по номеру группы. К примеру, для серы (в VI группе) максимальная СО = +6, которую она проявляет в соединениях: H2SO4, SO3.
На экзамене строка с готовыми «высшими» оксидами, как в таблице наверху, может отсутствовать. Считаю важным подготовить вас к этому. Предположим, что эта строчка внезапно исчезла из таблицы, и вам нужно записать высшие оксиды для фосфора и углерода.
С летучими водородными соединениями (ЛВС) ситуация аналогичная: их может не быть в периодической таблице Д.И. Менделеева, которая попадется на экзамене. Я расскажу вам, как легко их запомнить.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Улучшенная версия таблицы Менделеева

Артем Оганов — кристаллограф-теоретик, создатель ряда новых материалов, а главное, методов, которые позволяют открывать новые материалы. Решил считавшуюся нерешаемой задачу предсказания кристаллической структуры вещества на основе его химического состава. Создал программу USPEX, способную предсказывать устойчивые химические соединения по набору исходных элементов. Один из самых цитируемых в мире ученых.
Я хорошо помню, как мне пришло в голову решение этой задачи. Мы с семьей садились в самолет. У меня четверо детей, и все они расположились у меня на голове и прочих частях тела и к тому же продолжали непрерывно двигаться. Опытные родители знают, что сопротивляться этому бессмысленно, а беспокоиться неразумно. Поэтому мой мозг перестал метаться, анализируя внешние сигналы, и застыл, сфокусировавшись в одной точке. Точка эта оказалась на спинке впередистоящего кресла. Там-то и начал проступать основной график будущей работы. Я вдруг увидел, что элементы таблицы Менделеева не размазаны равномерно в пространстве своих свойств, а, как звезды в Галактике, расположены более-менее на плоскости.
Улучшенные менделеевские числа помогут находить новые соединения с полезными свойствами и смогут прояснить некоторые вопросы, связанные с привычной таблицей Менделеева. Например, уже сейчас можно ставить точку в споре, где должен находиться водород: над литием или над фтором. Согласно менделеевским числам, водород ближе к галогенам, чем к щелочным металлам.
Ссылка: Zahed Allahyari and Artem R. Oganov, Nonempirical Definition of the Mendeleev Numbers: Organizing the Chemical Space: J. Phys. Chem. C 2020, 124, 43, 23867-23878.
Химический элемент
Формой существования химических элементов в свободном виде являются простые вещества (одноэлементные) [3]
Содержание
История становления понятия
Слово «элемент» (лат. elementum ) использовалось еще в античности (Цицероном, Овидием, Горацием) как часть чего-то (элемент речи, элемент образования и т. п.). В древности было распространено изречение «Как слова состоят из букв, так и тела — из элементов». Отсюда — вероятное происхождение этого слова: по названию ряда согласных букв в латинском алфавите: l, m, n, t («el» — «em» — «en» — «tum»). [4]
Благодаря Джону Дальтону в начале XIX в. в химии возобладала атомно-молекулярная гипотеза, рассматривающая химический элемент как отдельный вид атомов и указывающая на природу простых и сложных веществ, как состоящих, соответственно, из атомов одного или различного видов. Дальтон же впервые указывает на атомный вес как важнейшее свойство элементов, определяющее его химическую природу. Благодаря усилиям Йенса Берцелиуса и его последователей были весьма точно определены атомные веса (атомные массы) известных элементов. Середина XIX в. ознаменовалась целым рядом открытий новых элементов. На международном съезде химиков в г. Карлсруэ в 1860 г. были приняты определения понятий молекулы и атома.
Ko времени открытия Периодического закона Д. И. Менделеевым (1869) было известно 63 элемента. Именно атомный вес был выделен им как свойство атомов, определяющее периодический характер изменения свойств химических элементов, а также образуемых ими простых и сложных веществ. Менделеев определял химические элементы как «материальные части простых или сложных тел, к-рые придают им известную совокупность физических и химических свойств». Oткрытие Mенделеева позволило предвидеть существование, a также свойства ряда неизвестных в то время элементов и послужило научной основой для их классификации.
Однако с открытием изотопов стало ясно, что различные совокупности атомов одного и того же элемента могут иметь различающиеся атомные массы; так, радиогенный гелий, выделенный из урановых минералов, в связи с преобладанием изотопа 4 He имеет атомную массу больше, чем гелий космических лучей.
Известные химические элементы
Право предложить название новому химическому элементу предоставляется первооткрывателям. Сообщение о новом открытии проверяется в течение нескольких лет независимыми лабораториями, и, в случае подтверждения, Международный союз теоретической и прикладной химии (ИЮПАК, IUPAC, en:International Union for Pure and Applied Chemistry) официально утверждает название нового элемента.
Не все из известных на сегодня 118 элементов имеют утвержденные ИЮПАК постоянные названия. Самым тяжёлым из официально признанных элементов, имеющих официальные постоянные названия, является 116-й, получивший в мае 2012 года имя ливерморий вместе со 114-м элементом флеровием.
Названия сверхтяжёлых элементов с номерами 113, 115, 117, 118, полученные в 2002—2010 годах в России и США, официально пока не утверждены. Они имеют временные систематические названия.
Символы химических элементов
Символы химических элементов используются как сокращения для названия элементов. В качестве символа обычно берут начальную букву названия элемента и в случае необходимости добавляют следующую или одну из следующих. Обычно это начальные буквы латинских названий элементов: Cu — медь (cuprum), Ag — серебро (argentum), Fe — железо (ferrum), Au — золото (aurum), Hg — ртуть (hydrargirum). Такая система химических символов была предложена в 1811 г. шведским химиком Я. Берцелиусом.
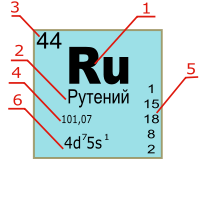
Цифрами меньшего размера возле символа элемента обозначаются: слева вверху — атомная масса, слева внизу — порядковый номер, справа вверху — заряд иона, справа внизу — число атомов в молекуле [7] :
| атомная масса | заряд иона |
| Символ элемента | |
|---|---|
| порядковый номер | число атомов в молекуле |
Временные символы элементов состоят из трёх букв, представляющих аббревиатуру их атомного номера на латыни.
В Периодической таблице карточка химического элемента обычно включает следующие характеристики:
Распространённость химических элементов в природе
Из всех химических элементов в природе найдено 88; такие элементы, как технеций Tc (порядковый номер 43), прометий Pm (61), астат At (85) и франций Fr (87), а также все элементы, следующие за ураном U (порядковый номер 92), впервые получены искусственно. Некоторые из них в исчезающе малых количествах обнаружены в природе.
Из химических элементов наиболее распространены в земной коре кислород и кремний. Эти элементы вместе с элементами алюминий, железо, кальций, натрий, калий, магний, водород и титан составляют более 99 % массы земной оболочки, так что на остальные элементы приходится менее 1 %. В морской воде, помимо кислорода и водорода — составных частей самой воды, высокое содержание имеют такие элементы, как хлор, натрий, магний, сера, калий, бром и углерод. Массовое содержание элемента в земной коре называется кларковым числом или кларком элемента.
Содержание элементов в коре Земли отличается от содержания элементов в Земле, взятой как целое, поскольку химсоставы коры, мантии и ядра Земли различны. Так, ядро состоит в основном из железа и никеля. В свою очередь, содержания элементов в Солнечной системе и в целом во Вселенной также отличаются от земных. Наиболее распространённым элементом во Вселенной является водород, за ним идёт гелий. Исследование относительных распространённостей химических элементов и их изотопов в космосе является важным источником информации о процессах нуклеосинтеза и об эволюции Солнечной системы и небесных тел.
Классификация химических элементов
Химические элементы как составная часть химических веществ
Химические вещества могут состоять как из одного химического элемента (простое вещество), так и из разных (сложное вещество или химическое соединение).
В обычных условиях 11 элементов существуют в виде газообразных простых веществ (H, He, N, O, F, Ne, Cl, Ar, Kr, Xe, Rn), 2 — жидкости (Br и Hg), остальные элементы образуют твёрдые тела.
См. также
Ссылки
Примечания
 | Химический портал — мир химии, веществ и превращений на страницах Википедии. |
Полезное
Смотреть что такое «Химический элемент» в других словарях:
химический элемент — — [http://www.eionet.europa.eu/gemet/alphabetic?langcode=en] EN chemical element A substance made up of atoms with the same atomic number; common examples are hydrogen, gold, and iron. (Source: MGH)… … Справочник технического переводчика
ХИМИЧЕСКИЙ ЭЛЕМЕНТ — совокупность атомов, имеющих одинаковый заряд ядра и, следовательно, одинаковое число электронов в электронной оболочке. Многие из них имеют несколько (см.). Хим. элементы обозначают знаками химическими (см. (9)), а их закономерную взаимосвязь… … Большая политехническая энциклопедия
химический элемент — совокупность атомов с одинаковым зарядом ядра Z (одинаковым порядковым, или атомным, номером в периодической системе химических элементов). В таблицу химических элементов, издаваемую ИЮПАК, на 1998 внесено 109 элементов, имеющих названия (имеются … Энциклопедический словарь
химический элемент — ▲ атом ↑ с, определенный, заряд, атомное ядро элемент, химический элемент вид атомов, обладающих одинаковым зарядом ядра (железо #). атомный [порядковый] номер равен числу протонов в атомном ядре. атомный вес. ▼ водород, гидроген. кислород,… … Идеографический словарь русского языка
химический элемент — cheminis elementas statusas T sritis chemija apibrėžtis Atomų rūšis, turinti vienodą branduolio krūvį. atitikmenys: angl. chemical element; element rus. химический элемент; элемент ryšiai: sinonimas – elementas … Chemijos terminų aiškinamasis žodynas
химический элемент — cheminis elementas statusas T sritis Standartizacija ir metrologija apibrėžtis Atomų rūšis, turinti vienodą branduolio krūvį. atitikmenys: angl. chemical element vok. chemisches Element, n rus. химический элемент, m pranc. élément chimique, m … Penkiakalbis aiškinamasis metrologijos terminų žodynas
химический элемент — cheminis elementas statusas T sritis chemija apibrėžtis Elektrocheminio elemento tipas. atitikmenys: angl. chemical element rus. химический элемент … Chemijos terminų aiškinamasis žodynas
химический элемент — cheminis elementas statusas T sritis fizika atitikmenys: angl. chemical element vok. chemisches Element, n rus. химический элемент, m pranc. élément chimique, m … Fizikos terminų žodynas
ХИМИЧЕСКИЙ ЭЛЕМЕНТ — вид атомов, обладающих одинаковым зарядом ядра. X. э. в свободном состоянии являются простыми (не разложимыми хим. методами на более простые) в вами. Мн. X. э. состоят из неск. изотопов. Взаимосвязь X. э. отражает периодическая система элементов… … Большой энциклопедический политехнический словарь
ХИМИЧЕСКИЙ ЭЛЕМЕНТ — совокупность атомов с одинаковым зарядом ядра Z (одинаковым порядковым, или атомным, номером в периодической системе химических элементов). В таблицу X. э., издаваемую ИЮПАК, на 1998 внесено 109 элементов, имеющих названия (есть сведения о… … Естествознание. Энциклопедический словарь
ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ
Полезное
Смотреть что такое «ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ» в других словарях:
Элементы химические — (a. chemical elements; н. chemische Elemente; ф. elements chimiques; и. elementos quimicos) составные части простых и сложных тел, представляющие собой совокупность атомов c одинаковым зарядом атомных ядер и одинаковым числом электронов в … Геологическая энциклопедия
Элементы химические — элементы Периодической таблицы элементов Менделеева, в которой каждый элемент это вся совокупность атомов с одинаковым зарядом атомных ядер и одинаковым числом электронов в атомной оболочке. В настоящее время число известных элементов 118 … Начала современного естествознания
Элементы химические — Периодическая система химических элементов Д. И. Менделеева H … Википедия
Элементы химические — Каждый Э. х. это совокупность Атомов с одинаковым зарядом атомных ядер и одинаковым числом электронов в атомной оболочке. Ядро атомное состоит из протонов, число которых равно атомному номеру (См. Атомный номер) элемента, и нейтронов,… … Большая советская энциклопедия
Элементы химические — [chemical elements] составные части всего многообразия простых и сложных веществ. Каждый химический элемент это совокупность атомов с одинаковым зарядом атомных ядер и одинаковым числом электронов в атомной оболочке. Атомное ядро состоит из… … Энциклопедический словарь по металлургии
Элементы химические* — Громадное разнообразие явлений и веществ природы, при её изучении, мысль человеческая всегда стремилась упростить при помощи допущения если не полного единства основных Э. (Демокрит, Эпикур), то, по крайней мере, при помощи небольшого числа Э.,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Элементы (химические) — Громадное разнообразие явлений и веществ природы, при её изучении, мысль человеческая всегда стремилась упростить при помощи допущения если не полного единства основных Э. (Демокрит, Эпикур), то, по крайней мере, при помощи небольшого числа Э.,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
P-элементы (химические) — p элементами называют химические элементы, в атомах которых электрон с наивысшей энергией занимает p орбиталь. p элементами являются: в 1 м периоде нет p элементов во 2 м периоде B Ne в 3 м периоде Al Ar в 4 м периоде Ga Kr в 5 м периоде In Xe в… … Википедия
Химические источники тока — (аббр. ХИТ) устройства, в которых энергия протекающих в них химических реакций непосредственно превращается в электрическую энергию. Содержание 1 История создания 2 Принцип действия … Википедия
Зачет по химии
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
Зачет по теме для учащихся 8-9 классов.
«Периодический закон. Периодическая система химических элементов Д.И. Менделеева. Строение атома»
1) Какая формулировка Периодического закона является современной?
а) Свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины их атомной массы.
б) Свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов их атомных ядер.
2) С увеличением порядкового номера элемента в периоде:
а) радиусы атомов увеличиваются
б) радиусы атомов уменьшаются
в) радиусы атомов не изменяются
3) Радиус какого атома больше:
4) Чем определяется место химического элемента в периодической системе Д.И.Менделеева?
а) количеством электронов на внешнем энергетическом уровне атома
б) количеством нейтронов в ядре атома
в) зарядом ядра атома
5)Как определить, используя периодическую систему химических элементов Д.И. Менделеева, количество энергетических уровней атома элемента?
а) по порядковому номеру элемента
б) по номеру группы
в) по номеру периода
6) Сколько энергетических уровней у атома скандия?
7) Чем определяются свойства химических элементов?
а) величиной относительной атомной массы элемента
б) числом электронов на внешнем энергетическом уровне атома
в) зарядом ядра атома
г) количеством валентных электронов
8) Как изменяются химические свойства элементов в периоде периодической системы химических элементов с увеличением заряда ядер их атомов?
а) усиливаются металлические свойства
б) усиливаются неметаллические свойства
в) ослабевают металлические свойства
г) ослабевают неметаллические свойства
9) Укажите элемент с металлическими свойствами, возглавляющий большой период периодической системы химических элементов ( см. периодическую таблицу).
а) медь (№29) б) серебро(№47) в) калий(№19) г)золото(№79)
10) Определите элемент, проявляющий наиболее ярко выраженные металлические свойства
а) магний б) алюминий в) кремний
11) В чём основная причина изменения свойств химических элементов в периоде периодической системы Д.И. Менделеева?
а) в постепенном увеличении числа электронов на внешнем энергетическом уровне
б) в увеличении атомных масс
в) в увеличении количества электронов в атоме
г) в увеличении количества нейтронов в ядре атома
12) Как изменяются свойства элементов внутри периода с увеличением заряда ядер их атомов?
а) плавно б) скачкообразно
а) появление нового электронного уровня
б) постепенное накопление электронов на внешнем энергетическом уровне атома
в) постепенное увеличение атомных масс
г) увеличение количества нейтронов в ядре атома
14) Как изменяются свойства химических элементов в главных подгруппах с увеличением заряда ядер их атомов?
а) усиливаются металлические свойства
б) ослабевают металлические свойства
в) усиливаются неметаллические свойства
г) ослабевают неметаллические свойства
15) В чём основная причина изменения свойств химических элементов в главных подгруппах периодической системы?
а) в постепенном увеличении атомных масс
б) в появлении нового энергетического уровня
в) в увеличении количества электронов в атоме
г) в увеличении количества нейтронов в ядре атома
16) Какой элемент возглавляет главную подгруппу четвертой группы периодической системы химических элементов?
а) селен(№34) б)углерод (№6) в)титан (№22) г)кремний (№14)
17)Какой элемент проявляет наиболее ярко выраженные неметаллические свойства?
18) Какой из высших оксидов относится к оксиду, образованному элементом четвёртой группы?
19) Какую общую формулу имеют гидроксиды, образованные элементами шестой группы?
20)Используя периодическую таблицу химических элементов, установите, какой из указанных элементов может образовывать газообразное водородное соединение
а) № 22 б) № 6 в) № 23 г) № 24
а) траектория, по которой движется электрон
б) вероятность нахождения электрона в данной точке атомного пространства
в) пространство вокруг ядра атома, в котором наиболее вероятно пребывание электрона
г) определённый энергетический уровень, на котором находится электрон
22) На какой орбитали электрон имеет наибольшую энергию
а) 1s б) 2 s в) 3s г) 2 p
23)Определите номер химического элемента в периодической системе, электронная формула атома которого 1 s 1 2 s 2 2 p 3
24)Какое число валентных электронов у атома кальция?
25) Используя периодическую систему химических элементов, определите низшую валентность хлора.
а) бор б) хлор в) магний г)фосфор
а) в химических реакциях вещество может быть как окислителем, так и восстановителем.
б) образует летучее водородное соединение
в) раствор водородного соединения в воде- слабая кислота
г) гидроксид высшего оксида обладает основными свойствами
28)Химические элементы каких групп периодической системы могут образовывать летучие водородные соединения?
29) Установите формулы кислотных оксидов, образованных элементами одного периода
30) Определите формулу амфотерного оксида, образованного элементом третьего периода
31) Укажите элемент, оксид которого проявляет основной характер
а) барий (№56) б)алюминий(№13) в)сурьма (№51) г)селен(№34)
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
Курс профессиональной переподготовки
Методическая работа в онлайн-образовании
Ищем педагогов в команду «Инфоурок»
Зачет по теме «Периодический закон. Периодическая система химических элементов Д. И. Менделеева. Строение атома» Зачет для учащихся 8 класса после изучении темы «Периодический закон. Периодическая система химических элементов Д. И. Менделеева. Строение атома». Этот зачет можно провести для учащихся 11 классов при подготовке к единому государственному экзамену. Зачет состоит из 31 вопросов в конце которого ответы на каждый вопрос. Большинство вопросов состоит из 4-х ответов, который ученик выбирает 1 или 2 правильных ответов.
Номер материала: 255003
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
МГУ откроет первую в России магистерскую программу по биоэтике
Время чтения: 2 минуты
Учителям предлагают 1,5 миллиона рублей за переезд в Златоуст
Время чтения: 1 минута
Учителям истории предлагают предоставить право бесплатно посещать музеи
Время чтения: 2 минуты
Путин поручил не считать выплаты за классное руководство в средней зарплате
Время чтения: 1 минута
В России утвердили новый порядок формирования федерального перечня учебников
Время чтения: 1 минута
В МГПУ сформулировали новые принципы повышения квалификации
Время чтения: 4 минуты
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.