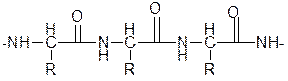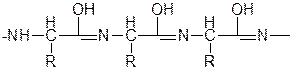Чем обусловлена реакция сакагучи
Чем обусловлена реакция сакагучи
Биуретовая реакция (реакция Пиотровского). В щелочной среде белки, а также продукты их гидролиза — полипептиды дают фиолетовое или красно-фиолетовое окрашивание с солями меди. Реакция обусловлена наличием пептидных связей. Положительная биуретовая реакция проявляется у соединений, содержащих не менее двух
пептидных групп. Интенсивность окраски зависит от длины пептида и варьирует от сине-фиолетовой до краснофиолетовой и красной.
Биуретовую реакцию дают также аспарагин (амид аспарагиновой кислоты) и аминокислоты гистидин, треонин и серин.
Свое название реакция получила от биурета — соединения, которое образуется при нагревании мочевины. Эта реакция сопровождается отщеплением молекулы аммиака
Комплексной медно-натриевой соли пептидов и белков приписывают следующее строение:
Реактивы: а) раствор яичного белка (без добавления хлористого натрия); б) раствор растительного белка (приготовление — см. с. 6); в) едкий натр, 10%-ный раствор; г) сернокислая медь, 1%-ный раствор.
В одну пробирку наливают 2 мл раствора яичного белка, в другую — столько же растительного, затем в каждую из них прибавляют равный объем раствора едкого натра и по 1—2 капли раствора сернокислой меди. Появляется красно-фиолетовое или сине-фиолетовое окрашивание.
Нингидриновая реакция.
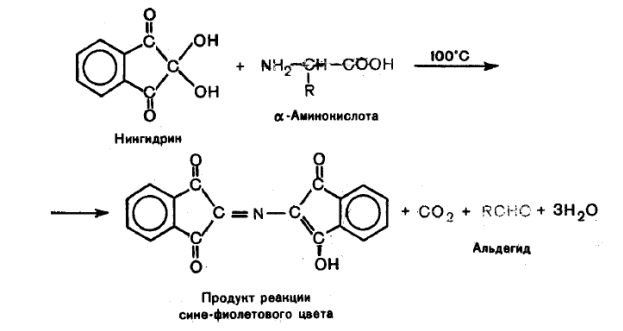
Нингидриновая реакция обусловлена наличием аминокислот, имеющих аминогруппы в a-положении. Белки, полипептиды и аминокислоты образуют с нингидрином соединение синего или сине-фиолетового цвета (при нагревании). Нингидриновая реакция является одной из наиболее чувствительных для обнаружения а-аминогрупп.
Сущность реакции заключается в том, что а-аминокислоты и пептиды, реагируя с нингидрином, подвергаются окислительному дезаминированию и декарбоксилированию:
Восстановленный нингидрин взаимодействует с аммиаком и второй молекулой нингидрина, в результате чего образуется окрашенное соединение (пурпурный Руэманна)
Реактивы: а) раствор белка (без хлористого натрия). Приготовление — см. с. 6; б) глицин, 0,1%-ный водный раствор; в) нингидрин, 0,1%-ный спиртовой раствор. В одну пробирку наливают 1-2 мл раствора глицина, в другую — столько же раствора белка. В обе пробирки добавляют раствор нингидрина (в первую 5—6 капель, во вторую — 10—12), нагревают около минуты. В пробирке с глицином быстро появляется фиолетово-синее или фиолетовое окрашивание, в пробирке с белком окрашивание развивается медленно и имеет красновато-фиолетовый оттенок (или даже желтовато-фиолетовый в случае наличия иминокислоты пролина).
Реакция Лоури.
Это одна из наиболее чувствительных реакций на белки. Ее дают циклические аминокислоты. Реагируя с реактивом Фолина, они образуют комплексы, окрашенные в синий цвет. Интенсивность окраски зависит от концентрации белков, поэтому реакция Лоури может быть использована и для количественного определения.
Реактивы: а) раствор яичного белка для цветных реакций и реакций осаждения (см. с. 6), разведенный дистиллированной водой в 100 раз; б) глицин, 0,02%-ный раствор; в) фенилаланин, 0,02%-ный раствор; г) реактив А: 2%-ный раствор углекислого натрия 






концентрированной соляной кислоты 

В три пробирки вносят соответственно растворы яичного белка, глицина и фенилаланина (по 2,5 мл), добавляют по 5 мл раствора С и оставляют на 10 мин., после чего приливают по 5 мл рабочего раствора реактива Фолина. Через 30 мин. наблюдают окрашивание жидкости: в пробирках с белком и фенилаланином развивается интенсивная синяя окраска, в пробирке с глицином сохраняется желтый цвет реактива.
Ксантопротеиновая реакция.
Характерна для некоторых ароматических аминокислот (фенилаланина, тирозина, триптофана). При нагревании белков и полипептидов с концентрированной азотной кислотой образуется нитросоединение желтого цвета.
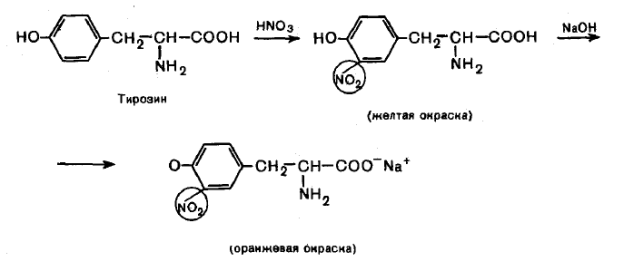
Реакция протекает в две стадии. На протяжении первой аминокислота, например тирозин, взаимодействуя с концентрированной азотной кислотой, подвергается нитрованию. При этом образуется динитротирозин (желтого цвета).
Примечание. В зависимости от количества прибавленной азотной кислоты может образоваться и смесь динитро- и нитротирозина.
Во второй стадии продукты нитрования тирозина (ди-нитро- и нитротирозин) реагируют с едким натром или гидроокисью аммония с образованием натриевой или аммонийной соли, имеющей желто-оранжевое окрашивание.
Ксантопротеиновую реакцию, кроме белков, пептидов и циклических аминокислот, дают также многие простые ароматические соединения (бензол, фенол и др.).
Реактивы: а) раствор яичного или растительного белка (приготовление — см. с. 6); б) раствор желатина, 


К 2-3 мл раствора фенола осторожно (по стенке пробирки) приливают 1-2 мл концентрированной азотной кислоты. Осторожно нагревают, появляется желтое окрашивание.
В другую пробирку наливают 1-2 мл раствора яичного или растительного белка, прибавляют 8—10 капель концентрированной азотной кислоты и осторожно нагревают. Выпадает осадок, который окрашивается в желтый цвет.
После охлаждения в пробирку осторожно (по стенке) приливают избыток концентрированного раствора аммиака или едкого натра — жидкость принимает оранжевое или желто-оранжевое окрашивание.
Реакцию следует проводить под тягой!
Те же реакции проводят с раствором желатина: желтого окрашивания не наступает, так как желатин не содержит ароматических аминокислот (иногда может появиться очень слабое желтоватое окрашивание, обусловленное примесью других белков).
Реакция Миллона.
С помощью реакции Миллона открывают наличие аминокислоты тирозина. Тирозин образует с реактивом Миллона ртутную соль нитротирозина красного цвета. Эта реакция характерна также почти для всех фенолов.
Реактивы: а) раствор яичного или растительного белка (см. с. 6); б) раствор желатина, 1%-ный; в) фенол, 0,1%-ный раствор; г) реактив Миллона: 40 г ртути растворяют в 57 мл концентрированной азотной кислоты вначале при комнатной температуре, затем слабо подогревая на водяной бане. Раствор разбавляют двумя объемами воды и после отстаивания сливают с осадка.
Все работы производят под тягой!
К 1 мл раствора фенола в пробирке приливают 0,5 мл реактива Миллона 
В пробирку наливают 1-2 мл раствора яичного или растительного белка и 5—6 капель реактива Миллона, осторожно нагревают.
Жидкость окрашивается в красный цвет, и затем выпадает осадок кирпично-красного цвета.
То же проделывают и с раствором желатина: красного окрашивания не наступает или оно проявляется очень слабо (если желатин не очищен от примеси других белков),
Реакции на триптофан.
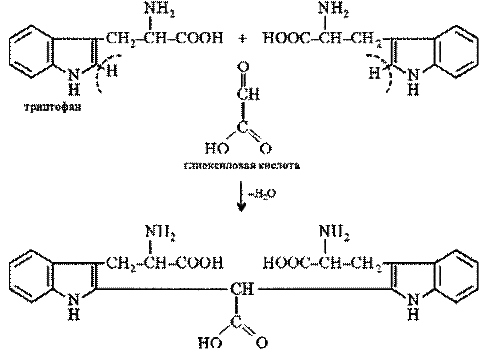
Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. Например, с глиоксиловой кислотой (являющейся примесью к концентрированной уксусной кислоте) реакция протекает по уравнению
По аналогичной схеме протекает также реакция триптофана с оксиметилфурфуролом или формальдегидом.
В указанных реакциях принимает участие серная кислота, являющаяся водоотнимающим средством.
Реакция Адамкевича. Реактивы: а) свежий яичный белок (неразбавленный); б) желатин, 1%-ный раствор; в) уксусная кислота, концентрированная; г) серная кислота, концентрированная.
В пробирку наливают несколько капель неразбавленного яичного белка, прибавляют 1-2 мл концентрированной уксусной кислоты (лучше ледяной) и осторожно нагревают до растворения выпавшего осадка, после чего охлаждают и (осторожно!) по стенке пробирки, наклонив ее, наслаивают 1 мл концентрированной серной кислоты, следя, чтобы не произошло смешения жидкостей. На границе двух слоев через некоторое время появляется красно-фиолетовое кольцо.
Эту же реакцию проделывают с раствором желатина — окрашивания не наступает, так как триптофан не входит в состав желатина.
Реакция с оксиметилфурфуролом (Шульце — Распайля). От фруктозы в присутствии концентрированной серной кислоты отщепляется три молекулы воды, она превращается в оксиметилфурфурол, который образует с триптофаном окрашенные продукты конденсации. Реакцию можно производить как с фруктозой, так
и с сахарозой, при гидролитическом расщеплении которой освобождаются равные количества глюкозы и фруктозы.
Реактивы: а) раствор яичного или растительного белка (приготовление — см. с. 6); б) сахароза, 5%-ный раствор; в) серная кислота, концентрированная.
К 1-2 мл раствора белка добавляют 2—4 капли раствора сахарозы и по стенке пробирки осторожно наслаивают 1 мл концентрированной серной кислоты. На границе жидкостей появляется кольцо темно-красного (вишневого) цвета.
Реакция с формальдегидом. Реактивы: а) раствор яичного или растительного белка; б) формалин, 5%-ный раствор; в) серная кислота, концентрированная.
К 1 мл раствора белка в пробирке добавляют 2 капли раствора формалина и затем осторожно (по стенке пробирки) наслаивают 1 мл концентрированной серной кислоты, следя, чтобы жидкости не перемешивались. На границе соприкосновения жидкостей появляется кольцо фиолетового или фиолетово-красноватого цвета.
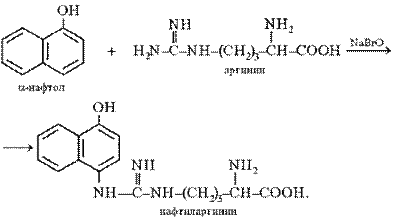
Реакция на аргинин (Сакагучи).
Производные гуанидина, как, например, аминокислота аргинин (гуанидина-миновалериановая кислота), метилгуанидин, гликоциамин (гуанидинуксусная кислота), реагируя с гипобромитом натрия (NaBrO) и а-нафтолом, образуют продукт конденсации кирпично-красного или малинового цвета. Метилгуанидин и глнкоциамин не входят в состав белковых веществ, и поэтому реакцию Сакагучи можно использовать для открытия аминокислоты аргинина.
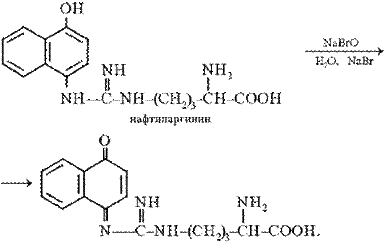
Гипобромит является окислителем. Окисленный аргинин,
потеряв одну иминогруппу 
Реактивы: а) раствор яичного или растительного белка; б) а-нафтол. Готовят 1%-ный раствор в 96%-ном этиловом спирте. Перед употреблением 10 мл раствора разбавляют спиртом в мерной колбе емкостью 
Примечание. Раствор гипобромита натрия готовится лаборантом.
К 1 мл раствора белка прибавляют 2—3 капли раствора едкого натра, 
Реакция на аминокислоты, содержащие серу (цистеин, цистин).
Известны три серусодержащие аминокислоты: цистеин, цистин и метионин.
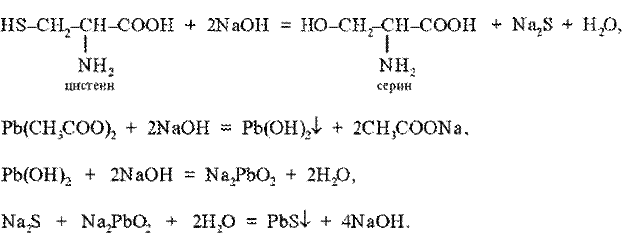
В молекулах цистеин а и цистин а сера связана относительно слабо и легко отщепляется при щелочном гидролизе в виде сероводорода, который реагирует со щелочью, образуя сульфиды натрия или калия. Сульфиды взаимодействуют с уксуснокислым свинцом (вернее, с плюмбитом) с образованием осадка сернистого свинца черного или буро-черного цвета. Реакции протекают по следующим уравнениям:
Реактивы: а) раствор яичного или растительного белка (см. с. 6); б) желатин, 1%-ный раствор; в) едкий натр, 15-20%-ный раствор; г) уксуснокислый свинец, 1%-ный раствор.
В одну пробирку наливают 2 мл раствора яичного или растительного белка, в другую — столько же раствора желатина. В обе пробирки добавляют по 1-1,5 мл раствора щелочи и осторожно нагревают до кипения, кипятят 1—2 мин., после чего в каждую пробирку прибавляют по 2—3 капли раствора уксуснокислого свинца.
В пробирке с яичным (или растительным) белком появляется буровато-черное или черное окрашивание, интенсивность которогозависит от концентрации раствора белка и содержания в нем цистеина и цистина. Раствор желатина окрашивания не дает. Это свидетельствует о том, что в состав желатина не входят серусодержащие аминокислоты.
Качественные реакции на аминокислоты, пептиды, белки
Аминокислоты можно обнаружить с помощью цветных реакций: нингидриновой, ксантопротеиновой, Фоля, Милона, биуретовой пробы и др. Эти реакции неспецифичны, т.к. основаны на обнаружении отдельных фрагментов в структуре аминокислот, которые могут встречаться и в других соединениях.
Нингидриновая реакция, цветная реакция, применяемая для качественного и количественного определения аминокислот, иминокислот и аминов. При нагревании в щелочной среде нингидрина (трикетогидринденгидрата, С9НбО4) с веществами, имеющими первичные аминогруппы (—NH2), образуется продукт, который имеет устойчивую интенсивную сине-фиолетовую окраску с максимальным поглощением около 570 нм. Т. к. поглощение при этой длине волны линейно зависит от числа свободных аминогрупп, нингидриновая реакция послужила основой для их количественного определения методами колориметрии или спектрофотометрии. Эта реакция используется также для определения вторичных аминогрупп (>NH) в иминокислотах — пролине и оксипролине; в этом случае образуется продукт ярко-жёлтого цвета. Чувствительность — до 0,01%. Современный автоматический аминокислотный анализ проводят, сочетая ионообменное разделение аминокислот и количественное определение их с помощью нингидриновой реакции. При разделении смесей аминокислот методом бумажной хроматографии позволяет определять каждую аминокислоту в количестве не менее 2—5 мкг.
По интенсивности окраски можно судить о количестве аминокислот.
Эта реакция положительна не только со свободными аминокислотами, но и пептидами, белками и др.
Ксантопротеиновая реакция позволяет обнаружить ароматические аминокислоты (фенилаланин, тирозин, гистидин, триптофан), основана на реакции электрофильного замещения в ароматическом ядре (нитрование).
При действии концентрированной азотной кислоты, например, на тирозин образуется продукт, окрашенный в желтый цвет.
Реакция Фоля. Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Описание опыта. В пробирку наливают 1 мл раствора цистина, прибавляют 0,5 мл 20%-го раствора гидроксида натрия. Смесь нагревают до кипения, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):
Реакция Циммермана. Это реакция на аминокислоту глицин.
Описание опыта. К 2 мл 0,1%-го раствора глицина, доведенного добавлением 10%-го раствора щелочи до рН = 8, приливают 0,5 мл водного раствора о-фталевого диальдегида. Реакционная смесь начинает медленно окрашиваться в ярко-зеленый цвет. Через несколько минут выпадает зеленый осадок.
Реакция на триптофан. Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. Например, с глиоксиловой кислотой (являющейся примесью к концентрированной уксусной кислоте) реакция протекает по уравнению:
По аналогичной схеме протекает и реакция триптофана с формальдегидом.
Реакция Сакагучи. Эта реакция на аминокислоту аргинин основана на взаимодействии аргинина с α-нафтолом в присутствии окислителя. Ее механизм еще полностью не выяснен. По-видимому, реакция осуществляется по следующему уравнению:
Поскольку производные хинониминов (в данном случае нафтохинона), у которых водород иминогруппы –NH– замещен на алкильный или арильный радикал, всегда окрашены в желто-красные тона, то, по-видимому, оранжево-красный цвет раствора при проведении реакции Сакагучи объясняется возникновением именно производного нафтохинонимина. Не исключена, однако, вероятность образования еще более сложного соединения за счет дальнейшего окисления оставшихся NH-групп аргининового остатка и бензольного ядра α-нафтола:
Описание опыта. В пробирку наливают 2 мл 0,01%-го раствора аргинина, затем добавляют 2 мл 10%-го раствора едкого натра и несколько капель 0,2% спиртового раствора α-нафтола. Содержимое пробирки хорошо перемешивают, приливают 0,5 мл раствора гипобромита и вновь перемешивают. Немедленно добавляют 1 мл 40%-го раствора мочевины для стабилизации быстро развивающегося оранжево-красного окрашивания.
Цвет комплекса, получаемый при биуретовой реакции с различными пептидами, несколько отличается и зависит от длины пептидной цепи. Пептиды с длиной цепи от четырех аминокислотных остатков и выше образуют красный комплекс, трипептиды – фиолетовый, а дипептиды – синий.
кетонная форма полипептида
енольная форма полипептида
При взаимодействии полипептида с Cu (OH)2 образуется комплекс, строение которого можно показать так:
Реакция Сакагучи
Реакция Сакагучи — качественная реакция на определение веществ, содержащих гуанидиновых группу, в частности аминокислоту аргинина. Заключается во взаимодействии этих соединений с гипохлоритом или гипобромиты натрия и α-нафтолом (или 8-гидрокси) в щелочной среде с образованием веществ, имеют красную окраску.
Была предложена Сакагучи 1925 для качественного определения аргинина. Для количественного анализа она не использовалась, потому, что красный цвет появлялось очень медленно, и за это время гипохлорит, который использовал Сакагучи, разрушал некоторые из гуанидиновых групп. В 1929 году Вебер предложил использовать гипобромит вместо гипохлорита, при этом окраска развивалось почти мгновенно (в течение 10 с), однако сразу же начинало исчезать и его полностью не становилось за 10 мин. Для того, чтобы предотвратить быстрое выцветание цвета, Вебер добавлял к реакционной смеси мочевину, которая связывает избыток гипобромиду. В таком случае окраска сохраняется в течение 10 мин, в результате чего становится возможным колориметрической (или спектрофотометрических, по поглощению при 500 нм) измерения и определения количества аргинина от 0,05 до 0,005 мг. Поскольку окраски, образующейся в реакции Сакагучи очень чувствительное к температуре, то все реагенты перед ее проведением охлаждают до 0 ° C, а реакцию проводят на ледяной бане.
Некоторые вещества, имеющиеся в гидролизатов белков, такие как аммиак, гистидин, тирозин и триптофан могут препятствовать нормальному прохождению реакции, поэтому было предложено использовать высокие концентрации α-нафтола, что позволяет уменьшить взаимодействие с другими аминокислотами. Однако очень большие концентрации α-нафтола нельзя использовать, потому что он дает желтую окраску с гипобромиты, что может препятствовать колориметрическом измерению. В некоторых модификациях реакции Сакагучи вместо α-нафтола используют 8-гидрокси.
ЦВЕТНЫЕ И ИМЕННЫЕ КАЧЕСТВЕННЫЕ РЕАКЦИИ НА БЕЛКИ
История химии в школьном курсе
РЕАКЦИЯ ПИОТРОВСКОГО (БИУРЕТОВАЯ РЕАКЦИЯ)
В белках аминокислоты связаны друг с другом по типу полипептидов и дикетопиперазинов. Образование полипептидов из аминокислот происходит путем отщепления молекулы воды от аминогруппы одной молекулы аминокислоты и карбоксильной группы другой молекулы:
Образующаяся группа –С(О)–NН– называется пептидной группой, связь С–N, соединяющая остатки млекул аминокислот, – пептидной связью.
При взаимодействии дипептида с новой молекулой аминокислоты получается трипептид и т. д.
Дикетопиперазины образуются при взаимодействии двух молекул аминокислот с отщеплением двух молекул воды:
Дикетопиперазины были выделены из белков Н.Д.Зелинским и В.С.Садиковым в 1923 г.
Наличие в белке повторяющихся пептидных групп подтверждается тем, что белки дают фиолетовое окрашивание при действии небольшого количества раствора медного купороса в присутствии щелочи (биуретовая реакция).
Реакция идет по схеме:
Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Описание опыта. В пробирку наливают 1 мл раствора цистина, прибавляют 0,5 мл 20%-го раствора гидроксида натрия. Смесь нагревают до кипения, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):
Описание опыта. В пробирку наливают 5 капель 1%-го раствора глицина и прибавляют 1 каплю индикатора метилового красного. Раствор окрашивается в желтый цвет (нейтральная среда). К полученной смеси добавляют равный объем 40%-го раствора формальдегида (формалин). Появляется красное окрашивание (кислая среда):
Это реакция на аминокислоту глицин.
В таких солях ион меди координационными связями соединен с аминогруппами.
Описание опыта. В пробирку наливают 3 мл 3%-го раствора сульфата меди(II), добавляют несколько капель 10%-го раствора гидроксида натрия до образования голубого осадка. К полученному осадку гидроксида меди(II) приливают 0,5 мл концентрированного раствора глицина. При этом образуется темно-синий раствор глицината меди:
Описание опыта. В пробирку наливают 1 мл раствора тирозина и добавляют 0,5 мл концентрированной азотной кислоты. Смесь нагревают до появления желтой окраски. После охлаждения добавляют 1–2 мл 20%-го раствора гидроксида натрия до появления оранжевой окраски раствора:
Описание опыта. В пробирку наливают около
0,5 мл раствора уксуснокислого свинца и прибавляют раствор едкого кали до растворения образовавшегося осадка гидроксида свинца. В другую пробирку наливают
Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. Например, с глиоксиловой кислотой (являющейся примесью к концентрированной уксусной кислоте) реакция протекает по уравнению:
По аналогичной схеме протекает и реакция триптофана с формальдегидом.
В ходе проведенного исследования мы выявили по литературным источникам имеющуюся информацию о цветных качественных реакциях на белковые аминокислоты; выполнили ряд перечисленных реакций и составили базу данных. Эта база может быть использована в школьной практике как в теоретическом плане, так и в практическом, т. к. мы приводим краткие, но подробные описания выполнения всех опытов.
Из предложенных 18 качественных реакций каждая практически осуществима в школьном курсе химии и имеет важное практическое значение. Сопровождение реакций химическими уравнениями конкретизирует и углубляет знания по биологической и органической химии, особенно знания учащихся специализированных биологических и химических классов.
Использованная литература
Ермаков А.Н., Арасимович В.В., Смирнова-Иконникова М.И., Мирри И.К. Методы биохимического исследования растений. М.,1952, 520 с.
Полянская А.С., Шевелева А.О. Методическая разработка по лабораторным работам: «Аминокислоты» и «Белки». Л., 1976, 37 с.
Пустовалова Л.М. Практикум по биохимии. 1999, 541 с.
Руководство к практическим занятиям по органической химии. Под ред. В.М.Родионова. М., 1954, 111 с.
Соловьев Н.А. Лабораторные работы по биологической химии. Методическая разработка. СПб., 1996, 70 с.
Филиппович Ю.Б., Егорова Т.А., Севастьянова Г.А. Практикум по общей биохимии. М., 1982, 311 с.
З.Саитов, С.В.Телешов, Б.Харитонцев,
секция «Юный химик» РХО им. Д.И.Менделеева (г. Тобольск)