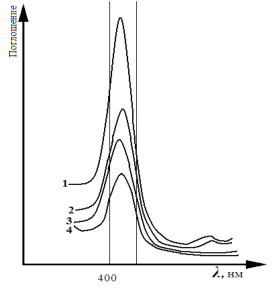
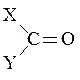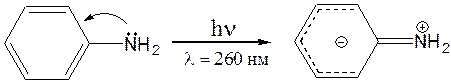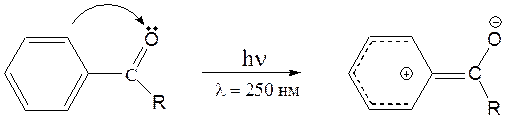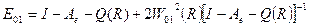Чем обусловлен внутренний перенос заряда и как это отражено в уф спектрах
Влияние строения и среды на УФ-спектры поглощения
На Уф-спектры поглощения многих веществ (хромофоров) оказывает влияние ряд факторов. Проявляться это влияние может изменением интенсивности, формы полос или длины волны, при которой наблюдается поглощения. Наиболее распространенными являются:
· изменение интенсивности полос.
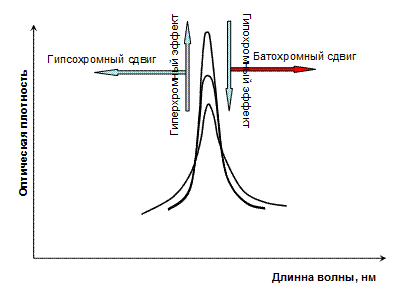
Полосы поглощения для данного хромофора могут смещаться как в сторону больших, так и меньших длин волн. Смещение в сторону меньших длин волн (больших частот и энергий) называется гипсохромных сдвигом или синим смещением. Смещение в сторону больших длин волн (меньших частот и энергий) называется батохромным сдвигом или красным смещением.
Увеличение интенсивности полосы – называется гиперхромным эффектом, уменьшение – гипохромным эффект (см рис. 2.2.1)
Типы смещений полосы поглощения в УФ-спектре
Наиболее чувствительны к различным факторам строения и среды являются n à p* и p à p* переходы. Здесь отчетливо проявляются эффекты сопряжения двойных связей в молекулах, полярность заместителей и среды. Рассмотрим последовательно эти три случая.
Сопряжение проявляется батохромным смещением полос поглощения для n à p* и p à p* переходов.
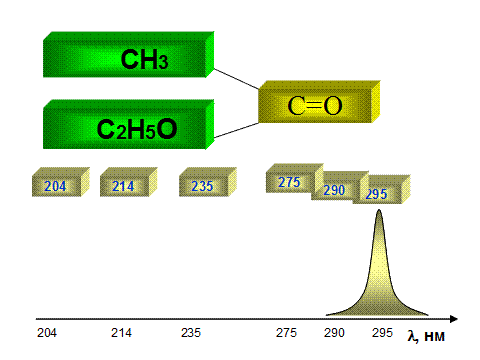
Увеличение полярности заместителя в a-положении такого хромофора как карбонильная группа сопровождается гипсохромным сдвигом n à p* полосы (см рис. 2.2.2).
Синее смещение полосы поглощения (n à p* переход)карбонильной группы в следующем ряду соединений (H-, H-); (H-, CH3-); (CH3-, CH3-); (CH3-, Cl-); (CH3-, NH2-); (CH3-, C2H5O-).
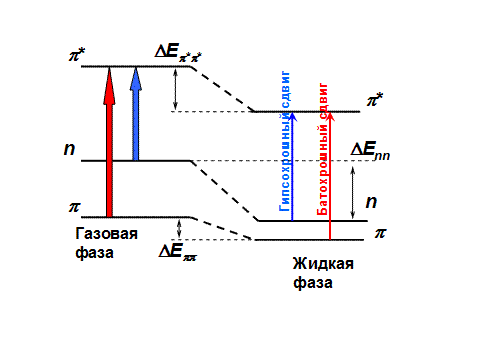
При переходе из газовой фазы в жидкую, или изменении полярности растворителя, энергия основного и возбужденного электронных состояний молекулы изменяется. Это также приводит к гипсо- или батохромным сдвигам полос поглощения для n à p* и p à p* переходов, т.е. оказывают влияние на разность энергий между электронными состояниями(см. рис.2.2.3).
Механизм возникновения гипсо- и батохромных сдвигов в электронных спектрах поглощения под влиянием растворителя.
В общем случае влияние растворителя должно проявляться в понижении средней энергии как основного так и возбужденного состояний. И чем больше полярность растворителя, тем сильнее должны быть такие взаимодействия. Однако для того, чтобы произошел сдвиг частоты поглощения, необходимо изменить относительную энергию двух состояний.
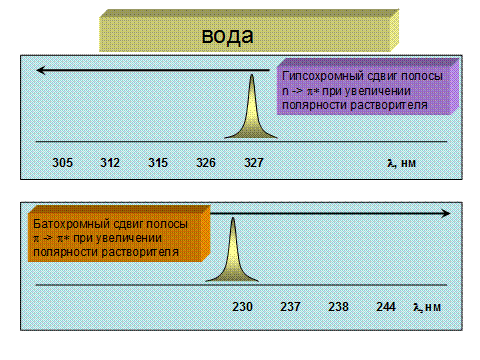
В качестве примера на рис. 2.2.4 приведены данные по влиянию растворителя на n à p* и p à p* переходы в карбонильной группе.
Гипсохромный и батохромный сдвиги для nà p* и p à p* переходов (карбонильная группа) в ряду растворителей: гексан, диэтиловый эфир, этанол, метанол, вода.
электронные спектры поглощения основных классов органических соединений.
Предельные углеводороды. В этих соединениях содержатся только s-связи, поэтому в их молекулах возможны только s à s* переходы. Соответствующие им полосы поглощения лежат в далеком ультрафиолете:

Численные значения этих инкрементов приведены в табл. 2.2.2 и считается, что их величины не зависят от структуры молекулы, в состав которой они входят.
Значения инкрементов некоторых групп для расчета максимума полосы поглощения соединений с сопряженными двойными связями
1. Вещество из класса стеринов, формула:
Карбонилсодержащие соединения. К ним будем относить соединения с общей формулой:
где X, Y –насыщенные фрагменты. При X, Y = H,R –альдегиды и кетоны.
Для них наиболее вероятны следующие переходы:
· n à p*
· n à s*
· p à p*
Карбонильная группа наиболее легко обнаруживается в УФ-спектре по наиболее длинноволновой полосе n à p* перехода. Положение этой полосы, как уже отмечалось выше, очень чувствительно к полярности растворителя и характеру заместителей X, Y. В полярных растворителях (особенно склонных к образованию водородных связей) эта полоса смещается гипсохромно. Замена Н-атома другими заместителями X, Y увеличивает, как правило энергию p* орбитали и практически не влияет на энергию n-орбитали. Поэтому замещение Н на X, Y также приводит к гипсохромному сдвигу (см. табл. 2.2.3).
a, b-Ненасыщенные альдегиды имеют интенсивную (emax » 10 4 ) полосу поглощения lmax » 200 – 230 нм, отвечающую p à p* переходу. Полоса n à p* перехода наблюдается при 230 нм и имеет намного меньшую интенсивность (emax » 100)
Ароматические соединения. В УФ-спектре бензола наблюдается три полосы различной интенсивности (см. табл. 2.2.3)
Полосы поглощения в УФ-спектре бензола
| Максимум полосы, нм | Коэффициент экстинкции, л/моль см |
| 6×10 4 | |
| 8×10 3 | |
| 200 – 300 |
На положение полосы в области 200 – 300 нм значительное влияние оказывают заместители и растворители. Она имеет, как правило, отчетливо выраженную колебательную структуру. На рис. 2.2.6, 2.2.7 и 2.2.8 в качестве примера приведены спектры поглощения бензола, толуола и бензальдегида соответственно.
Электронный спектр поглощения бензола
Электронный спектр поглощения толуола
Электронный спектр поглощения бензальдегида
Все наблюдаемые в бензоле полосы обусловлены p à p * переходами. Конденсация ароматических колец (бензол à нафталин à антрацен à и т.д. приводит к батохромному сдвигу полос поглощения.
Гетероциклические соединения. УФ-спектры поглощения гетероциклических и ароматических соединений очень похожи между собой. Отличие в том, что для гетероциклов помимо p à p * переходов наблюдаются и n à p * полосы. Интенсивность этих переходов невелика.
Конденсация гетероциклов также приводит к батохромному смещению полос поглощения.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Ультрафиолетовая и видимая спектроскопия. УФ-спектры
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Ультрафиолетовая и видимая спектроскопия
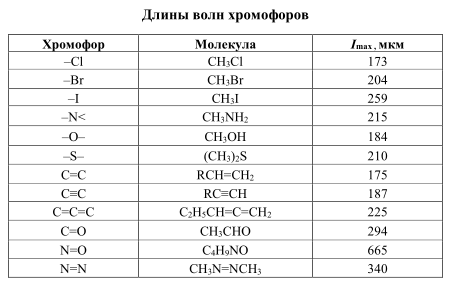
В ультрафиолетовой и видимой спектроскопии исследуются электронные спектры поглощения, связанные с переходом электронов на более высокие энергетические уровни. Наблюдаются спектры органических молекул, содержащие двойные или тройные связи, либо атомы с неподеленными электронными парами (поглощающие группы называются хромофорами) (табл. 6.2). Обнаружение в спектрах таких полос показывает входящие в молекулу группы, что важно для качественного анализа. Количественный анализ основан на измерении коэффициента поглощения света исследуемым раствором на определенных частотах.
Таблица 6.2 Длины волн хромофоров
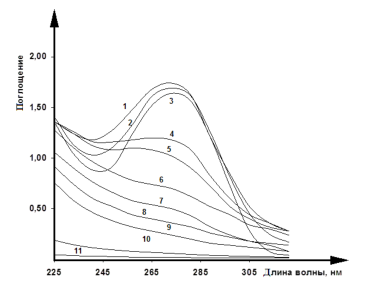
Спектрофотометрия в УФ- и видимом диапазонах широко применяется при анализе веществ, в частности, для определения окрашенных соединений ряда металлов, а также As, P, для установления некоторых функциональных групп органических соединений, например фенолов и соединений с кратными химическими связями (рис. 6.4). Минимальная концентрация, определяемая спектрофотометрическим методом, не ниже 10 –7 М, т. е. чувствительность метода средняя.
Рис. 6.4. УФ-спектры водного раствора тетрациклина, от 200 мг/л (1) до полного отсутствия его в растворе (11)
При необходимости определения двух веществ в смеси без предварительного разделения компонентов метод спектроскопии возможен в ряде случаев. Получение результатов при проведении анализа зависит от расположения спектров поглощения обоих веществ. Рассмотрим возможные случаи.
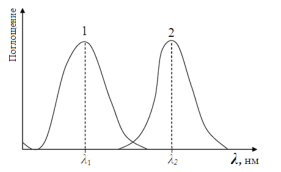
1. Спектры поглощения компонентов не накладываются (рис. 6.5).
Рис. 6.5. Спектры поглощения компонентов не накладываются
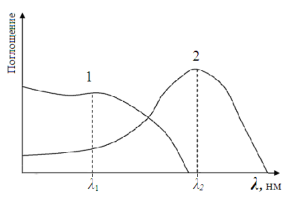
2. Спектры поглощения компонентов частично накладываются (рис. 6.6).
Рис. 6.6. Спектры поглощения компонентов частично накладываются
В этом случае предварительно строят три градуировочных графика для каждого компонента и смеси, затем производят расчеты по закону аддитивности по специальной программе. В случае частичного наложения спектров поглощения компонентов смеси спектрофотометрическое определение каждого компонента возможно, но достаточно трудоемко.
3. Спектры поглощения компонентов накладываются по всей области длин волн (рис. 6.7). В этом случае фотометрическое определение каждого компонента провести невозможно. Используя метод спектроскопии, можно определить состав комбинированных фаршевых изделий в видимом и УФ-диапазонах. Например, для определения компонентов фарша спектр регистрируется в диапазоне 300–500 нм (рис. 6.8).
Рис. 6.7. Спектры поглощения компонентов накладываются во всей области
Характерный максимум поглощения мясных компонентов регистрируется в диапазоне 410–430 нм.
Рис. 6.8. Спектры компонентов фарша и комбинированной котлетной массы 1 — лук репчатый; 2 — рыба (ставрида); 3 — свинина жирная; 4 — говядина II категории; 5 — говядина — ставрида (50 / 50 %)
Из рис. 6.8 следует, что в указанном диапазоне именно для мяса имеет место интенсивное поглощение излучения в выявленном диапазоне контроля. Это явление объясняется наличием в мясе миоглобина.
Полоса поглощения 420 нм известна как переход Соре для спектра поглощения миоглобина. Наличие или отсутствие этой полосы связано со структурными изменениями стереохимии железопорфирина в гемопротеинах. При отщеплении или связывании молекулы О2 вследствие изменений спирали соединения белка, содержащих координирующий остаток гистидина. По-видимому, стереохимия железопорфирина в гемопротеинах рыбы и мяса различны, вследствие чего на спектре поглощения водной вытяжки из рыбы при длине волны 420 нм полоса поглощения отсутствует, а водной вытяжки мяса — присутствует.
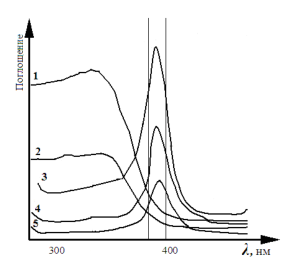
Следовательно, присутствие полосы поглощения свидетельствует о наличии мяса в комбинированном продукте (фарше), а по величине поглощения можно судить о количестве мяса в продукте. Поглощающая способность (высота пика) прямо пропорциональна количеству мяса в образце (рис. 6.9).
Рис. 6.9. Способ определения количества котлетного мяса в комбинированных белковых продуктах в видимом и ультрафиолетовом диапазонах 1 — мясо (100 %); 2 — мясо — рыба (50 / 50 %); 3 — мясо — рыба (25 / 75 %); 4 — мясо — рыба (10 / 90 %)
Такие продукты, как лук, рыба, хлеб в этом диапазоне не дают характерного пика, что облегчает установление факта присутствия в комбинированном продукте мяса. Поглощающая способность раствора тем больше, чем больше процентное содержание мяса в готовом изделии, причем эта зависимость носит линейный характер, что существенно упрощает обработку результатов. Использование данного метода позволяет оперативно и просто, с высокой точностью дать качественную оценку продукта и количественно оценить его состав.
Комплексы с переносом заряда и эксиплексы



Образования комплексов с переносом заряда (КПЗ), эксимеров и эксиплексов приводят к существенным изменениям спектроскопических характеристик молекулярных систем и поэтому могут быть использованы в молекулярной оптической сенсорике. Здесь мы рассмотрим эти эффекты для молекул ароматических углеводородов и их некоторых метильных замещенных. Кратко изложены основные теоретические представления о природе комплексов с переносом заряда эксиплексов и эксимеров.
Начнем с классических представлений о природе КПЗ.
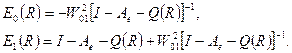
Главный результат теоретического рассмотрения Малликена заключается в установлении связи энергии перехода с переносом заряда и потенциалом ионизации донора электрона и величиной энергии электронного сродства молекулы акцептора электрона. Как следует из (1) энергия перехода равна

Отсюда видно что полоса переноса заряда смещается в длинноволновую область с уменьшением потенциала ионизации донора электрона и
Положение максимума полосы ПЗ (λ) и значение коэффициента
экстинции (ε) комплексов некоторых углеводородов с хлоранилом. В последнем столбце указан потенциал ионизации углеводорода (I).
1 –растворы в четыреххлористом углероде, 2- растворы в циклогексане.
Совокупность экспериментальных данных по спектрам поглощения и
Волновая функция системы в общем случае строится в виде:
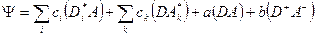
Таблица 4.Средняя частота флуоресценции (ν) измеренная (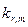
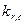
Таблица 5. Средняя частота флуоресценции (ν) измеренная (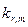
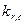
Образование комплексов с переносом заряда и эксиплексов приводит не только к возникновению нового излучения, но и к тушению лминесценции молекул образующих комплекс. Новая люминесценция, тушение люминесценции
Чем обусловлен внутренний перенос заряда и как это отражено в уф спектрах
Техника измерения УФ спектров в осн. такая же, как спектров в видимой области (см. Спектрофотометрия ). Спектральные приборы для УФС отличаются тем, что вместо стеклянных оптич. деталей применяют аналогичные кварцевые (реже флюоритовые или сапфировые), к-рые не поглощают УФ излучение. Для отражения УФ излучения используют алюминиевые покрытия. Приемниками служат обычные или маложелатиновые фотоматериалы, а также фотоэлектрич. приборы, гл. обр. фотоэлектронные умножители, счетчики фотонов, фотодиоды, ионизационные камеры. Для увеличения чувствительности при использовании фотоматериалов иногда регистрируют флуоресценцию, вызванную исследуемым УФ излучением.
Для возбуждения УФ спектров испускания атомов и молекул служат пламя (см. Фотометрия пламени эмиссионная ), дуга постоянного или переменного тока, низко- и высоковольтные искры, ВЧ и СВЧ разряд (в т.ч. безэлектродный), плазмотроны, разряд в полом катоде, лазерное излучение и др. (см. Спектральный анализ ). УФ спектры поглощения и отражения получают в осн. с использованием таких источников излучения, как дейтериевые (водородные), ртутные, ксеноновые и др. газоразрядные лампы. Используют также нагретые до ок. 3000 К твердые тела, напр. разл. вольфрамовые лампы (с ленточным излучателем или со сферич. анодом, разогреваемым дуговым разрядом, и др.). Источниками линейчатых спектров служат спектральные лампы разл. конструкций (напр., с полым катодом). Применяют также лазеры, излучающие в УФ области (водородный лазер).
В УФ области находятся также электронно-колебат. полосы молекул (колебат. структура проявляется только при низких т-рах; в обычных условиях она приводит к диффузным, т. е. размытым, спектрам), что широко используют в хим. анализе и исследованиях. Появление этих полос связано с переходами электронов между связывающими 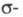
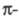
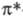
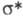
Полосы поглощения сложных эфиров, амидов, галогенан-гидридов смещены в коротковолновую область, а полосы тиокарбонильных соед.- в длинноволновую область по сравнению с полосами поглощения соответствующих карбонильных соед., напр.: максимумы поглощения CH 3 C(O)H, CH 3 C(O)NH 2 и CH 3 C(S)NH 2 наблюдаются при 290, 214 и 358 нм соответственно. Вследствие гибридизации неподеленной пары электронов азота в соед., содержащих группу C = N, интенсивность полосы 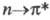
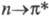
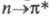
Характер спектра поглощения зависит от взаимного расположения хромофоров. Если хромофорные группы соединены непосредственно, то в спектре наблюдаются сильные изменения по сравнению со спектрами соед. с изолированными хромофорными группами. Относит. расположение хромофоров у кратных связей позволяет различать цис- и транс-изомеры.
Насыщ. гетероциклы имеют полосы, соответствующие 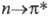
Замена в ароматич. кольце группы =СН на =N приводит к повышению интенсивности длинноволновой полосы поглощения и появлению полосы 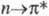
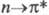
УФС применяют также для изучения кинетики хим. и фотохим. р-ций, исследования люминесценции, уровней энергии и вероятностей квантовых переходов в твердых телах и т. д. Особое значение имеет УФС для установления состава космич. объектов и изучения протекающих на них процессов.