Что значит стабилизация в онкологии
Что значит стабилизация в онкологии
1. Сокращения:
• Критерии оценки ответа солидных опухолей на лечение (RECIST)
2. Определение:
• Новая версия критериев была опубликована в 2009 г.
• Используются модифицированные критерии RECIST
3. Ключевые принципы:
• Критерии включения пациентов:
о Пациенты с наличием измеряемых проявлений заболевания при первичном исследовании
— Наличие как минимум одного измеряемого очага
о Первичной конечной точкой является оценка объективного ответа опухоли на лечение
• Оценка опухоли при первичном исследовании:
о Обнаружение измеряемых проявлений заболевания
о Выбор целевых и нецелевых очагов
о Измерение целевых очагов
о Опухолевая нагрузка: сумма размеров целевых очагов
• Оценка опухоли при повторном исследовании:
о Измерение целевых очагов
о Оценка нецелевых очагов
о Обнаружение новых очагов
о Расчет ответа опухоли на лечение в данной временной точке
4. Существенные различия между RECIST и RECIST 1.1:
• Внесены изменения в определения следующих понятий:
о Опухолевая нагрузка
о Размер лимфатических узлов
о Прогрессирование заболевания
о Прогрессирование неизмеряемых проявлений заболевания о Подтверждение ответа о Новые очаги



б) Лучевая анатомия:
1. Измеряемые и неизмеряемые проявления заболевания:
• Измеряемые проявления:
о Опухоль с наибольшим диаметром (LD) > 10 мм, измеренным при КТ или МРТ в аксиальной плоскости с интервалом реконструкции 5 мм LD должен превышать толщину среза как минимум в два раза
о Опухоль с наибольшим диаметром (LD) >20 мм, измеренным при рентгенографии органов грудной клетки (если очаг имеет четкий контур и окружен воздушной легочной тканью)
— Предпочтительнее проводить КТ
о Опухоль с наибольшим диаметром (LD) > 10 мм, измеренным клинически (по фотографии) электронным штангенциркулем:
— На фотографиях на кожных покровах следует располагать линейку
— Образования, размер которых не удается с точностью определить с помощью штангенциркуля, следует считать неизмеряемыми
о Размер лимфатических узлов по короткой оси при КТ должен составлять > 15 мм (толщина среза 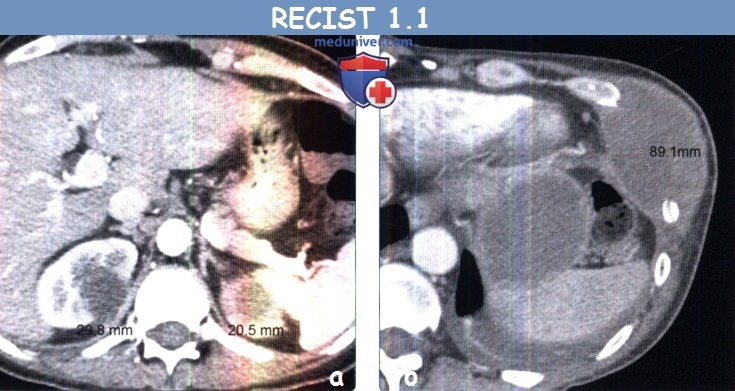
(б) Мужчина 47 лет с метастазами немелкоклеточного рака легкого. При КТ с контрастным усилением в грудной стенке визуализируется метастаз. В соответствии с RECIST 1.1 метастазы в костях считаются целевыми очагами только в том случае, если содержат мягкотканный компонент, отвечающий критериям размера. 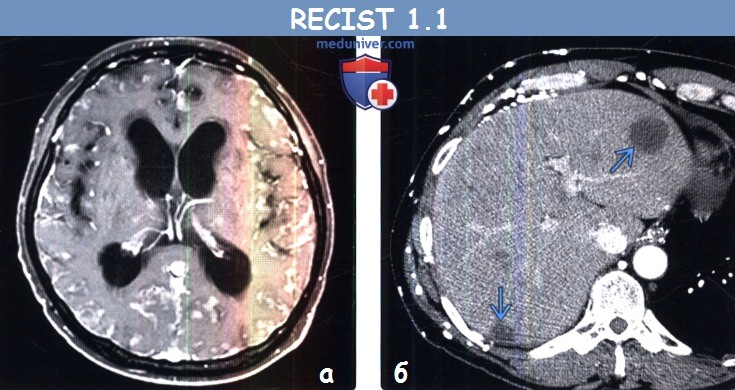
(б) Мужчина 4 7 года с метастазами муцинозной аденокарциномы легкого. При КТ с контрастным усилением в печени визуализируется гиподенсный кистозный метастаз, расцененный как измеряемый очаг. 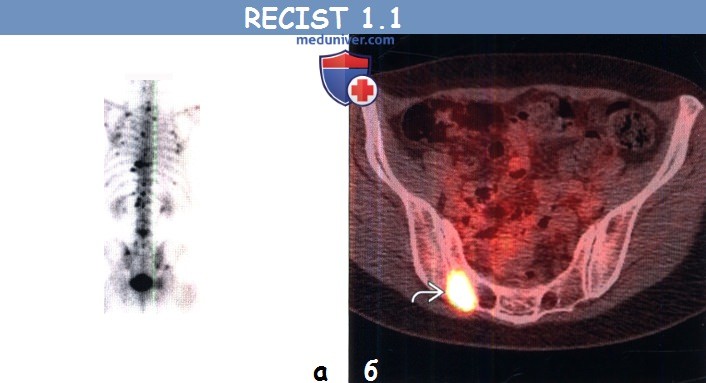
(б) Пациент, страдающий немелкоклеточным раком легкого. При ФДГ-ПЭТ/КТ в правой половине крестца визуализируется очаг с повышенным уровнем поглощения ФДГ. При КТ в данной области патологический участок не выявлен. Остеосцинтиграфия и ПЭТ/КТ могут быть использованы для обнаружения метастазов в костях, но не для их измерения.
1. Ключевые принципы:
• Измерение ранее выбранных целевых очагов (даже если их размер перестал быть наибольшим)
• Оценка всех ранее выбранных нецелевых очагов
• Оценка новых очагов
2. Оценка целевых очагов:
• Расчет SLD:
о Измерение LD каждого целевого очага
о Измерение размера целевых лимфатических узлов по короткой оси
о Если размер образования слишком мал для того, чтобы быть измеренным, считают, что его размер составляет 5 мм (величина по умолчанию)
о Если образование исчезло, считают его размер равным 0
о Распадающиеся или сливающиеся очаги:
— Если целевой очаг распадается на множество меньших по размеру фрагментов, то суммируются LD всех фрагментов
— Если целевые очаги сливаются, то используется LD конгломерата
3. Новые очаги:
• Новые очаги должны быть исключительно опухолевой этиологии:
о Сомнительные очаги, возникновение которых обусловлено разницей в методиках исследования или потенциально неопухолевым процессом, не учитывают
о Не обязательно должны быть измеряемыми
• Сомнительные очаги:
о Оценивают повторно при исследовании в следующей временной точке
о Если наличие очага подтверждается при повторном исследовании, то регистрируется прогрессирование заболевания по дате первого выявления такого очага
• Очаги, обнаруженные за пределами зоны первичного исследования, считают новыми
• Наличие новых очагов, выявленных при УЗИ, следует подтвердить с помощью КТ или МРТ
4. Общий ответ:
• Категории:
о Полный ответ (CR)
о Частичный ответ (PR) о Стабилизация заболевания (SD)
о Оценка невозможна (NE) о Прогрессирование заболевания (PD)
5. ФДГ-ПЭТ и ПЭТ/КТ:
• Критерий «положительного» результата при ПЭТ:
о Уровень поглощения ФДГ образованием в два раза превышает уровень поглощения ФДГ окружающими тканями при выполнении исследования с коррекцией аттенуации сигнала
• Влияние на категории ответа:
о Отрицательный результат при первичной ПЭТ и положительный результат при повторной ПЭТ: прогрессирование заболевания (новый очаг)
о Отсутствие первичной ПЭТ и положительный результат при повторной ПЭТ: прогрессирование заболевания:
— Требует подтверждения наличия очага по данным КТ
При подтверждении наличия очага регистрируется прогрессирование заболевания по дате выполнения первой ПЭТ
о Ключевая особенность:
— При отсутствии первичной ПЭТ и положительном результате повторной ПЭТ наличие выявленного ранее при КТ очага без признаков прогрессии не следует расценивать, как прогрессирование заболевания
6. Ошибочная оценка и случаи, когда оценка невозможна:
• NE: все очаги не могут быть оценены в определенной временной точке:
о Обычно причиной служит потеря данных или низкое качество изображений
о Также данная категория ответа соответствует невозможности оценки некоторой части очагов:
— Исключение: если данные очаги не повлияют на оценку ответа на лечение в определенной временной точке
7. Рецидивирование очагов:
• Влияние рецидивирования очагов зависит от общего ответа:
о Стабилизация заболевания/частичный ответ:
— Образование, подвергшееся обратному развитию, а затем рецидивировавшее, продолжает учитываться
— Категория ответа зависит от состояния других очагов
о Полный ответ
— Рецидивирования образования свидетельствует о прогрессировании заболевания
8. Подтверждение ответа на лечение:
• Частичный ответ/полный ответ:
о Подтверждение необходимо в случае нерандомизированных клинических исследований, в которых эффективность лечения является первичной конечной точкой
о В случае стабилизации заболевания в первой промежуточной точке допускается последующее подтверждение частичного ответа
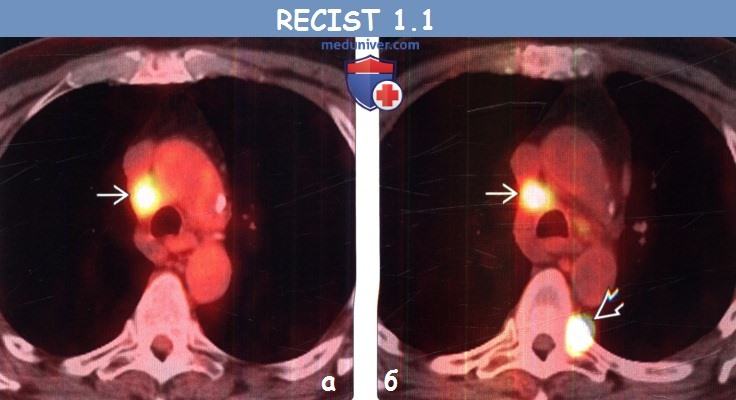
(б) У этого же пациента после курса химиотерапии при ФДГ-ПЭТ/КТ уровень поглощения ФДГ правым паратрахеальным лимфатическим узлом остался без изменений, однако в грудном позвонке возник новый интенсивно накапливающий ФДГ метастаз, что соответствует прогрессированию заболевания. 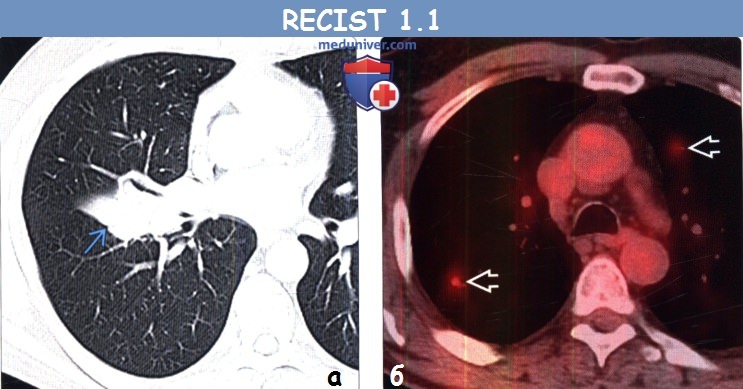
(б) У этого же пациента после курса химиотерапии при ФДГ-ПЭТ/КТ в легких визуализируются новые интенсивно поглощающие ФДГ узелки, соответствующие метастазам. Поскольку данные метастазы при первичной КТ не выявлялись, а при последующей КТ их наличие было подтверждено, то картина соответствует прогрессированию заболевания. 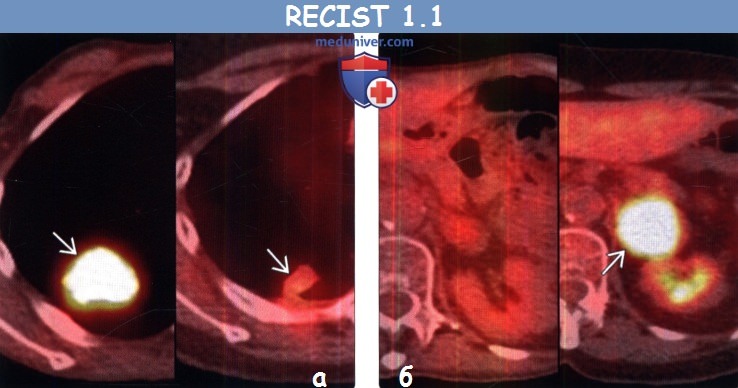
(б) У этого же пациента на совмещенных изображениях при первичной ФДГ-ПЭТ/КТ (слева) и после курса химиотерапии (справа) визуализируется возникновение интенсивно поглощающего ФДГ метастаза в левом надпочечнике, что соответствует прогрессированию заболевания.
в) Список литературы:
1. Litiere S et al: The components of progression as explanatory variables for overall survival in the Response Evaluation Criteria in Solid Tumours 1.1 database. Eur J Cancer. 50(10)4847-53, 2014
2. Nishino M et al: Revised RECIST guideline version 1,1: What oncologists want to know and what radiologists need to know. AJR Am J Roentgenol. 195(2):281-9, 2010
3. van Persijn van Meerten EL et al: RECIST revised: implications for the radiologist. A review article on the modified RECIST guideline. Eur Radiol. 20(6)4 456-67, 2010
4. Eisenhauer EA et al: New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1). Eur J Cancer, 45(2):228-47, 2009
5. Eisenhauer EA et al: Response assessment in solid tumours (RECIST) and supporting papers (version 14). Eur J. Cancer. 45(2):225-310, 2009
Редактор: Искандер Милевски. Дата публикации: 24.2.2019
Как организовать жизнь после рака
Ремиссия при онкологических заболеваниях – это состояние, при котором все симптомы патологии пропадают и дальнейшее развитие опухоли не происходит.
Обычно под выздоровлением понимают пятилетнюю выживаемость после рака. При этом, у человека в течение пяти лет не должно появиться никаких симптомов опухоли, а также она не должна определяться на диагностических исследованиях. Такое состояние называют устойчивой ремиссией. По сути, тут врачи слегка перестраховываются и редко используют термин «выздоровление». Ведь гарантировать уничтожение всех без исключения раковых клеток в организме пока, увы, невозможно. Однако ремиссия на протяжении пяти и более лет – достаточно надежное тому подтверждение.
Каждый пациент должен четко знать, что возвращение к нормальной и полноценной жизни после рака возможно и даже необходимо. Но для этого ему потребуется несколько скорректировать привычки и крайне внимательно следить за состоянием здоровья.
Страхи выздоровевших пациентов
Разумеется, это, прежде всего, опасение, что болезнь вернется, страх рецидива после рака. Побороть его поможет четкое соблюдение рекомендаций врача, нужной диеты и распорядка дня. Однако если страх нарастает, приводя к развитию навязчивой тревожности и фобии – это уже серьезная проблема. Она может провоцировать ненужные самоограничения, создавать трудности во взаимоотношениях с окружающими и т.д. Решить эту проблему поможет обращение к профессиональному психологу.
Возвращение к нормальному образу жизни
Появятся ли у пациента, перенесшего онкозаболевание, какие-либо ограничения? Вполне возможно. Например, современное лечение рака нередко предполагает использование масштабных хирургических вмешательств. В зависимости от того, какой именно орган или его часть были удалены, может понадобиться определенная коррекция образа жизни человека, а также специальные уходовые процедуры.
Универсальные советы врачей
Вне зависимости от типа злокачественной патологии основой успешной реабилитации после рака специалисты считают:
Физические нагрузки
Опухолевые заболевания практически всегда сопровождаются синдромом повышенной усталости. Эффекты, связанные с плохим общим самочувствием, могут преследовать пациента еще некоторое время после завершения лечебного курса. И избавиться от таких проблем можно как раз с помощью физических упражнений.
Разумеется, вся активность должна быть строго дозирована, а увеличивать или корректировать ее должен специалист по лечебной физкультуре. Кроме того, очень важно, чтобы пациент имел достаточное время не только для труда, тренировок и бытовых забот, но и для полноценного отдыха. Данные многочисленных исследований доказывают, что те пациенты, которые проходят индивидуальные тренировочные программы и регулярно подвергают свой организм адекватным физическим нагрузкам, намного скорее возвращаются к полноценному образу жизни.
Благодаря правильно дозированной активности можно:
Питание
И во время, и после лечения пациенты должны уделять особенное внимание тому, какие продукты входят в их ежедневный рацион. При этом необходимо помнить, что применяемые в онкологии фармакологические препараты могут в значительной степени влиять на изменение вкусовых ощущений. Кроме того, одним из распространенных побочных эффектов этих лекарственных средств служит снижение аппетита, а также появление тошноты.
Однако подобные нарушения носят временный характер и после окончания курса лечения будут постепенно ослабевать вплоть до полного исчезновения. Но, пока они не пропали, лучше стараться разбить приемы пищи на несколько небольших порций, а для выбора блюд обратиться к профессиональному диетологу. Он поможет составить сбалансированный рацион, со всеми необходимыми для правильного обмена веществ элементами. И при этом учитываются индивидуальные особенности пациента, в том числе сложность перенесенного заболевания.
Вредные привычки
Конечно же, человеку необходимо избавиться от привычек, наносящих вред его здоровью, таких как употребление спиртных напитков и табакокурение. Они повышают риск развития рецидивов, усиливают побочные эффекты фармакологической терапии и значительно удлиняют период восстановления после онкологии.
Психологическая поддержка
Нередко всплеск эйфории и радости после победы над злокачественным заболеванием со временем переходит в некое разочарование, человек с трудом находит себе занятие, ему все кажется малозначимым. Таким пациентам потребуется, в первую очередь, помощь родных и близких, которые заново покажут ему ценность отношений, красоты мира и вызовут интерес к жизни. Иногда в таких случаях будет полезно и вмешательство психолога.
Профилактические скрининги
Важнейшее значение в жизни после рака имеют меры, направленные на предотвращение повторного развития заболевания. Ведущую роль играет регулярное посещение консультаций специалиста и прохождение медицинских обследований, согласно разработанному лечащим врачом графику.
Не меньшей значимостью обладают также и самостоятельные осмотры доступных частей тела: кожных покровов, слизистых оболочек, мягких тканей (например, молочной железы). К сожалению, уже случившийся эпизод онкологического заболевания означает, что вероятность появления другой злокачественной патологии у данного человека повышена. Теперь он автоматически относится к группе риска.
Соблюдение всех врачебных рекомендаций, здоровый образ жизни, сбалансированная диета и адекватные физические нагрузки помогут справиться со всеми последствиями раковой опухоли и в кратчайшие сроки вернуться к полноценной жизни.
Материал подготовлен по согласованию с врачом «Анадолу» медицинским онкологом Синаном Караасланом.
Поддерживающая терапия и ее значение в современной онкологии
Об эффективности лечения злокачественных новообразований и улучшении качества жизни онкологических больных трудно говорить в ситуации, когда противоопухолевая терапия проводится препаратами, вызывающими тяжелые побочные эффекты. Поэтому тема поддерживающей терапии онкологических больных выходит на первый план.
История вопроса
Термин «поддерживающая терапия» был предложен Международной ассоциацией по поддерживающей терапии в онкологии в 2008 г. А уже в 2009 г. в России состоялся первый семинар по этой теме. В этом году можно отметить десятилетие внедрения этого направления в нашей стране.
Чуть больше десяти лет назад на нашем рынке появились биосимиляры – препараты, позволяющие корректировать побочные эффекты химиотерапии. В частности филграстим, который применяется против одного из самых тяжелых побочных эффектов – фебрильной нейтропении.
Когда в 80–90-х гг. прошлого века химиотерапия стала основным методом противоопухолевого лечения, многие пациенты вообще отказывались от ее проведения самыми современными на тот момент препаратами, так как не могли перенести невыносимые тошноту и рвоту. Кратность тошноты и рвоты могла доходить до 30–40 раз в день. Пациент, который испытывал такие ощущения, на второй-третий раз отказывался от курса химиотерапии. Поэтому у медиков и зародилась идея создавать не только препараты для терапии онкологических заболеваний, но и лекарства и методики для облегчения осложнений, рассказывает один из основоположников направления поддерживающей терапии профессор А.В. Снеговой.
Осложнения повышают риск смертности. И если вероятность летального исхода от тошноты у пациента минимальная, то от инфекционных осложнений – большая. Поэтому одним из факторов необходимости применять поддерживающую терапию является возможность профилактики фебрильной нейтропении с помощью специализированных препаратов, которые восстанавливают функцию костного мозга после лекарственного противоопухолевого лечения и таким образом защищают пациента от инфекционных осложнений.
В конце 80-х и начале 90-х гг. впервые было показано, что те пациенты с диагнозом «рак поджелудочной железы», которые получали вместе с химиотерапией еще и поддерживающую терапию, продемонстрировали значительно лучшие показатели общей выживаемости.
Концепция качества жизни
Концепция качества жизни во время заболевания – того, что пациент не должен испытывать страданий во время лечения, – пришла в Россию в 90-е гг. Ее активно развивали наши врачи в Санкт-Петербурге под руководством профессора А.А. Новика. Они дали определение понятию «качество жизни», разработали методологию исследования этого понятия, основные направления применения этого определения в медицине. Теперь онкологических пациентов распределяют по группам в зависимости от их диагноза и состояния и определяют степень необходимой им помощи, рассказывает д.м.н. Л.М. Когония.
Начиная с 90-х гг. врачи ставят качество жизни пациентов по важности на второе место после показателей общей выживаемости при любой лекарственной терапии, и противоопухолевой в том числе. Такого принципа придерживается ВОЗ. А сегодня можно не только бороться с осложнениями противоопухолевого лечения, но и предотвращать их развитие. Использование препаратов поддерживающей терапии позволяет значительно ускорить восстановление иммунной защиты после проведения химиотерапии. И растущая доступность этих препаратов позволяет обеспечить ими все большее число нуждающихся.
Фебрильная нейтропения, которая развивается после химиотерапии, может вызвать у пациента септическое состояние и угрожать его жизни. Поэтому назначение препаратов гранулоцитарного колониестимулирующего фактора (Г-КСФ) – средств лечения иммунных осложнений и идиопатической нейтропении – крайне важно. Дополнительная поддерживающая терапия должна назначаться всем пациентам, которые получают противоопухолевое лечение, и прямо с момента постановки диагноза, считает профессор А.В. Снеговой. Объем и варианты поддерживающего лечения будут отличаться у разных пациентов. Но с помощью сопроводительного лечения онкологи должны не только бороться с возникшими осложнениями, но и профилактировать их. На заре развития противоопухолевого лечения многие пациенты погибали от инфекционных осложнений. И тогда европейские врачи, которые были первопроходцами этого направления медицины, поняли: для того чтобы улучшить результаты лечения, недостаточно создать новые мощные препараты, надо еще создать методологию, чтобы пациент смог перенести это мощное лечение.
Можно ли поставить знак равенства?
Можно ли поставить знак равенства между поддерживающей терапией и паллиативной помощью? Этот вопрос часто возникает у пациентов. И врач должен объяснить больному разницу.

Задача паллиативной помощи иная: улучшить качество оставшейся жизни, когда противоопухолевое лечение уже не помогает. И здесь самое важное – борьба с хроническим болевым синдромом.
Паллиативная помощь предназначена пациентам с четвертой стадией заболевания. Ее основная цель – облегчить симптомы. Вылечить пациента уже нельзя, так как болезнь достигла слишком больших размеров. Но если врачи не могут вылечить пациента, это не значит, что они не могут ему помочь.
В приказе Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. № 915н «Об утверждении Порядка оказания медицинской помощи населению по профилю „онкология“» (редакция от 04.07.2017) есть раздел «паллиативная медицинская помощь», где дается определение этому понятию. Вычленение понятия «паллиативная медицинская помощь в клинической онкологии» позволяет начать подготовку кадров этого профиля. Онколог не в состоянии решать все вопросы, касающиеся и методов лечения, и поддерживающей терапии, и паллиативной помощи. Теперь паллиативной помощью будут заниматься отдельные специалисты.
В России у истоков этой области медицины стоит заведующий кафедрой паллиативной медицины МГМСУ им. А.И. Евдокимова профессор Г.А. Новиков. Он разрабатывает паллиативную помощь на протяжении последних 30 лет, и благодаря его усилиям и работе его кафедры был принят этот закон. Первая в России кафедра паллиативной медицины была организована в 2013 г., а к марту 2018 г. ее сотрудниками было подготовлено около 2000 специалистов этого профиля. Но если поддерживающая терапия уже присутствует в клинических рекомендациях на протяжении шести лет, то рекомендации по паллиативной помощи еще только предстоит разработать.
Положение дел в Москве
Как поддерживающая терапия применяется сейчас в Москве, рассказала профессор Л.Г. Жукова.
За последние несколько лет закупка препаратов Г-КСФ для поддерживающей или, как ее еще называют, сопроводительной терапии увеличилась в полтора раза. После консультации в крупном онкологическом учреждении пациент получает рекомендации не только по тактике лечения, схеме химиотерапии, но и рекомендации по поддерживающей терапии.
У онкологов на местах есть возможность проводить коррекцию осложнений, которые возникают у пациентов. Изменилась и сама процедура применения препаратов, что позволило избавить пациентов от ежедневных визитов в клинику для их введения.
При поддержке Департамента здравоохранения г. Москвы недавно было достигнуто предварительное соглашение с Фондом обязательного медицинского страхования города Москвы о введении нового тарифа ОМС по коррекции осложнений после фебрильной нейтропении. Это очень важное достижение, поскольку пациенты, у которых развивается фебрильная нейтропения, к сожалению, оказываются самыми незащищенными. Теперь появится возможность оказывать этим пациентам качественную и своевременную помощь в рамках ОМС.
Улучшается маршрутизация больных с развившимися осложнениями. Это позволяет экстренно оказывать им неотложную помощь в случае возникновения серьезных осложнений при проведении лечения.
«Достигнуто предварительное соглашение с Фондом обязательного медицинского страхования города Москвы о введении нового тарифа ОМС по коррекции осложнений после фебрильной нейтропении».
Большое внимание уделяется и просветительской работе: пациентов обучают обращать внимание на ранние тревожные симптомы, свидетельствующие о развитии тяжелых осложнений. И инструктируют, как действовать в случае возникновения этих осложнений. Эта работа крайне важна, потому что в профилактике осложнений пациент является полноценным членом команды, которая борется за его жизнь и здоровье. Немотивированный и неподготовленный пациент может пропустить тревожные симптомы. А именно благодаря поддерживающей терапии удается «отвязать» многих пациентов от больничной койки и позволить им вести полноценную жизнь.
Возможности регионов
Но одно дело столица с ее возможностями, другое дело – регионы. Знают ли там, что такое поддерживающая терапия, и применяют ли ее? С этого года на лекарственное обеспечение онкологических пациентов государство выделило практически в два раза больше денег по сравнению с прошлым годом. Врачи имеют возможность назначать поддерживающую терапию, главное не забывать это делать.
Конечно, регионы различаются по своим возможностям. Когда в 2008–2009 гг. направление поддерживающей терапии только начинало развиваться, разница в возможностях между регионами и Москвой была колоссальной. Если в столице онкологи знали о поддерживающей терапии, то в провинции знания врачей о том, как проводить профилактику тех или иных осложнений, были практически нулевые. Но сегодня ситуация изменилась кардинально, были предприняты большие усилия по образованию врачей. Сегодня онколог может посмотреть рекомендации, что можно сделать для пациента, чтобы провести адекватную поддерживающую терапию или профилактику либо скорректировать осложнение. Все информационные возможности у регионов есть. Современные методики уже применяют врачи Санкт-Петербурга, Северо-Западного региона, ЦФО, Томска, Тюмени.
Что касается соответствия международному уровню, то те технологии и препараты, которые применяются в развитых странах, зарегистрированы и в России, говорит профессор А.В. Снеговой. И мы можем ими пользоваться. Сейчас мы являемся равноправными партнерами наших итальянских и французских коллег, у нас есть какие-то разработки, интересные для них, у них – интересные для нас. Флагмана выделить невозможно. Российская концепция поддерживающей терапии принята международным сообществом. Наша концепция – это не просто заимствованный опыт североамериканских и европейских онкологов. У нас свой большой опыт, мы одни из первых получили положительные результаты этого вида лечения. У нас есть очень интересные популяционные исследования, которых нет у зарубежных онкологов, но мы активно обмениваемся опытом и работаем вместе, то есть являемся равноправными партнерами.



