Что значит резистентность организма человека
Что такое резистентность?
Резистентность — сопротивляемость (устойчивость, невосприимчивость) организма к воздействию различных факторов — инфекций, ядов, загрязнений, паразитов, и т.п. В частности, «неспецифической резистентностью» называют средства врождённого иммунитета.
Термин чаще применяется в отношении микроорганизмов (возникновение механизмов невосприимчивости к антимикробным лекарственным средствам, к антибиотикам); или растений (к болезням).
В отношении человека и животных чаще используется термин иммунитет.
Резистентность организма не является постоянной величиной, а зависит от экологических условий, ослабевая при сильном переохлаждении, недостаточном питании, физическом переутомлении. У млекопитающих, впадающих в спячку, во время её отмечена высокая сопротивляемость воздействию инфекций и токсинов; так, даже столь острая инфекция, как чума, у пребывающих в спячке сусликов и сурков принимает латентную форму.
ВВ микробиологии
Примером первого способа является синтез бактериями бета-лактамаз, разлагающих антибиотики семейства пенициллинов и других бета-лактамных антибиотиков.
Вторым способом защищается от лекарств метициллин-резистентный золотистый стафилококк, опаснейшая внутрибольничная инфекция. У такого стафилококка изменяется структура белка PBP2a, с которым связываются антибиотики пенициллинового ряда. Стафилококк с изменённой структурой белка становится β-лактам-резистентным, т.е. устойчивым к воздействию бета-лактамных антибиотиков.
Резистентность тесно связана с реактивностью организма, представляя собой одно из основных ее следствий и выражений. Различают неспецифическую и специфическую резистентность. Под неспецифической резистентностью понимают способность организма противостоять воздействию разнообразных по своей природе факторов. Специфическая резистентность характеризует высокую степень противодействия организма воздействию определенных факторов или их близких групп.
Резистентность организма может определять относительно стабильными свойствами различных органов, тканей и физиологических систем, в т.ч. не связанными с активными реакциями на данное воздействие. К ним относят, например, барьерные физико-химические свойства кожи, препятствующие проникновению через нее микроорганизмов.
Подкожная клетчатка обладает высокими теплоизоляционными свойствами, костная ткань отличается большой устойчивостью к механическим нагрузкам и т.д. Подобные механизмы резистентности включают и такие свойства, как отсутствие рецепторов, обладающих сродством к патогенному агенту (например, токсину) или недоразвитость механизмов, необходимых для реализации соответствующего патологического процесса (например, аллергических реакций).
В других случаях формирования Р.о. решающее значение имеют активные защитно-приспособитсльные реакции, направленные на сохранение гомеостаза при потенциально вредных воздействиях факторов внешней среды или неблагоприятных сдвигах во внутренней среде организма. Эффективность таких реакций и, следовательно, степень резистентности к различным факторам зависит от врожденных и приобретенных индивидуальных особенностей организма.
Так, у некоторых лиц в течение всей жизни отмечается высокая (или, напротив, низкая) резистентность к различным инфекционным болезням, охлаждению, перегреванию, действию определенных химических веществ, ядов, токсинов.
Значительные колебания индивидуальной резистентности могут быть связаны с особенностями реактивности организма во время его взаимодействия с повреждающим агентом. Резистентность может понижаться при недостатке, избытке или качественной неадекватности биологически значимых факторов (питания, двигательной активности, трудовой деятельности, информационной нагрузки и стрессовых ситуаций, различных интоксикаций, экологических факторов и др.). Наибольшей резистентностью организм обладает в оптимальных биолого-социальных условиях существования.
Резистентность изменяется в процессе онтогенеза, причем ее возрастная динамика по отношению к различным воздействиям неодинакова, однако в целом она оказывается наиболее высокой в зрелом возрасте и снижается по мере старения организма. Некоторые особенности резистентности связаны с полом.
Значительное повышение как неспецифической, так и специфической резистентности может быть достигнуто посредством адаптации к различным воздействиям: физическим нагрузкам, холоду, гипоксии, психогенным факторам и др. При этом адаптация и высокая резистентность по отношению к какому-либо воздействию может сопровождаться повышением резистентности и к другим факторам. Иногда могут возникать и противоположные отношения, когда повышение устойчивости к одной категории воздействий сопровождается снижением ее к другим.
Особое место занимает высокоспецифичная мобилизация защитно-приспособительных свойств организма при воздействиях на иммунную систему. В целом реализация механизмов Р.о. обеспечивается, как правило, не одним каким-либо органом или системой, а взаимодействием комплекса различных органов и физиологических систем, включая все звенья регуляторных процессов.
Состояние и особенности Р. о. могут быть в известной степени определены методом функциональных проб и нагрузок, используемых, в частности, при профессиональном отборе и в медицинской практике.
( Сиротинин И.Н. Эволюция резистентности и реактивности организма)
РЕЗИСТЕНТНОСТЬ ОРГАНИЗМА
РЕЗИСТЕНТНОСТЬ ОРГАНИЗМА (лат. resistentia сопротивление, противодействие) устойчивость организма к воздействию различных повреждающих факторов.
Организм человека и животных в процессе филогенеза приобрел морфо-функциональные свойства, обеспечивающие его существование в условиях непрерывного взаимодействия со средой, многие факторы к-рой (физические, химические, биологические) могли бы вызвать нарушение жизнедеятельности, повреждение и даже гибель организма при недостаточной его устойчивости — недоразвитии или ослаблении защитных механизмов и приспособительных реакций.
Резистентность организма тесно связана с его реактивностью (см. Реактивность организма). Способность организма противостоять повреждающим воздействиям в конечном итоге определяется его реакцией как единого целого на эти воздействия. Резистентность организма, таким образом, представляет собой одно из основных следствий и выражений его реактивности.
Понятие «резистентность организма» охватывает широкий круг явлений. В ряде случаев она зависит от свойств различных органов и систем, не связанных с активными реакциями на воздействия. Напр., барьерные свойства многих структур, препятствующие проникновению через них микроорганизмов, чужеродных веществ и др., в значительной мере обусловлены их физическими особенностями: подкожная клетчатка обладает хорошими теплоизоляционными свойствами; кости, сухожилия и другие ткани опорно-двигательного аппарата отличаются большой устойчивостью к механическим нагрузкам; череп имеет большое значение в защите головного мозга от повреждения и т. д.
Помимо таких, относительно пассивных, механизмов Р. о., исключительно большое значение имеют приспособительные реакции (см.Приспособление), направленные на сохранение гомеостаза (см.) при вредоносных воздействиях окружающей среды или при изменениях, наступающих в самом организме. Эти реакции, лежащие в основе Р. о., могут быть каждая в отдельности свойственны определенному биол. виду (видовая Р. о.). Так, различные виды млекопитающих обладают неодинаковой устойчивостью к ядам (морфину, гистамину и др.), инфекционным агентам, охлаждению. Высокая видовая Р. о. может быть связана либо с особой мощностью защитных систем (напр., высокая устойчивость к бактериальному фактору у крыс), либо отсутствием специализированных рецепторов, либо недоразвитостью механизмов, необходимых для реализации соответствующего патол. процесса (напр., слабая выраженность аллергических реакций у рыб и амфибий).
Р. о. к различным факторам может зависеть от врожденных индивидуальных особенностей. Известно, что даже при эпидемиях, вызванных весьма вирулентными микроорганизмами (чума, холера и др.), заболевают не все люди, находившиеся в тесном контакте с больными, а у заболевших процесс протекает не одинаково. Нек-рые лица резистентны к кинетозам и не поддаются укачиванию; различна врожденная устойчивость к охлаждению, перегреванию, действию различных хим. веществ (лекарственных средств, ядов, токсинов) и к воздействию ионизирующего излучения.
Большие колебания индивидуальной Р. о. связаны не только с врожденными факторами, но и с особенностями Р. о. в момент его взаимодействия с повреждающим агентом. При этом многочисленные факторы, изменяющие индивидуальную реактивность, могут повышать или понижать Р. о. к тому или иному воздействию. Известны колебания Р. о. в зависимости от времени года, в течение суток. На Р. о. существенное влияние оказывают факторы окружающей среды. Наибольшей резистентностью организм обладает при адекватном его взаимоотношении с окружающей средой. Как недостаточные, так и избыточные влияния биологически значимых факторов окружающей среды понижают резистентность. Напр., голодание значительно ослабляет Р. о., способствуя повышению заболеваемости инфекционными и различными соматическими болезнями. Избыточное питание также способствует понижению Р. о. к факторам, вызывающим нарушения обмена веществ, функций эндокринных желез, системы кровообращения и др. В наст, время большое значение приобретает гипокинезия (см.), к-рая существенно понижает Р. о. Однако и перетренировка, напр, у спортсменов, также понижает Р. о. Правильно организованный общественно полезный труд, чередующийся с отдыхом, нормальные семейные и бытовые условия являются важными предпосылками нормального течения психических и физиол. процессов и способствуют повышению общей Р. о. В то же время отсутствие положительной мотивации трудовой деятельности, постоянная профессиональная перегрузка, нарушение биоритмов и другие факторы, способствующие нервно-психической травматизации, снижают Р. о. и предрасполагают к различным заболеваниям. В этом же направлении изменяется Р. о. под влиянием таких социально опосредованных вредных факторов, как алкоголизм, курение, наркомания и др.
Р. о. изменяется в процессе онтогенеза. Новорожденные, получившие от матери запас антител, нек-рое время оказываются высокорезистентными к ряду инф. болезней. Наряду с этим вследствие незрелости систем адаптации они отличаются повышенной чувствительностью к изменениям окружающей среды (охлаждению, перегреванию), к недоеданию, водному голоданию и др. В дальнейшем повышается чувствительность к определенным инф. факторам (детские инфекции). Юношескому возрасту свойственна неустойчивость нейроэндокринной системы, а при акселерации, характерной для промышленно развитых стран, нередко наблюдается дополнительное ослабление Р. о., что способствует возникновению ряда нервных и соматических заболеваний. В зрелом возрасте Р. о. наиболее высокая. В пожилом и старческом возрасте в связи с развитием атеросклероза, нарушений кровообращения, понижением функции эндокринных желез, атрофией тканей и другими процессами, приводящими к ограничению функциональных и структурных резервов организма, общая Р. о. понижается. Однако лица пожилого возраста могут оказаться более резистентными к действию факторов, осуществляющих свое патогенное действие через гиперреакции (аллергия и др.), т. к. способность к таким реакциям с возрастом ослабевает. В пожилом возрасте понижается обмен веществ, что может способствовать повышению Р. о. к пищевому и водному голоданию.
Нек-рые особенности Р. о. связаны с полом. Так, женщины отличаются большей резистентностью к гипоксии, кровопотере, травмам. У них реже наблюдается гиперхолестеринемия и позднее развивается атеросклероз. Биоритмы у женщин, связанные с менструальным циклом, существенно изменяют Р. о., поэтому в нек-рые периоды этого цикла женщины особенно чувствительны к психическим, инфекционным и другим факторам.
Различают неспецифическую и специфическую Р. о. Специфическая резистентность характеризует высокую переносимость только определенных факторов среды, как это наблюдается у людей, перенесших нек-рые инфекции (корь, оспа и др.), или специально иммунизированных вакцинами (Иммунитет, Инфекция). Повышенная резистентность к определенным факторам среды формируется в процессе адаптации (см.), напр, к условиям высокогорья, низким температурам, повышенным физическим нагрузкам и др. При этом адаптация и высокая Р. о. по отношению к какому-либо воздействию может сопровождаться повышением Р. о. и к другим факторам (напр., к физическим нагрузкам и к гипоксии). Возможно, однако, что успешная защита против одной категории воздействий сопровождается снижением Р. о. к другим; напр., при адаптации к мышечным нагрузкам может понижаться устойчивость организма к нек-рым инфекциям и ядам. Механизмы специфической резистентности к микробам и вирусам определяются в основном напряженностью гуморального и клеточного иммунитета (см.).
Под неспецифической Р. о. обычно понимают устойчивость к действию многих разнообразных по своей природе факторов, в т. ч. носящих экстремальный характер. Весьма высокая Р. о. такого рода характеризует, напр., космонавтов, летчиков, водолазов и представителей других специальностей, связанных с большими и подчас непредсказуемыми нагрузками.
Механизмы неспецифической резистентности пока не получили достаточно полного объяснения. Имеются в разной степени обоснованные гипотезы о роли нек-рых органов и систем в неспецифической резистентности. А. А. Богомолец, а позднее Г. Селье обратили внимание на значение в Р. о. коркового вещества надпочечников. Его гормоны (глюко-и минералокортикоиды) играют большую и разностороннюю роль в адаптации организма к действию на него многих повреждающих факторов среды. У эпинефрэктомированных животных, как и у людей с недостаточностью коркового вещества надпочечников, неспецифическая Р. о. оказывается пониженной, что связано гл. обр. с недостатком глюкокортикоидов, потребность в к-рых в условиях стресса (см.) значительно возрастает. При анализе Р. о. отчетливо выступает интегрирующая роль различных отделов ц. н. с. Л.А.Орбели привел убедительные доказательства адаптационно-трофической роли симпатического отдела нервной системы, А. Д. Сперанский показал участие различных нервных механизмов в формировании Р. о. к ядам, токсинам, травмам, а также роль нервной системы в развитии дистрофических процессов. Конкретные механизмы нервного контроля Р. о. во многих случаях недостаточно ясны. Однако несомненно, что ответ на действие повреждающего фактора независимо от уровня его непосредственной реализации формируется как реакция целостной системы, осуществляющей свое влияние на органы и ткани через эфферентные нервы и опосредованно, через эндокринные железы. Большую роль играют и физиологически активные вещества, образующиеся в процессе метаболизма при реакции напряжения и при повреждении тканей. Р. о. обеспечивается не каким-либо специальным органом или одной системой, а целенаправленным взаимодействием различных органов и физиологических систем. При этом большое значение имеет адекватность регуляции и состояние исполнительных систем (кровообращения, дыхания, выделения, крови и др.)* Система клеточного иммунитета, в к-рой большую роль играют Т- и В-лимфоциты (см. Иммунокомпетентные клетки), а также макрофаги (см.), имеет существенное значение не только в борьбе с инфекцией, но и в поддержании общей Р. о. В частности, выявлено, что соматические мутации, вызываемые онкогенными веществами (см.), при нормальном клеточном иммунитете часто не приводят к образованию опухолевого зачатка, т. к. мутантные клетки как чужеродные для организма подвергаются лизису.
При общей высокой неспецифической резистентности организм может быть недостаточно устойчив к определенным воздействиям. В экстремальных условиях, напр, у космонавтов, могут выявиться признаки недостаточной резистентности вестибулярного аппарата, что приводит к нарушению ряда вегетативных функций. Нек-рые лица с весьма высокой общей резистентностью не переносят алкоголь вследствие низкой активности алкогольдегидрогеназы.
Состояние и особенности Р. о. могут быть в известной степени выявлены с помощью функциональных проб и нагрузок, к-рые используются при проф. отборе и в клинике для оценки функциональных резервов органов и систем. В ряде случаев Р. о. по отношению к определенным воздействиям можно оценить прямыми исследованиями наиболее существенных компонентов систем, участвующих в формировании Р. о. (напр., показателей иммунитета). Направленное изменение Р. о. является одним из перспективных направлений профилактической и леч. медицины.
Библиография: Адо А. Д. Некоторые возрастные особенности аллергической реактивности организма, Труды Конф. по возрасти. изменениям обмена в-в и реактивности организма, с. 74, Киев, 1951; он же, Общая аллергология, с. 321, М., 1970;
Анохин П. К. Очерки по физиологии функциональных систем, М., 1975; Вернет Ф. М. Целостность организма и иммунитет, пер. с англ., М., 1964; он же, Клеточная иммунология, пер. с англ., М., 1971; Богомолец А. А. Избранные труды, т. 2, Киев, 1957; Бочков Н. П. Генетика человека, Наследственность и патология, М., 1978; Гомеостаз, под ред. П. Д. Горизонтова, М., 1976; Казначеев В. П. Современные аспекты адаптации, Новосибирск, 1980, библиогр.; Лазарев Н. В., Люблина Е. И. и Розин М. А. Состояние неспецифически повышенной сопротивляемости, Пат. фи-зиол. и эксперим. тер., т. 3, № 4, с. 16, 1959; Меерсон Ф. 3. Адаптация, стресс и профилактика, М., 1981, библиогр.; Орбели Л. А. Вопросы эволюционной физиологии, Избранные труды, т. 1, М.—Л., 1961; Пархон К. И. Возрастная биология, пер. с румын., Бухарест, 1959; Пианка Э. Эволюционная экология, пер. с англ., М., 1981; Селье П. Очерки об адаптационном синдроме, пер. с англ., М., 1960; он же, Неспецифическая резистентность, Пат. фи-зиол. и эксперим. тер., т. 5, № 3, с. 3, № 4, с. 3, 1961, библиогр.; Сиротинин H. Н. Эволюция резистентности и реактивности организма, М., 1981, библиогр.; Сперанский А. Д. Нервная система в патологии, М.—Л., 1930; Cell biology and immunology of leukocyte function, ed. by М. B. Quastel, N. Y. a. o., 1979; The immune system, functions and therapy of dysfunction, ed. ByG. Doria, L. a. o., 1980.
Что делать с резистентностью к антибиотикам? Новые данные: распространение между странами и борьба с мультилекарственной устойчивостью
Что делать с резистентностью к антибиотикам? Новые данные: распространение между странами и борьба с мультилекарственной устойчивостью
Антибиотикорезистентные бактерии одолевают один препарат за другим и неконтролируемо распространяются
Авторы
Редакторы
Статья на конкурс «Био/Мол/Текст»: Устойчивость бактерий к антибиотикам — серьезная угроза здоровью людей. Из-за распространения резистентности с каждым годом подобрать эффективное лечение становится все сложнее. Человечество использует антибиотики повсеместно и тем самым только ускоряет процесс. К сожалению, резистентные штаммы могут передаваться от одного человека к другому, и масштаб проблемы до сих пор известен не до конца. Может ли, например, высокий уровень потребления антибиотиков в одной стране ухудшить эпидемиологическую обстановку в другой, где правительство регулирует использование противомикробных препаратов? Недавнее исследование, о котором мы расскажем в первой части статьи, утверждает, что да, может. А значит, опасность еще серьезнее, чем мы думали. Поэтому необходимо искать препараты, ломающие сам механизм устойчивости, так как уже сейчас существуют бактерии, которые невозможно остановить практически ни одним антибиотиком. Во второй части статьи мы расскажем об исследовании, открывшем новые свойства уже известных препаратов, как об одном из способов «отключить» резистентность и тем самым спасти миллионы жизней.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Вступление
С тех пор как Александр Флеминг впервые выделил пенициллин, жить стало значительно веселее: теперь можно было не умирать от остеомиелита, родильной горячки, гангрены или сифилиса. За последующие девяносто лет человечество успело обзавестись внушительным арсеналом противомикробных препаратов и начать их активно использовать везде: от медицины до сельского хозяйства. И все бы хорошо, если бы не одно но: со временем антибиотики, которые призваны убивать бактерии или останавливать их рост, предотвращая развитие болезни, перестают работать. Некоторые микроорганизмы выживают после применения того или иного лекарства. Они мутируют и продолжают расти и размножаться, уже не встречая конкуренции со стороны других штаммов. К таким «суперзлодеям» от мира бактерий относятся, например, метициллинрезистентный золотистый стафилококк (рис. 1) или микобактерии туберкулеза со множественной лекарственной устойчивостью.
Рисунок 1. Нейтрофил обезвреживает метициллин-резистентную бактерию Staphylococcus aureus, фагоцитируя ее. Фото конфокального микроскопа, цвета условны. Подробнее о конфокальной микроскопии можно прочесть в материале «12 методов в картинках: микроскопия» [1].
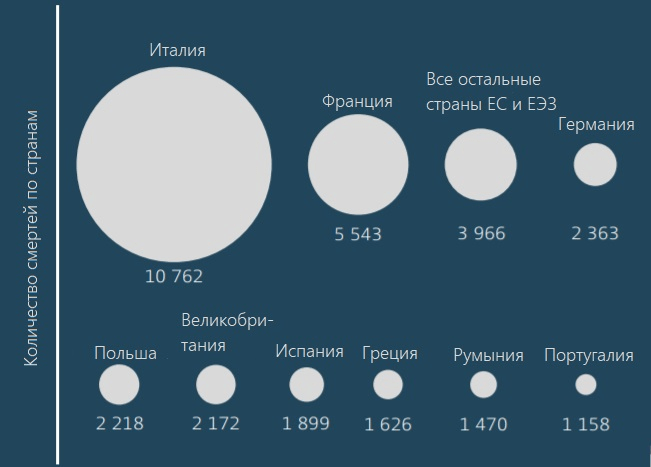
По данным комиссии, собранной британским министерством здравоохранения в 2014–2016 гг., ежегодно около 700 000 человек по всему миру умирает от бактериальных инфекций, которые вызваны невосприимчивыми к действию антибиотиков патогенами. К 2050-му эта цифра может вырасти до 10 миллионов человек в год [2]. А по данным за 2019 год, только в США и европейских странах суммарно от болезней, вызванных резистентными бактериями, умирает около 68 000 человек в год (рис. 2) [3], [4].
Рисунок 2. Количество смертей от болезней, вызванных резистентными к антибиотикам бактериями, в европейских странах по данным за 2015 год
О механизмах резистентности и ее передаче можно подробнее почитать в материалах [5] и [6].
Распространение резистентности: связь с уровнем потребления антибиотиков и влияние окружения
Многие исследования говорят в пользу существования прямой зависимости между увеличением потребления антибиотиков и распространением устойчивости бактерий к их действию [2–4], [7]. Помимо прямого влияния, когда из-за малых доз или недостаточно долгого применения лекарства бактерии быстро адаптируются к враждебной среде, существуют и косвенные «преимущества», которые дает устойчивым штаммам прием противомикробных препаратов: такие как устранение конкурентов в лице восприимчивых штаммов или подавление полезной микрофлоры, которая помогает организму справляться с инфекционной нагрузкой.
Иногда случается так, что потребление антибиотиков сокращается, а уровень устойчивости наоборот, только растет. Например, так произошло в Исландии 20 лет назад. В 2002 году было опубликовано исследование [8], согласно которому, несмотря на сокращение потребления противомикробных препаратов с 1,5 до 1,1 курса в год на одного ребенка (возрастом от одного года до шести лет), за пять лет распространенность устойчивых к пенициллину пневмококков выросла в двух наиболее удаленных от столицы регионах в четыре и в десять раз. Причем в десять раз она выросла там, где сокращение потребления антибиотиков было самым значительным по стране. Хотя в среднем за этот период уровень резистентности в Исландии действительно сократился: на 5%. Авторы исследования предположили, что из-за слабого коллективного иммунитета жители сельских регионов (рис. 3, 4) оказываются более уязвимыми к новым патогенам, которые сначала распространяются в крупных городах и только спустя время доходят до деревень. Можно было бы предположить, что свою роль сыграли и маленькие дозы лекарства или некорректная длительность терапии, однако, по данным исследования, все дети получали адекватное лечение.
Рисунок 3. Поселение Болунгарвик (исл. Bolungarvík), где зарегистрировали самый значительный рост резистентности при наиболее сильном снижении объема потребления антибиотиков.
Рисунок 4. Маяк Оусхоулавити (исл. Óshólaviti) в Болунгарвике. Фотограф: Герберт Ортнер, Вена (Herbert Ortner, Vienna).
Тем не менее исландский кейс остается скорее частным примером того, как на резистентность могут влиять и другие факторы, помимо объема потребления противомикробных препаратов. В целом же, прием антибиотиков остается одной из главных причин распространения устойчивости в мире [2–4].
К сожалению, даже если человек никогда не злоупотреблял антибиотиками, он может получить резистентную микрофлору от кого-то из своего непосредственного окружения, например, от родственников.
Исследование [9] на основе данных, полученных в 1998 году в двух деревнях штата Юта (рис. 5), показало, что вероятность получить как устойчивые, так и чувствительные штаммы растет с увеличением количества детей в семье. А прием антибиотиков ребенком увеличивает количество именно устойчивых бактерий у братьев и сестер.
Рисунок 5. Билборд на въезде в штат Юта со слоганом штата: Life Elevated («Возвышенная жизнь»)
В 2019 году израильские ученые показали, что прием матерями фторхинолонов (противомикробных лекарств широкого действия) повышал риск заражения резистентными штаммами не принимавших эти лекарства детей на 50% [10].
Бактерии распространяются не только в семьях, но и в других небольших сообществах, где люди тесно взаимодействуют, например в больницах. Так, в 2001 году другой исследовательский коллектив из Израиля подтвердил, что прием цефалоспоринов и амикацина (полусинтетического антибиотика группы аминогликозидов) в шести отделениях больницы был связан с повышенным риском заражения устойчивыми патогенами в течение последующих месяцев, в том числе и у пациентов, не принимавших эти антибиотики в течение предыдущего года. Причем у принимавших этот риск был выше 1,5–3 раза [11].
Распространение резистентности в больших сообществах
Второго ноября было опубликовано исследование [12] ученых Гарвардского университета, которое показало, что на степень распространения резистентности к антибиотикам среди населения одного региона существенно влияет уровень их потребления в соседних — точнее, в тех, которые интенсивнее всего с этим регионом взаимодействуют: например, если люди активно перемещаются между ними. Для описания таких ситуаций авторы статьи используют термин «спилловер-эффект» (от англ. to spill over — «выходить за пределы чего-либо, распространяться на другие области»; существительное spillover обозначает соответствующий процесс «распространения»).
Исследователи рассматривали данные о потреблении антибиотиков и распространенности устойчивости к ним в американских штатах и европейских странах. Они предположили, что чем два штата или две страны теснее взаимодействуют, тем меньше между ними разница в уровне резистентности к антибиотикам, и непосредственное влияние объема потребления антибиотиков на устойчивость будет ниже, чем в идеальной ситуации, когда регион полностью изолирован от других.
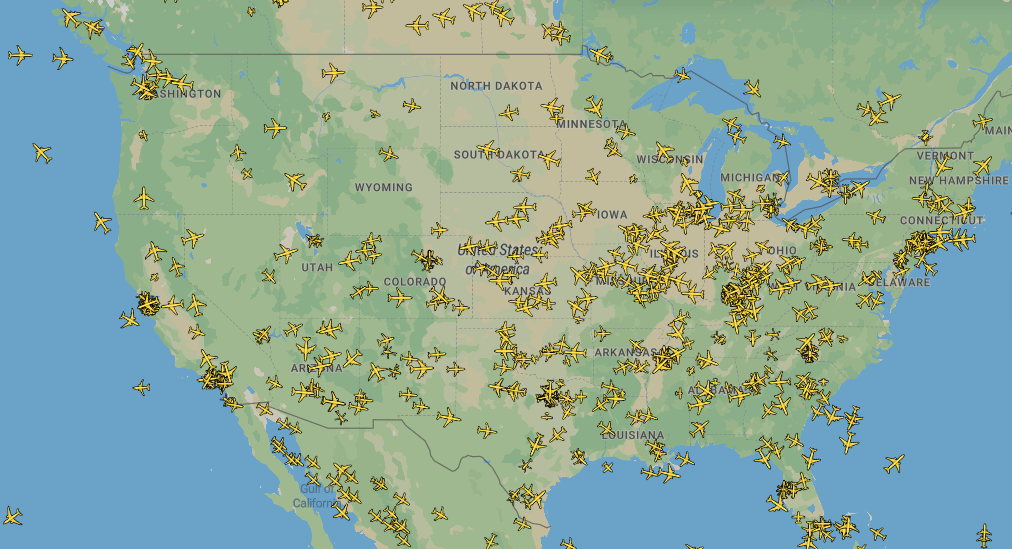
Чтобы проверить гипотезу, ученые сначала использовали математические модели, с помощью которых они делали численные предсказания того, насколько спилловер-эффект увеличится от усиления интенсивности взаимодействия сообществ. А затем они обратились к эмпирическим данным и соотнесли разницу в уровне резистентности внутри регионов с интенсивностью их взаимодействия друг с другом. Степень интенсивности определяли по данным о перелетах американскими и европейскими авиалиниями — ученые предположили, что чем меньше рейсов между регионами, тем слабее эти регионы взаимодействуют (рис. 6).
Рисунок 6. Карта авиаперелетов
В результате две математические модели, применявшиеся в исследовании, — WHN и D-type (см. «Расшифровки» в конце статьи), — подтвердили предположение, что у активно взаимодействующих между собой сообществ разница в уровне устойчивости ниже, чем у тех, которые взаимодействуют меньше. Конкретные величины зависят от выбора модели, однако согласно обеим, достаточно, чтобы было всего на 1% больше взаимодействий между сообществами, для сокращения разницы в уровне резистентности между ними на треть, а то и на 50% — опять же, зависит от выбора модели.
Исследователи рассматривали три пары патогенов и антибиотиков: «пневмококки и макролиды», «пневмококки и β-лактамы» и «кишечная палочка и фторхинолоны». Именно эти комбинации наиболее часто исследовали прежде.
Источники информации о потреблении антибиотиков и распространении устойчивости внутри регионов ученые распределили по трем группам: первые две включали в себя американские базы данных, а третья — данные по европейским странам.
Но в итоге было сформировано шесть датасетов вместо девяти: два убрали, потому что пришлось исключить данные по устойчивости пневмококков к β-лактамам в США — в предыдущих исследованиях на этих датасетах связь между объемом потребления антибиотиков и уровнем резистентности получила отрицательную точечную оценку. Кроме того, информация по потреблению фторхинолонов для США была только во втором наборе данных, так что для этой комбинации патогена и антибиотика собрали два датасета вместо трех, как у остальных (один европейский и один американский).
После попарного сравнения регионов, связь между интенсивностью взаимодействия и снижением зависимости уровня резистентности от объема потребления антибиотиков оказалась статистически значимой в четырех из шести датасетов. Иными словами, чем активнее люди перемещались между сообществами, тем меньшее влияние на распространенность устойчивости оказывал уровень потребления антибиотиков внутри каждого из них — значительную роль начинали играть соседи.
Ученые также сгруппировали все сообщества по парам и ранжировали список по степени интенсивности взаимодействия. Затем они сравнили первые 10% пар из начала с 10% пар с конца и выяснили, что для пар в начале рейтинга связь между объемом потребления антибиотиков и резистентностью в среднем на 50% слабее, чем для пар, которые взаимодействовали меньше всего.
О чем говорят эти данные? В первую очередь о том, что спилловер-эффект оказывает значимое влияние на распространение устойчивости бактерий к антибиотикам на уровне США и европейских стран. Из этого наблюдения следуют несколько важных выводов. Во-первых, бессмысленно проводить какую бы то ни было политику по сокращению потребления антибиотиков с целью снизить уровень резистентности, не учитывая ситуацию в соседних регионах. Во-вторых, куда эффективнее любые меры принимать не на уровне отдельной страны или штата, а на уровне более крупных регионов: США или Евросоюза целиком. В-третьих, массовые испытания антибиотиков могут привести к росту устойчивости внутри всей контрольной популяции (если она не полностью изолирована от испытуемых) за счет все того же спилловер-эффекта.
Однако на распространение устойчивости влияют не только потребление антибиотиков или путешествия между регионами. Свою роль могут играть и другие факторы. Так, исследование 2017 года показало, что устойчивость бактерий к антибиотикам растет с повышением среднегодовой температуры на 2–4% [13]. А согласно другому исследованию, уже 2018 года, на распространение резистентности влияют и социально-экономические факторы (рис. 7): чем лучше развита инфраструктура и выше расходы государства на здравоохранение, тем ниже уровень распространения устойчивости к антибиотикам [14]. Поэтому не исключено, что схожесть в уровне резистентности у тесно взаимодействующих регионов может быть связана с их схожестью в плане географии или на экономическом уровне. Также, различия в образе жизни между разными социальными группами (разделенными по гендерному, этническому или экономическому признакам) может оказаться очень высокой — возможно, сравнение между собой административных единиц не совсем корректно, и куда эффективнее было бы сравнивать разные социальных слои [15], [16]. Кроме того, в исследовании не учитывались другие способы передвижения между регионами, помимо авиаперелетов. Кажется, что на близкие расстояния люди могут чаще перемещаться наземным транспортом: поездами или автомобилями, поэтому небольшое количество рейсов между двумя регионами еще не говорит об их слабом взаимодействии. Поэтому для получения адекватной картины происходящего необходимо принимать во внимание даже такие «мелочи», как дорожная инфраструктура региона или стоимость перемещения разными видами транспорта.
Рисунок 7. Разница в уровне доходов у американского населения по штатам. Экономическое неравенство сказывается и на сфере здравоохранения: у людей с высоким и низким доходом разные условия проживания, неравный доступ к медицине и др. Это может быть релевантно при анализе эпидемиологической обстановки региона.
К тому же, чтобы упростить себе задачу, в рамках исследования ученые исходили из того, что связь между объемом потребления антибиотиков и уровнем резистентности неоспорима, а изменения в распространенности устойчивости следуют за изменениями в объеме потребления антибиотиков в течение какого-то относительно небольшого и обозримого отрезка времени, хотя оба эти положения являются предметом активного изучения. Попарное сравнение сообществ также существенно упрощает задачу построения математической модели и обработки данных. Однако надо понимать, что на деле регионы взаимодействуют между собой одновременно, и это взаимодействие может иметь сезонный характер, или его интенсивность может меняться в зависимости от каких-то социальных, политических или экологических процессов. Так что теоретические выкладки, полученные исследователями, довольно грубы и позволяют составить только беглое представление о проблеме.
Борьба с резистентностью: поиск новых решений
Итак, мы выяснили: устойчивость к антибиотикам страшна не только тем, что ее уровень растет по мере того, как увеличиваются объемы потребления антибиотиков, но и своей способностью распространяться внутри сообществ любого размера: от семей до государств. Особенное беспокойство вызывает распространение мультилекарственной резистентности некоторых патогенов — защищенности сразу от нескольких групп препаратов. Борьба с угрозой идет в основном по двум фронтам: во-первых, человечество создает все новые и новые препараты, способные эффективно подавлять устойчивые микроорганизмы, а во-вторых, придумывает способы замедлить распространение резистентности (как правило, за счет снижения объемов потребления антибиотиков) и выиграть время. Однако эта гонка бесконечна (см. обзор [17]). Как долго мы сможем «убегать»?
Хорошо бы научиться «отключать» резистентность, чтобы уже известные антибиотики заново стали эффективным «оружием». Для этого нужно проанализировать механизмы передачи, хранения и реализации устойчивости к антибиотикам. О некоторых из уже существующих способов борьбы с мультилекарственной резистентностью можно почитать в материалах [6] и [18].
Рисунок 8. Инфографика по карбапенем-резистентным энтеробактериям из доклада Департамента здравоохранения и социальных служб США. Согласно ей, в 2017 году насчитывалось 13 100 случаев госпитализации пациентов с инфекциями, вызванными карбапенем-резистентными энтеробактериями, в том числе и 1100 случаев летального исхода, а соответствующие затраты на здравоохранение в Америке составили 130 миллионов долларов США. Карбапанем-резистентные энтеробактерии представляют серьезную проблему для пациентов медицинских учреждений: некоторые штаммы развили устойчивости почти ко всем распространенным антибиотикам, что вынуждает врачей прибегать к более токсичным или менее эффективным препаратам.
А здесь мы рассмотрим, как может решаться проблема мультилекарственной резистентности, на примере карбапенем-резистентных энтеробактерий (CRE, от Сarbapenem-Resistant Enterobacteriaceae). CRE могут поражать органы мочеполовой системы, кровь или легкие, но главная их опасность заключается в устойчивости к самым серьезным препаратам, направленным против них (рис. 8). Карбапенемы — антибиотики «последней надежды», то есть средства, которые применяются лишь в крайних ситуациях, когда ничто больше не помогает. Часто CRE устойчивы не только к карбапенемам, но и ко многим другим классам антибиотиков, что делает лечение от них чрезвычайно тяжелым [19]. В 2019 году Центр по контролю и профилактике заболеваний США поместил карбапенем-резистентных энтеробактерий среди пяти групп микроорганизмов, защиту от которых из-за угрозы здравоохранению необходимо разрабатывать в первую очередь [3].
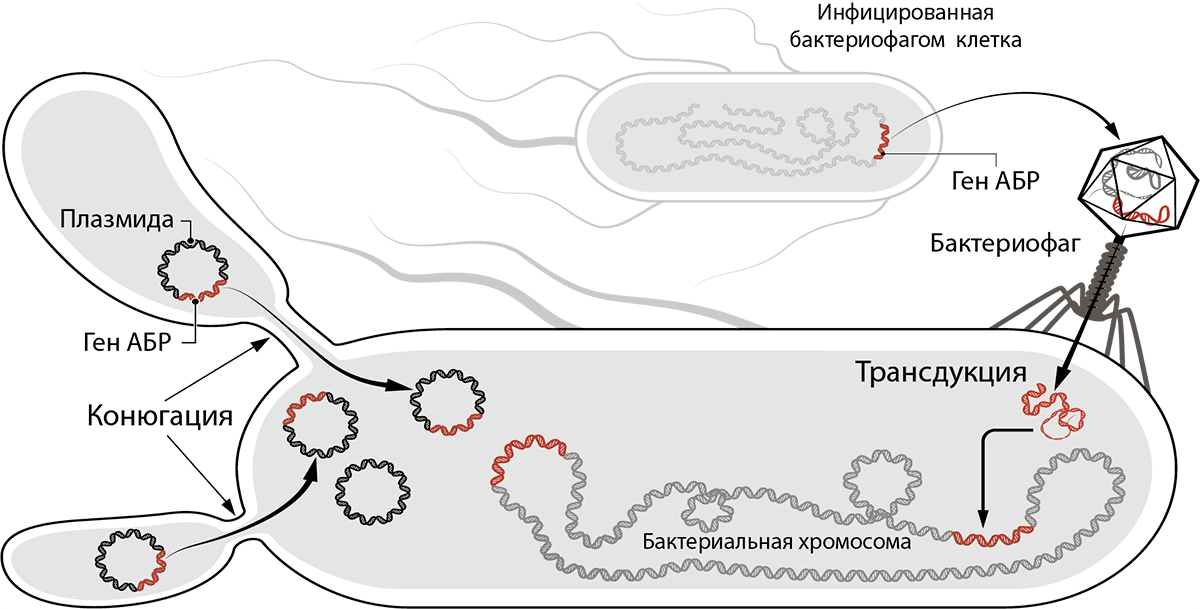
Рисунок 9. Как последовательности ДНК, ответственные за резистентность, попадают в клетку бактерии и хранятся в ней? Последовательности ДНК, кодирующие ферменты, которые обеспечивают резистентность, могут находиться в плазмидах — кольцевых ДНК внутри клеток бактерий, — передаваться в составе плазмид потомкам и родственникам при коньюгации. Еще такие последовательности ДНК могут передаваться из ДНК одной бактерии в ДНК другой путем трансдукции — переноса внутри вируса.
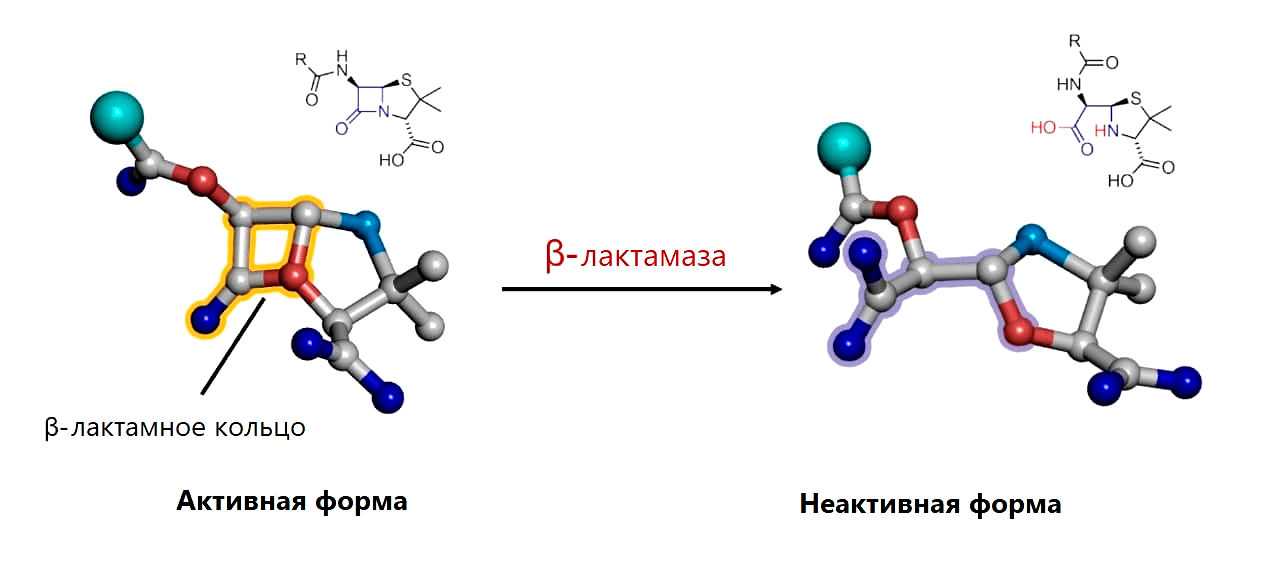
Устойчивость CRE работает по проверенной механике Докинза: резистентность переносится плазмидами устойчивости CRE (pCRE, CRE resistance plasmids), которые так и хочется назвать эгоистичными (рис. 9). Ведь карбапенем-резистентные энтеробактерии платят высокую цену за свою неуязвимость: если клетка утрачивает pCRE, то она погибает из-за токсина, который был закодирован в плазмиде и остался в клетке [20]. (До утраты pCRE с нее синтезировался неустойчивый антидот, блокирующий действие токсина.) pCRE очень большие, поэтому количество их копий в одной клетке CRE можно сосчитать по пальцам. Чтобы не потеряться во время деления, в pCRE закодирован механизм распределения по дочерним клеткам, как и множество ферментов, «обслуживающих» плазмиду, в которой заложено всё для ее распространения и выживания ее носителя, в том числе карбапенемаза — фермент, расщепляющий не только карбапенемы, но и многие другие β-лактамные антибиотики (рис. 10) [21]. Фермент, закодированный в плазмиде, «защищает» ее носителя. То есть в первую очередь опасность представляют не бактерии, а плазмида, поэтому методы борьбы должны быть направлены главным образом против нее.
Рисунок 10. Разрушение β-лактамного кольца β-лактамазой путем гидролиза связи между атомами углерода (серыми) и азота (голубыми)
Кэйтлин Зулауфа и Джеймс Кирби из Гарвардской медицинской школы нашли подходящие для вмешательства в работу плазмиды препараты среди тех, которые уже используются, но в иных целях, и попробовали объяснить их эффективность в борьбе с резистентными штаммами [22]. Это исследование кажется нам важным, поэтому ниже мы расскажем об экспериментах, проведенных коллегами-учеными, и данных, говорящих в пользу их открытия.
В результате скрининга более 12 000 биоактивных соединений исследователи выделили три, после воздействия которых копии pCRE не распространялись в культуре бактерий при делениях, что делало последующие поколения восприимчивыми к карбапенемам.
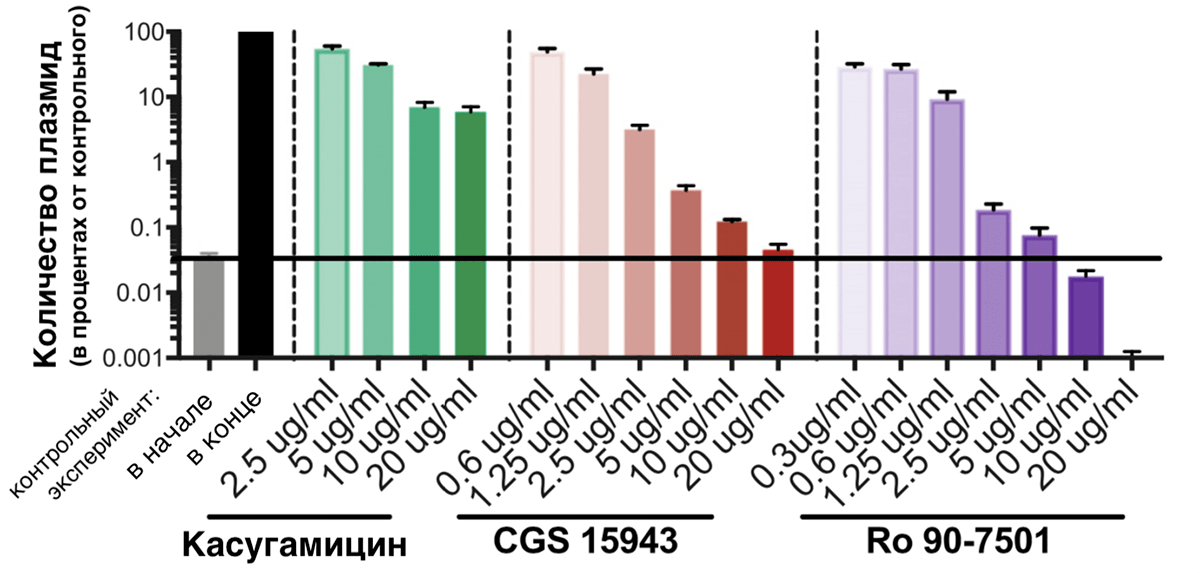
Наш первый кандидат — касугамицин — аминогликозидный антибиотик, который, судя по данным исследователей, мешает процессу синтеза белка RepE, играющего ключевую роль в размножении pCRE путем репликации (удвоения) [23]. То есть без RepE плазмида, скорее всего, не передастся новым поколениям бактерий. После воздействия касугамицина в течение 24 часов репликация pCRE случалась реже более чем в 10 раз (рис. 11), по сравнению с необработанными бактериями (более 90% потомков бактерий, резистентных еще сутки назад, утратили защиту). Однако даже во время применения максимальной в этом исследовании дозы касугамицина плазмиды все же размножались (их становилось больше на два порядка). Зафиксируем, что касугамицин не блокирует репликацию полностью, а лишь сильно замедляет ее.
Рисунок 11. Зависимость активности размножения плазмид в растущей бактериальной культуре от воздействия препаратов. По вертикальной шкале — количество плазмид бактерий после инкубирования при разных концентрациях препаратов, выраженное в процентах от количества плазмид в посевах в обычных условиях. Первые два столбца — контрольный эксперимент (без воздействия препаратов): серый столбец — количество в начале контрольного эксперимента; черный — в бактериях после обычных условий культивирования. Зеленые столбики — после культивирования при разных концентрациях касугамицина; красные столбики — после культивирования при разных концентрациях CGS 15943; фиолетовые столбики — после культивирования при разных концентрациях Ro 90-7501.
Наш второй кандидат — CGS 15943 (см. «Расшифровки» в конце статьи) — возможно, нарушает считывание последовательности RepE. В любом случае, он мешает репликации плазмид настолько, что их количество при максимальной дозе CGS 15943 почти не увеличилось (рис. 11). Отметим, что CGS 15943 способен почти полностью останавливать репликацию pCRE.
Третий кандидат — Ro 90-7501 (см. «Расшифровки» в конце статьи) — имеет самые впечатляющие результаты. Взглянув на рисунок 11, хочется назвать его «убийцей» pCRE. Дело в том, что Ro 90-7501 — интеркалятор ДНК, то есть соединение, которое встраивается между цепями ДНК, «ломая» ее структуру и мешая репликации. Только начиная исследование, ученые не хотели использовать интеркаляторы, потому что для человека целостность собственной ДНК не менее важна, чем для плазмиды целостность своей. Например, зафиксировано воздействие этого же Ro 90-7501 на клетки млекопитающих: он влияет на сборку фибрилл амилоида β42 (связанного с болезнью Альцгеймера) [24], на активность врожденного иммунитета [25] и ингибирует протеинфосфатазу 5 — фермент, важный в регуляции ключевых событий жизни клетки [26], [27]. Однако Ro 90-7501 оказался селективным к pCRE, и ученые изучили его особенно тщательно. Оговорив, что концентрация Ro 90-7501, при которой достигается максимальный антиплазмидный эффект, ниже токсичной для клеток млекопитающих почти в 30 раз [28].
Сравним препараты: CGS 15943 не имеет известных побочных эффектов для клеток человека, однако он и не истребляет плазмиды так, как это делает Ro 90-7501. То есть после окончания курса CGS 15943 резистентные патогены могут выжить и размножиться опять. Возможно, получится изменить последовательность Ro 90-7501 так, чтобы он перестал воздействовать на процессы в клетках млекопитающих. Однако обоим препаратам стоит «поучиться» у касугамицина проникать в клетки грамотрицательных бактерий (к которым относятся и энтеробактерии), видимо, для их применения в реальных условиях нужно разработать подходящий способ проникновения молекул препарата внутрь клетки.
Таким образом, использование каких-то из этих препаратов может привести нас к победе над опасными карбапенем-резистентными энтеробактериями. Ученым предстоит долгая и кропотливая работа по поиску или синтезу веществ, которые окажутся действенными в устранении описанного нами механизма резистентности.
Исследования, подобные этому, внушают надежду на то, что нам удастся не просто вечно бежать на шаг впереди, создавая препараты, к которым у бактерий еще не выработалась устойчивость, но и «поворачивать время вспять» — сопротивляться уже существующим механизмам резистентности, придумывая способы для непосредственной остановки их действия. И тогда пугающая цифра в 10 миллионов смертей в год никогда не станет реальностью.