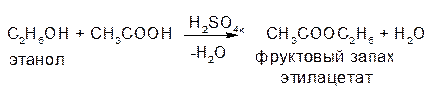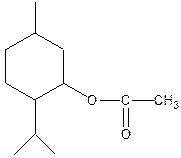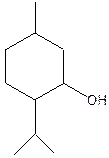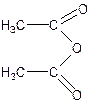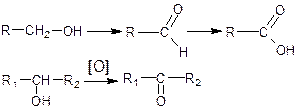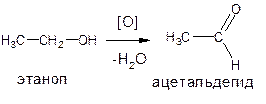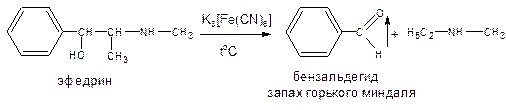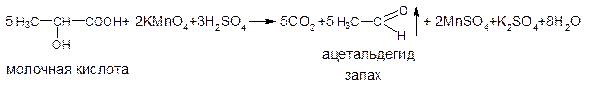Что значит реакция протекает количественно
ВЫХОД РЕАКЦИИ
Масса продуктов, образовавшихся в химической реакции, называется ее выходом. Выход продукта, вычисленный на основе химического уравнения, называется теоретическим выходом. Действительный выход, полученный в эксперименте или промышленном процессе, называется фактическим выходом.
Когда фактический выход оказывается равен теоретическому, говорят, что реакция имеет количественный выход. Химическую реакцию, протекающую с количественным выходом, называют стехиометрическим процессом. Количественный выход дают многие ионные реакции. Примерами таких реакций являются реакции нейтрализации и ионного осаждения. Однако многие химические реакции не имеют количественного выхода. Это относится, в частности, к органическим реакциям. Во всех подобных случаях приходится вычислять относительный выход. Он определяется следующим соотношением:
Относительный выход служит мерой эффективности реакции. Так, химическая реакция, протекающая с количественным выходом, имеет 100%-ную эффективность. Химические реакции, которые не дают количественного выхода, иногда называют нестехиометрическими процессами. Однако, в сущности, такое выражение неправильно, поскольку, согласно основным количественным законам химии, все химические реакции должны быть стехиометрическими. Другими словами, во всех реакциях непременно должны участвовать целочисленные количества элементарных химических частиц (атомы, ионы либо молекулы) в постоянных, строго определенных соотношениях. Нестехиометрия реакции может быть обусловлена целым рядом причин, например недостаточной чистотой реагентов, протеканием побочных реакций или такими практическими факторами, как потери при кристаллизации.
Для повышения относительного выхода нестехиометрического процесса обычно используют избыточное количество одного или нескольких реагентов. В этом случае теоретический выход вычисляют по количеству того реагента, который не используется в избытке. Такой реагент называется лимитирующим реагентом.
Классификация химических реакций
Темы кодификатора ЕГЭ: Классификация химических реакций в органической и неорганической химии.
В ходе химической реакции разрушаются химические связи, и образуются новые.
Химические реакции классифицируют по разным признакам. Рассмотрим основные виды классификации химических реакций.
Классификация по числу и составу реагирующих веществ
По составу и числу реагирующих веществ разделяют реакции, протекающие без изменения состава веществ, и реакции, протекающие с изменением состава веществ:
1. Реакции, протекающие без изменения состава веществ (A → B)
К таким реакциям в неорганической химии можно отнести аллотропные переходы простых веществ из одной модификации в другую:
Sромбическая → Sмоноклинная.
2. Реакции, протекающие с изменением состава
Как правило, в названии таких реакций есть приставка «де». Реакции разложения в органической химии происходят, как правило, с разрывом углеродной цепи.
2KI + Cl2 → 2KCl + I2.
Замещаться могут как отдельные атомы, так и молекулы.
В органической химии реакции замещения — это такие реакции, в ходе которых часть органической молекулы замещается на другие частицы. При этом замещенная частица, как правило, соединяется с частью молекулы-заместителя.
По числу частиц и составу продуктов взаимодействия эта реакция больше похожа на реакцию обмена. Тем не менее, по механизму такая реакция является реакцией замещения.
AB + CD = AC + BD
К реакциям обмена относятся реакции ионного обмена, протекающие в растворах; реакции, иллюстрирующие кислотно-основные свойства веществ и другие.
Пример реакции обмена в неорганической химии — нейтрализация соляной кислоты щелочью:
NaOH + HCl = NaCl + H2O
Пример реакции обмена в органической химии — щелочной гидролиз хлорэтана:
Классификация химических реакций по изменению степени окисления элементов, образующих вещества
По изменению степени окисления элементов химические реакции делят на окислительно-восстановительные реакции, и реакции, идущие без изменения степеней окисления химических элементов.
В неорганической химии к таким реакциям относятся, как правило, реакции разложения, замещения, соединения, и все реакции, идущие с участием простых веществ. Для уравнивания ОВР используют метод электронного баланса (количество отданных электронов должно быть равно количеству полученных) или метод электронно-ионного баланса.
В органической химии разделяют реакции окисления и восстановления, в зависимости от того, что происходит с органической молекулой.
Реакции окисления в органической химии — это реакции, в ходе которых уменьшается число атомов водорода или увеличивается число атомов кислорода в исходной органической молекуле.
Реакции восстановления в органической химии — это реакции, в ходе которых увеличивается число атомов водорода или уменьшается число атомов кислорода в органической молекуле.
Классификация реакций по тепловому эффекту
По тепловому эффекту реакции разделяют на экзотермические и эндотермические.
Экзотермические реакции — это реакции, сопровождающиеся выделением энергии в форме теплоты (+Q). К таким реакциям относятся почти все реакции соединения.
Исключения — реакция азота с кислородом с образованием оксида азота (II) — эндотермическая:
Реакция газообразного водорода с твердым йодом также эндотермическая:
Экзотермические реакции, в ходе которых выделяется свет, называют реакциями горения.
Также экзотермическими являются:
Эндотермические реакции — это реакции, сопровождающиеся поглощением энергии в форме теплоты (— Q). Как правило, с поглощением теплоты идет большинство реакций разложения (реакции, требующие длительного нагревания).
Также эндотермическими являются:
Классификация химических реакций по агрегатному состоянию реагирующих веществ (по фазовому составу)
Для классификации реакций по фазовому состоянию полезно уметь определять фазовые состояния веществ. Это достаточно легко сделать, используя знания о строении вещества, в частности, о типах кристаллической решетки.
Вещества с ионной, атомной или металлической кристаллической решеткой, как правило твердые при обычных условиях; вещества с молекулярной решеткой, как правило, жидкости или газы при обычных условиях.
Обратите внимание, что при нагревании или охлаждении вещества могут переходить из одного фазового состояния в другое. В таком случае необходимо ориентироваться на условия проведения конкретной реакции и физические свойства вещества.
Таким образом, паровая конверсия метана — гомогенная реакция.
Классификация химических реакций по участию катализатора
Катализатор — это такое вещество, которое ускоряет реакцию, но не входит в состав продуктов реакции. Катализатор участвует в реакции, но практичсеки не расходуется в ходе реакции. Условно схему действия катализатора К при взаимодействии веществ A + B можно изобразить так: A + K = AK; AK + B = AB + K.
В зависимости от наличия катализатора различают каталитические и некаталитические реакции.
Все реакции, протекающие с участием в клетках живых организмов, протекают с участием особых белковых катализаторов — ферментов. Такие реакции называют ферментативными.
Более подробно механизм действия и функции катализаторов рассматриваются в отдельной статье.
Классификация реакций по способности протекать в обратном направлении
Обратимые реакции — это реакции, которые могут протекать и в прямом, и в и обратном направлении, т.е. когда при данных условиях продукты реакции могут взаимодействовать друг с другом. К обратимым реакциям относятся большинство гомогенных реакций, этерификация; реакции гидролиза; гидрирование-дегидрирование, гидратация-дегидратация; получение аммиака из простых веществ, окисление сернистого газа, получение галогеноводородов (кроме фтороводорода) и сероводорода; синтез метанола; получение и разложение карбонатов и гидрокарбонатов, и т.д.
Необратимые реакции — это реакции, которые протекают преимущественно в одном направлении, т.е. продукты реакции не могут взаимодействовать друг с другом при данных условиях. Примеры необратимых реакций: горение; реакции, идущие со взрывом; реакции, идущие с образованием газа, осадка или воды в растворах; растворение щелочных металлов в воде; и др.
Если реакция протекает количественно и стехиометрично, они могут быть использованы для количественного определения.
Прочие
R-Hal ковалентно связанный галоген (Cl, Br, J, F).
R – S – R1 ковалентно связанная сера
R – SH сульфгидрильная (меркаптогруппа) и т.д.
Реакции на ФГ, за редким исключением, носят универсальный характер, следовательно, знание свойств ФГ дает возможность предсказать способы испытаний любого органического вещества.
ЛВ являются, как правило, полифункциональными соединениями, что позволяет надежно идентифицировать это соединение, используя комплекс реакций. В то же время, наличие нескольких ФГ в одном веществе оказывает влияние на эффект некоторых общих реакций и на свойства их продуктов. Это повышает избирательность реакций, позволяет обнаруживать одним реактивом в смесях близкие по строению ЛВ.
Если реакция протекает количественно и стехиометрично, они могут быть использованы для количественного определения.
ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВОЙ ГИДРОКСИЛ.
Спиртовой гидроксил – гидроксильная группа, связанная с алифатическим или алициклическим углеродным радикалом.
Его содержат ЛВ из группы спиртов (этиловый спирт, глицерин), карбоновых кислот и их солей (кальция лактат, кальция глюконат), терпены (ментол, терпингидрат) и др. (эфедрина гидрохлорид, левомицетин, прегнин, метилтестостерон).
1. Реакция этерификации. Идет в присутствии водопритягивающих средств (Н2SО4 к.) с карбоновыми кислотами и их ангидридами. Основана на способности спиртов образовывать сложные эфиры.
· Для низкомолекулярных спиртов (например, этилового) продукт обнаруживается по фруктовому запаху,
· Для высокомолекулярных – по температуре плавления.
|
| |
| |
 |
ментол уксусный ангидрид белый кристаллический
2. Реакция окисления. Основана на свойстве спиртов окисляться до альдегидов (первичные – до альдегидов, иногда до кислот; вторичные – до кетонов; третичные – в жестких условиях до разрушения молекулы);
спирты проявляют слабые восстановительные свойства. Окисляются только сильными окислителями. В качестве реагентов используют сильные окислители: калия перманганат, калия бихромат, хлорная кислота, гексацианоферрат (III) калия и др. Наибольшую аналитическую ценность имеет калия перманганат, который восстанавливаясь, меняет степень окисления от (+7) до (+2) и обесцвечивается, т.е. делает реакцию наиболее эффектной.
ацетальдегид имеет запах
Окислению могут сопутствовать побочные химические реакции. Например:
— в случае эфедрина (фармакопейная реакция) – гидраминное разложение по схеме:
— в случае молочной кислоты (фармакопейная реакция на кальция лактат) – декарбоксилирование:
Дата добавления: 2015-09-07 ; просмотров: 1218 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Что такое химическая реакция
Химическая реакция — это преобразование, происходящее, когда несколько химических веществ вступают в контакт, или когда один химический вид получает внешний источник энергии, что приводит к появлению новых химических видов или элементов.
Химия
Фундаментальная операция, посредством которой создаются новые вещества, химическая реакция состоит в трансформации материи. При этом атомы молекул реагентов разделяются, а затем перестраиваются, чтобы создать новые молекулы, которые составляют продукты реакции. Перед началом реакции необходимо задуматься, будут ли вещества, вступающие в контакт, реагировать с образованием ожидаемых продуктов. Большинство химических реакций протекают в благоприятном направлении. В некоторых случаях происходит противоположное желаемой реакции! Решение этой проблемы требует использования знаний по химической термодинамики.
Когда реакция «возможна» — тогда она имеет тенденцию происходить спонтанно в заданном направлении — важно знать ее скорость. Это обуславливает переход из лаборатории в промышленное производство, которое должно функционировать бесперебойно и без преждевременных реакций.
Механизмы реакции
Химическая реакция сопровождается перестройками в положении атомов, а также изменениями в межатомных связях. То, как эти изменения происходят во времени, является механизмом реакции.
Очень часто химическая реакция может быть разбита на более простые реакции, называемые элементарными реакциями. Например, окисление HI (йодистого водорода) H2O2 (перекисью водорода) происходит в две стадии:
В этой схеме частицы HOI, которые создаются в реакции (1), но потребляются в реакции (2), являются промежуточным продуктом реакции. Срок его службы может быть очень коротким, но в принципе он измерим. Этот промежуточный продукт можно наблюдать с помощью спектроскопических методов.
Написание химических реакций
Количественные реакции
Со времени введения в 1815 году бароном Йенсом Якобом Берцелиусом представления химических элементов символами, с которыми связаны атомные массы, химические реакции описывались химическими уравнениями, в которых появляются формулы исходных химических частиц и окончательный результат реакции.
Эти уравнения, однако, предоставляют гораздо больше информации, чем простое качественное указание элементов, которые вступают в реакцию, и тех элементов, которые образуются в конце реакции: знание атомных масс (которые были установлены с большой точностью при исключении радиоактивных элементов) позволяет количественно определить массы реагентов, которые должны быть приведены в контакт для получения продуктов реакции без остатка в виде осадка или не вступивших во взаимодействия элементов.
Таким образом, путем взаимодействия алюминия (Al) и серы (S), сульфид алюминия (Al2S3) получается в соответствии с реакцией: 2Al + 3S → Al2S3. Коэффициенты, помещенные перед химическими символами (называемые стехиометрическими коэффициентами), представляют собой число молей каждого реагента, которые должны присутствовать для завершения реакции. Два моля алюминия (с молярной массой М = 27 г), то есть 54 г, смешанных с тремя молями серы (М = 32 г), то есть 96 г, дают, таким образом, один моль Al2S3.(М=2 × 27 + 3 × 32 = 150 г). Реакция завершается до тех пор, пока соблюдается соотношение 54/96. Выразим, в этом примере, закон сохранения массы Лавуазье, согласно которому масса вещества, образующегося в результате химической реакции равна массе исходных веществ.
Это означает, в частности, что химическое уравнение должно всегда показывать символ элемента в правой части химического уравнения столько раз, сколько в его левой части (исходные реагенты).
В случае, когда в реакции участвует газ, как в реакции полного окисления железа диоксидом: 3Fe + 2O2 → Fe3O4, более полезно использовать молярный объем (одинаковый для всех газов), который составляет 22,4 л при 0°С. Таким образом, 3 моля железа (М = 56 г) или 168 г реагируют с 2 молями кислорода, т.е. 44,8 л, с получением одного моля оксида железа (М = 3 × 56 + 4 × 16), то есть 232 г Fe3O4.
Полная или ограниченная реакция
Химические уравнения также используются, чтобы указать, являются ли реакции, которые они представляют, полными или ограниченными. Когда реакция завершена, она выражается в уравнении стрелкой, направленной слева направо (→), расположенной между формулами исходных реагентов и формул образовавшихся веществ.
Когда реакция ограничена, она приводит к химическому равновесию, это выражается двумя стрелками противоположных направлений (⇄) при написании уравнения: таким образом, указывается, что в условиях эксперимента (давление, температура), в котором происходит реакция, химические частицы, упомянутые слева, частично реагируют друг с другом с образованием веществ, упомянутых справа, но что при тех же условиях химические частицы справа могут частично реагировать друг с другом, образуя элементы слева,
Так обстоит дело с уксусной кислотой и этанолом, которые при объединении в эквимолярной пропорции, при комнатной температуре, лишь частично реагируют, образуя этилацетат и воду:
При тех же условиях, если мы помещаем этилацетат и воду в эквимолярной пропорции, они частично превращаются в уксусную кислоту и этанол, и полученное состояние равновесия идентично в оба направления.
Катализ и скорость реакции
Некоторые химические реакции имеют место только в присутствии очень специфических веществ, называемых катализаторами, которые помогают продуктам образовываться, но не входят в состав продуктов в реакции. Например, внутри клетки биохимические реакции обычно катализируются специфическими белками, называемыми ферментами, и ферментов почти столько же, сколько и химических реакций.
Выделив в 1833 году амилазу, фермент, способный расщеплять крахмал, Ансельме Пайен и Жан-Франсуа Персоз продемонстрировали важность этих катализаторов (которые они называли в то время диастазами). Эти ферменты позволяют извлекать энергию, содержащуюся в длинных углеродных цепях, например, в пище человека. Таким образом, липаза помогает переваривать жиры, расщепляя их на более простые элементы, называемые жирными кислотами, лактаза расщепляет лактозу или молочный сахар на усваиваемые сахара (глюкозу и галактозу).
Химическая реакция и умение ее правильно записывать является необходимым условием проверки на знание химии, поэтому задания на составление химической реакции, а также проверки правильности ее написания есть в ЕГЭ по химии.
Аналитическая химия. Качественный и количественный анализ, титр
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
ОСНОВНЫЕ ПОНЯТИЯ АНАЛИТИЧЕСКОЙ ХИМИИ
Виды и методы проведения химического анализа
Аналитическая химия — наука о методах определения химического состава вещества и его структуры. Выделяют качественный и количественный анализ.
Качественный анализ — установление присутствия или отсутствия отдельных компонентов в анализируемом объекте.
Количественный анализ — определение содержания компонентов в анализируемом объекте. Качественный анализ предшествует количественному. Результат его — «да — нет».
В качественном анализе различают:
В зависимости от массы пробы вещества, используемого для проведения анализа, методы анализа классифицируют следующим образом:
Методы анализа подразделяются на химические и физико-химические (инструментальные). Химические методы анализа основаны на способности определяемого компонента вступать в химическую реакцию с последующим определением его количества.
Достоинства химического метода анализа:
Недостатки химического метода анализа
Химические реакции, пригодные для качественного анализа, должны сопровождаться заметным внешним эффектом. Это может быть:
В первых четырех случаях за протеканием реакции наблюдают невооруженным глазом, кристаллы рассматривают под микроскопом. Классификация видов химического анализа по объектам определения приведена в табл. 1.1.
Таблица 1.1 Классификация видов химического анализа по объектам определения
В физико-химических методах анализа конец реакции определяют не визуально, как в химических методах, а при помощи приборов, которые фиксируют изменения физических свойств исследуемого вещества.
Качественный анализ
Для получения достоверных результатов анализа конкретного иона необходимы реакции, выполнению которых не мешает присутствие других ионов. Для этого нужны специфические реагенты (взаимодействующие только с определяемым ионом).
Примером реакции с участием специфического реагента является выделение газообразного аммиака NH 3 при действии щелочей (KOH или NaOH) на вещество, содержащее ион аммония NH4 +. Ни один катион не помешает обнаружению иона NH4+, потому что только он реагирует со щелочами с выделением аммиака:
. Еще один пример — специфические реагенты на ионы железа. Специфический реактив гексацианоферрат (III) калия К3[Fе(СN)6] (красная кровяная соль) образует синий осадок (турнбуллева синь) только с ионами двухвалентного железа Fe 2+. Гексацианоферрат (II) калия K4[Fe(CN)6] (желтая кровяная соль) образует синий осадок (берлинская лазурь) только с ионами трехвалентного железа Fe3+. Специфический реагент на ионы меди (II) — аммиак:
Окрашивание пламени горелки является также способом определения некоторых катионов, т. е. качественной реакцией на их присутствие:
Li + — окрашивание пламени в красный цвет;
Na + — окрашивание пламени в желтый цвет;
K + — окрашивание пламени в фиолетовый цвет.
Селективные реагенты — это реагенты, которые реагируют лишь с немногими веществами. Диметилглиоксим (реагент Чугаева) служит примером селективного реагента в щелочной среде он реагирует с ионами Ni +2, Co +2, Fe +2; в кислой — только с ионами Pd +2.
К сожалению, селективных, а тем более специфических реагентов очень мало. Поэтому смеси катионов и анионов разделяют на части с помощью реактива, который называется групповым реактивом.
Действуя на смесь катионов в строго определенном порядке растворами соляной кислоты HCl, серной кислоты H2SO4, аммиака NH3 и гидроксида натрия NaOH, можно разделить содержащиеся в смеси катионы на шесть аналитических групп. Эти растворы называются групповыми реагентами, а схема — кислотно-щелочной (по используемым групповым реагентам).
В сероводородной схеме групповыми реагентами являются соляная кислота HCl, сероводород H2S и карбонат аммония (NH4)2CO3.
Разделение катионов на пять аналитических групп основано на различии свойств образуемых ими хлоридов, сульфидов и карбонатов:
Общепринятой классификации для разделения анионов, как для разделения катионов, не существует. Используют разделение анионов на три аналитические группы по растворимости солей бария и серебра.
Методы качественного анализа классифицируют следующим образом:
— анализ сложных смесей.
Количественный анализ
Количественный анализ проводят после проведения качественного химического анализа, т. е. после установления компонентов анализируемой пробы.
Например, общие свойства спиртов изучают химики-органики, а способы определения спиртов как класса органических соединений и каждого отдельного спирта (например, этанола) разрабатывают аналитики. Для этого они выявляют те особенности химических и физических свойств спиртов, которые отличают их от других органических соединений. Еще важнее выявить характеристические свойства отдельных спиртов (например, этанола), отличающие их друг от друга.
Изучение характеристических свойств индивидуальных объектов особенно важно в тех случаях, когда изучают материалы сложного состава, содержащие смеси родственных веществ.
Также аналитическая химия воспринимает и развивает знания, полученные в рамках смежных научных дисциплин. Разумеется, знания, полученные одной наукой и используемые другой, всегда существенно перерабатываются, подобно тому, как в организме продукты питания превращаются в новые соединения, а уже из них строятся собственные ткани организма. Эта аналогия подходит и для рассматриваемого случая. На основе творчески переработанных достижений других наук и собственных фундаментальных исследований аналитики выявляют общие закономерности химического анализа, создают новые методы и методики.
К химическим методам количественного анализа относятся:
В ходе количественного анализа можно выделить основные его этапы:
Волюмометрические методы анализа основаны на измерении объема реагента, израсходованного на взаимодействие с веществом.
Кинетические методы анализа заключаются в определении зависимости скорости химической реакции от концентрации реагирующих веществ.
Для решения аналитических задач довольно широко применяют биохимические реакции с участием ферментов, а также исключительно специфические реакции, протекающие по схеме «антиген — антитело» (иммуноанализ). Весьма перспективным способом получения информации о составе веществ оказалось изучение реакции живых клеток, тканей, органов и организмов на изменения в составе окружающей их среды. Естественно, соответствующие методы анализа создают на базе достижений биологических наук.
Методика исследования. Чтобы подобрать оптимальную (лучшую) методику химического анализа, в каждом случае следует учитывать ряд практических требований
1. Точность. Это главное требование. Оно означает, что относительная или абсолютная погрешность анализа не должна превышать некоторого предельного значения. Для разных видов анализа, безусловно, требуется разная точность. В одних случаях достаточно, чтобы результат был получен с относительной погрешностью, не превышающей 10 или даже 20%, в других — чтобы погрешность была менее 2 %. При проведении арбитражных анализов относительная погрешность не должна превышать 0,1 или даже 0,01%. Столь высокую точность могут дать лишь некоторые методы и немногие методики. 15 Не следует добиваться высокой точности, если она не требуется, ведь высокая точность обходится очень дорого.
2. Чувствительность. Этим понятием иногда заменяют более строгие термины «предел определения», «нижняя граница определяемых концентраций». Высокочувствительные методики — это те, по которым мы можем обнаружить и определить компонент даже при низком его содержании в исследуемом материале. Чем ниже ожидаемое содержание, тем более чувствительная методика требуется.
3. Селективность. Важно, чтобы на результат анализа не оказывали влияния другие вещества, входящие в состав пробы. Чем меньше таких веществ, чем слабее выражено влияние каждого из них, тем избирательнее методика. Если посторонние вещества вообще не воздействуют на результат анализа, методику называют специфической. Разработать селективную, а тем более специфическую методику анализа очень трудно. Примером может служить методика обнаружения гемоглобина, «созданная» героем одного из произведений А. Конан Дойля. Основным достижением Шерлока Холмса как химика-аналитика стала специфичность разработанной им методики; некий осадок образовывался только в присутствии гемоглобина, что достоверно указывало на наличие следов крови на одежде подозреваемого. На самом деле специфические и высокочувствительные методики обнаружения следов крови появились лишь в середине XX в. С их помощью теперь можно установить, принадлежит обнаруженная кровь человеку или животному, может она принадлежать подозреваемому или нет и т. п.
4. Экспрессность. Речь идет о продолжительности анализа одной пробы — от пробоотбора до выдачи заключения. Чем быстрее будут получены результаты, тем лучше.
5. Стоимость. Эта характеристика методики не требует комментариев. В массовом масштабе можно применять лишь относительно недорогие анализы. Стоимость аналитического контроля в промышленности обычно не превышает 1 % стоимости продукции. Очень дорого стоят уникальные по сложности и редко выполняемые анализы.
Существуют и другие требования к методике — безопасность выполнения анализа, возможность проводить анализ без непоредственного участия человека, устойчивость результатов к случайным колебаниям условий и т. п.
Для наиболее распространенных и часто выполняемых анализов методики изложены в специальных нормативных документах, например государственных стандартах (ГОСТах). В стандартных методиках используют распространенные приборы, общеизвестные способы расчета, привычные приемы анализа. Периодически (один раз в 5–10 лет) ГОСТы обновляют и утверждают заново.
Отбор средней пробы. Это очень важная стадия анализа. С отбора проб начинается проведение химического анализа. Техника отбора средней пробы описывается в специальных инструкциях, ГОСТах. Нужно найти такую пробу по составу, чтобы она отвечала действительному среднему составу анализируемого вещества. Особенно трудно выбрать среднюю пробу твердого вещества. В этом случае используются следующие действия размалывание, высверливание, распиливание, дробление.
При санитарно-эпидемиологической экспертизе отбор проб пищевых продуктов проводит, как правило, врач по гигиене питания, при его отсутствии — помощник санитарного врача. При производственном контроле его проводит специально обученный работник данного предприятия, имеющий свидетельство о прохождении обучения.
Порядок отбора проб пищевых продуктов при экспертизе партии включает выделение однородной партии, определение числа и отбор точечных проб, составление объединенной пробы и формирование из нее средней, которая направляется на лабораторные исследования. Экспертиза партии проводится в соответствии с действующей инструкцией о порядке проведения гигиенической экспертизы пищевых продуктов в учреждениях госсанэпидслужбы. Пример отбора и хранения проб представлен на рис. 1.1.
Рис. 1.1. Отбор и хранение проб тканей и кормов
Измерения в аналитической химии
Результаты количественного химического анализа оценивают такими метрологическими характеристиками, как правильность, воспроизводимость и точность.
Правильность — качество измерений, отражающее близость к нулю систематических погрешностей.
Воспроизводимость — качество измерений, выполненных в различных условиях, но свидетельствующих о близости результатов друг другу.
Точность — качество измерений, показывающее близость их результатов к истинному значению измеряемой величины. Точность измерения соответствует малым погрешностям всех видов. Количественно она выражается обратной величиной модуля относительной погрешности. Погрешность в расчетах приводит к получению неверных результатов химического анализа. Кроме того, есть еще погрешность (ошибка) измерений (∆). Это отклонение результата измерения (Х) от истинного значения измеряемой величины (μ). Абсолютная погрешность определяется по формуле:
относительная погрешность (%) — по формуле
Истинное значение можно получить путем анализа образца множеством различных независимых методов анализа. Анализ его проводят в форме межлабораторного эксперимента (проводится анализ разными лабораториями). Затем проводят оценку массива данных. Также можно использовать стандартный образец (с известным содержанием компонента) для анализа.
Если погрешность при повторных измерениях остается постоянной, то это систематическая погрешность (имеет знак плюс или минус). Если погрешность изменяется случайным образом, то это случайная погрешность (имеет знак и плюс, и минус). Грубые погрешности, существенно отличающиеся от истинного значения, называются грубой ошибкой.
Все погрешности зависят от класса точности прибора и от профессионализма химика-аналитика. Применение статистической обработки образцов рассмотрим на примере анализа пробы сточной воды. Трижды было определено содержание фенола стандартной методикой (DIN 38 409 H 16). Найдено среднее значение содержания фенола в пробе (0,51 гл). Предельно допустимая концентрация фенола в сточных водах в странах ЕС составляет 0,5 гл. Можно ли сказать, что концентрация превышена Статистические тесты помогут учесть степень разброса данных.
Предел обнаружения — минимальная концентрация вещества, которая может быть обнаружена методом. Возможность обнаружения вещества с помощью любой аналитической методики ограничена. Особенно это важно при определении следовых количеств веществ.
Основной химической величиной является количество вещества (n), а основной единицей измерения — моль. По определению, 1 моль — количество вещества, содержащее столько частиц, сколько атомов содержится в 0,012 кг изотопно чистого простого вещества 12 C. Оно составляет приблизительно 6,02214·10 23 частиц. Таким образом, по смыслу количество вещества есть число частиц, составляющих вещество. Эту величину не следует отождествлять ни с массой, ни с объемом, ни с какими иными физическими характеристиками.
Наряду с количеством вещества в химии широко используют и производные от него величины. Важнейшая из них — концентрация (c), представляющая собой количество вещества (n) в единице объема V:
Единица измерения концентрации — моль/л. В дальнейшем все химические величины, как само количество вещества, так и производные от него, мы будем обозначать собирательным термином «содержание».
При проведении анализа часто компонент переводится в раствор. Состав раствора количественно выражается через относительные величины — доли (массовые, мольные, молярные) и размерные величины — концентрации.
Массовая доля — безразмерная относительная величина, равная отношению массы компонента к общей массе образца, раствора, смеси веществ.
Единицей измерения массовой доли является также процент (сотая доля числа — %), промилле (тысячная доля числа, 110 доля процента — ‰), ppm (миллионная доля числа), ppb (миллиардная доля числа).
1‰ = 0,1 %, 1 ppm = 10 –4 %, 1 ppb = 10 –7 %.
Концентрация показывает отношение массы или количества растворенного вещества к объему раствора или массе растворителя.
Химический эквивалент
Это условная частица, которая может присоединять или высвобождать один ион водорода в кислотно-основных реакциях или один электрон в окислительно-восстановительной реакции. Под частицей понимается молекула, ион, электрон и т. д. Фактор эквивалентности f показывает, какая доля реальной частицы вещества эквивалентна одному иону водорода в реакции или одному электрону в окислительно-восстановительной реакции. Рассмотрим реакцию:
Фактор эквивалентности соляной кислоты f экв (HCl) = 1, f экв (Na2CO3) =12.
Для окислительно-восстановительной реакции:
Для реакций комплексообразования фактор эквивалентности определяют из числа координационных мест у комплексообразователя:
Масса одного моль-эквивалента сложного вещества (Мэ), называемая молярной массой эквивалента, равна молярной массе вещества М, деленной на число реакционноспособных химических связей (n х.св):
Число реакционноспособных химических связей n х.св в зависимости от класса соединения можно определить следующим образом:
— для кислот — число протонов (n H +);
— для оснований — число гидроксильных групп (n OH –);
— для солей — произведение числа катионов на его заряд (nkt * Zkt).
Эквивалентность реагирующих и образующихся веществ отражает закон эквивалентов.
Титр раствора
Титр раствора характеризует его концентрацию. Это масса вещества в 1 мл раствора
Т = m в-ва / V р-р, г/мл.
Например, титр раствора соляной кислоты Т(HCl) = 0,003648 г/мл показывает, что в 1 мл раствора кислоты содержится 0,003648 г HCl.
Запись Т(HCl/NaOH) = 0,004000 г/мл означает, что 1 мл раствора кислоты реагирует с 0,004000 г NaOH.
Титр (Т) раствора вещества связан с молярной концентрацией вещества в растворе:
Таким образом, использование законов аналитической химии позволяет разрабатывать и идентифицировать состав пищевых продуктов, устанавливать механизм их воздействия на организм человека. Необходимость количественной и качественной оценки питания обусловлена его влиянием на здоровье и работоспособность человека. При количественной оценке суточного рациона определяется не его объем, а энергия, высвобождающаяся при метаболизме в организме основных пищевых веществ. Качественная характеристика рациона исходит из содержания в нем отдельных пищевых веществ (белков, жиров, углеводов, витаминов, минеральных веществ) и их соотношений. Только при количественной достаточности и благоприятных соотношениях пищевых веществ обеспечиваются наиболее полное проявление их биологических свойств и максимальное использование, а также оптимальное течение обменных процессов.