Что значит разбавленная серная кислота
Серная кислота
Обладает выраженным дегидратационным (водоотнимающим) действием. При попадании на кожу или слизистые оболочки приводит к тяжелым ожогам.
Получение
Известны несколько способов получения серной кислоты. Применяется промышленный (контактный) способ, основанный на сжигании пирита, окислении образовавшегося SO2 до SO3 и последующим взаимодействием с водой.
Нитрозный способ получения основан на взаимодействии сернистого газа с диоксидом азота IV в присутствии воды. Он состоит из нескольких этапов:
В окислительной башне смешивают оксиды азота (II) и (IV) с воздухом:
Смесь газов подается в башни, орошаемые 75-ной% серной кислотой, здесь смесь оксидов азота поглощается с образованием нитрозилсерной кислоты:
В ходе гидролиза нитрозилсерной кислоты получают азотистую кислоту и серную:
В упрощенном виде нитрозный способ можно записать так:
Химические свойства
В водном растворе диссоциирует ступенчато.
С солями реакция идет, если в результате выпадает осадок, образуется газ или слабый электролит (вода). Серная кислота, как и многие другие кислоты, способна растворять осадки.
Подчеркну, что реакции разбавленной серной кислоты с железом и хромом не сопровождаются переходом этих элементов в максимальную степень окисления. Они окисляются до +2.
Cu + H2SO4(разб.) ⇸ (реакция не идет, медь не может вытеснить водород из кислоты)
Холодная концентрированная серная кислота пассивирует Al, Cr, Fe, Ni, Be, Co. При нагревании или амальгамировании данных металлов реакция идет.
Обратите особое внимание, что при реакции железа, хрома с концентрированной серной кислотой достигается степень окисления +3. В подобных реакциях с разбавленной серной кислотой (написаны выше) достигается степень окисления +2.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Серная кислота
Серная кислота
Строение молекулы и физические свойства
Серная кислота H2SO4 – это сильная кислота, двухосновная, прочная и нелетучая. При обычных условиях серная кислота – тяжелая маслянистая жидкость, хорошо растворимая в воде.
Растворение серной кислоты в воде сопровождается выделением значительного количества кислоты. Поэтому по правилам безопасности в лаборатории при смешивании серной кислоты и воды мы добавляем серную кислоту в воду небольшими порциями при постоянном перемешивании.
Валентность серы в серной кислоте равна VI.
Способы получения
1. Серную кислоту в промышленности производят из серы, сульфидов металлов, сероводорода и др. Один из вариантов — производство серной кислоты из пирита FeS2.
Основные стадии получения серной кислоты :
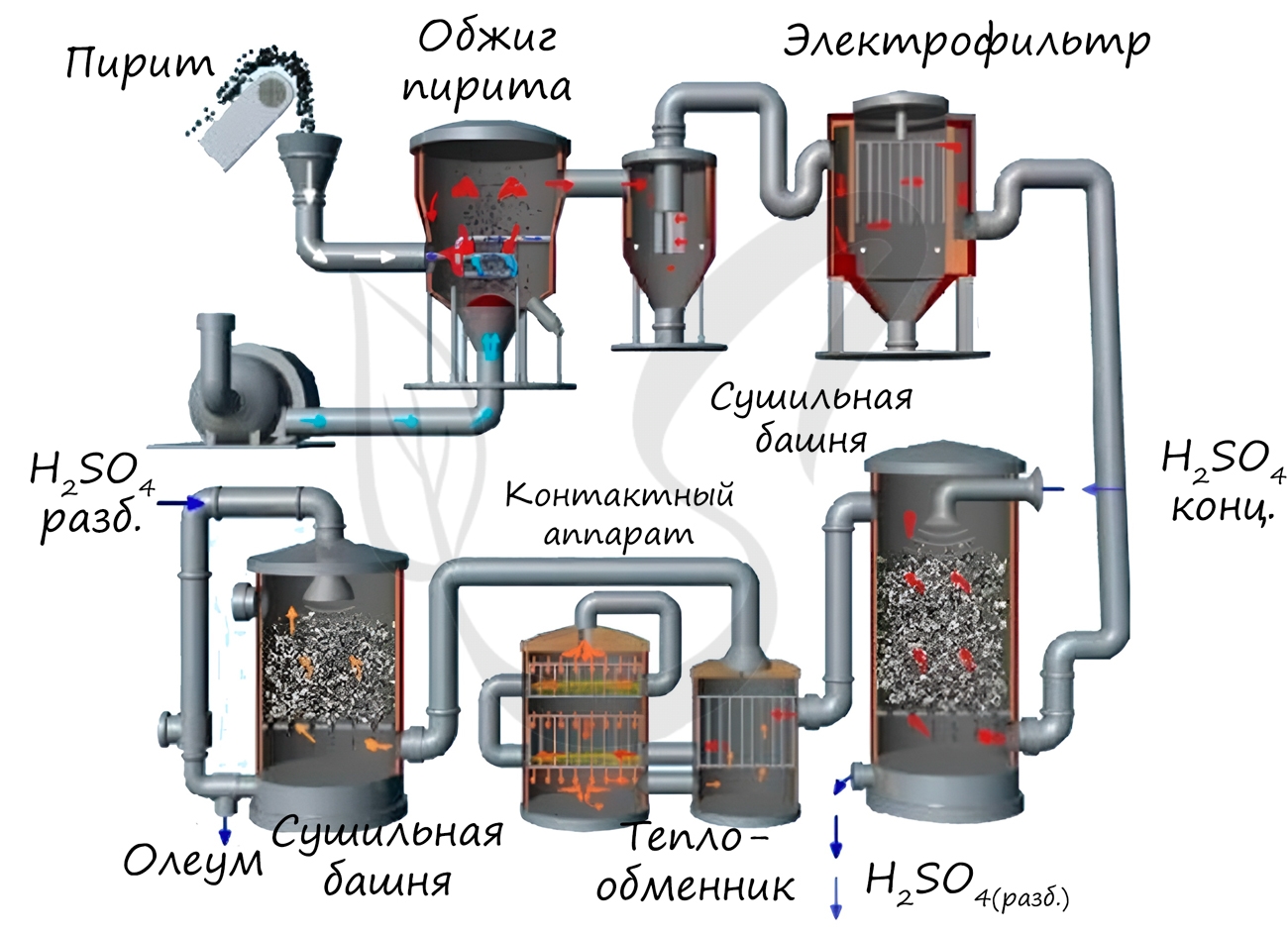
Рассмотрим основные аппараты, используемые при производстве серной кислоты из пирита (контактный метод):
| Аппарат | Назначение и уравнения реакций |
| Печь для обжига | 4FeS2 + 11O2 → 2Fe2O3 + 8SO2 + Q Измельченный очищенный пирит сверху засыпают в печь для обжига в «кипящем слое». Снизу (принцип противотока) пропускают воздух, обогащенный кислородом, для более полного обжига пирита. Температура в печи для обжига достигает 800 о С |
| Циклон | Из печи выходит печной газ, который состоит из SO2, кислорода, паров воды и мельчайших частиц оксида железа. Такой печной газ очищают от примесей. Очистку печного газа проводят в два этапа. Первый этап — очистка газа в циклоне. При этом за счет центробежной силы твердые частички ссыпаются вниз. |
| Электрофильтр | Второй этап очистки газа проводится в электрофильтрах. При этом используется электростатическое притяжение, частицы огарка прилипают к наэлектризованным пластинам электрофильтра). |
| Сушильная башня | Осушку печного газа проводят в сушильной башне – снизу вверх поднимается печной газ, а сверху вниз льется концентрированная серная кислота. |
| Теплообменник | Очищенный обжиговый газ перед поступлением в контактный аппарат нагревают за счет теплоты газов, выходящих из контактного аппарата. |
| Контактный аппарат | 2SO2 + O2 ↔ 2SO3 + Q В контактном аппарате производится окисление сернистого газа до серного ангидрида. Процесс является обратимым. Поэтому необходимо выбрать оптимальные условия протекания прямой реакции (получения SO3): Как только смесь оксида серы и кислорода достигнет слоев катализатора, начинается процесс окисления SO2 в SO3. Образовавшийся оксид серы SO3 выходит из контактного аппарата и через теплообменник попадает в поглотительную башню. |
| Поглотительная башня | Получение H2SO4 протекает в поглотительной башне. Однако, если для поглощения оксида серы использовать воду, то образуется серная кислота в виде тумана, состоящего из мельчайших капелек серной кислоты. Для того, чтобы не образовывался сернокислотный туман, используют 98%-ную концентрированную серную кислоту. Оксид серы очень хорошо растворяется в такой кислоте, образуя олеум: H2SO4·nSO3. Образовавшийся олеум сливают в металлические резервуары и отправляют на склад. Затем олеумом заполняют цистерны, формируют железнодорожные составы и отправляют потребителю. |
Общие научные принципы химического производства:
Химические свойства
1. Серная кислота практически полностью диссоциирует в разбавленном в растворе по первой ступени:
По второй ступени серная кислота диссоциирует частично, ведет себя, как кислота средней силы:
HSO4 – ⇄ H + + SO4 2–
2. Серная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Еще пример : при взаимодействии серной кислоты с гидроксидом калия образуются сульфаты или гидросульфаты:
Серная кислота взаимодействует с амфотерным гидроксидом алюминия:
3. Серная кислота вытесняет более слабые из солей в растворе (карбонаты, сульфиды и др.). Также серная кислота вытесняет летучие кислоты из их солей (кроме солей HBr и HI).
Или с силикатом натрия:
Концентрированная серная кислота реагирует с твердым нитратом натрия. При этом менее летучая серная кислота вытесняет азотную кислоту:
4. Т акже серная кислота вступает в обменные реакции с солями.
5. Разбавленная серная кислота взаимодействует с металлами, которые расположены в ряду активности металлов до водорода. При этом образуются соль и водород.
Серная кислота взаимодействует с аммиаком с образованием солей аммония:
Железо Fe, алюминий Al, хром Cr пассивируются концентрированной серной кислотой на холоде. При нагревании реакция возможна.
При взаимодействии с неактивными металлами концентрированная серная кислота восстанавливается до сернистого газа:
При взаимодействии с щелочноземельными металлами и магнием концентрированная серная кислота восстанавливается до серы:
При взаимодействии с щелочными металлами и цинком концентрированная серная кислота восстанавливается до сероводорода:
6. Качественная реакция на сульфат-ионы – взаимодействие с растворимыми солями бария. При этом образуется белый кристаллический осадок сульфата бария:
Видеоопыт взаимодействия хлорида бария и сульфата натрия в растворе (качественная реакция на сульфат-ион) можно посмотреть здесь.
7. Окислительные свойства концентрированной серной кислоты проявляются и при взаимодействии с неметаллами.
Уже при комнатной температуре концентрированная серная кислота окисляет галогеноводороды и сероводород:
Урок №14. Серный ангидрид и серная кислота
Повторите темы уроков 9 класса:
Оксид серы (VI)
Оксид серы (VI) – это кислотный оксид. При обычных условиях – бесцветная ядовитая жидкость, «дымит» на воздухе, поглощая пары воды.
Способы получения
Оксид серы (VI) получают в реакциях окисления:
SO 2 + NO 2 = SO 3 + NO
Разложением сульфата железа (III):
Химические свойства оксида серы (VI)
1. Оксид серы (VI) активно поглощает влагу и реагирует с водой с образованием серной кислоты:
2. Серный ангидрид – типичным кислотный оксид, взаимодействует с щелочами и основными оксидами.
SO 3 + 2NaOH ( избыток) = Na 2 SO 4 + H 2 O
SO 3 + NaOH ( избыток) = NaHSO 4
SO 3 + MgO = t = MgSO 4
3. Серный ангидрид – очень сильный окислитель:
SO 3 + 2KI = I 2 + K 2 SO 3
3SO 3 + H 2 S = 4SO 2 + H 2 O
5SO 3 + 2P = P 2 O 5 + 5SO 2
4. Растворяется в концентрированной серной кислоте, образуя олеум – раствор SO 3 в H 2 SO 4
РЕАКЦИИ СЕРНОЙ КИСЛОТЫ
Химические свойства разбавленной серной кислоты
1) Диссоциация протекает ступенчато:
(первая ступень, образуется гидросульфат – ион)
(вторая ступень, образуется сульфат – ион)
2) Взаимодействие с металлами:
Разбавленная серная кислота растворяет только металлы, стоящие в ряду напряжений левее водорода:
Zn 0 + H 2 +1 SO 4 (разб) → Zn +2 SO 4 + H 2 0 ↑
Zn 0 + 2H + → Zn 2+ + H 2 0 ↑
3) Взаимодействие с основными и амфотерными оксидами:
CuO + H 2 SO 4 → CuSO 4 + H 2 O
CuO + 2H + → Cu 2+ + H 2 O
4) Взаимодействие с основаниями:
H 2 SO 4 + 2NaOH → Na 2 SO 4 + 2H 2 O
Если кислота в избытке, то образуется кислая соль:
H 2 SO 4 + NaOH → NaНSO 4 + H 2 O
H 2 SO 4 + Cu(OH) 2 → CuSO 4 + 2H 2 O
2H + + Cu(OH) 2 → Cu 2+ + 2H 2 O
5) Обменные реакции с солями:
Серная кислота – сильная нелетучая кислота, вытесняет из солей другие менее сильные кислоты:
MgCO 3 + H 2 SO 4 → MgSO 4 + H 2 O + CO 2 ↑
MgCO 3 + 2H + → Mg 2+ + H 2 O + CO 2 ↑
Н 2 SO 4 + 2NaHCO 3 = Na 2 SO 4 + CO 2 ↑ + H 2 O
H 2 SO 4 + Na 2 SiO 3 = Na 2 SO 4 + H 2 SiO 3 ↓
Качественная реакция на сульфат-ион
BaCl 2 + H 2 SO 4 → BaSO 4 ↓ + 2HCl
Ba 2+ + SO 4 2- → BaSO 4 ↓
Образование белого осадка BaSO 4 (нерастворимого в кислотах) используется для идентификации серной кислоты и растворимых сульфатов.
6) Реагирует с аммиаком
Химические свойства концентрированной серной кислоты
1. С водой образуются гидраты:
H 2 SO 4 + nH 2 O = H 2 SO 4 ·nH 2 O + Q
Органические вещества обугливаются!
2H 2 SO 4 + C = CO 2 + 2SO 2 + 2H 2 O
2. Серная кислота окисляет неметаллы
неМе + H 2 SO 4 (конц.) = H 2 O + SO 2 + Кислотный гидроксид
, где степень окисления неметалла – высшая
C + 2H 2 SO 4 = 2H 2 O + CO 2 + 2SO 2
S + 2H 2 SO 4 = 3SO 2 + 2H 2 O
2P + 5H 2 SO 4 = 2H 3 PO 4 + 5SO 2 + 2H 2 O
3. Взаимодействие серной кислоты с металлами
H 2 SO 4 (конц.) + Me = t = соль + H 2 O + Х
Железо Fe, алюминий Al, хром Cr пассивируются концентрированной серной кислотой на холоде. При нагревании образуется газа SO 2 :
6H 2 SO 4 (конц.) + 2Fe = t = Fe 2 (SO 4 ) 3 + 3SO 2 + 6H 2 O
6H 2 SO 4(конц.) + 2Al = t = Al 2 (SO 4 ) 3 + 3SO 2 + 6H 2 O
При взаимодействии с неактивными металлами концентрированная серная кислота восстанавливается до сернистого газа:
2H 2 SO 4 (конц.) + Cu = CuSO 4 + SO 2 ↑ + 2H 2 O
2H 2 SO 4 (конц.) + Hg = HgSO 4 + SO 2 ↑ + 2H 2 O
2H 2 SO 4 (конц.) + 2Ag = Ag 2 SO 4 + SO 2 ↑ + 2H 2 O
При взаимодействии с щелочноземельными металлами и магнием концентрированная серная кислота восстанавливается до серы:
3Mg + 4H 2 SO 4 = 3MgSO 4 + S + 4H 2 O
При взаимодействии со щелочными металлами и цинком концентрированная серная кислота восстанавливается до сероводорода:
5H 2 SO 4 (конц.) + 4Zn = 4ZnSO 4 + H 2 S↑ + 4H 2 O
4. Взаимодействие с восстановителями
Концентрированная серная кислота окисляет галогеноводороды и сероводород при комнатной температуре:
3H 2 SO 4 (конц.) + 2KBr = Br 2 ↓ + SO 2 ↑ + 2KHSO 4 + 2H 2 O
5H 2 SO 4 (конц.) + 8KI = 4I 2 ↓ + H 2 S↑ + K 2 SO 4 + 4H 2 O
H 2 SO 4 (конц.) + 3H 2 S = 4S↓ + 4H 2 O
СОЛИ СЕРНОЙ КИСЛОТЫ
1) Разложение сульфатов
Термически устойчивые сульфаты – сульфаты щелочных металлов (в том числе лития), они плавятся не разлагаясь
Остальные сульфаты при нагревании разлагаются на оксид серы(IV), оксид металла и кислород:
2CuSO 4 = t = 2CuO + SO 2 + O 2 (SO 3 )
2Al 2 (SO 4 ) 3 = t = 2Al 2 O 3 + 6SO 2 + 3O 2
2ZnSO 4 = t = 2ZnO + SO 2 + O 2
2Cr 2 (SO 4 ) 3 = t = 2Cr 2 O 3 + 6SO 2 + 3O 2
4FeSO 4 = t = 2Fe 2 O 3 + 4SO 2 + O 2
Так как оксиды тяжёлых и благородных металлов разлагаются сами, разложение их сульфатов следует записывать до металла:
Ag 2 SO 4 = t = 2Ag + SO 2 + O 2
HgSO 4 = t = Hg + SO 2 + O 2
2) Сульфаты проявляют окислительные свойства и могут взаимодействовать с восстановителями, восстанавливаясь до сульфидов.
CaSO 4 + 4C = CaS + 4CO
3) Многие средние сульфаты образуют устойчивые кристаллогидраты
Na 2 SO 4 ∙ 10H 2 O − глауберова соль
CaSO 4 ∙ 2H 2 O − гипс
CuSO 4 ∙ 5H 2 O − медный купорос
FeSO 4 ∙ 7H 2 O − железный купорос
ZnSO 4 ∙ 7H 2 O − цинковый купорос
Na 2 CO 3 ∙ 10H 2 O − кристаллическая сода
Серная кислота. Свойства серной кислоты.
Серная кислота H2SO4 – нелетучая тяжелая жидкость, хорошо растворима в воде (при нагревании). tпл. = 10,3°C, tкип. = 296°С,
Отлично впитывает влагу, поэтому часто выступает в качестве осушителя.
Производство серной кислоты представляет собой контактный процесс. Его можно разделить на 3 этапа:
1. Получение SO2 путем сжигания серы или обжигом сульфидов.
3. Поглощение SO3 серной кислотой, в результате чего образуется 100% серная кислота (олеум):
Воду использовать нельзя из-за образования тумана.
Химические свойства серной кислоты.
Серная кислота H2SO4 – двухосновная кислота, которая обладает большой силой. В воде она диссоциирует ступенчато:
Разбавленная серная кислота реагирует только с металлами, стоящими в ряду напряжения до водорода:
В реакциях с щелочами или основными оксидами образует сульфаты или гидрофильфаты:
Необходимо отметить, что сульфат бария является нерастворимым сульфатом, поэтому его используют в качестве индикатора на присутствие сульфат-ионов.
Концентрированная H2SO4 окисляет медь, серебро, углерод и фосфор:
Концентрированная H2SO4 при обычных условиях не взаимодействует с Al, Cr, Fe, но при нагревании вступает в реакцию.
Концентрированная H2SO4 быстро вступает в реакцию с водой, выделяя пр этом огромное количество тепла.
Серная кислота — Все что необходимо знать
Вещество серная кислота – токсичный и смертельно опасный реагент. Но без него современное человечество обойтись не может. используют при производстве лекарственных препаратов, химической продукции, металлургии, удобрений, нефтепродуктов. Вещество не имеет особого запаха, бесцветно, вязкой консистенции, но имеет привкус меди. Отлично взаимодействует с водой в любых пропорциях. Из-за хорошего взаимодействия с другими веществами и водой имеет неофициальное название «кровь химии».
Где применяется серная кислота
За год во всем мире используют более 200 миллионов тонн вещества. В основном оно уходит на производство удобрений и химической продукции:
Разбавленная серная кислота – 7 типов солей
Серная кислота используется в концентрированном виде и в виде растворов точнее солей. Смеси различных химических веществ:
Еще разбавленная серная кислота используется при производстве аккумуляторов в виде дистиллята. Так же такой вид раствора как Олеум. Он чаще всего необходим для транспортировки, так как не воздействует со сталью в отличие от концентрированной серной кислоты.
История. Кто начал использовать раствор серной кислоты
Всем, кто имеет дачный участок или дом в деревне известен медный купорос. Изучением и производством растворов с содержанием серной кислоты активно начали заниматься в 13 веке. Химики того времени придумали нагревать алюмокалиевые квасцы. В 15 веке химики продвинулись и придумали «купоросное масло». В 16 веке Иоганн Глаубер придумал другой способ добычи вещества. С помощью горения нитрата калия серы в присутствии водных паров, он получил Серную кислоту. Уже в это время Серную кислоту использовали химики, фармацевты и ювелиры.
В дальнейшем в Англии ученый Джон Робак решил удешевить производство и заменил стеклянные резервуары на освинцованные. Этим способом он получал 65% раствор вещества Н2SO4.
Современный метод добычи открыли в 19 веке. Он получил название «Нитрозный». К концу 19 века в Европе выпускали за год 1 миллион тонн серной кислоты.
В России первые фабрики по производству открылись в Москве в 1805 году.
Как производят серную кислоту в наше время
На сегодняшний день используют два метода Контактный и Нитрозный.
Контактный метод используется по всему миру. Его распространённость обусловлена следующими преимуществами:
При Контактном методе используют следующие виды сырья:
Пирит измельчают для ускорения прохождения химической реакции. Далее измельченные пирит смешивают с водой. Это позволяет удалить не нужные примеси, они остаются на поверхности. Далее под воздействием высокой температуры (800 °C) вода испаряется не нужные взвеси сгорают. Далее Добавляют катализатор и уменьшают температуру (420-550 °C) Происходит процесс окисления и диоксид серы превращается в ангидрид серной кислоты. Далее в поглотительной башне ангидрит отделяется и появляется чистая серная кислота. В процессе производства вырабатывается огромное количество тепла, которое используют как вспомогательный источник энергии. При использовании данного метода получения Н2SO4 почти нет отходов.
Нитрозный метод представлен в двух вариантах камерный и башенный. При его использовании получится 75% серная кислота. В составе остается железо оксид азота, и иных примесей. Данный способ вреден для экологии, но до сих пор достаточно часто применяется, так как он проще и дешевле Контактного метода.
Основные производители серной кислоты в России
В России ежегодно производят около 10 миллионов тонн серной кислоты. Заводы представляют собой комплекс различных производств и поэтому в основном самостоятельно перерабатывают почти все полученное вещество. В основном это производители удобрений, но так же выпускают следующие виды серной кислоты:
Основные крупнейшие производители серной кислоты в России:
Не маловажную роль играют поставщики вещества пирит. В России их добывают на двух горно-обогатительных комбинатах Талнахский и Норильский.
Транспортировка вещества серная кислота
Серная кислота вещество повышенной опасности и требует определенных мер при транспортировке. Вещество взрывоопасно и имеет 8 класс опасности в перевозке грузов. В случае ошибки водителя и аварии велика вероятность разлива серной кислоты и нанесения вреда экологии.
Поэтому для перевозки опасных грузов требуются особе правила. Подпирается специальная устойчивая емкость для перевозки. Цистерны или специальные бочки и ёмкости, которые изготовлены из определённых сплавов, на которые не оказывает воздействие кислоты и яды.
Транспорт обязательно должен иметь соответствующую маркировку предупреждающую других водителей об опасном грузе. Водитель проходит специальное обучение и получает свидетельство АДР. Для каждой транспортировки разрабатывается специальный маршрут следования, которые исключает места большого количества людей и крупные производственные объекты. Чтобы избежать экологической катастрофы в случае ДТП и воздействия опасных химических веществ на людей.
В чем опасность серной кислоты для человека
Н2SO4 очень токсичное вещество. Легко растворяется в воде и вступает в контакт с другими химическими веществами. В чистом виде сильно поглощает влагу и может распространиться в газообразной форме, в случае аварии на производстве или при транспортировке. Серная кислота в большой концентрации взрывоопасна.
В случае если на человека попадут капли вещества на кожу либо он вдохнет пары или что еще хуже каким-то образом выпьет даже несколько капель последствия могут очень плачевными. Серная кислота очень агрессивна плюс в её состав входит мышьяк, который усиливает отравление организма человека. Но существует безвредная доза серной кислоты, содержащаяся в воздухе, 0.3мг на 1 кв. метр. При воздействии серной кислоты на человека часто возникает трахеит, бронхит, ларингит. Если кислота попала на кожный покров, то кожа разъедается, и рана очень долго заживает. При этом если не обратиться за профессиональной медицинской помощью место ожога может разрастись и привести к летальному исходу пострадавшего. Какие признаки отравления серной кислотой бывают:
Последний пункт очень опасный симптом. Человек в этом случае очень близок к удушью и летальному исходу.
Варианты первой помощи при отравлении серной кислотой
Если вы находитесь в зоне, где в воздухе скапливается серная кислота, необходимо немедленно выйти на чистый воздух. Далее обратиться к мед. работникам, вызвать скорую помощь. В момент ожидание помощи, можно попробовать облегчить свое состояние после отравления серной кислотой. Если раствор вещества попал внутрь, то нужно сделать промывание желудка большим количеством теплой воды. Если Н2SO4 попало на слизистую, то необходимо сразу промыть ее чистой водой в большом количестве. Дальнейшую помощь и последующее лечение окажут профессиональные сотрудники мед. учреждений. Самолечение невозможно, так как это может привести к ухудшению состояния человека и к летальному исходу.
Ликвидация разлива серной кислоты
В случае аварии на производстве либо в момент транспортировки может произойти возгорание или разлив серной кислоты. Устранение аварии производят в специальных костюмах химической защиты, например, изолирующие костюмы Стрелец. Газоспасатели в костюмах химзащиты эвакуируют пострадавших в безопасную зону. Устраняют течь и с помощью большого количества воды гасят серную кислоту. В дальнейшем собирают жидкость в специальные емкости и утилизируют. Газоспасателям оказывают помощь пожарные, им так же приходится работать в костюмах химзащиты.