Что такое cuso4 в химии
Сульфат меди и медный купорос, характеристика, свойства и химические реакции
Сульфат меди и медный купорос, характеристика, свойства и химические реакции.
Сульфат меди – неорганическое вещество, имеет химическую формулу CuSO4.
Краткая характеристика сульфата меди:
Сульфат меди – неорганическое вещество белого цвета.
Химическая формула сульфата меди CuSO4.
Сульфат меди – неорганическое химическое соединение, соль серной кислоты и меди.
С водой сульфат меди образует кристаллогидраты: пентагидрат сульфата меди CuSO4·5H2O, именуемый также медный купорос, тетрагидрат сульфата меди CuSO4·4H2O, тригидрат сульфата меди CuSO4·3H2O, гидрат сульфата меди CuSO4·H2O.
Растворим также в глицерине, метаноле, этиленгликоле. Не растворим в ацетоне, этаноле.
Сульфат меди негорюч, пожаро- и взрывобезопасен.
Сульфат меди является пищевой добавкой Е519.
В природе сульфат меди встречается в виде минералов халькантита (CuSO4·5H2O), халькокианита (CuSO4), бонаттита (CuSO4·3H2O), бутита (CuSO4·7H2O) и в составе некоторых других минералов.
Краткая характеристика медного купороса:
Медный купорос – неорганическое вещество синего цвета различных оттенков.
Химическая формула медного купороса CuSO4·5H2O.
Медный купорос – пентагидрат сульфата меди.
Хорошо растворяется в воде. Растворим также в глицерине, метаноле, этаноле, этиленгликоле.
На воздухе постепенно выветривается (теряет кристаллизационную воду).
Медный купорос негорюч, пожаро- и взрывобезопасен.
Медный купорос относится к веществам 2-го класса опасности в соответствии с ГОСТ 12.1.007.
Физические свойства сульфата меди:
| Наименование параметра: | Значение: |
| Химическая формула | CuSO4 |
| Синонимы и названия иностранном языке | copper(II) sulphate (сopper(II) sulfate (англ.) |
халькокианит (рус.)
Физические свойства медного купороса:
| Наименование параметра: | Значение: |
| Химическая формула | CuSO4·5H2O |
| Синонимы и названия иностранном языке | sodium sulfate (англ.) |
copper(II) sulfate pentahydrate (англ.)
меди(II) сульфат пентагидрат (рус.)
медный купорос (рус.)
медь сернокислая пятиводная (рус.)
халькантит (рус.)
Химические свойства сульфата меди. Химические реакции сульфата меди и кристаллогидратов меди:
1. реакция сульфата меди и железа :
2. реакция сульфата меди и цинка :
В результате реакции образуются сульфат цинка и медь.
3. реакция сульфата меди и олова :
В результате реакции образуются сульфат олова и медь.
4. реакция взаимодействия сульфата меди, меди и хлорида натрия:
CuSO4 + Cu + 2NaCl → 2CuCl + Na2SO4 (t = 70 °C).
В результате реакции образуются хлорид меди и сульфат натрия.
5. реакция взаимодействия сульфата меди и аммиака :
В результате реакции образуется сульфат тетраамминмеди (II).
6. реакция взаимодействия сульфата меди и гидроксида натрия:
7. реакция взаимодействия сульфата меди и гидроксида калия:
В результате реакции образуются сульфат калия и гидроксид меди.
8. реакция взаимодействия сульфата меди и гидроксида лития:
В результате реакции образуются сульфат лития и гидроксид меди.
9. реакция взаимодействия сульфата меди и гидроксида кальция:
В результате реакции образуются сульфат кальция и гидроксид меди.
10. реакция взаимодействия сульфата меди и сульфида калия:
В результате реакции образуются сульфат калия и сульфид меди.
11. реакция взаимодействия сульфата меди и хлорида бария:
В результате реакции образуются сульфат бария и хлорид меди.
12. реакция взаимодействия сульфата меди и сульфита натрия:
В результате реакции образуются сульфат натрия и сульфит меди.
13. реакция взаимодействия сульфата меди и сульфата железа (II) :
В результате реакции образуются медь и сульфат железа (III). В ходе реакции используется концентрированный раствор сульфата железа (II).
14. реакция термического разложения сульфата меди:
15. реакция термического разложения кристаллогидратов сульфата меди:
Пентагидрат сульфата меди CuSO4·5H2O разлагается на тетрагидрат сульфата меди CuSO4·4H2O и воду.
Тетрагидрат сульфата меди CuSO4·4H2O разлагается на гидрат сульфата меди CuSO4·H2O и воду.
Гидрат сульфата меди CuSO4·H2O разлагается на сульфат меди CuSO4 и воду.
Применение и использование сульфата меди и медного купороса:
Сульфат меди и медный купорос используется во множестве отраслей промышленности и для бытовых нужд:
– в химической промышленности как исходное сырьё для получения других соединений меди ;
– в сельском хозяйстве медный купорос применяется как антисептик, фунгицид и медно-серное удобрение ;
– в пищевой промышленности в качестве пищевой добавки 519 как фиксатор окраски и консервант;
– в быту для выведения пятен ржавчины на потолке после затоплений.
Примечание: © Фото //www.pexels.com, //pixabay.com
сульфат меди реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие сульфата меди
реакции
CuSO4
Смотреть что такое «CuSO4» в других словарях:
CuSO4 — Kristallstruktur Cu2+ … Deutsch Wikipedia
CuSO4 — Sulfate de cuivre Sulfate de cuivre cristal de sulfate de cuivre hydraté Général Nom IUPAC Sulfate de cuivre (II) … Wikipédia en Français
CuSO4 — Water Wa ter (w[add] t[ e]r), n. [AS. w[ae]ter; akin to OS. watar, OFries. wetir, weter, LG. & D. water, G. wasser, OHG. wazzar, Icel. vatn, Sw. vatten, Dan. vand, Goth. wat[=o], O. Slav. & Russ. voda, Gr. y dwr, Skr. udan water, ud to wet, and… … The Collaborative International Dictionary of English
CuSO4,5H2O — Sulfate de cuivre Sulfate de cuivre cristal de sulfate de cuivre hydraté Général Nom IUPAC Sulfate de cuivre (II) … Wikipédia en Français
МЕДИ СУЛЬФАТ — CuSO4, кристаллы (см. табл.); разлагается ок. 650 °С до CuO, SO2, O2; парамагнетик, магн. восприимчивость + 1,33.10 3, ниже 54,3 К (точка Нееля) антиферромагнетик; показатели преломления: больший … Химическая энциклопедия
МЕДИ СУЛЬФАТ — CuSO4 белый порошок, хорошо растворимый в воде. Образует ярко синий кристаллогидрат CuSO4*5H2O медный купорос. Применяется как протрава при крашении, пигмент, пестицид, антисептик, в гальванотехнике и фотографии; исходный продукт для получения др … Большой энциклопедический политехнический словарь
МЕДИ СУЛЬФАТ — CuSO4, бесцв. кристаллы. Растворяется в воде. Из водных р ров кристаллизуется CuSO4*5H2O медный купорос (ярко синего цвета), к рый применяется в с. х ве (для борьбы с вредителями и для протравливания зерна) и при получении минер. красок … Естествознание. Энциклопедический словарь
МЕДНЫЙ КУПОРОС — CuSO4*5H2O, см. Меди сульфат … Естествознание. Энциклопедический словарь
calcantita — [CuSO4·5H2O] ► femenino MINERALOGÍA Sulfato de cobre hidratado … Enciclopedia Universal
Медь — (хим.) Cu (от лат. Cuprum), атомный вес около 63,3. По некоторым археологическим данным М. была хорошо известна египтянам еще за 4000 лет до Р. Хр. Знакомство человечества с М. относится к более ранней эпохе, чем с железом; это объясняется, с… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Медный купорос ГОСТ 19347-99
| Медный купорос | |
|---|---|
| Систематическое наименование | медный купорос |
| Традиционные названия | пентагидрат: сульфат меди (II), медь сернокислая техническая |
| Хим. формула | CuSO 4 |
| Состояние | кристаллическое |
| Молярная масса | 159,609 (сульфат) 249.685 (пентагидрат) г/моль |
| Плотность | 3,64 г/см³ |
| Твёрдость | 2,5 |
| Т. разл. | выше 650 °C |
| pKa | 5⋅10 −3 |
| Координационная геометрия | Октаэдрическая |
| Кристаллическая структура | безв. — ромбическая пентагидрат — триклинная пинакоидальная тригидрат — моноклинная |
| ГОСТ | ГОСТ 19347-99 |
| Рег. номер CAS | 7758-98-7 |
| PubChem | 24462 |
| Рег. номер EINECS | 231-847-6 |
| SMILES | |
| Кодекс Алиментариус | E519 |
| RTECS | GL8800000 |
| ChEBI | 23414 |
| ChemSpider | 22870 |
| ПДК | в воздухе: мр 0,009, сс 0,004; в воде: 0,001 |
| ЛД50 | крысы, орально: 612,9 мг/кг мыши, орально: 87 мг/кг |
| Токсичность | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Медный купорос (медь сернокислая, сульфат меди (II) ) — неорганическое соединение, медная соль серной кислоты с формулой CuSO 4. Нелетучее вещество, не имеет запаха. В безводном виде — белый порошок, очень гигроскопичное. В виде кристаллогидратов — прозрачные негигроскопичные кристаллы различных оттенков синего с горьковато-металлическим вяжущим вкусом, на воздухе постепенно выветриваются (теряют кристаллизационную воду).
Сульфат меди(II) хорошо растворим в воде. Из водных растворов кристаллизуется голубой пентагидрат CuSO4·5H2O — медный купорос. Токсичность медного купороса для теплокровных животных относительно невысока, в то же время, он высокотоксичен для рыб.
Обладает дезинфицирующими, антисептическими, вяжущими свойствами. Применяется в медицине, в растениеводстве как антисептик, фунгицид или медно-серное удобрение.
Реакция гидратации безводного сульфата меди (II) экзотермическая и проходит со значительным выделением тепла.
Содержание
Нахождение в природе
В природе встречается в виде минералов халькантита (CuSO4·5H2O), халькокианита (CuSO4), бонаттита (CuSO4·3H2O), бутита (CuSO4·7H2O) и в составе некоторых других минералов.
Получение
В промышленности
В промышленности загрязненный сульфат меди(II) получают растворением меди и медных отходов в разбавленной серной кислоте H2SO4 при продувании воздуха:
растворением оксида меди(II) CuO в H2SO4:
сульфатизирующим обжигом сульфидов меди и как побочный продукт электролитического рафинирования меди.
В лабораторных условиях
В лаборатории CuSO4 можно получить действием концентрированной серной кислоты на медь при нагревании:
температура не должна превышать 60 °С, при большей температуре в значительных количествах образуется побочный продукт — сульфид меди(I):
Также в лабораторных условиях сульфат меди (II) может быть получен реакцией нейтрализации гидроксида меди(II) серной кислотой, для получения сульфата меди высокой чистоты используют соответственно чистые реактивы:
Чистый сульфат меди может быть получен следующим образом. В фарфоровую чашку наливают 120 мл дистиллированной воды, прибавляют 46 мл химически чистой серной кислоты плотностью 1,8 г/см 3 и помещают в смесь 40 г чистой меди (например, электролитической). Затем нагревают до 70—80 °С и при этой температуре в течение часа постепенно, порциями по 1 мл, прибавляют 11 мл конц. азотной кислоты. Если медь покроется кристаллами, прибавить 10—20 мл воды. Когда реакция закончится (прекратится выделение пузырьков газа), остатки меди вынимают, а раствор упаривают до появления на поверхности пленки кристаллов и дают остыть. Выпавшие кристаллы следует 2—3 перекристаллизовать из дистиллированной воды и высушить.
Очистка
Очистить загрязненный или технический сульфат меди можно перекристаллизацией — вещество растворяется в кипящей дистиллированной воде до насыщения раствора, после чего охлаждается до приблизительно +5 °С. Полученный осадок кристаллов отфильтровывается. Однако даже многократная перекристаллизация не позволяет избавиться от примеси соединений железа, которые являются наиболее распространенной примесью в сульфате меди.
Для полной очистки медный купорос кипятят с диоксидом свинца PbO2 или пероксидом бария BaO2, пока отфильтрованная проба раствора не покажет отсутствия железа. Затем раствор фильтруют и упаривают до появления на поверхности пленки кристаллов, после чего охлаждают для кристаллизации.
По Н. Шоорлю очистить сульфат меди можно так: к горячему раствору CuSO4 прибавить небольшие количества пероксида водорода H2O2 и гидроксида натрия NaOH, прокипятить и отфильтровать осадок. Выпавшие из фильтрата кристаллы дважды подвергаются перекристаллизации. Полученное вещество имеет чистоту не ниже квалификации «ХЧ».
Глубокая очистка
Для этого готовится водный, насыщенный при 20°С раствор сульфата меди (вода используются только бидистиллированная). В него добавляют перекись водорода в количестве 2-3 мл 30 % раствора на 1 литр, перемешивают, вносят свежеосаждённый основной карбонат меди в количестве 3-5 грамм, нагревают и кипятят 10 минут для разложения H2O2.
Затем раствор охлаждают до 30—35 °С, фильтруют и приливают 15 мл 3%-ного раствора диэтилдитиокарбамата натрия и выдерживают в мешалке три-четыре часа не понижая температуры. Далее раствор быстро процеживают от крупных хлопьев комплексов и вносят активированный уголь БАУ-А на полчаса при перемешивании. Затем раствор следует отфильтровать вакуумным методом.
Дальше в раствор CuSO4 приливают на 1 л около 200 мл насыщенного раствора NaCl квалификации «Ч» и вносят чистый алюминий в проволоке или обрезках до полного прохождения реакции, выделения меди и просветления раствора (при этом выделяется водород). Выделенную медь отделяют от алюминия взбалтыванием, осадок промывают декантацией сперва водой затем заливают горячим 5—10 % раствором соляной кислоты ХЧ при взбалтывании в течение часа и постоянным подогревом до 70—80 °С, затем промывают водой и заливают 10—15%-ной серной кислотой (ОСЧ 20-4) на час с подогревом при том же интервале температур. От степени и тщательности промывания кислотами, а также квалификации применяемых далее реактивов зависит чистота дальнейших продуктов.
После промывки кислотами медь снова моют водой и растворяют в 15—20%-ной серной кислоте (ОСЧ 20-4) без её большого избытка с добавлением перекиси водорода (ОСЧ 15-3). После прохождения реакции полученный кислый раствор сульфата меди кипятят для разложения избытка перекиси и нейтрализуют до полного растворения вначале выпавшего осадка перегнанным 25%-ным раствором аммиака (ОСЧ 25-5) или приливают раствор карбоната аммония, очищенного комплексно-адсорбционным методом до особо чистого.
После выстаивания в течение суток раствор медленно фильтруют. В фильтрат добавляют серную кислоту (ОСЧ) до полного выпадения голубовато-зелёного осадка и выдерживают до укрупнения и перехода в зелёный основной сульфат меди. Зелёный осадок выстаивают до компактности и тщательно промывают водой до полного удаления растворимых примесей. Затем осадок растворяют в серной кислоте, фильтруют, устанавливают рН=2,5—3,0 и перекристаллизовывают два раза при быстром охлаждении, причем при охлаждении раствор каждый раз перемешивают для получения более мелких кристаллов сульфата меди. Выпавшие кристаллы переносят на воронку Бюхнера и удаляют остатки маточного раствора с помощью водоструйного насоса. Третья кристаллизация проводится без подкисления раствора с получением чуть более крупных и оформленных кристаллов.
Физические свойства
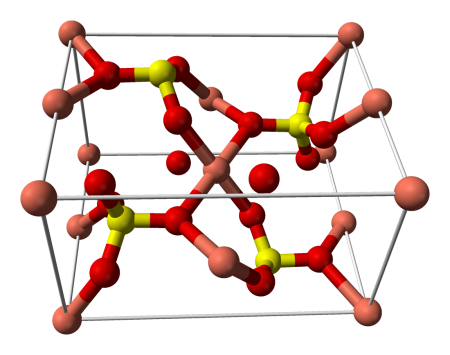
Строение кристаллогидрата
Структура медного купороса приведена на рисунке. Как видно, вокруг иона меди координированы два аниона SO4 2− по осям и четыре молекулы воды (в плоскости), а пятая молекула воды играет роль мостиков, которые при помощи водородных связей объединяют молекулы воды из плоскости и сульфатную группу.
Термическое воздействие
При нагревании пентагидрат последовательно отщепляет две молекулы воды, переходя в тригидрат CuSO4·3H2O (этот процесс, выветривание, медленно идёт и при более низких температурах [в том числе при 20—25 °С]), затем в моногидрат (при 110 °С) CuSO4·H2O, и выше 258 °C образуется безводная соль.
Выше 650 °C становится интенсивным пиролиз безводного сульфата по реакции:
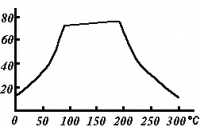
Растворимость
Растворимость сульфата меди (II) по мере роста температуры проходит через плоский максимум, в течение которого растворимость соли почти не меняется (в интервале 80—200 °C). (см. рис.)
Химические свойства
Электролитическая диссоциация
CuSO4 — хорошо растворимая в воде соль и сильный электролит, в растворах сульфат меди(II) так же, как и все растворимые соли, диссоциирует в одну стадию:
Реакция замещения
Реакция замещения возможна в водных растворах сульфата меди с использованием металлов активнее меди, стоящих левее меди в электрохимическом ряду напряжения металлов:
Реакция с растворимыми основаниями (щелочами)
Сульфат меди(II) реагирует с щелочами с образованием осадка гидроксида меди(II) голубого цвета:
Сокращённое ионное уравнение (Правило Бертолле)
Реакция обмена с другими солями
Сульфат меди вступает также в обменные реакции по ионам Cu 2+ и SO4 2-
Прочее
С сульфатами щелочных металлов и аммония образует комплексные соли, например, Na2[Cu(SO4)2]·6H2O.