Что такое cro3 в химии
Хромовый ангидрид (триоксид хрома, трёхокись хрома, оксид хрома IV), CrO3 — соединение хрома с кислородом, тёмно-красные кристаллы, хорошо растворимые в воде. Ангидрид хромовой и дихромовой кислот.
Физические свойства
Чёрно-красные с фиолетовым оттенком кристаллы — пластины или иголки. Гигроскопичен, расплывается на воздухе.
tпл=196 °C, при атмосферном давлении разлагается ниже температуры кипения.
Плотность 2,8 г/см³; Растворимость в воде — 166 г/100 г (15 °C), 199 г/100 г (100 °C).
Химические свойства
CrO3 — кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO3):
При взаимодействии CrO3 со щелочами образуются хроматы:
При нагревании выше 250 °C разлагается с образованием оксида хрома(III) и кислорода:
Как и все соединения Cr(VI), CrO3 является сильным окислителем (восстанавливается до Cr2O3). Например этанол, ацетон и многие другие органические вещества самовоспламеняются или даже взрываются при контакте с ним (хотя некоторые справочники указывают «растворим в спирте и эфире»). Окисляет иод, серу, фосфор, уголь, например:
Получение
Применение
Используется для получения хрома электролизом, электролитического хромирования; хроматирования оцинкованных деталей, в качестве сильного окислителя, изредка в пиросоставах.
Применяют также, как окислитель в органической химии (в производстве изатина, индиго и т. д.).
В смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит».
Растворы хромового ангидрида (или, чаще, дихромата калия) в серной кислоте широко используются в лабораторной практике для очистки посуды от органических загрязнений (хромовая смесь).
Токсичность
Оксид хрома(VI) очень ядовит, как и многие другие соединения шестивалентного хрома. Летальная доза для человека при попадании внутрь 0,08 г/кг.
Техника безопасности
Хромовый ангидрид — весьма химически активное вещество, способен вызвать при соприкосновении с органическими веществами возгорания и взрывы. Воспламеняет бензин при комнатной температуре и используется в качестве воспламенителя топлива в ракетной технике. При попадании на кожу вызывает сильные раздражения, экземы и дерматиты, а также может спровоцировать развитие рака кожи. Даже при своевременном удалении с кожных покровов оставляет пятна коричневого цвета. Весьма опасно вдыхание паров хромового ангидрида, хотя он и малолетуч.
Для хранения его применяется стеклянная или пластиковая герметичная посуда, необходимо исключение контакта с органическими веществами. Работа с ним требует применения спецодежды и средств индивидуальной защиты.
Хромовый ангидрид
| Хромовый ангидрид | |
|---|---|
 | |
 | |
| Систематическое наименование | Оксид хрома (VI) |
| Хим. формула | CrO3 |
| Рац. формула | CrO3 |
| Молярная масса | 99,99 г/моль |
| Плотность | 2,8 г/см³ |
| Температура | |
| • плавления | 197 °C |
| • разложения | 250 °C |
| ГОСТ | ГОСТ 2548-77 |
| Рег. номер CAS | 1333-82-0 |
| PubChem | 14915 |
| Рег. номер EINECS | 215-607-8 |
| SMILES | |
| RTECS | GB6650000 |
| ChEBI | 48240 |
| Номер ООН | 1463 |
| ChemSpider | 14212 |
| ЛД50 | 80 мг/кг (крысы, орально) |
| Токсичность | высокотоксичен, канцерогенен, сильный окислитель |
| Пиктограммы ECB |    |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Содержание
Свойства
Физические свойства
Чёрно-красные с фиолетовым оттенком кристаллы — пластины или иголки. Гигроскопичен, расплывается на воздухе.
tпл=196 °C, при атмосферном давлении разлагается ниже температуры кипения.
Плотность 2,8 г/см³; Растворимость в воде — 166 г/100 г (15 °C), 199 г/100 г (100 °C).
Химические свойства
CrO3 — кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO3):
или дихромовая кислота (при избытке CrO3):
При взаимодействии CrO3 со щелочами образуются хроматы:
При нагревании выше 250 °C разлагается с образованием оксида хрома (III) и кислорода:
Как и все соединения Cr(VI), CrO3 является сильным окислителем (восстанавливается до Cr2O3). Например этанол, ацетон и многие другие органические вещества самовоспламеняются или даже взрываются при контакте с ним (хотя некоторые справочники указывают «растворим в спирте и эфире»). Окисляет йод, серу, фосфор, уголь, например:
Комплекс триоксида хрома с пиридином используется для окисления спиртов в соответствующие карбонильные соединения (реакция Саретта).
Получение
Применение
Используется для получения хрома электролизом, электролитического хромирования; хроматирования оцинкованных деталей, в качестве сильного окислителя, изредка в пиросоставах.
Применяют также, как окислитель в органической химии (в производстве изатина, индиго и т. д.).
В смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит».
Растворы хромового ангидрида (или, чаще, дихромата калия) в серной кислоте широко используются в лабораторной практике для очистки посуды от органических загрязнений (хромовая смесь).
Токсичность

Техника безопасности


Для хранения его применяется стеклянная или фарфоровая герметичная посуда, необходимо исключение контакта с органическими веществами. Работа с ним требует применения спецодежды и средств индивидуальной защиты.
Содержание
Производство, структура и основные реакции
Триоксид хрома генерируются путем обработки хромата натрия или соответствующее дихромата натрия с серной кислотой :
По этому или подобным маршрутам ежегодно производится около 100 000 тонн.
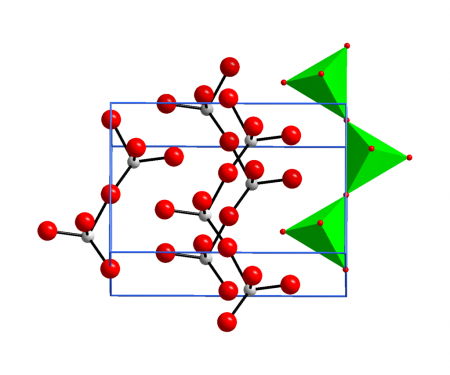
Твердое тело состоит из цепочек тетраэдрически координированных атомов хрома, имеющих общие вершины. Таким образом, каждый центр хрома имеет два общих кислородных центра с соседями. Два атома кислорода не являются общими, что дает общую стехиометрию 1: 3.
Структура мономерного CrO 3 была рассчитана с использованием теории функционала плотности и, согласно прогнозам, является пирамидальной ( точечная группа C 3v ), а не планарной (точечная группа D 3h ).
Приложения
Безопасность
Картинки
Концентрированный раствор дихромата калия в воде.
Оксид хрома(VI)
| Оксид хрома(VI) | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Оксид хрома (VI) |
| Химическая формула | CrO3 |
| Физические свойства | |
| Отн. молек. масса | 100 а. е. м. |
| Молярная масса | 99,99 г/моль |
| Плотность | 2,8 г/см³ |
| Термические свойства | |
| Температура плавления | 197 °C |
| Температура разложения | 250 °C |
| Классификация | |
| Рег. номер CAS | 1333-82-0 |
Окси́д хро́ма(VI) (трёхокись хрома, хромовый ангидрид), CrO3 — соединение хрома с кислородом, тёмно-красные кристаллы, хорошо растворимые в воде. Ангидрид хромовой и дихромовой кислот.
Содержание
Свойства
Физические свойства
Чёрно-красные с фиолетовым оттенком кристаллы — пластины или иголки. Гигроскопичен, расплывается на воздухе.
tпл=196 °C, при атмосферном давлении разлагается ниже температуры кипения.
Плотность 2,8 г/см³; Растворимость в воде — 166 г/100 г (15 °C), 199 г/100 г (100 °C).
Химические свойства
CrO3 — кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO3):
или дихромовая кислота (при избытке CrO3):
При взаимодействии CrO3 со щелочами образуются хроматы:
При нагревании выше 250 °C разлагается с образованием оксида хрома(III) и кислорода:
Как и все соединения Cr(VI), CrO3 является сильным окислителем (восстанавливается до Cr2O3). Например этанол, ацетон и многие другие органические вещества самовоспламеняются или даже взрываются при контакте с ним (хотя некоторые справочники указывают «растворим в спирте и эфире»). Окисляет йод, серу, фосфор, уголь, например:
Получение
Применение
Используется для получения хрома электролизом, электролитического хромирования; хроматирования оцинкованных деталей, в качестве сильного окислителя, изредка в пиросоставах.
Применяют также, как окислитель в органической химии (в производстве изатина, индиго и т. д.).
В смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит».
Растворы хромового ангидрида (или, чаще, дихромата калия) в серной кислоте широко используются в лабораторной практике для очистки посуды от органических загрязнений (хромовая смесь).
Токсичность
Оксид хрома(VI) очень ядовит, как и многие другие соединения шестивалентного хрома. Летальная доза для человека при попадании внутрь 0,1 г.
Техника безопасности
Хромовый ангидрид — весьма химически активное вещество, способен вызвать при соприкосновении с органическими веществами возгорания и взрывы. Воспламеняет бензин при комнатной температуре и используется в качестве воспламенителя топлива в ракетной технике. При попадании на кожу вызывает сильные раздражения, экземы и дерматиты, а также может спровоцировать развитие рака кожи. Даже при своевременном удалении с кожных покровов оставляет пятна коричневого цвета. Весьма опасно вдыхание паров хромового ангидрида, хотя он и малолетуч.
Для хранения его применяется стеклянная или пластиковая герметичная посуда, и исключение контакта с органическими веществами. Работа с ним требует применения спецодежды и средств индивидуальной защиты.
См. также
Полезное
Смотреть что такое «Оксид хрома(VI)» в других словарях:
Оксид хрома(II) — Общие … Википедия
Оксид хрома(IV) — Оксид хрома(IV) … Википедия
Оксид хрома (VI) — Оксид хрома(VI) Общие Систематическое наименование Оксид хрома (VI) Химическая формула CrO3 Отн. молек. масса 100 а. е. м … Википедия
оксид хрома — (Cr2O3) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN chromic oxidechrome oxide … Справочник технического переводчика
Оксид хрома — – Cr2O3 с небольшим количеством примесей водорастворимых солей – пигмент темно зеленого цвета. Устойчив к воздействию щелочей, кислот и повышенных температур. Получают путем нагревания смеси хромпика с каким либо восстановителем, например… … Энциклопедия терминов, определений и пояснений строительных материалов
Оксид хрома(III) — Оксид хрома(III) … Википедия
Хрома оксиды — Существуют следующие хлориды хрома: Название Формула Температура плавления Температура кипения Цвет Оксид хрома(II) CrO черный Оксид хрома(III) Cr2O3 2440 °C 3000 °C зеленый Оксид хрома(IV) CrO2 … Википедия
ХРОМА СЕМЕЙСТВО — ПОДГРУППА VIB. СЕМЕЙСТВО ХРОМА ХРОМ, МОЛИБДЕН, ВОЛЬФРАМ Все три элемента VIB подгруппы хром Cr, молибден Mo, вольфрам W играют большую роль в промышленности, особенно в металлургии и электротехнике. Каждый из этих элементов занимает среднее… … Энциклопедия Кольера
Оксид-сульфат титана — Общие Систематическое наименование Оксид сульфат титана Традиционные названия Основной сернокислый титан; оксосульфат титана; сульфат титанила Химическая формула TiOSO4 Физические свойства … Википедия
Оксид калия — Общие … Википедия
Оксид хрома CrO(II)
Низший оксид для элементов 6-й группы состава MeO получен только для хрома.
Физические свойства CrO(II):
Химические свойства CrO(II):
Гидроксид хрома Cr(OH)2(II)
Физические свойства Cr(OH)2(II):
Химические свойства Cr(OH)2(II):
Соединения хрома со степенью окисления +2 являются неустойчивыми, легко окисляются кислородом воздуха в более устойчивые соединения хрома со степенью окисления +3:
4Cr(OH)2+O2+2H2O = 4Cr(OH)3
Cr2O3 в мелкоизмельченном состоянии применяют в качестве абразивного материала (паста ГОИ), зеленого пигмента, катализатора в органическом синтезе. Оксид хрома (III) является основной добавкой к корунду при выращивании искусственных рубинов, используемых в ювелирной промышленности и часовом деле, а также в качестве лазерного материала в оптоэлектронике.
Физические свойства Cr2O3(III):
Химические свойства Cr2O3(III):
Гидроксид хрома Cr(OH)3(III)
Физические свойства Cr(OH)3(III):
Химические свойства Cr(OH)3(III):
Оксид хрома CrO2(IV) (диоксид хрома)
Диоксид хрома применяется в производстве элементов памяти для компьютеров.
Оксид хрома CrO3(VI) (хромовый ангидрид)
Физические свойства CrO3(VI):
Химические свойства CrO3(VI):
Триоксид хрома получают действием концентрированной серной кислоты на концентрированные растворы хроматов/дихроматов калия/натрия:
K2Cr2O7+H2SO4 = 2CrO3↓+K2SO4+H2O
Гидроксиды хрома
Примечательно, что хромат-ионы и дихромат-ионы при изменении среды растворов без проблем переходят друг в друга, меняя при этом окраску раствора:
Хроматы получают сплавлением хромистого железняка или оксида хрома (III) с карбонатами в присутствии кислорода (t=1000°C):
4Fe(CrO2)2+8Na2CO3+7O2 = 8Na2CrO4+2Fe2O3+8CO2
Дихроматы получают из растворов хроматов, подкисляя их.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе











