Что такое bethesda 5
Опыт применения системы Bethesda в оценке результатов тонкоигольной аспирационной биопсии узловых образований щитовидной железы
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Цель исследования: оценка точности метода тонкоигольной аспирационной биопсии (ТАБ) в верификации карциномы щитовидной железы (ЩЖ).
Материал и методы: проведен ретроспективный анализ данных электронных медицинских историй болезни 1675 пациентов, которым в течение 2016 г. была проведена ТАБ узловых образований ЩЖ. Цитологическое заключение носило описательный характер и включало категорию от I до VI в соответствии с системой Bethesda. При статистической обработке рассчитывали относительные и абсолютные частоты встречаемости значений признаков (категории по шкале Bethesda, злокачественность новообразований и т. д.), значения чувствительности, специфичности, прогностической ценности положительного и отрицательного результатов.
Результаты и обсуждение: среди 115 оперированных больных злокачественные новообразования ЩЖ при гистологическом исследовании были обнаружены у 46 (40%) пациентов. Чувствительность цитологического исследования в выявлении карциномы для категорий IV+V+VI составила 89,1% (95% ДИ 77–95,3%). Для категории Bethesda IV специфичность составила 46,3% (35,1–58%), для категории Bethesda V – 97,1% (90–99,2%) и для категории Bethesda VI – 100% (94,7–100%). Рассчитана прогностическая ценность положительного (PPV) и отрицательного (NPV) результатов цитологического исследования для выявления рака ЩЖ в узловых образованиях Bethesda IV–VI. Наиболее высокая ценность положительного и отрицательного результатов отмечена именно в категории Bethesda VI, т. е. положительный результат (наличие злокачественной опухоли) при цитологическом исследовании был подтвержден данными гистологического исследования. Наименьшая ценность положительного и отрицательного результатов цитологического исследования ожидаемо была отмечена в категории Bethesda IV: только в 30,4% метод позволил выявить рак ЩЖ и только в 53,6% позволил его исключить.
Выводы: цитологическое исследование биоптатов ЩЖ с оценкой по системе Bethesda является информативным методом диагностики рака ЩЖ, однако необходимы дальнейшие исследования для верификации карцином в образцах узловых образований с цитологическими заключениями категории Bethesda IV.
Ключевые слова: карцинома, система Bethesda, щитовидная железа, тонкоигольная аспирационная биопсия, чувствительность, специфичность, прогностическая ценность.
Для цитирования: Нечаева О.А., Бавыкина Л.Г., Глазков А.А., Бритвин Т.А. Опыт применения системы Bethesda в оценке результатов тонкоигольной аспирационной биопсии узловых образований щитовидной железы. РМЖ. 2018;1(I):23-27.
Experience with the new Bethesda system for reporting thyroid cytopathology in evaluating the results of fine needle aspiration cytology of thyroid nodules
O.A. Nechaeva, L.G. Bavykina, A.A. Glazkov, T.A. Britvin
Moscow Regional Research and Clinical Institute named after M.F. Vladimirskiy
Aim: to assess the accuracy on fine needle aspiration (FNA) cytology in verification of thyroid carcinoma.
Patients and Methods: the retrospective study of 1675 case report form was performed. Thyroid ultrasound and FNA were performed on all patients during 2016. All thyroid cyto-pathological slides were reviewed and classified according to the Bethesda System for Reporting Thyroid Cytopathology (TBSRTC). During statistical processing, the relative and absolute frequencies of occurrence of characteristic values (categories on TBSRTC in the prediction of thyroid cancer malignancy of tumors, etc.), the sensitivity, specificity, the prognostic value of the positive (PPV) and negative result (NPV) were calculated.
Results and Discussion: 115 cases with high cancer risk were communicated to the surgeon, thyroid carcinoma was detected in 46 (40%) cases. The sensitivity of FNA cytology diagnostic in the detection of thyroid carcinoma for categories IV+V+VI on TBSRTC were 89,1% (95% CI 77–95,3%). The specificity of FNA diagnostic accuracy were 46,3% (35,1–58%) for category IV malignant, 97,1% (90–99,2%) for category V and 100% (94,7–100%) for category VI category on TBSRTC. The prognostic value of the PPV and NPV results of the cytological study for detection of thyroid cancer in the nodules of IV–VI categories on TBSRTC is calculated. The highest value of positive and negative results was recorded in VI category, that is, a positive result (the presence of a malignant tumor) in a cytological study was confirmed by histological examination. The least value of positive and negative cytological results was expected in IV category, the method allowed to reveal thyroid cancer only in 30,4% and allowed to exclude it only in 53,6%.
Conclusions: fine needle aspiration cytology in the diagnosis of thyroid lesion using the Bethesda system for reporting thyroid carcinoma is an informative method. However, further studies are still needed to verify thyroid cancer in IV category on TBSRTC.
Key words: carcinoma, Bethesda system, thyroid, fine needle aspiration, sensitivity, specificity, prognostic value.
For citation: Nechaeva O.A., Bavykina L.G., Glazkov A.A., Britvin T.A. Experience of using the Bethesda system in evaluating the results of fine needle biopsy of thyroid nodules // RMJ. 2018. № 1 (I). P. 23–27.
Статья посвящена возможностям применения системы Bethesda в оценке результатов тонкоигольной аспирационной биопсии узловых образований щитовидной железы. Показано, что данный метод является информативным для диагностики рака щитовидной железы, однако необходимы дальнейшие исследования.
Введение
Узловые образования щитовидной железы (ЩЖ) являются частыми находками и, согласно обобщенным статистическим данным, встречаются у 3–7% населения с ежегодной идентификацией около 300 тыс. новых случаев [1–3]. В России нет точной информации о распространенности узловой патологии ЩЖ, однако, по данным статистического отчета Минздрава России за 2016 г., у взрослого населения нашей страны заболевания ЩЖ, не сопровождавшиеся тиреотоксикозом, были выявлены с частотой 355,1 на 100 тыс. населения [4].
Ультразвуковое исследование (УЗИ) является самым распространенным и доступным методом визуализации ЩЖ, при этом использование современных аппаратов с высокой разрешающей способностью позволяет диагностировать узловые образования ЩЖ у 68% случайно отобранных людей [5], что ставит перед клиницистами задачу объективной оценки их реальной онкологической опасности.
Большинство узловых образований ЩЖ являются доброкачественными. Злокачественный характер имеют не более 5–15% тиреоидных узлов, а его вероятность возрастает при наличии таких факторов риска, как возраст, наследственность, контакт с радиоактивным излучением в анамнезе [6, 7].
Основной задачей клинициста при обнаружении узлового образования в ЩЖ является стратификация риска его злокачественности с учетом клинических, лабораторных и УЗ-признаков. При этом единственным дооперационным методом прямой оценки структурных изменений в ЩЖ является тонкоигольная аспирационная биопсия (ТАБ).
В 2009 г. для оценки клеточного состава биоптатов узловых образований ЩЖ Национальным институтом рака США была разработана система TBSRTC (The Bethesda System For Reporting Thyroid Cytopathology) [8], которая с 2015 г. рекомендована Российской ассоциацией эндокринологов к использованию на территории РФ [9]. Гибкая структура этой системы (табл. 1), включающей 6 основных диагностических категорий, позволяет облегчить взаимопонимание между врачами различных специальностей (цитологами, эндокринологами, хирургами, радиологами), принимающими участие в диагностическом и лечебном процессе. В результате ее применения стала возможной, с одной стороны, ранняя диагностика злокачественных новообразований, с другой стороны, уменьшилось количество неоправданных хирургических вмешательств по поводу неопухолевых заболеваний и доброкачественных опухолей ЩЖ. 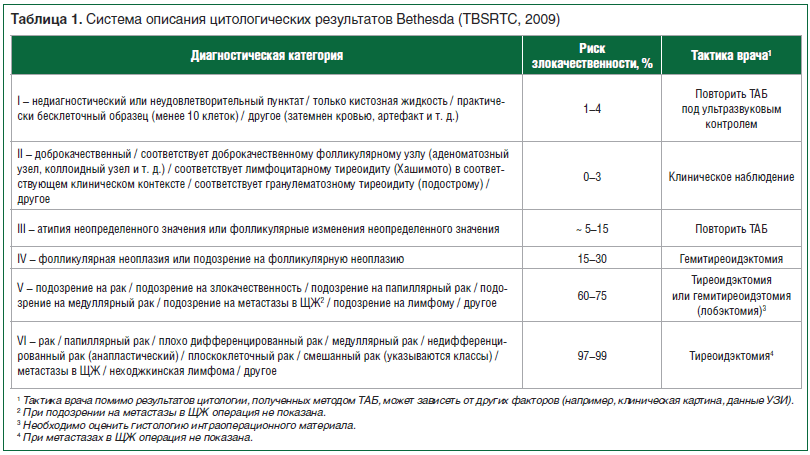
Цель настоящего исследования: на основании сравнительного анализа данных цитологического исследования биоптатов узловых образований ЩЖ с результатами послеоперационного гистологического исследования оценить точность метода ТАБ в верификации карциномы ЩЖ.
Материал и методы
Дизайн исследования и процедура проведения ТАБ
Описание цитологических образцов
Послеоперационное гистологическое исследование
Статистический анализ
Результаты
Результаты ТАБ
Сравнение результатов цитологического и морфологического исследований
Обсуждение
Выводы:
Только для зарегистрированных пользователей
Опухоли щитовидной железы
Щитовидная железа расположена на передней поверхности шеи человека и состоит из двух долей – правой и левой, соединённых узким перешейком, также довольно часто встречается пирамидальная доля. Вес железы у взрослого человека составляет 12—25 г. Нормальный объем железы у женщин до 18 мл, у мужчин до 25 мл.
Необходимо отметить, что рядом с щитовидной железой расположены такие жизненно важные органы, как: пищевод, сонные артерии, яремные вены, трахея, которые могут быть повреждены во время операции. Позади железы, с обеих сторон от трахеи расположены возвратные гортанные нервы, регулирующие подвижность голосовых складок, которые в свою очередь отвечают за дыхание у человека. Также, по задней поверхности щитовидной железы расположены околощитовидные железы, вырабатывающие паратгормон, отвечающий за обмен кальция и фосфора. Их размер обычно 3-5 мм. Иногда околощитовидные железы бывает сложно обнаружить и можно их случайно удалить во время операции на щитовидной железе.
Щитовидная железа относится к эндокринным органам (она вырабатывает гормоны Т4, Т3, кальцитонин). Выработка этих гормонов контролируется гипофизом по типу обратной связи – когда уровень тиреоидных гормонов (Т4, Т3) в крови становится достаточно высоким, количество выделяемого гипофизом ТТГ уменьшается, что сокращает выработку Т4 и Т3, и наоборот, при снижении концентрации Т4 и Т3 в крови количество выделяемого ТТГ увеличивается, стимулируя секрецию Т4 и Т3.
Кальцитонин: в отличие от других гормонов он не является йодсодержащим. От количества кальцитонина зависит уровень фосфора и кальция в крови.
Тироксин: является тиреоидным гормоном. Тироксин влияет на процессы обмена веществ, особенности роста и развития в организме человека. Клетки мозга подвержены окислительным реакциям, проходящим с участием вещества. Недостаток или избыток этого гормона способен вызывать различные осложнения. А также, данное вещество находится в тесной связи с выработкой белка.
Трийодтиронин:когда дейодируется тироксин, высвобождается этот гормон. Но его образование таким образом происходит в печени и почках. Щитовидной железой трийодтиронин выделяется в меньших объемах.
Эти вырабатываемые гормоны принимают участие в процессе обмена веществ в организме. А также, они влияют на работу других систем, в том числе нервной системы.
Каким образом выявляются опухоли щитовидной железы?
Вы можете самостоятельно обратить внимание на то, что на шее появилась припухлость или врач эндокринолог при осмотре выявит узлы в щитовидной железе. Далее необходимо выполнить УЗИ шеи, для подтверждения, что опухоль расположена именно в щитовидной железе. Также необходимо сдать анализ крови на гормоны щитовидной железы, для оценки функции исследуемого органа.
Если при УЗИ выявляется узловое образование менее 1 см и признаков злокачественности не выявлено, то такой узел динамически наблюдается, но при изменении узла с наличием признаков злокачественности, требуется выполнить пункционную тонкоигольную аспирационную биопсию (ПТАБ) узла под контролем УЗИ. При обнаружении узлового образования более 1 см, для подтверждения диагноза необходимо выполнить ПТАБ. Далее полученный материал исследуется в лаборатории под микроскопом, на основании чего определяется дальнейшая тактика лечения пациента.
Если же у пациента выявлена повышенная функция щитовидной железы, то дополнительным методом исследования будет сцинтиграфия. А при недостаточной визуализации железы (особенно при загрудинном расположении узла), методом выбора является компьютерная томография.
Опухоли щитовидной железы:
В щитовидной железе могут встречаться как доброкачественные так и злокачественные опухоли. На сегодняшний день во всем мире при цитологическом исследовании щитовидной железы используется классификация по Bethesda (The Bethesda System for Reporting Thyroid Cytopathology), которая была принята на конференции Национального Института Рака, в октябре 2007 в г. Бетесда (США, Мэриланд). В соответствии с этой терминологией описание каждой ПТАБ начинают с основных диагностических категорий, каждая из которых имеет определенный риск злокачественности и в зависимости от степени риска каждая категория связана с дальнейшей клинически обоснованной тактикой:
I. Недиагностический или неудовлетворительный материал.
Необходимо повторить ПТАБ.
II. Доброкачественные изменения.
Риск злокачественности не более 3%.
III. Атипия неясного значения или фолликулярные поражения неясного значения.
Необходимо повторить ПТАБ.
IV. Фолликулярная опухоль или подозрение на фолликулярную опухоль.
Риск злокачественности 20-30%.
V. Подозрение на злокачественную опухоль.
Риск злокачественности 98%.
VI. Злокачественная опухоль.
При получении полноценного материала, можно ожидать от врача-цитолога более точное заключение в уверенной или предположительной форме в соответствии с цитологическими и гистологическими классификациями новообразования в щитовидной железе можно разделить на четыре большие группы:
Также возможны заключения от цитолога “материал получен из участка кистозной дегенерации” или “лимфоидной инфильтрации” обычно связаны с доброкачественными поражениями (зоб с кистозной дегенерацией, лимфоматозный тиреоидит и др.).
Таким образом коллоидный зоб – наиболее часто встречаемые опухоли щитовидной железы. Он всегда является доброкачественным и риск его перерождения в рак составляет менее 3%.
В зависимости от морфологического строения различают фолликулярную, папиллярную, оксифильную, функционирующую, светлоклеточную и др. виды аденомы щитовидной железы. Источником развития аденом служат А- и В-фолликулярные клетки щитовидной железы.
Фолликулярные аденомы представляют собой округлые инкапсулированные узлы, плотноэластической консистенции, обладающие достаточной подвижностью. Среди эутиреоидных узловых образований железы они составляют 15-20%. К фолликулярным образованиям относятся такие разновидности, как коллоидная (или макрофолликулярная), микрофолликулярная, фетальная, трабекулярная (или эмбриональная) аденома щитовидной железы.
Папиллярные аденомы щитовидной железы имеют кистозное строение; внутри кист выявляются сосочковидные разрастания, окруженные коричневатой жидкостью. Функционирующие (токсические) аденомы щитовидной железы. Аденома, развивающаяся из В-клеток (оксифильная аденома из клеток Гюртле-Асканази, опухоль Лангханса, онкоцитарная аденома), имеет наиболее агрессивное течение и в 10-35% случаев при гистологическом исследовании оказывается злокачественной.
Рак щитовидной железы разделяют на 5 групп и используют TNM классификацию, где T – размер опухоли, N – метастазы в регионарные лимфатические лимфоузлы, M – отдаленные метастазы.
Папиллярный или фолликулярный рак у пациента младше 45 лет имеет только две стадии заболевания:
I Стадия– Любая T Любая N M0.
II Стадия– Любая T Любая N M1.
У пациентов старше 45 лет с этими же видами рака выделяют четыре стадии заболевания:
II Стадия (T2 N0 M0).
III Стадия (T3 N0 M0), (T1–3 N1a M0).
IVa Стадия (T4a N0–1a M0), (T1–4a N1b M0).
IVb Стадия (T4b ЛюбаяN M0).
IVc Стадия (Любая T Любая N M1).
Медуллярный рак имеет следующие стадии:
Стадия II T2–3 N0 M0.
Стадия III T1–3 N1a M0.
Стадия IVb T4b Любая N M0.
Стадия IVс Любая T Любая N M1.
Недифференцированный рак щитовидной железы стразу же считают, как IV стадию заболевания со следующими подстадиями:
IVa Стадия (T4a ЛюбаяN M0)
IVb Стадия (T4b ЛюбаяN M0)
IVc Стадия (Любая T Любая N M1)
Прогноз при раке щитовидной железы, обнаруженном на ранних стадиях, достаточно благоприятный.
При папиллярной форме рака щитовидной железы пятилетняя выживаемость может достигать 100%.
У пациентов с четвертой стадией фолликулярной карциномы выживаемость не более 50%.
При медуллярном раке щитовидной железы и своевременной операции показатель выживаемости очень высок и составляет около 98%.
Анапластическая форма заболевания характеризуется неблагоприятным прогнозом, даже после проведения операции продолжительность жизни таких пациентов, как правило, не превышает одного года. Но к счастью анапластический рак щитовидной железы бывает достаточно редко.
Таким образом, основным методом лечения при опухолевых поражениях щитовидной железы является комплексное лечение, состоящее из операции на щитовидной железе, с последующим лечением радиоактивным йодом. Только при комплексном лечении возможно добиться хорошего результата.
В настоящее время существует 3 вида объема операций на щитовидной железе:
Как и при любых операциях, после операций на щитовидной железе бывают как общехирургические осложнения, так и специфические.
К общехирургическим относятся такие осложнения как:
К специфическим относятся осложнения такие, как:
Диагностика очаговых изменений щитовидной железы и правила отбора их для хирургического лечения, 2-ая часть
Сокращения: ТАБ — тонкоигольная аспирационная биопсия, ПТАБ — прицельная тонкоигольная аспирационная биопсия, УЗИ — ультразвуковое исследование
В этой статье представлены рекомендации и отдельные практические сведения о диагностических процедурах и правилах отбора для хирургического лечения очаговых изменений щитовидной железы. Сила рекомендаций и качество (достоверность) данных, на которых они основаны, приведены в квадратных скобках: сила рекомендации: 1 — сильная (рекомендуется), 2 — слабая (предлагается); качество данных: В — высокое, СР — среднее, Н — низкое, ОН — очень низкое; из-за отсутствия данных, постановление было согласовано группой из 62 польских экспертов путем голосования.
Цитологическое исследование материала, собранного во время ПТАБ очагового изменения щитовидной железы, классификация Bethesda и последующая тактика ведения
Для того чтобы результат цитологического исследования мазка был достоверным, он должен содержать ≥5 групп ≥10 фолликулярных клеток щитовидной железы, хорошо фиксированных и окрашенных. Цитологическая картина не всегда дает право принять диагностическое решение, поэтому в некоторых случаях полученный результат не указывает на точный диагноз, но он облегчает дифференциальную диагностику или выбор дальнейших процедур, при которых всегда следует учитывать клинический контекст. Результат цитологического исследования щитовидной железы должен быть отнесен патологом к одной из шести категорий диагнозов в соответствии с классификацией Bethesda 1,2 (табл.) [1/СР]. Эти категории были определены National Cancer Institute (NCI). The Bethesda System for Reporting Thyroid Cytopathology (BSRTC). 3
Категория I по классификации Bethesda — недиагностическая или неудовлетворительная биопсия
Такой диагноз может быть результатом:
1) недостаточного количества собранных клеток;
2) отсутствия фолликулярных клеток в мазке;
3) ошибок фиксации и хранения полученного материала [1/СР].
Показания к следующей ПТАБ и время ее выполнения, если был получен один недиагностический результат
Если исследуемое изменение представляет собой простую кисту без солидной части, повторная ПТАБ может быть выполнена через 6–18 месяцев; риск развития рака очень низкий, но его нельзя полностью исключить [2/ОН]. Если было исследовано солидное очаговое изменение без клинических признаков злокачественности, то оно требует клинического мониторинга, УЗИ и последующей ПТАБ в зависимости от степени риска (рамка 2 и рамка 3), как правило, через 3–12 месяцев [2/ОН]. В солидном узле с кистозной дегенерацией следует стремиться выполнить ПТАБ солидной части.
Интервал между недиагностической и повторной ПТАБ должен составлять ≥3 месяца, если только клинические признаки не указывают на особенно высокий риск злокачественности (подозрение на недифференцированный, или анапластический рак, или лимфому), что требует дальнейшей экстренной диагностики. В большинстве случаев, когда клинический и УЗИ риск невелик, следующая ПТАБ может быть выполнена через 6–12 месяцев [2/ОН].
Дальнейшая тактика и показания к хирургическому лечению, если были получены 2 недиагностических результата ПТАБ
В случае недиагностической ПТАБ American Thyroid Association (ATA) рекомендует рассмотреть возможность хирургического вмешательства. Авторы польских рекомендаций предлагают опираться на клинические и УЗИ- признаки злокачественности (рамка 2 и рамка 3) [1/ОН].
Если исследуемое изменение представляет собой простую кисту с двумя недиагностическими результатами ПТАБ, следует помнить, что риск рака очень низкий (
Таблица. Категории диагнозов при цитологическом исследовании щитовидной железы по классификации Bethesda а
Категория диагноза
Риск рака щитовидной железы
Наиболее частые гистопатологические диагнозы
Показания к последующей ТАБ
Наиболее часто рекомендуемое лечение
I — недиагностическая или неудовлетворительная биопсия
может соответствовать каждому диагнозу
необходима последующая ТАБ, обычно через 3–12 мес., в зависимости от риска; при клиническом подозрении на нед ифференцируемый рак необходимо немедленно продолжать диагностику
– показания к оперативному лечению зависят от клинического риска злокачественности
– неясные результаты диагностической биопсии часто встречаются при кистах и воспалении щитовидной железы
II — доброкачественное изменение
узловой зоб, в том числе гиперпластические и коллоидные узлы; тиреоидит
да, если с самого начала обнаружены при УЗИ признаки риска злокачественности, если увеличение узла клинически существенно или появляются новые признаки риска при УЗИ
III — фолликулярное изменение неопределенного значения (FLUS) или
атипия неопределенного значения (AUS)
категория используется только тогда, если нет возможности цитологической детализации диагноза
да (через 3–6 мес., в зависимости от риска)
такой диагноз per se является основанием для рассмотрения вопроса о необходимости оперативного лечения в случае существенных признаков риска на картине УЗИ
IV — фолликулярная опухоль или подозрение на фолликулярную опухоль г
может соответствовать как неопухолевому поражению (в ≥25 % случаев это гиперпластические узлы или воспаление), так и доброкачественной опухоли, которые невозможно отличить на цитологии от злокачественной опухоли
нет, но если планируется оперативное лечение, то необходимо подтверждение диагноза другим цитологом; в случае наблюдения узлов следующая ТАБ выполняется через 3-6 месяцев, в зависимости от риска
подозрение на: папиллярный рак, медуллярный рак, метастаз в щитовидную железу, лимфому, анапластический рак или сосудистую саркому
нет, но необходимо подтверждение диагноза другим цитологом
VI — злокачественная опухоль
папиллярный рак; медуллярный рак, лимфома, метастаз в щитовидную железу, анапластический рак щитовидной железы, сосудистая саркома или иное злокачественное новообразование
нет, но необходимо подтверждение диагноза другим цитологом
а на основании Bethesda System for Reporting Thyroid Cytopathology 2017
б риск рака в польской популяции на основании: Diagnostyka i leczenie raka tarczycy – rekomendacje polskie. Endokrynol. Pol., 2018; 69: 34–74
в риск рака, исключая случаи послеоперационных диагнозов неинвазивного фолликулярного рака щитовидной железы с клеточными ядрами, напоминающими папиллярный рак (в настоящее время рассматривается как доброкачественная опухоль) – на основании: Cibas E.S., Ali S.Z.: The Bethesda system for reporting thyroid cytopathology. Thyroid 2017; 27: 1341–1346
г диагноз «подозрение на фолликулярную опухоль» включает в себя также «подозрение на опухоль из клеток Гюртля» (ранее оксифильная опухоль), которое отягощено большим (15–25 %) риском злокачественности и чаще является однозначным показанием для оперативного лечения.
ТАБ – тонкоигольная аспирационная биопсия
Категория II по классификации Bethesda — доброкачественное изменение
Эта диагностическая категория может соответствовать клиническому диагнозу узловой зоб, тиреоидит (острый, подострый и аутоиммунный), гиперпластический узел при узловом зобе, коллоидный узел (наличие большого количества коллоида и достаточного количества клеток) или киста щитовидной железы. Риск злокачественности такой опухоли минимален [1/В].
Термин «изображение предполагает коллоидный узел» означает, что при ПТАБ было получено много коллоида без достаточного количества клеток. Наличие большого количества коллоида является надежным сигналом доброкачественного изменения, поэтому в этом случае ПТАБ может быть диагностической, несмотря на небольшое количество клеток [2/Н], особенно если при повторной ПТАБ также получено в основном коллоид и мало клеток, которые не вызывают подозрения на злокачественность [1/ОН].
Дальнейшая тактика после диагностики доброкачественного изменения с помощью ПТАБ
Если было обследовано солидное очаговое изменение, то оно требует клинического мониторинга (физикальное обследование или УЗИ) каждые 6–18 месяцев [1/В]. Повторение ПТАБ в ходе последующего наблюдения не требуется, если нет клинических сомнений и качество первой ПТАБ хорошее [1/СР]. Появление новых УЗИ-признаков высокого риска злокачественности в таком очаговом изменении является однозначным показанием для повторной ПТАБ [1/В]. Если есть признаки, которые указывают на инвазивность изменения, повторную ПТАБ необходимо выполнить в течение 3–6 месяцев [1/СР]. Повторение ПТАБ в течение 6–12 месяцев показано в случае значительного (клинически значимого) увеличения узла, т. е. ≥20 % каждого из измерений в течение года, наличия усилившихся признаков клинического риска, или появления новых признаков клинического или ультразвукового риска, либо при более низкой достоверности первой ПТАБ (из-за очень малого размера изменения и/или расположения в задней части доли щитовидной железы) [2/ОН]. Если результат ПТАБ не дает оснований для диагностики рака, но клиническое подозрение на злокачественную опухоль сохраняется, следует рассмотреть необходимость хирургического вмешательства; интраоперационное исследование подозреваемых изменений щитовидной железы может быть полезным, но оно не является обязательным [2/ОН]. Однако, как правило, если снова получен результат ПТАБ, указывающий на доброкачественное изменение, консервативное лечение допускается даже при значительном увеличении узла [2/ОН].
Если исследуемое очаговое изменение, диагностированное как доброкачественное, с самого начала наблюдения имеет УЗИ-признаки риска злокачественности, то ПТАБ также следует повторить, поскольку это снижает риск пропустить рак [1/ОН]. Повторная ПТАБ также показана в случае значительного увеличения солидной части кистозно-солидного изменения [2/ОН]. Если нет признаков клинического риска, увеличения узла или появления новых УЗИ-признаков риска, повторная ПТАБ может быть необходима не ранее, чем через 6–12 месяцев [1/ОН].
Категория III по классификации Bethesda — фолликулярные изменения неопределенного значения
Эту диагностическую категорию следует использовать только в случае крайней необходимости, когда невозможно уточнить цитологический диагноз [1/ОН]. Поскольку это неоднозначный диагноз, требуется повторить ПТАБ, результат которой интерпретируется с учетом ультразвуковых и клинических признаков риска. Эта категория является категорией исключения, которая в основном содержит цитологические картины, которые не соответствуют квалификационным критериям для категории IV («подозрение на фолликулярную опухоль») или V («подозрение на рак») [2/Н].
Категория III делится на две подкатегории:
1) «фолликулярное изменение неопределенного значения» (follicular lesion of undetermined significance — FLUS) — фолликулярные изменения неопределенного значения, которые характеризуются аспиратом с большим количеством клеток, изменчивой цитоплазматической оксифильностью, наличием многочисленных розеточных систем, бедным коллоидным фоном [2/Н];
Однако следует учитывать более высокий риск, если в мазке обнаружены нарушения в структуре клеток [2/ОН] и необходимо установить соответствующий УЗИ-мониторинг.
Дальнейшая тактика после диагностики фолликулярного изменения неопределенного значения с помощью ПТАБ
Консервативные процедуры включают наблюдение и УЗИ контроль каждые 6 месяцев, повторная ПТАБ через 6–12 месяцев, но не ранее, чем через 3 месяца, из-за риска визуализации изменений, возникающих в результате восстановительных процессов [2/ОН].
Если обнаруживаются УЗИ-признаки риска злокачественности (рамка 2) или в описании ПТАБ есть информация о нарушениях клеточной структуры, вызывающих подозрение на злокачественность, рекомендуется выполнить повторную ПТАБ с интервалом 3–6 месяцев, в зависимости от клинического риска.
Определение концентрации кальцитонина в сыворотке крови позволяет исключить медуллярный рак. 4
Показания к хирургическому лечению после диагностики фолликулярного изменения неопределенного значения с помощью ПТАБ
Как правило, в случае диагностики при цитологическом исследовании фолликулярного изменения неопределенного значения хирургическое лечение не является обязательным, но оно должно учитываться при следующих показаниях [2/ОН]:
1) размер узла щитовидной железы >4 см;
2) при меньших очаговых изменениях — обнаружение их значительного увеличения, появления других выраженных признаков клинического риска (рамка 3) или если при повторной ПТАБ цитологический диагноз указывает на более высокий риск рака [2/СР];
3) наличие в очаге выраженных УЗИ-признаков риска (рамка 2) или признаков инвазивности, а также информации о нарушениях клеточной структуры, которые указывают на вероятность злокачественности.
Показания к лечению радиоактивным йодом ( 131 I) после диагностики фолликулярного изменения неопределенного значения с помощью ПТАБ
Если узел с диагнозом «фолликулярное изменение неопределенного значения» проявляет автономную активность по данным сцинтиграфии, можно рекомендовать изотопную терапию 131 I, так как риск развития рака в этом узле составляет ≤2 % [2/СР].
Категория IV по классификации Bethesda — подозрение на фолликулярную опухоль
Эта категория может соответствовать окончательным гистопатологическим данным фолликулярной аденомы, фолликулярного рака и фолликулярной разновидности папиллярной карциномы и их оксифильным вариантам, однако эта картина также может быть получена при неопухолевых изменениях, таких как гиперпластический узел или лимфоцитарный тиреоидит (при которых часто встречаются признаки нарушенной клеточной структуры), что может составлять около 25 % этих диагнозов [1/СР]. Следовательно, термин «подозрение на фолликулярную опухоль» является более соответствующим, чем уже неиспользуемый термин «фолликулярная опухоль» или «фолликулярный рак».
Этот диагноз также включает в себя подкласс «подозрение на опухоль из клеток Гюртля», т.е. опухоль, которая состоит из онкоцитов, ранее называемая оксифильной (онкоцитарной) аденомой. В настоящее время термин «клетки Гюртля» используется исключительно для раковых клеток или подозрений на рак с целью облегчения интерпретации цитологических диагнозов, а также различения раковых изменений и подозрения на рак (с клетками Гюртля) от незлокачественных, например воспалительных изменений (протекающих с оксифильной метаплазией) [2/ОН].
Диагноз IV категория при цитологическом исследовании также означает, что не было признаков, характерных для ядер папиллярного рака.
Дальнейшая тактика после постановки диагноза «подозрение на фолликулярную опухоль» с помощью ПТАБ и показания к хирургическому лечению
При подозрении на фолликулярную опухоль при цитологическом исследовании (включая опухоль из клеток Гюртля) нет возможности дальнейшей предоперационной цитологической дифференцировки доброкачественной и злокачественной опухоли [1/В]. Следовательно, хирургическое вмешательство должно рассматриваться для устранения диагностических сомнений, особенно когда сосуществуют клинические и/или УЗИ-признаки риска. Интраоперационное обследование не рекомендуется как при фолликулярных изменениях неопределенного значения, так и при подозрении на фолликулярную опухоль [2/ОН]. Хирургическое лечение особенно показано в случае постановки диагноза «подозрение на опухоль из клеток Гюртля» из-за риска обнаружения рака ≥ 15 % [2/ОН].
Прежде чем принять решение о хирургическом лечении, предлагается подтвердить этот диагноз вторым патологом [2/ОН]. После этого можно отказаться от повторного выполнения ПТАБ, поскольку это, как правило, не вносит существенных изменений в диагноз [1/ОН]. Если планируется повторить ПТАБ (у лиц, для которых было принято решение о дальнейшем наблюдении), это можно сделать не ранее, чем через 3 месяца, обычно через 6 месяцев.
Предлагается определять концентрацию кальцитонина в крови в случае фолликулярных изменений (при цитологическом диагнозе «фолликулярного изменения неопределенного значения», «подозрения на фолликулярную опухоль» и особенно «подозрения на опухоль из клеток Гюртля»), особенно если планируется отказ от хирургического вмешательства, так как некоторые из них могут быть медуллярным раком щитовидной железы [2/ОН].
Когда можно отказаться от хирургического вмешательства после получения результата «подозрение на фолликулярную опухоль» с помощью ПТАБ
При небольших узлах (≤1 см) без клинических и УЗИ-признаков риска разрешается отказаться от хирургического вмешательства и применить консервативный подход при условии тщательного клинического и УЗИ контроля [2/ОН]. Также при небольших узлах (диаметр 131 I или 99mTc, риск злокачественности невелик, и поэтому нет абсолютных показаний для хирургического лечения [2/ОН]. Следует помнить о возможности сцинтиграфической оценки, особенно у тех пациентов, у которых концентрация ТТГ близка к нижней границе референтного диапазона или ниже.
Объем хирургического лечения при цитологическом диагнозе «подозрение на фолликулярную опухоль»
Минимальный объем операции зависит от наличия других очаговых изменений щитовидной железы:
1) при одном узле включает полное удаление одной доли с перешейком, а удаление второй доли (почти полное или полное удаление второй доли щитовидной железы) зависит от индивидуальной оценки риска злокачественной опухоли и наличия очаговых изменений во второй доле [2/ОН];
2) в случае узлового зоба, расположенного только в одной доле щитовидной железы, когда подозрение относится только к одному очаговому изменению, может рассматриваться полное или почти полное удаление этой доли щитовидной железы с перешейком, однако допустимо полное удаление пораженной доли щитовидной железы и субтотальное удаление второй доли щитовидной железы [2/ОН];
3) при подозрении на фолликулярную опухоль в одном из узлов многоузлового зоба (с очаговыми изменениями в обеих долях), двухсторонняя субтотальная тиреоидэктомия неуместна, должна быть выполнена почти полная тиреоидэктомия, если есть показания к хирургическому лечению [1/ОН].
Категория V в классификации Bethesda — подозрение на злокачественную опухоль
Этот диагноз означает, что были обнаружены некоторые морфологические признаки злокачественной опухоли, но не были выполнены все критерии для постановки точного диагноза злокачественной опухоли. В польских исследованиях риск злокачественности составляет 50–75 % [1/Н]. Диагноз «подозрения на злокачественную опухоль» включает подозрение на папиллярный рак (чаще всего его везикулярный вариант [1/СР]), медуллярный рак, лимфому, метастаз в щитовидную железу, анапластический рак или сосудистую саркому из-за наличия мертвых тканей.
В случае подозрения на медуллярный рак следует определить концентрацию кальцитонина в крови (результат >100 пг/мл позволяет диагностировать его с высокой вероятностью) [1/В].
Дальнейшая тактика после постановки диагноза подозрение на злокачественную опухоль с помощью ПТАБ
Подозрение на злокачественность или цитологическое определение V категории по классификации Bethesda является показанием к хирургическому лечению, независимо от наличия УЗИ-признаков риска [1/ОН]. Перед проведением хирургического лечения обязательно необходимо получить подтверждение этого диагноза у второго патолога [2/ОН]. Объем хирургического лечения аналогичен таковому при диагностике злокачественной опухоли щитовидной железы — см. ниже. В случае сомнений также может быть рассмотрено интраоперационное исследование [2/СР].
Категория VI по классификации Bethesda — злокачественная опухоль
Такой цитологический диагноз может указывать на папиллярный рак щитовидной железы, медуллярный рак, лимфому, метастаз в щитовидную железу, анапластический рак или сосудистую саркому [1/В].
При таком диагнозе решение о хирургическом лечении является очевидным и не подлежит обсуждению [1/ОН]. В качестве дополнения диагностики в случаях подозрения на медуллярный рак, метастазирование другой опухоли и лимфому могут быть использованы иммуноцитохимические исследования [1/ОН], на лимфому — также проточная цитометрия [1/СР], а при подозрении на медуллярный рак — определение концентрации кальцитонина в крови [1/В].
Дальнейшая тактика после постановки диагноза злокачественная опухоль с помощью ПТАБ
В каждом случае диагностики злокачественной опухоли при цитологическом исследовании необходимо хирургическое лечение [1/В]. Однако перед этим рекомендуется подтвердить диагноз вторым патологом [2/ОН]. В случае предоперационной диагностики анапластического рака, лимфомы или метастаза другого рака в щитовидную железу перед операцией необходима более широкая диагностика, чтобы определить его операбельность и составить план дальнейшего лечения. Если подозревается анапластический рак, эти исследования следует рассматривать как срочные [2/ОН]. В случае диагноза медуллярного рака щитовидной железы до планируемой операции следует исключить сосуществование феохромоцитомы [1/В].
Хирургическое лечение при цитологическом диагнозе злокачественная опухоль щитовидной железы (или подозрение на злокачественную опухоль щитовидной железы)
Основой хирургического лечения является резекция щитовидной железы (тиреоидэктомия): полная или почти полная (послеоперационные остатки обеих долей, оцениваемые с помощью УЗИ, имеют объем ≤1 мл с каждой стороны) [2/ОН].
Только у пациентов с предоперационным диагнозом папиллярного рака в одиночном изменении щитовидной железы размером ≤1,0 см на стадии cN0 (без метастазов в лимфатических узлах) приемлемой хирургической процедурой является полное удаление доли щитовидной железы с перешейком, но только если нет очевидных показаний для двусторонней операции, и лечащая группа получила согласие пациента на такую тактику лечения [2/ОН]. Тиреоидэктомия при раке должна выполняться опытным хирургом в специализированных центрах с соответствующим опытом работы и диагностическими возможностями [2/В].
Осложнения после операции на щитовидной железе
Наиболее частыми осложнениями после хирургического лечения щитовидной железы являются паралич возвратного гортанного нерва и гипопаратиреоз [1/В]. Они могут быть временными или постоянными. Временный гипопаратиреоз обычно длится 1–6 месяцев, но может исчезнуть даже через 1–2 года. Следовательно, в случае его появления и лечения показания к продолжению терапии должны оцениваться через 6 месяцев, год и 2 года после операции [1/СР].
Частота постоянных осложнений является важным показателем опыта центра, хотя это также связано со степенью тяжести заболевания [1/СР]. Риск осложнений ниже, если хирургическое лечение проводится в центре с большим опытом выполнения не только тотальной тиреоидэктомии, но и центральной лимфаденэктомии [1/СР].
Резюме
Рекомендации польских научных обществ, часть которых, касающаяся лечения очаговых изменений щитовидной железы, была представлена в этой статье, являются согласованной позицией представителей всех специальностей, занимающихся диагностикой и лечением рака щитовидной железы. Большим достижением стала разработка в них оптимальных и последовательных диагностических процедур.
Такие обширные рекомендации предназначены для защиты пациентов от чрезмерного/ненужного лечения а, с другой стороны, от недостаточной диагностики или задержки в проведении соответствующего лечения, что в некоторых ситуациях может иметь катастрофические последствия.
Нам также нужно напомнить об анапластическом раке щитовидной железы, опасном раке, для которого нет эффективного лечения. Следует помнить, что рекомендации, в их полной версии, касаются главным образом диагностики и лечения дифференцированных раков щитовидной железы, которые составляют >98 % всех злокачественных опухолей этой железы.
Тем не менее, при дифференцированных опухолях счет времени идет иначе, чем при анапластическом раке; поэтому необходимо различать подозрение на дифференцированный рак щитовидной железы от подозрения на анапластический рак, при котором задержка диагностики и лечения снижает шансы пациента на выживание. Следует подумать о повышенном риске развития этого рака, если, например, вы заметите быстрый рост узелка при многолетнем узловом зобе — нельзя ждать или откладывать направление пациента в соответствующее медицинское учреждение. Подозрение особенно сильно, если этот быстрый рост происходит в течение нескольких недель. Оценка риска злокачественности наблюдаемых очаговых изменений щитовидной железы иногда бывает трудной, но следует уделить ей должное внимание, чтобы скорректировать лечение в зависимости от степени агрессивности наблюдаемых изменений и чтобы оно наилучшим образом помогло больным.

