Что такое абляция печени
Что такое абляция печени
Хотя хирургическая резекция и остаётся основным радикальным вмешательством, выполняемым по поводу первичного и метастатического рака печени, многим больным такая операция противопоказана. Кроме того, у некоторых пациентов возникают рецидивные опухоли печени после предшествующей резекции, и немногим из них можно сделать резекцию повторно.
По этим причинам всё больший интерес привлекают операции, разрушающие опухоли печени. В настоящее время чаще всего используют метод радиочастотной абляции (РЧА). При РИА в опухоль вводят тонкие, частично изолированные электроды (14-21-го калибра). Электроды и заземляющие пластины соединяются с радиочастотным генератором. Во время лечения ток с частотой 500 кГц проходит от оголённой части активного электрода к пластине заземления.
Ток вызывает возбуждение ионов ткани, окружающих электрод, которое трансформируется в тепло, приводящее к гибели клеток от коагуляционного некроза. Существуют различные аппараты для РЧА, среди них — электроды с множеством зубцов, параллельные зонды, контакты, заполненные физиологическим раствором, охлаждающим наконечники. Электроды можно вводить чрескожно либо при лапароскопических или открытых операциях. Кроме того, предложены новые методы температурной абляции при помощи микроволн.
Хотя мы и описываем здесь лишь открытую и лапароскопическую РЧА, это не столь уж важно, поскольку все методики основаны на одинаковых принципах введения зонда в опухоль под лучевым контролем и термической деструкции опухоли.
Локализация и размер опухоли могут мешать эффективной лечебной деструкции опухоли. Опухоли размерами более 4-5 см часто рецидивируют локально. Расположение опухоли около основных воротных триад считают относительным противопоказанием к РЧА. Кроме того, что эффективная абляция невозможна в зонах с ускоренным кровотоком, её проведение в области ворот печени может закончиться печёночной недостаточностью вследствие повреждения и стриктуры общего печёночного протока.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое абляция печени
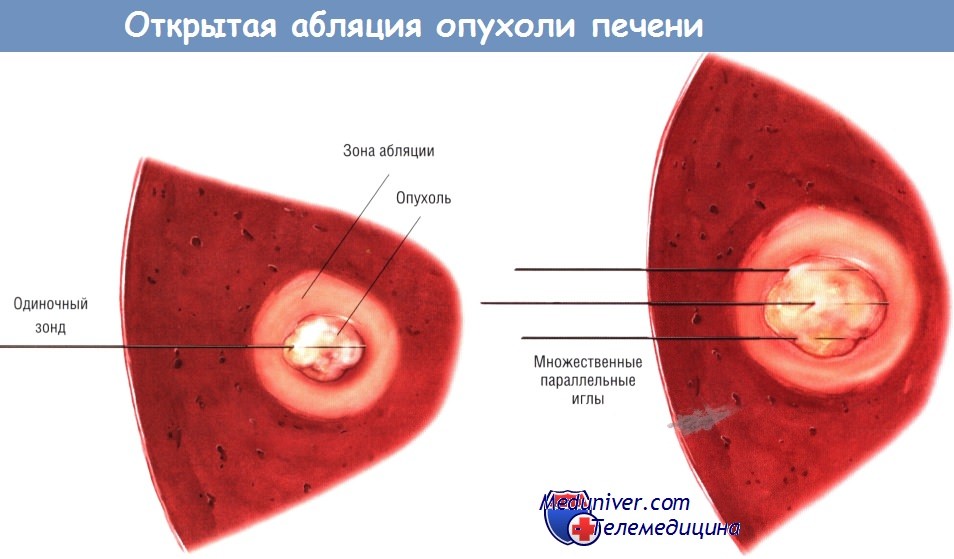
а) Радиочастотная абляция через открытый доступ. РЧА можно выполнить во время лапаротомии. Так поступают в случаях, когда нужно дополнить РЧА резекцию печени, если необходимо обработать много опухолей, а также если локализация опухоли не позволяет применить другой доступ.
Проводя РЧА при открытой лапаротомии, в первую очередь тщательно исследуют брюшную полость, чтобы исключить опухоли внепечёночной локализации. В том числе осматривают листки брюшины и области перипортальных лимфатических узлов. Затем выполняют тщательную пальпацию и интраоперационное УЗИ печени. Если биопсию не проводили ранее, следует иметь в виду необходимость биопсии центральной части опухоли под контролем интраоперационного УЗИ.
Большое значение имеет тщательное планирование зоны абляции, обеспечивающее полный некроз цели. В некоторых случаях, при использовании удлиняющейся многоэлектродной иглы достаточного размера, абляцию можно провести за одно введение иглы в центр опухоли. Например, сферическая опухоль диаметром 3 см и окружающая её зона шириной 1 см могут быть обработаны устройством, создающим некротический участок диаметром 5 см.
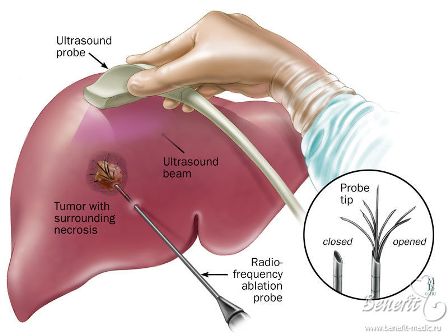
После того как опухоль обнаружена датчиком интраоперационного УЗИ, в неё под ультразвуковым контролем вводят игольчатый электрод для РЧА. Лучше всего проводить электрод в плоскости излучателя: в этом случае путь иглы можно увидеть полностью. При использовании многоэлектродной иглы её контакты развёртываются внутри опухоли, причём их расположение подтверждают с помощью УЗИ, сделанного в двух проекциях.
Другие конструкции зондов имеют одну или множество параллельных игл. Некоторыми устройствами для РЧА абляцию центральной части опухоли проводят частично разведёнными электродами, в последующем последние раздвигают на желаемый объём.
Наблюдение за термической абляцией можно проводить различными способами. Некоторые устройства для РЧА позволяют измерить температуру ткани вмонтированными в них термисторами. Другой способ контроля—мониторирование импеданса ткани и величины тока. В некоторых устройствах ток на выходе регулируется автоматически для контроля импеданса и поддержания температуры тканей в пределах 70-105 °С. Зона абляции во время лечения визуализируется интраоперационным УЗИ.
Обычно образование микроскопических газовых пузырей приводит к гиперэхогенности обрабатываемой ткани.
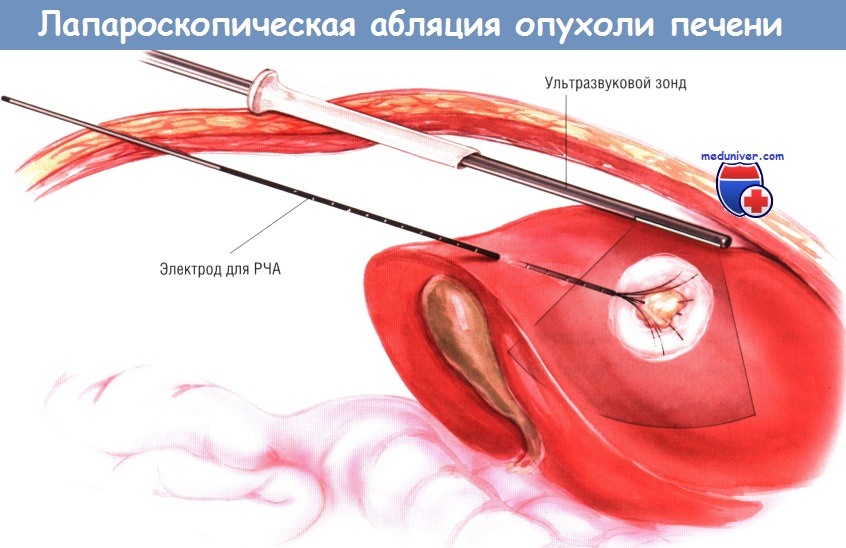
б) Лапароскопическая радиочастотная абляция. Лапароскопическая РЧА выгодна своей малой инвазивностью, возможностью осмотра брюшной полости и проведения лечения под контролем УЗИ. Процедуру проводят под общим обезболиванием. Больной обычно лежит на спине. В большинстве случаев операцию можно сделать через два или три порта. Лапароскоп проводят через порт около пупка, а датчик интраоперационного УЗИ устанавливают через 12-миллиметровый порт, расположенный справа.
При необходимости можно добавить «рабочий» порт с 5-миллиметровой гильзой троакара. Обычно печень частично мобилизуют и отодвигают ткани на 2 см от периферии предполагаемой зоны абляции. Если разрушаемая опухоль лежит около желчного пузыря, можно выполнить холецистэктомию. Электрод для РЧА вводят в брюшную полость чуть ниже и параллельно датчику для интраоперационного УЗИ либо чрескожно, либо через 5-миллиметровый троакар.
Иглу устанавливают в опухоль под контролем интраоперационного УЗИ, причём абляцию проводят и мониторируют так же, как и при открытой операции.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Хирургия»
Микроволновая абляция
Микроволновая абляция — это альтернативный высокоэффективный минимально инвазивный метод локального лечения различных онкологических заболеваний, позволяющий врачам лечить опухоли, не прибегая к традиционной инвазивной хирургии или ионизирующей радиации.
При микроволновой абляции врач, используя различные методы лучевой визуализации тканей, например, ультразвук, вводит в тело опухоли специальный инструмент — микроволновый аппликатор или антенну, излучающий на кончике высокочастотное микроволновое излучение при частоте в диапазоне от 902 до 982 МГц или постоянной частоте 2 450 МГц.
После установки микроволнового аппликатора в опухоль и подтверждения его точности расположения, запрограммированная доза микроволновой энергии прицельно доставляется в опухолевую ткань. Под воздействием микроволнового излучения, находящиеся в опухоли молекулы воды начинают непрерывно вращаться до 5 миллиардов раз в секунду. В связи с этим под действием силы трения происходит преобразование кинетической энергии в тепловую, что приводит к мгновенному локальному нагреву опухолевой ткани до температур, превышающих >150°C, и образованию, так называемой зоны коагуляционного некроза. При этом зона коагуляционного некроза является контролируемой и зависит от длительности и мощности микроволнового излучения.
Воздействие на опухолевую ткань столь высоких температур приводит к очень быстрой денатурации белковых структур и моментальной гибели раковых клеток. Важно отметить, что микроволновая энергия направленно воздействует исключительно на опухолевую ткань, поэтому здоровые ткани и структуры не подвергаются термическому повреждению. Таким образом, после микроволновой абляции вместо опухоли остается мертвая и нежизнеспособная ткань.
В настоящее время микроволновая абляция широко применяется при лечении доброкачественных и злокачественных опухолей печени, легких, почек, костей и мягких тканей, щитовидной железы и опухолей других локализаций с доказанной клинической эффективностью.
Микроволновая абляция печени
Рак печени является крайне коварным онкологическим заболеванием. Без лечения средняя продолжительность жизни пациентов с диагнозом гепатоцеллюлярный рак печени не превышает 6 месяцев, а медиана выживаемости пациентов с метастатическим колоректальным раком не превышает 5 месяцев. Единственными радикальными методами лечения первичного или метастатического рака печени является оперативное вмешательство — хирургическая резекция и трансплантация. Однако по объективным причинам большинство пациентов с первичным или метастатическим раком печени являются неоперабельными. Так, согласно статистическим данным лишь у 20% пациентов с диагнозом гепатоцеллюлярный рак возможно выполнить резекцию или трансплантацию. При метастатическом колоректальном раке резекция возможна не более чем в 10 — 20% случаев, при этом послеоперационная летальность может достигать 5%. Неоперабельность пациентов с раком печени связана как с прогрессивной стадией заболевания и неудобном для резекции расположением опухоли, так и с общим неудовлетворительным состоянием пациента наличия различных сопутствующих заболеваний, в том числе ограниченными функциональными резервами печени, что в совокупности влечет за собой высокие потенциальные риски оперативной хирургии. Если в качестве метода терапии первичного или метастатического рака печени рассматривать системную химиотерапию, в том числе с использованием таргетных препаратов, то ее отдаленные результаты крайне неутешительны. К примеру, применение современных схем химиотерапии у пациентов с метастатическим раком печени позволяют достичь медиану выживаемости в 2 года, однако показатель выживаемости составляет 0%.
В связи с этим, в особенности в последние годы, активно внедряются в повседневную клиническую практику различные методы локальной терапии для лечения неоперабельного рака печени, к которым относятся радиочастотная абляция, микроволновая абляция, лазерная абляция, ультразвуковая абляция (HIFU или ), необратимая электропорация () и криоабляция. Однако только 3 технологии из перечисленных в 2016 году были включены в клинические рекомендации Европейского Сообщества Медицинской Онкологии (EMSO) по лечению метастатического колоректального рака — радиочастотная абляция, микроволновая абляция и криоабляция.
Несмотря на то, что радиочастотная абляция является более распространенным методом локального лечения рака печени и других онкологических заболеваний, микроволновая абляция считается более перспективной технологией и облагает рядом важных преимуществ перед радиочастотной абляцией:
Показания к применению
Микроволновая абляция широко применяется при лечении первичного и метастатического рака печени, как самостоятельный метод лечения, так и в комбинации с другими методами. К общим показаниям к применению микроволновой абляции при лечении рака печени относятся:
Перечисленные выше показания к применению микроволновой абляции при лечении рака печени являются общими и не ограничивают применение метода. Окончательное решение о применении микроволновой абляции принимает врач индивидуально для каждого пациента в зависимости от прогрессивности заболевания и общего состояния здоровья.
Позаботьтесь о себе, запишитесь на консультацию сейчас
Радиочастотная абляция опухолей печени
Общая информация
Краткое описание
Одобрено
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения и социального развития Республики Казахстан
от «29» ноября 2016 года
Протокол №16
Приложение 1
к типовой структуре
Клинического протокола диагностики и лечения
Название оперативного и диагностического вмешательства: Радиочастотная абляция опухолей печени.
Лечение
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Цель проведения процедуры/вмешательства: целью радиочастотной абляции (РЧА) является полный некроз злокачественного новообразования в печени (первичного и метастатического) с возможностью длительной безрецидивной выживаемостью.
Радиочастотная абляция – это метод разрушения опухолевой ткани с помощью высокоэнергетических радиоволн, в процессе которого происходит нагревание клеток опухоли до высоких температур и, как следствие, их гибель. Радиочастотная абляция способствует как частичному, так и полному удалению опухоли.
Показания и противопоказания для проведения процедуры/ вмешательства:
Показания к проведению РЧА злокачественных (первичных и метастатических) опухолей печени:
· наличие противопоказаний к хирургической резекции печени, отказ в хирургическом лечении;
· отсутствие внепеченочных проявлений заболевания;
· наличие в печени 1 опухолевого узла до 5 см либо 3–4 узлов до 3 см в диаметре;
· остаточная опухоль после ранее проведенной РЧА либо другого метода лечения;
· местный рецидив после ранее проведенной РЧА, резекции печени либо другого метода лечения;
· опухоли, визуализируемые при УЗКТ, РКТ;
· возможность безопасного доступа к опухоли (расположение узлов не ближе 1 см от воротной либо печеночных вен, долевых желчных протоков);
· согласие больного на проведение лечения.
Противопоказания к проведению РЧА злокачественных опухолей печени
Абсолютные:
· некорригируемая коагулопатия;
· сепсис;
· энцефалопатия;
· декомпенсированный цирроз (Child-Pugh C);
· терминальная стадия болезни (Okuda III);
· активное желудочно-кишечное кровотечение;
· некупируемый асцит.
Относительные:
· наличие у пациента искусственного водителя ритма;
· внепеченочные проявления заболевания;
· почечная недостаточность;
· несмещаемое прилежание опухолевого узла к соседним органам (желчный пузырь, желудок, кишечник) и крупным желчным протокам.
Перечень основных и дополнительных диагностических мероприятий (отдельно перечислить основные/обязательные и дополнительные обследования, консультации специалистов с указанием цели и показаний):
Основные (обязательные) диагностические обследования:
· ОАК с тромбоцитами;
· ОАМ;
· Группа крови и резус-фактор;
· Биохимический анализ крови: общий белок с фракциями, АЛТ, АСТ, общий/прямой билирубин, ЩФ, ГГТП, ЛДГ, креатинин, мочевина, амилаза, глюкоза;
· Электролиты: калий, натрий;
· Микрореакция;
· Коагулограмма: протромбиновое время, МНО, АЧТВ, фибриноген;
· Маркеры вирусных гепатитов: HBsAg, anti-HCV, ВИЧ;
· Альфа-фетопротеин;
· УЗИ органов брюшной полости;
· Рентгенография органов грудной клетки
Методика проведения процедуры/вмешательства
Требования к оснащению, расходным материалам, лекарственным средствам: согласно приказа и.о. Министра здравоохранения Республики Казахстан от 12 августа 2011 года № 540 «Об утверждении Положения о деятельности организаций здравоохранения, оказывающих онкологическую помощь населению Республики Казахстан».
Требования к оснащению, расходным материалам, медикаментам:
· Наличие всех инструментов/оборудования, необходимых для радиочастотной абляции рака печени-генератора, системы охлаждения;
· Помещение должно быть оснащено системой вентиляции, обеспечивающей оптимальные условия для профилактики хирургической инфекции и работы с газами, используемыми при анестезии;
· Наличие инструментов, расходных материалов и оборудования для проведения анестезиологического пособия. Инструменты и оборудование должны находиться непосредственно в операционной или смежных помещениях и быть доступны в любое время;
· Любая сертифицированная система для РЧА опухолей: одноигольчатые электроды с максимальным диаметром воздействия 3 см, выдвигающиеся электроды с максимальным диаметром воздействия 5см и др;
· Система лучевой навигации: РКТ,УЗИ, МРТ;
· Анестезиологическое оборудование (аппарат для искусственной вентиляции легких, монитор для контроля сердечной деятельности, артериального давления, сатурации и др.);
· Динамический контроль: КТ с внутривенным контрастным усилением, ПЭТ/КТ, МРТ с внутривенным контрастным усилением. Критерии оценки результатов: mRECIST, EASL.
Основные расходные материалы:
· Набор белья для чреспеченочных процедур;
· Комплект кластерных или 1-3 одиночных электродов для РЧА;
· Генератор;
· Насос и Система охлаждения;
· Емкость для воды;
· Ножной выключатель;
· Ультразвуковой аппарат
Дополнительные расходные материалы:
· Венозный катетер;
· Система одноразовая для инфузий;
· Скальпель одноразовый;
· Марля медицинская;
· Шприцы 20 мл;
· Шприцы 10 мл;
· Перчатки стерильные;
· Перчатки нестерильные;
· Шапочки одноразовые;
· Маски хирургические;
· Бахилы одноразовые;
· Одноразовые электроды для ЭКГ
Требования к подготовке пациента:
· вечером накануне операции легкий ужин до 20.00;
· в день операции – голод;
· побрить операционное поле накануне операции;
· провести перед операцией все гигиенические процедуры: прополоскать полость рта, почистить зубы, снять съемные зубные протезы, очистить полость носа, мужчинам побриться;
· обработка операционного поля препаратами бактерицидного действия;
Методика проведения процедуры/вмешательства:
· Собрать систему для радиочастотной абляции по инструкции;
· Положение больного – лежа на спине, либо на боку в зависимости от доступа;
· Возвратные электроды пациента зафиксировать на бедрах пациента;
· Процедура проводится, как правило, под внутривенной наркозом или интубационным анестезией;
· Выбор электрода определялся размером очага и удаленностью от поверхности кожи;
· Пункция очага производится под УЗ-контролем (консвексный датчик 3.5 МГц с пункционным адаптером), необходимо, чтобы аблационная часть иглы располагалась в центре опухоли. При выявлении эксцентрического расположения электрода необходимо произвести повторную пункцию очага с предварительной термообработкой старого пункционного канала во избежание кровотечения или опухолевой диссеминации, либо введение дополнительных электродов в очаг и обработка его из нескольких точек;
· Можно ввести несколько электродов одномоментно при наличии несколько рядом расположенных очагов во избежание «потери» очага после РЧА соседнего;
· Удостоверившись в правильном расположении электрода, начинается воздействие на опухоль током частотой 450-500 кГц. В результате опухолевая ткань разогревается до температуры (60-90°С), при которой происходят необратимые изменения в клетках. Опухолевая масса некротизируется. Время воздействия на опухоль 12 минут, если опухоль до 3см. Для очень крупных опухолей игольчатые электроды группируют по три в одной рукоятке (электрод-кластер) на расстоянии 0,5 см параллельно друг другу. Именно такие охлаждаемые инструменты позволяют быстро коагулировать опухоли 5-7 см в диаметре и больше. В конце 12-минутного сеанса лечения электрод извлекается при работающем генераторе и коагулирует пункционный канал.
Индикаторы эффективности процедуры/вмешательства:
· отсутствие в послеоперационный период выявляемого всеми доступными визуализационными методами роста резидуальных опухолевых очагов в зоне выполненной абляции;
· отсутствие послеоперационных осложнений (осложнений, связанных с доступом и процедурой);
· снижение количества инвалидизирующих оперативных вмешательств;
· возможность многократного миниинвазивного проведения РЧА деструкции;
· повышение ожидаемой продолжительности жизни;
· повышение качества жизни.
Информация
Источники и литература
Информация
Список разработчиков протокола с указанием квалификационных данных:
1) Боровский Сергей Петрович – доктор медицинских наук, АО «Национальный научный центр онкологии и трансплантологии», заведующий отделением интервенционной рентгенохирургии.
2) Калиаскарова Кульпаш Сагындыковна – доктор медицинских наук, главный внештатный гепатолог МЗСР РК, руководитель координационного центра гепатологии и гастроэнтерологии КФ «UMC».
3) Малаев Нияз Бейсенович – MSc, MBA., АО «Национальный научный центр онкологии и трансплантологии», врач рентгенохирург высшей категории, отделения «Интервенционной рентгенохирургии».
4) Нурсеитов Ильяс Ержанович – врач интервенционный рентгенохирург, «Казахский национальный научный исследовательский институт онкологии и радиологии».
Указание на отсутствие конфликта интересов: нет.
Рецензент:
1) Кузикеев Марат Оразович – доктор медицинских наук, профессор, руководитель центра абдоминальной онкологии «Казахская научно-исследовательский институт онкологии и радиологии».
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Абляция опухолей печени
Главный врач
Доктор Елена Кацман
Гастроэнтеролог
Обзор
Преимущества и недостатки абляционной терапии опухолей печени
По сравнению с другими способами лечения опухолей печени, абляционные методы представляют собой быстрый подход с меньшим количеством побочных эффектов и более коротким периодом госпитализации. Процедуры минимально инвазивны, вследствие чего период восстановления значительно сокращается. Благодаря использованию методов визуализации при введении и размещении иглы, здоровые ткани не страдают и только пораженный опухолью участок подвергается обработке. В отличие от других видов терапии, положительные результаты абляционного вмешательства достигаются практически немедленно. Этот вид терапии при необходимости можно легко повторить, и он может быть использован в сочетании с противоопухолевыми препаратами.
Побочные эффекты абляционной терапии включают боли в животе и, иногда, лихорадку, но обе эти проблемы могут быть решены с использованием соответствующих медикаментозных средств.
Показания к процедуре

Факторы риска
Противопоказания
Применение абляции не рекомендуется для опухолей размером более 3 см в диаметре. Для опухолей от 3 до 5 сантиметров в размере абляция может быть использована только в сочетании с процедурами эмболизации (избирательной закупорки кровеносных сосудов, снабжающих опухоль кровью).
Несмотря на то, что абляция – это локальная малоинвазивная процедура, существует риск повреждения соседних здоровых тканей. В связи с этим не рекомендуется применять абляцию к опухолям, расположенным рядом с основными кровеносными сосудами, диафрагмой или желчными протоками.