Что такое 5fes в химии
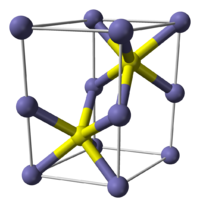
Сульфид железа(II)
| Сульфид железа(II) | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Сульфид железа(II) |
| Химическая формула | FeS |
| Эмпирическая формула | FeS |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 87,910 г/моль |
| Плотность | 4,84 г/см³ |
| Термические свойства | |
| Температура плавления | 1194 °C |
| Классификация | |
| Рег. номер CAS | 1317-37-9 |
Сульфид железа (II) — сложное неорганическое вещество с химической формулой FeS.
Содержание
Описание
Сульфид железа (II) — бескислородная соль. Черно-серого цвета с зеленым оттенком, тугоплавкий, разлагается при нагревании в вакууме. Во влажном состоянии чувствителен к кислороду воздуха. Нерастворим в воде. Не выпадает в осадок при насыщении растворов солей железа (II) сероводородом. Разлагается кислотами. Применяется как сырье в производстве чугуна, твердый источник сероводорода.
Получение
1. Взаимодействие железа с серой:
Химические свойства
1. Взаимодействие с концентрированной HCl:
2. Взаимодействие с концентрированной HNO3:
См. также
Литература
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | — | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Сульфид железа(II)» в других словарях:
сульфид железа(II) — односернистое железо, сернистое железо(II) … Cловарь химических синонимов I
Сульфид меди(I) — Кристалличесая структура халькозина … Википедия
Сульфид бериллия — Общие Систематическое наименование Сульфид бериллия Традиционные названия Сернистый бериллий Химическая формула BeS Эмпирическая формула BeS Физ … Википедия
Сульфид кальция — Общие … Википедия
Сульфид хрома(II) — Общие Систематическое наименование Сульфид хрома(II) Традиционные названия Сернистый хром Химическая формула CrS Физические свойства Состояние ( … Википедия
Сульфид хрома(III) — Общие Систематическое наименование Сульфид хрома(III) Традиционные названия Сернистый хром Химическая формула Cr2S3 Физические свойства … Википедия
Сульфид рутения(IV) — Общие Систематическое наименование Сульфид рутения(IV) Традиционные названия Сернистый рутений(IV) Химическая формула RuS2 Физические свойства Со … Википедия
железа(III) сульфид — geležies(III) sulfidas statusas T sritis chemija formulė Fe₂S₃ atitikmenys: angl. ferric sulfide; iron(III) sulfide rus. железа трисульфид; железа(III) сульфид ryšiai: sinonimas – digeležies trisulfidas … Chemijos terminų aiškinamasis žodynas
железа(II) сульфид — geležies(II) sulfidas statusas T sritis chemija formulė FeS atitikmenys: angl. ferrous sulfide; iron(II) sulfide rus. железа(II) сульфид; железо сернистое … Chemijos terminų aiškinamasis žodynas
железа трисульфид — geležies(III) sulfidas statusas T sritis chemija formulė Fe₂S₃ atitikmenys: angl. ferric sulfide; iron(III) sulfide rus. железа трисульфид; железа(III) сульфид ryšiai: sinonimas – digeležies trisulfidas … Chemijos terminų aiškinamasis žodynas
Что означают записи: 4h, 2h2, hgo, 5fes, 3h2so4?
Значит по-порядку. 4h это скорее всего количество атомарного водорода в веществе к примеру в H4P2O7 количество атомарного водорода равно 4, а в HCl оно равно 1. 2h2 во-первых h2 это водород как вещество 2 передним это коэффициент, значит это вырвано их како-то реакции к примеру 2h2+O2=2h2O или любые другие. HgO это просто оксид двухвалентной ртути. Теперь 5fes(сульфид железа 2) и 3h2so4(серная кислота) это я уже рассматривал. Это просто вещества вырванные из реакций.
Поля удобряют одинаково нитратами (чаще всего комплексные удобрения, включая селитру), но тут дело в том что у них разные ткани. В арбузе больше воды, а значит и способность накапливать нитраты выше, но у дыни меньше воды и большая плотность, значит накопленные химикаты будут более концентрированы. Тут уже вопрос в другом. Насколько порядочен фермер, который их выращивает, и насколько он злоупотребляет этими самыми химикатами. Плюс влияет сезон дождей, чем их больше, тем меньше химикатов может удержаться и почве, они просто смываются в грунтовые воды (которые мы потом и пьем). А вот если дожди редкие и не затяжные (например раз в неделю или реже в 2 недели), то это оптимальные условия для впитывания растениями всех удобрений.
Сделаем вывод. Тут зависит от крупности и водянистости плода, от сезона дождей и самого фермера.
Использованный в задаче технический карбид кальция содержит примеси, массовая доля которых равна 0,36. Значит, массовая доля самого соединения карбид кальция (СаС2) равна 0,64. Соответственно, в 45 г технического продукта содержится 45*0,64=28,8 г карбида кальция. Молярная масса карбида кальция 40+2*12=64 г. 28,8 г СаС2 составляют 28,8/64=0,45 моль. Пишем уравнение реакции:
Но существует множество задач, когда объёмы газов пересчитываются к иным параметрам, не являющимся «нормальными условиями».
Хотел подредактировать, но система почему-то решила не дать возможность подредактировать. Пришлось давать второй ответ.
31 января (12 февраля)1865 года на заседании Совета физико-математического факультета Санкт-Петербургского университета Д.И.Менделеев защитил докторскую диссертацию «О соединении спирта с водой», в которой были заложены основы его учения о растворах.
В ней он исследовал удельный вес водно-спиртовых растворов, содержащих от 50 до 100 весовых % спирта, и контракцию (явление уменьшения объёма при смешивании жидкостей) растворов, содержащих от 40 до 55 весовых % спирта. Поэтому, вопреки распространенному заблуждению диссертация нисколько не связана с крепостью водки, так как была посвящена исследованию удельного веса высоких концентраций спирта, водочные же 40° при 20 °С соответствуют всего 33,3 весовым %.
Кроме того сам Менделеев предпочитал сухое вино, водку не пил и отзывался о ней так: «Неужели, в самом деле, положение наше таково, что в кабаке, казенном или частном, должно видеть спасение для экономического быта народа, то есть России, и в водке, да в способах ее потребления искать исхода для улучшения современного состояния дел народных и государственных»
Сера. Химия серы и ее соединений
Положение в периодической системе химических элементов
Сера расположена в главной подгруппе VI группы (или в 15 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение серы
Электронная конфигурация серы в основном состоянии :
Атом серы содержит на внешнем энергетическом уровне 2 неспаренных электрона и две неподеленные электронные пары в основном энергетическом состоянии. Следовательно, атом серы может образовывать 2 связи по обменному механизму, как и кислород. Однако, в отличие от кислорода, за счет вакантной 3d орбитали атом серы может переходить в возбужденные энергетические состояния. Электронная конфигурация серы в первом возбужденном состоянии:
Электронная конфигурация серы во втором возбужденном состоянии:
Таким образом, максимальная валентность серы в соединениях равна VI (в отличие от кислорода). Также для серы характерна валентность — IV.
Физические свойства и нахождение в природе
Сера образует различные простые вещества (аллотропные модификации).
Пластическая сера – это вещество, состоящее из длинных полимерных цепей. Коричневая резиноподобная аморфная масса, нерастворимая в воде.
В природе сера встречается:
Соединения серы
Типичные соединения серы:
| Степень окисления | Типичные соединения |
| +6 | Оксид серы(VI) SO3 Галогенангидриды: SО2Cl2 |
| +4 | Оксид серы (IV) SO2 Галогенангидриды: SOCl2 |
| –2 | Сероводород H2S Сульфиды металлов MeS |
Способы получения серы
1. В промышленных масштабах серу получают открытым способом на месторождениях самородной серы, либо из вулканов. Из серной руды серу получают также пароводяными, фильтрационными, термическими, центрифугальными и экстракционными методами. Пароводяной метод — это выплавление из руды с помощью водяного пара.
2. Способ получения серы в лаборатории – неполное окисление сероводорода.
3. Еще один способ получения серы – взаимодействие сероводорода с оксидом серы (IV):
Химические свойства серы
В нормальных условиях химическая активность серы невелика: при нагревании сера активна, и может быть как окислителем, так и восстановителем.
1.1. При горении серы на воздухе образуется оксид серы (IV) :
1.2. При взаимодействии серы с галогенами (со всеми, кроме йода) образуются галогениды серы:
1.3. При взаимодействии фосфора и углерода с серой образуются сульфиды фосфора и сероуглерод:
2S + C → CS2
1.4. При взаимодействии с металлами сера проявляет свойства окислителя, продукты реакции называют сульфидами. С щелочными металлами сера реагирует без нагревания, а с остальными металлами (кроме золота и платины) – только при нагревании.
S + Fe → FeS
S + Hg → HgS
Еще пример : алюминий взаимодействует с серой с образованием сульфида алюминия:
1.5. С водородом сера взаимодействует при нагревании с образованием сероводорода:
2. Со сложными веществами сера реагирует, также проявляя окислительные и восстановительные свойства. Сера диспропорционирует при взаимодействии с некоторыми веществами.
2.1. При взаимодействии с окислителями сера окисляется до оксида серы (IV) или до серной кислоты (если реакция протекает в растворе).
Серная кислота также окисляет серу. Но, поскольку S +6 не может окислить серу же до степени окисления +6, образуется оксид серы (IV):
S + 2KClO3 → 3SO2 + 2KCl
Взаимодействие серы с сульфитами (при кипячении) приводит к образованию тиосульфатов:
2.2. При растворении в щелочах сера диспропорционирует до сульфита и сульфида.
При взаимодействии с перегретым паром сера диспропорционирует:
Сероводород
Строение молекулы и физические свойства
Сероводород H2S – это бинарное соединение водорода с серой, относится к летучим водородным соединениям. Следовательно, сероводород бесцветный ядовитый газ, с запахом тухлых яиц. Образуется при гниении. В твердом состоянии имеет молекулярную кристаллическую решетку.
Способы получения сероводорода
В лаборатории сероводород получают действием минеральных кислот на сульфиды металлов, расположенных в ряду напряжений левее железа.
FeS + 2HCl → FeCl2 + H2S↑
Еще один способ получения сероводорода – прямой синтез из водорода и серы:
Еще один лабораторный способ получения сероводорода – нагревание парафина с серой.
Видеоопыт получения и обнаружения сероводорода можно посмотреть здесь.
Химические свойства сероводорода
1. В водном растворе сероводород проявляет слабые кислотные свойства. Взаимодействует с сильными основаниями, образуя сульфиды и гидросульфиды:
H2S + 2NaOH → Na2S + 2H2O
H2S + NaOH → NaНS + H2O
В избытке кислорода:
3. Как сильный восстановитель, сероводород легко окисляется под действием окислителей.
Например, бром и хлор окисляют сероводород до молекулярной серы:
H2S + Br2 → 2HBr + S↓
H2S + Cl2 → 2HCl + S↓
Под действием избытка хлора в водном растворе сероводород окисляется до серной кислоты:
При кипячении сера окисляется до серной кислоты:
Прочие окислители окисляют сероводород, как правило, до молекулярной серы.
Соединения железа (III) также окисляют сероводород:
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
Бихроматы, хроматы и прочие окислители также окисляют сероводород до молекулярной серы:
Серная кислота окисляет сероводород либо до молекулярной серы:
Либо до оксида серы (IV):
4. Сероводород в растворе реагирует с растворимыми солями тяжелых металлов : меди, серебра, свинца, ртути, образуя черные сульфиды, нерастворимые ни в воде, ни в минеральных кислотах.
Взаимодействие с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Видеоопыт взаимодействия сероводорода с нитратом свинца можно посмотреть здесь.
Сульфиды
Сульфиды – это бинарные соединения серы и металлов или некоторых неметаллов, соли сероводородной кислоты.
По растворимости в воде и кислотах сульфиды разделяют на растворимые в воде, нерастворимые в воде, но растворимые в минеральных кислотах, нерастворимые ни в воде, ни в минеральных кислотах, гидролизуемые водой.



















