Что снижает ферритин у женщин в крови
Синдром перегрузки железом при хронических заболеваниях печени: фокус на неалкогольную жировую болезнь печени
Статья посвящена вопросам терапии синдрома перегрузки железом (СПЖ) при хронических заболеваниях печени (ХЗП). Рассмотрены роль железа и его метаболизм в организме человека, механизмы и диагностика СПЖ у пациента с ХЗП, особенности клинических проявлений
The article is dedicated to the issues of therapy of iron overload syndrome (IOS) in chronic hepatic diseases (CHD). Role of iron and its metabolism in human organism were considered, as well as the mechanisms and diagnostics of IOS in a patient with CHD, features of clinical manifestations of iron metabolism disorders and methods of IOS treatment.
На сегодняшний день синдром перегрузки железом (СПЖ) при хронических заболеваниях печени (ХЗП) недостаточно полно освещен в литературе и малоизвестен практикующему врачу. При этом СПЖ у данной категории больных часто является более тяжелым нарушением, нежели дефицит железа, и может приводить к необратимым последствиям [2, 5, 16].
В последние годы регистрируется высокая распространенность первичного СПЖ — наследственного гемохроматоза (НГ) в популяции (до 1:250 среди жителей Северной Европы, манифестные формы — 2:1000), а также обнаружены новые мутации в генах, регулирующих обмен железа [8, 18, 23]. Тогда как далеко не все клиницисты осведомлены, что вторичный СПЖ, возникающий при развитии ХЗП, в том числе при такой частой на сегодняшний день патологии, как неалкогольная жировая болезнь печени (НЖБП), наблюдается почти у каждого третьего пациента (в 20–30% случаев). Нередко при этом, по данным некоторых авторов, у 36,7% больных ХЗП обнаруживаются мутантные гены в гетерозиготном состоянии (C282/N, H63D/N), которые сами по себе не приводят к развитию НГ, однако при возникновении патологии печени способствуют манифестации СПЖ [18, 28].
Результаты исследований свидетельствуют, что раннее обнаружение и лечение СПЖ у пациентов с ХЗП позволяет предотвратить прогрессирование заболевания печени до цирротической стадии и значительно уменьшает риск гепатоцеллюлярной карциномы (ГЦК) [2, 4, 26, 31].
В этой связи необходимы новые подходы к диагностике, оценке клинической картины, лечению данного состояния и практическому специалисту актуально получение ответов на следующие вопросы:
Роль железа и его метаболизм в организме человека
В литературе последних лет появились новые данные о метаболизме железа (Fe) в организме человека, в связи с открытием белков-регуляторов, участвующих в обмене этого микроэлемента [1, 17, 20].
Известно, что железо является важнейшим элементом, участвующим в метаболизме организмов, живущих в среде, богатой кислородом. Обладая выраженными окислительно-восстановительными свойствами, оно необходимо для транспорта кислорода гемоглобином, синтеза дезоксирибонуклеиновой кислоты (ДНК), работы митохондриальных ферментов. Как металл с переменной валентностью, железо в составе негемовых энзимов (каталазы, пероксидазы, цитохрома) нейтрализует активные формы кислорода. Однако увеличение пула Fe III может являться катализатором образования свободных радикалов и инициатором оксидативного стресса. С целью компенсации, в организме предусмотрены естественные антиоксиданты — хелаторы Fe III, к которым относятся мочевая кислота (МК), церулоплазмин, супероксиддисмутаза, ферритин, трансферрин.
У человека в норме содержится около 3–4 г железа (40–50 мг Fe/кг). Суточная потребность в этом элементе в пище составляет около 10 мг для мужчин и 20 мг для женщин детородного возраста. При этом всасывается лишь 1–2 мг и почти столько же теряется со слущиваемым эпителием желудочно-кишечного тракта, эпидермисом, потом и мочой. Основная масса необходимого железа ежедневно поступает в циркуляцию из клеток ретикулоэндотелиальной системы (РЭС) (селезенка, печень, костный мозг).
Всасывание железа осуществляется эпителиальными клетками двенадцатиперстной кишки и начальных отделов тощей кишки и находится под строгим контролем белков-регуляторов обмена железа.
Известно, что гемовое железо (Fe II), находящееся в составе гемоглобина и миоглобина (в мясных продуктах), усваивается человеком на 20–30% независимо от желудочной секреции и состава пищи. Гемовое железо легко эндоцитируется энтероцитом после сливания с транспортером гемового железа (НСР1). Негемовое железо (Fe III), содержащееся в растительной пище, усваивается человеком на 1–7% и во многом зависит от сопутствующих пищевых факторов (табл. 1).
Всасывание негемового железа — сложный энергозависимый транспортный процесс. Оно происходит после восстановления Fe III до Fe II при помощи соляной кислоты желудочного сока и дуоденального цитохрома — ферроредуктазы (Dcyt b). Затем Fe II переносится в энтероцит специальным транспортером двухвалентных ионов (ДMT1).
Часть железа, которая не используется клеткой, депонируется в виде ферритина и гемосидерина в печени, селезенке, костном мозге, мышечной ткани. Ферритин — внутриклеточный комплекс, содержащий белок-апоферритин, связывающий до 4 тысяч атомов железа. Существует 5 изоформ ферритина: щелочные изоформы печени и селезенки отвечают за депонирование железа, а кислые изоформы миокарда, плаценты, опухолевых клеток являются посредниками в процессах синтеза и участвуют в регуляции Т-клеточного иммунного ответа. Поэтому ферритин является еще и белком острого воспаления и опухолевого роста. Гемосидерин — нерастворимая часть ферритина, форма депонирования избыточного железа.
Поступление железа (Fe II) в кровь из энтероцита, а также из клеток печени, макрофагов селезенки, костного мозга осуществляется единственным белком-переносчиком — ферропортином. В 2001 г. был открыт важнейший регулятор обмена железа и функции ферропортина — гепсидин. Этот белок, состоящий из 25 аминокислот, синтезируется печенью, а также, по некоторым данным, клетками жировой ткани при ожирении [24].
Ранее он был известен как белок острой фазы, обладающий антибактериальными свойствами, благодаря способности уменьшать поступление железа к микроорганизмам, блокировать их размножение, разрушать бактериальные мембраны. Основными стимуляторами синтеза гепсидина при воспалении являются провоспалительные цитокины — ИЛ-6 и ФНО-а. На сегодняшний день известно, что именно гепсидин, уровень которого повышается при воспалении, а также опухолевом процессе, играет основную роль в развитии анемии хронического воспаления [35]. Гепсидин регулирует сывороточную концентрацию железа, путем «выключения» работы ферропортина (в этом случае железо накапливается в энтероцитах, макрофагах, гепатоцитах). При повышении железа в крови — увеличивается синтез гепсидина. В результате блокируются процессы всасывания (угнетается работа ДMT1), рециркуляции и высвобождения железа из депо.
Транспорт железа от энтероцитов и органов-депо к костному мозгу и другим тканям осуществляет трансферрин, синтезируемый печенью. Этот белок способен переносить только Fe III. Поэтому на поверхности мембран клеток происходит окисление Fe II в Fe III при помощи ферментов-ферроксидаз — гефестина и церулоплазмина. Трансферрин является отрицательным белком острой фазы.
Железо (Fе III), связанное с трансферрином, поступает внутрь клетки посредством специальных трансферриновых рецепторов 1-го и 2-го типа (TfR). Под действием внутриклеточных ферроредуктаз Fe III вновь восстанавливается в Fe II. Синтез трансферриновых рецепторов в клетке зависит от ее потребностей в железе и строго регулируется системой внутриклеточных белков (IRP1, IRP2, IRE). Образование комплекса трансферрина с TfR и их эндоцитоз внутрь клетки контролируется белком HFE, при мутации гена которого развивается НГ.
Механизмы развития СПЖ
По имеющимся на сегодняшний день данным, организм человека не имеет средств контроля за экскрецией железа. Интестинальная абсорбция — основной этап, который тщательно регулируется. Поэтому любые ситуации, связанные с избыточным поступлением железа в кровь (при парентеральном введении препаратов железа, переливании крови, гемолизе) или всасыванием (наследственные и приобретенные механизмы), могут приводить к СПЖ.
Таким образом, развитие СПЖ обуславливается как наследственными причинами, так и приобретенными факторами (табл. 2).
Среди основных этиологических факторов можно выделить «триаду»:
1) гемолиз эритроцитов (сидероахрестические анемии, талассемия, недостаточность глюкозо-6-фосфатдегидрогеназы, микросфероцитоз, дефицит витамина В12);
2) избыточное экзогенное поступление железа (диета, многократные гемотрансфузии, длительное бесконтрольное применение парентеральных препаратов железа, хронический гемодиализ);
3) заболевания печени (хронический вирусный гепатит С, реже В, алкогольная болезнь печени, НЖБП, кожная порфирия).
При СПЖ железо оказывает негативное влияние на организм. Перенасыщение трансферрина железом сопровождается включением дополнительного транcпорта железа, связанного с альбумином. Данный комплекс легко проникает в клетки, не предназначенные для депонирования железа (миокард, гонады, поджелудочная железа и др.), и вызывает токсические эффекты. При избыточном накоплении железа в органах-депо, а также тканях, не являющихся таковыми, происходит усиление образования коллагена и прямое повреждение ДНК. При переходе Fe III в Fe II образуются токсичные свободные радикалы, активирующие процессы перекисного окисления. При выраженном СПЖ в организме работа собственных антиоксидантных систем защиты становится неэффективной.
Тем не менее патогенез СПЖ у больных с ХЗП остается не до конца ясным. Возможными механизмами могут являться:
Признаки СПЖ
СПЖ выявляется при оценке совокупности признаков:
1. Клинические признаки
В зависимости от причины СПЖ весьма вариабельны. Могут наблюдаться проявления стеатоза или цирроза печени, меланодермия, гипогонадизм, дисфункция надпочечников, гипотиреоз, артропатия, сахарный диабет 2-го типа, гиперурикемия [5, 13, 18, 29].
2. Лабораторные маркеры СПЖ
Показатели клинического анализа крови при СПЖ не являются специфичными, гемоглобин, эритроциты, цветовой показатель могут быть даже снижены (например, при гемолитической анемии, талассемии). При НГ, а также СПЖ, связанном с ХЗП, нередко обнаруживается повышение уровня гемоглобина.
Согласно мнению специалистов, лабораторными маркерами СПЖ являются [26]:
Рекомендации Европейского общества по изучению заболеваний печени (European association for the study of the liver, EASL) по лабораторной диагностике СПЖ, 2010 [26]:
Как правило, при воспалении повышение ферритина сочетается с нормальными показателями НТЖ. В ряде случаев требуется учитывать, что повышение НТЖ может быть «ложным» при печеночно-клеточной недостаточности и снижении синтеза трансферрина, а также при синдроме мальабсорбции белков. Однако, по мнению специалистов, НТЖ — самый информативный показатель статуса железа и может использоваться для скрининга патогенетически значимых нарушений обмена железом у больных с ХЗП [18].
3. Генетическое тестирование
Применяется для исключения первичного СПЖ. На сегодняшний день доступными методами диагностики НГ являются:
Рекомендации EASL по генетическому тестированию, 2010 [26]:
4. Морфологическое исследование
Для подтверждения СПЖ в случаях, когда его маркеры сомнительны, а также в целях дифференциальной диагностики заболеваний печени показано проведение биопсии печени с окраской берлинской лазурью на железо (гемосидерин) по Перлсу и определением количественного содержания железа в препарате (печеночный индекс железа (ПИЖ) — Fе в печени/возраст). При НГ данный показатель более 1,9.
Рекомендации EASL по проведению гепатобиопсии при СПЖ, 2010 [26]:
5. МРТ печени и сердца в режиме Т2
Может использоваться как метод дополнительного измерения содержания железа в печени, а также миокарде, как альтернатива биопсии [11].
6. Десфераловая проба
Проводится в сомнительных случаях СПЖ и при необходимости проведения дифференциального диагноза между первичным и вторичным СПЖ. После внутримышечго введения 0,5 г Десферала производится последующий анализ суточной экскреции железа. В норме этот показатель составляет менее 1 мг/сут (менее 18 мкмоль/л), при СПЖ — 18–27 мкмоль/л, при НГ — более 27 мкмоль/л [4, 11].
Механизмы развития и клинические проявления СПЖ при НЖБП
На сегодняшний день установлено, что СПЖ обнаруживается примерно у 1/3 больных НЖБП: у 30% пациентов с жировым гепатозом (ЖГ), у 34% больных с неалкогольным стеатогепатитом (НАСГ) [4, 6, 15].
Впервые СПЖ у пациентов с НЖБП был описан в 1997 г. R. Moirand и Y. Deugnier, которые предложили термин «дисметаболический синдром перегрузки железом» (ДСПЖ, Dysmetabolic iron overload syndrome (DIOS)) [25]. В 1999 г. M. Mendler и соавт. доказали наличие СПЖ у пациентов с ИР и метаболическим синдромом (Insulin resistance hepatic iron overload syndrom (IR-HIO)) [32]. Был описан «железный фенотип» синдрома ИР. В 2008 г. A. Riva и соавт. предложили критерии синдрома DIOS/IR-HIO [34].
Важно знать, что СПЖ у данной категории пациентов является фактором риска, предрасполагающим к развитию и прогрессированию ИР, СД и сердечно-сосудистых заболеваний. Так, установлено, что высокий ферритин более 400 мкг/л у мужчин и более 300 мкг/л у женщин с ожирением является маркером ИР [34]. Гиперферритинемия, при исключении воспалительного процесса, требует тщательного контроля за уровнем гликемии у больных НЖБП, так как увеличивает риск СД в 4,6 раза [16]. Повышенный уровень ферритина может быть также предиктором стеатоза печени и предшествовать его развитию, что свидетельствует о том, что причиной гиперферритинемии является не НЖБП, а гиперферритинемия, связанная с ожирением и ИР, что приводит к НЖБП [14, 15].
В основе развития СПЖ при НЖБП лежит ИР, гипергликемия и висцеральное ожирение.
При ИР и гиперинсулинемии происходит повышенная транслокация трансферриновых рецепторов на мембранах гепатоцитов, энтероцитов, приводящая к увеличению поступления железа в клетку и стимулированию синтеза ферритина [27]. В свою очередь, при перегрузке железом гепатоцитов нарушается поглощение и деградация инсулина печенью, что усугубляет гиперинсулинемию. Избыток железа (Fe III), катализируя образование свободных радикалов, нарушает процесс проведения инсулинового сигнала и соединение инсулина с инсулиновым рецептором. Стимулируется синтез глюкозы в печени. При стойкой гипергликемии возникает гликирование трансферрина, приводящее к нарушению связывания Fe III и его транспорта к органам-потребителям.
Абдоминальная жировая ткань, обладающая собственной гормональной активностью, при липолизе выделяет провоспалительные цитокины (ФНО, ИЛ-6, ИЛ-8, ИЛ-10), что приводит к инфильтрации жировой ткани макрофагами, которые активно накапливают железо. Это индуцирует окислительный стресс и воспалительную реакцию. Таким образом, формируется порочный круг. Повышенная продукция вышеперечисленных цитокинов стимулирует синтез гепсидина, причем не только в гепатоцитах, но и в клетках жировой ткани [24]. Гепсидин блокирует работу ферропортина, в результате чего тормозятся процессы абсорбции пищевого железа, высвобождения железа из клеток, соответственно, стимулируется синтез ферритина. При этом, в результате повышенного синтеза гепсидина, у некоторых пациентов, чаще подростков и фертильных женщин, а также лиц с морбидным ожирением (индекс массы тела более 40), может даже развиваться анемия хронического воспаления, с недостаточностью железа, вследствие уменьшения его всасывания в тонкой кишке и перераспределения в клетки РЭС, а не на нужды синтеза гемоглобина [6, 7, 14].
Этот «железодефицитный» фенотип ожирения характеризуется как признаками относительного железодефицита, так и ДСПЖ. В данном случае оценка такого параметра крови, как количество растворимых трансферриновых рецепторов, может помочь в диагностике истинного дефицита железа, так как не зависит от активности воспалительного процесса, влияющего на содержание ферритина. Дополнительным предиктором наличия «функционального» дефицита железа служит также уровень С-реактивного белка.
Преимущественное накопление железа в гепатоцитах и клетках Купфера в перисинусоидальном пространстве запускает процессы проапоптоза, некроза, коллагенообразования и является триггерным механизмом прогрессирования ЖГ в НАСГ, с последующим развитием ФП, ЦП и ГЦК.
Дополнительным фактором, усугубляющим СПЖ у пациентов с НЖБП, по мнению некоторых авторов, может быть нарушение экскреции МК почками (например, при диабетической нефропатии) [5]. МК, являясь естественным хелатором негемового железа (Fe III), в условиях гиперферремии усиленно продуцируется в ксантинооксидазной реакции. Первоначально повышение уровня МК в крови и/или ее экскреции с мочой свидетельствует о включении компенсаторной реакции организма, Так, при НТЖ ниже 30%, повышение МК и ее экскреции способствует адекватному выведению с мочой избытка железа и поддержанию его физиологического уровня. При НТЖ 30–45% наблюдается более выраженное повышение МК, при недостаточно эффективной экскреции. При НТЖ более 45% уровень урикемии не соответствует механизму антиоксидантной защиты [5].
Критерии постановки диагноза ДСПЖ:
1) наличие двух и более компонентов метаболического синдрома (ожирение, дислипидемия, артериальная гипертензия, гипергликемия или нарушение толерантности к глюкозе);
2) гиперферритинемия при нормальном или незначительно повышенном НТЖ;
3) наличие стеатоза печени;
4) легкое или умеренное повышение содержания железа в печени (по данным МРТ или гепатобиопсии, ПИЖ менее 1,9 (рис. 1)).
Дополнительными маркерами СПЖ при НЖБП могут служить также повышение уровня гепсидина (определение данного показателя в настоящее время малодоступно), МК в крови и/или ее суточной экскреции с мочой.
Лечение СПЖ при ХЗП
Согласно мнению большинства специалистов, показаниями для лечения СПЖ у больных ХЗП являются:
1) клинически манифестный НГ;
2) повышение ферритина более 200 мкг/л у женщин и более 300 мкг/л у мужчин и женщин в постменопаузе или более 500 мкг/л у мужчин моложе 40 лет и у женщин до наступления менопаузы (при исключении острого воспаления, опухолевого процесса, алкогольного эксцесса);
3) НТЖ более 45%;
4) при НЖБП целесообразно рассматривать дополнительное показание: НТЖ 30–45% в сочетании с гиперурикемией и/или повышенной суточной экскрецией мочевой кислоты и гипергликемией [5].
Способы лечения СПЖ при ХЗП включают: этиотропную терапию, строгий отказ от алкоголя, соблюдение диеты с ограничением содержания железа до 8–10 мг/сут, лечебные кровопускания (флеботомии), с эксфузией до 300–400 мл крови 1 раз в неделю, до достижения целевого уровня ферритина ≤ 50 мкг/л и НТЖ ≤ 30%, использование антиоксидантов.
Согласно клиническим рекомендациям Европейских обществ по изучению заболеваний печени, ожирения и диабета (EASL, Европейского общества изучения диабета (European association for the study of diabetes, EASD), Европейского общества изучения ожирения (European Association for the Study of Obesity, EASO)), проведение флеботомии с целью уменьшения запасов железа почти до уровня железодефицита улучшает статус больных НЖБП по шкале NAS без прогрессирования фиброза, однако необходимы дополнительные данные. Как свидетельствуют специалисты, флеботомии при НЖБП уменьшают ИР, выраженность воспалительных изменений в печени, замедляют темпы прогрессирования фиброза печени и риски развития ГЦК [12].
При противопоказаниях к флеботомии (прежде всего, в случае НГ с повышением уровня ферритина более 1000 мкг/л, сочетающимся с анемией средней и тяжелой степени, выраженной гипотонией, гипоальбуминемией, СН) используются хелаторы железа (деферазирокс (Эксиджад), менее предпочтителен дефероксамин (Десферал)). Однако высокая стоимость препаратов и возможные побочные эффекты (диспептические расстройства, нарушение функции почек, печени, зрения, слуха и др.) ограничивают их применение.
В терапию СПЖ всем больным целесообразно включать антиоксиданты. Для этого могут применяться препараты янтарной кислоты, урсодезоксихолевая кислота (Урдокса), глицирризиновая кислота, липоевая кислота, адеметионин [5, 9].
Так, например, установлено, что антиоксидантный эффект янтарной кислоты связан с повышением активности глутатионпероксидазы и каталазы, важнейших ферментов, участвующих в разрушении активных форм кислорода, перекисей. Препарат также способствует увеличению уровня восстановленного глутатиона и подавлению активности ксантиноксидазы, что приводит к снижению продукции высокоактивных форм кислорода [9].
Глицирризиновая кислота как антиоксидант способна ингибировать образование супероксидного радикала и перекиси водорода [10].
Антиоксидантное действие урсодезоксихолевой кислоты связано с изменением метаболизма простагландинов и жирных кислот, а также снижением оксидативной активации клеток Купфера гидрофобными желчными кислотами. Несомненным достоинством данного препарата у пациентов с ХЗП и СПЖ является опосредованное антифибротическое действие, обусловленное снижением содержания активаторов фиброгенеза и угнетением активности звездчатых клеток [22, 30]. В исследовании J. Holoman и соавт. [38] продемонстрировано, что на фоне применения УДХК снижалась сывороточная концентрация N-терминального пептида коллагена III типа и матриксных металлопротеиназ и одновременно повышался уровень их тканевых ингибиторов, что клинически выражается в замедлении развития фиброза.
ФГБОУ ВО СПбГМУ им. И. П. Павлова МЗ РФ, Санкт-Петербург
Синдром перегрузки железом при хронических заболеваниях печени: фокус на неалкогольную жировую болезнь печени/ С. Н. Мехтиев, О. А. Мехтиева
Для цитирования: Лечащий врач №12/2017; Номера страниц в выпуске: 60-67
Теги: гемохроматоз, метаболизм, наследственность, метаболизм железа
Белок Ферритин
Записаться на прием
Задать вопрос онлайн
Заказать обратный звонок
Низкий уровень ферритина
Какие симптомы указывают на то, что стоит проверить уровень ферритина?
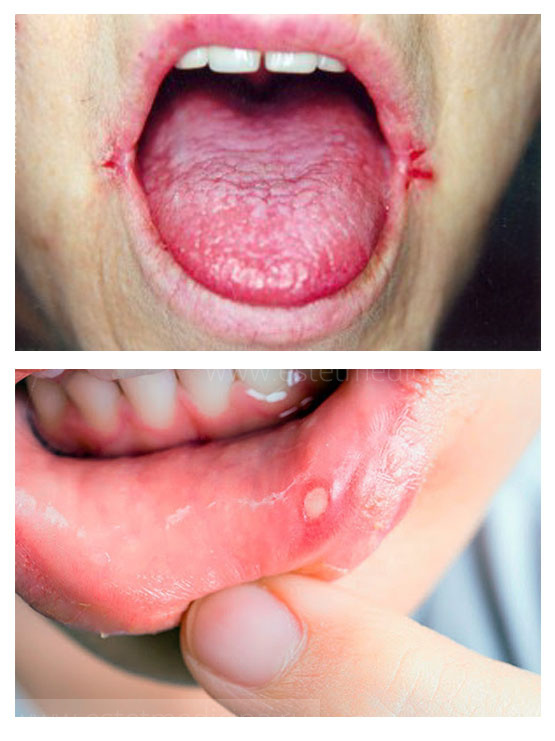
Полость рта. Заеды в уголках рта, сухие, обветренные губы, рецидивирующие и долго не проходящие стоматиты. Повреждение кончика языка, пощипывание, кислый вкус – это происходит не только из-за рефлюкса и эзофагита, но и когда слизистая в полости рта не может восстановиться.
Желудок. Язвы, эрозии, неприятный запах изо рта, который не проходит на фоне полученного медикаментозного лечения.
Кишечник. Частые поносы, жидкий или кашицеобразный стул, газообразование и вздутие.
Помимо лечения ЖКТ, в обязательном порядке стоит проверить уровень ферритина.
Влагалище и уретральный канал. Непроходящий и рецидивирующий кандидоз, цистит, который может протекать без болевого синдрома.
Лимфостаз. Лимфа на 80% состоит из белка – ферритина. Она представляет собой транспортную жидкость, которая забирает токсины из места интоксикации и доставляет их в кровь. Таким образом происходит самоочищение организма. Нарушение этого процесса имеет несколько проявлений – это отеки и частые, либо длительные простудные заболевания. Отеки наиболее выражены в первой половине дня, самостоятельно проходят к обеду или к вечеру. Отекает не только лицо, но и конечности. Простудные заболевания имеют вялотекущий характер, рецидивируют.
Плохое заживление кожи. Низкий уровень ферритина приводит к плохой выработке коллагена. Кожа теряет свои защитные свойства, так как содержащего в ней коллагена недостаточно, чтобы противостоять ультрафиолету, перемене температур (холод или жара). На коже могут образовываться пигментные пятна, в том числе по типу витилиго. Снижается тургор. Небольшие раны и порезы не заживают длительное время. На местах повреждений образуются пятна, которые не проходят в течение 2-3 лет. После пластических операций вместо незаметных швов образуются рубцы, иногда с пигментацией. При нанесении татуажа, вместо желаемого черного оттенка может получиться зеленоватый или серый, который к тому же будет плохо держаться. Асимметрия лица при введении ботокса также может возникнуть по причине низкого уровня коллагена в коже.
Как восполнить уровень ферритина?
Препараты железа не повышают уровень ферритина, по причине того, что ферритин является белком. Пациенты, которые принимали препараты железа в течение 2-3 месяцев, либо получили железо внутривенно, сталкиваются с тем, что уровень железа в крови повышен, тогда как уровень ферритина не изменился. Несмотря на то, что ферритин можно получить из пищи, восполнить недостаток подобным способом не получится. Необходимо принимать искусственные препараты. При стационарном лечении пациент получает капельницы с плазмой и плазмозамещающими растворами. В амбулаторных условиях для повышения уровня ферритина используются спирулина, хлорелла и коллаген.
Водоросли с пирулина и хлорелла
Спирулина и хлорелла – это сине-зеленые пресноводные водоросли. Они не содержат йод, поэтому могут назначаться пациентам с заболеваниями щитовидной железы. Спирулина и хлорелла идентичны по химическому составу. Отличие состоит в процентном соотношении микроэлементов и электролитов в их составе. В хлорелле белка содержится на 30% меньше, чем в спирулине. Коллаген может приводить к кристаллизации желчи и мочи. Если у пациента в анамнезе желчнокаменная болезнь или сладжирование желчи на фоне длительного приема контрацептивов и гормонов, то коллаген назначается коротким курсом, не более 1 месяца, под контролем УЗИ желчного пузыря в динамике. Поэтому из трех препаратов предпочтение отдается спирулине, как наиболее эффективному и безопасному.
Курс приема спирулины в среднем 3 месяца. Препарат принимают по 3 000 мг (единоразово) в сутки. Уровень ферритина необходимо проверять в динамике. Анализ сдается через 1 месяц приема. Если уровень ферритина повысился минимум на 20 единиц, можно говорить о положительной динамике и продолжать принимать препарат еще на протяжении 2-х месяцев. При повышении на 5-10 единиц необходимо увеличивать дозировку до 5 000 мг (единоразово) в сутки, либо комбинировать с коллагеном. Контрольный анализ также через 1 месяц приема. Курс необходимо повторять 1 раз в полгода, так как запас белка расходуется на обеспечение нормального функционирования организма, его нужно периодически восполнять.
Не рекомендуется давать спирулину детям в качестве профилактики. Прежде, чем принимать препарат стоит проверить уровень ферритина.
Белковая недостаточность. Почему не повышается уровень ферритина на фоне проводимой терапии?
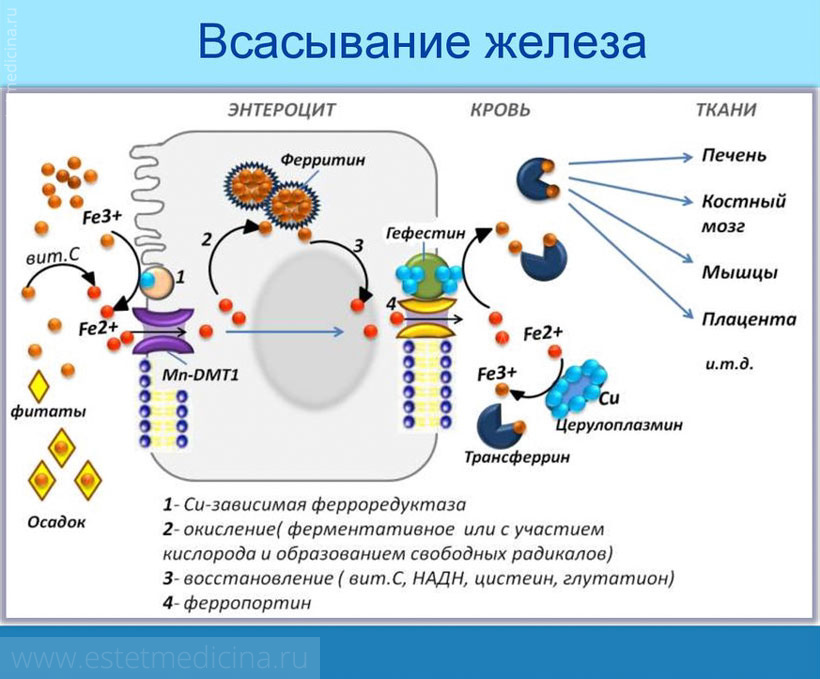
Где и как всасывается железо?
Железо, содержащееся в продуктах растительного и животного происхождения, всасывается в двенадцатиперстной и тощей кишках. Для этого железо должно пройти ряд превращений в желудке.
Попадая в желудок, под воздействием соляной кислоты пищевые белки должны расщепиться до аминокислот. Этот процесс называется денатурацией или первичным гидролизом белка. Синтезу аминокислот и накоплению белка в организме способствуют витамины В12 и В6 (фолиевая кислота), всасываемость которых зависит от кислотности в желудке. В норме pH составляет 2,8, вне желудка – 3,5.
Остались вопросы? Свяжитесь с нами:
Что происходит при низкой кислотности в желудке?
Низкая кислотность в желудке приводит к ухудшению расщепления белка. Трехвалентное железо не превращается в двухвалентное, и, попадая в кишечник в неизмененном виде, плохо всасывается. При низкой кислотности снижается выработка в желудке внутреннего фактора Кастла. Это белок, который превращает витамин В12 в усваиваемую форму и переносит его в кишечник. При низкой кислотности практически полностью разрушается витамин В9 (фолиевая кислота), а он необходим для синтеза аминокислот и всасывания витамина В12.
Что влияет на выработку соляной кислоты?
Функция гипоталамуса тесно связана с функцией щитовидной железы и гипофиза. При нарушениях белок из пищи не будет всасываться.
Комплексный подход: ферритин, гормоны, железо, фолиевая кислота, ТТГ
Для эффективного лечения, помимо уровня ферритина, необходимо проверить гормональный фон, уровень сывороточного железа, витаминов В12 и В9 (фолиевой кислоты). При низком уровне железа и витаминов В12 и В9 только препаратами белка повысить уровень ферритина не получится. Проблему необходимо решать в комплексе. Стоит отметить, что уровни меди, кальция, витамина С особенной роли в этом процессе не играют.
Ферритин и щитовидная железа
Выработка ферритина зависит от гормонального фона, и, в частности, от работы щитовидной железы. Гормоны щитовидной железы влияют на синтез эритроцитов, всасываемость железа в желудке и на усвоение витаминов В12 и В9.
Среди всех заболеваний щитовидной железы есть 2 заболевания, которые характеризуются нарушением гормонального фона:
низкий уровень концентрации гормонов щитовидный железы – гипотиреоз;
повышенная выработка гормонов щитовидной железа – гипертиреоз.
Как влияет гипотиреоз на уровень ферритина:
обновление эритроцитов замедляется. Чем реже обновляются эритроциты, тем меньше высвобождается железа, или катаболического ферритина;
снижается кислотность в желудке. В такой среде не образуется анаболический ферритин, иными словами, трехвалентное железо не превращается в двухвалентное. Оно либо плохо, либо совсем не усваивается в кишечнике;
фактор Кастла, необходимый для усваивания витаминов В12 и В9, вырабатывается в меньшем количестве;
гормоны тесно взаимосвязаны, снижение уровня одно из них непременно приводит к снижению уровня другого. Уровень тиреотропного гормона (ТТГ) зависит от уровня гормонов тироксина (Т4) и трийодтиронина (Т3). На них в свою очередь оказывает воздействие фермент тиреопероксидазы, на которую влияет уровень железа в крови.
Умственное развитие ребенка (при вынашивании) напрямую зависит от уровня фолиевой кислоты, ферритина и тиреотропного гормона (ТТГ)
Женщинам с низким уровнем ферритина необходимо дополнительно обследовать функцию щитовидной железы. Это особенно важно при планировании беременности, так как умственное развитие ребенка напрямую зависит от уровня фолиевой кислоты, ферритина и тиреотропного гормона (ТТГ).
Когда низкий уровень ферритина сохраняется продолжительное время (1 год и более), это оказывает негативное воздействие на работу щитовидной железы. В последствии из-за дисфункции щитовидная железа не будет давать ферритину повышаться. Поэтому необходимо одновременно повышать уровень ферритина и корректировать функцию щитовидной железы. Бесполезно принимать препараты белка, если уровень ТТГ не будет между 1 и 2 микро-международных единиц на миллилитр (мкМЕ/л).
Остались вопросы? Свяжитесь с нами:
Повышенный уровень ферритина и витамина В12
Как понижение, так и повышение уровня ферритина связано с нарушением гормонального фона, а именно функции щитовидной железы и гипофиза. Есть еще ряд причин, которые могут спровоцировать рост уровня ферритина.
Причины повышения уровня ферритина:
повышение гормона пролактина при гиперпролактинемии;
сниженный уровень ТТГ при гипертиреозе;
острые и хронические заболевания печени. Определять причину повышения ферритина в данном случае должен лечащий врач. К примеру, хронический холецистит и гепатиты не во всех случаях являются причиной повышения уровня ферритина;
наследственное заболевание – гиперхроматоз. При этом заболевании железо, содержащееся в продуктах питания, всасывается в избыточном количестве, распределяется в тканях, где разрушается. Это приводит к интоксикации и повышению уровня ферритина;
гемолитическая анемия – заболевание крови, при котором идет патологическое повреждение и последующий распад эритроцитов;
воспалительные процессы в организме, онкологические заболевания (рак костного мозга, молочных желез, лимфома Ходжкина);
прием комбинированных оральных контрацептивов. Прием эстрогена на протяжении более чем 6 месяцев;
злоупотребление диетами, голодание;
бесконтрольный прием поливитаминов, БАДов, препаратов железа (особенно в инъекционной форме – внутривенно или внутримышечно);
в ряде случаев прием алкоголя.
Причины повышения уровня витамина В12:
Человек рождается с нормальным уровнем витамина В12. Причина повышенного уровня витамина В12 банальна – это передозировка. Нельзя принимать витамин В12 не сдав анализ. При нормальном уровне витамина В12 дополнительный прием «для профилактики» приведет к избыточному накоплению.
Как снизить повышенный уровень ферритина и В12?
Снизить повышенный уровень ферритина и витамина В12 лекарственным путем не получится. Антидота не существует. Применяется тактика выжидания. Пациент обследуется на наличие сопутствующих заболеваний. В случае выявления назначается лечение. При этом уровень ферритина и витамина В12 наблюдается в динамике. Если через 1,5 месяца анализ показывает, что уровень снизился, то можно говорить о хорошей динамике, и стоит еще 1 раз сдать анализ через 1,5 месяца, чтобы подтвердить результат. Если же уровень, наоборот, стал еще выше, то необходимо дообследовать пациента.
Для этих методов есть противопоказания, применение любого из них нужно обсудить с лечащим врачом.
Перед прохождением курса гирудотерапии необходимо сдать кровь на свертываемость (коагулограмму). Людям с высоким давлением и сахарным диабетом также необходимо предварительно проконсультироваться с врачом.
В настоящее время существует два метода кровопускания: забор крови из вены и Хиджама. Забор венозной крови осуществляется исключительно в процедурном кабинете под контролем врача. Минимальное количество забираемой крови 150-200 мл, максимальное – 300 мл. Процедуру повторяют 2 раза с интервалом в 1 неделю. В методике Хиджама используются банки. Происходит это следующим образом: на коже делается надрез, кровь отсасывается с помощью банок.
Что касается временного исключения красного мяса из рациона, если не получается полностью отказаться от этого продукта, стоит хотя бы уменьшить потребление. Красное мясо (говядина, свинина, баранина, конина, верблюжатина и другое мясо животных) стоит употреблять 1 раз в 10 дней, или хотя бы 1 раз в неделю. Если человек совсем не может исключить красное мясо, то можно добавлять в рацион белое мясо (птица, кролик, рыба). Однократный прием в количестве 150-200 гр. 2 раза в неделю, в первой половине дня, либо не позднее 16:00.
.gif)
.gif)