Чем отличаются атомы двух изотопов одного и того же химического элемента
Разница между изотопами одного элемента
Установлено, что каждый химический элемент, находящийся в природе – это смесь изотопов (отсюда у них дробные атомные массы). Чтобы понять, чем отличаются изотопы один от другого, необходимо детально рассмотреть строение атома. Атом образует ядро и электронное облако. На массу атома влияют электроны, движущиеся с ошеломительной скоростью по орбиталям в электронном облаке, нейтроны и протоны, входящие в состав ядра.
Определение
Изотопы – это разновидность атомов какого-либо химического элемента. Электронов и протонов в любом атоме всегда равное количество. Поскольку они обладают противоположными зарядами (электроны – отрицательным, а протоны – положительным), атом всегда нейтрален (эта элементарная частица не несет заряда, он равен у нее нулю). При потере или захвате электрона атом теряет нейтральность, становясь либо отрицательным, либо положительным ионом.
Нейтроны не имеют заряда, зато их количество в атомном ядре одного и того же элемента может быть разным. Это никак не сказывается на нейтральности атома, однако влияет на его массу и свойства. Например, в любом изотопе атома водорода есть по одному электрону и протону. А количество нейтронов разное. В протии имеется всего лишь 1 нейтрон, в дейтерии – 2 нейтрона и в тритии – 3 нейтрона. Эти три изотопа заметно отличаются друг от друга по свойствам.
Сравнение
В них разное количество нейтронов, неодинаковая масса и различные свойства. Изотопы обладают идентичным строением электронных оболочек. Это значит, что они довольно близки по химическим свойствам. Поэтому им отведено в периодической системе одно место.
В природе обнаружены изотопы стабильные и радиоактивные (нестабильные). Ядра атомов радиоактивных изотопов способны самопроизвольно превращаться в другие ядра. В процессе радиоактивного распада они испускают различные частицы.
Большинство элементов имеет свыше двух десятков радиоактивных изотопов. К тому же радиоактивные изотопы искусственно синтезированы абсолютно для всех элементов. В естественной смеси изотопов их содержание незначительно колеблется.
Существование изотопов позволило понять, почему в отдельных случаях элементы с меньшей атомной массой обладают большим порядковым номером, чем элементы с большей атомной массой. Например, в паре аргон-калий аргон включает тяжелые изотопы, а калий – легкие изотопы. Поэтому масса аргона больше, чем калия.
Тестовые задания к параграфу 52
1. Изотопы одного и того же химического элемента различаются
| 1) числом электронов | 3) числом нейтронов |
| 2) числом протонов | 4) зарядом ядра |
Думаю, нужно прокомментировать.
Если разница в числе электронов – то это ионы. Если электронов меньше, чем должно быть, то атом имеет общий положительный заряд и называется катионом. Если общее число электронов больше, чем должно быть, то общий заряд атома имеет отрицательную величину, а сам такой атом называется анионом.
Заряд ядра = числу протонов в ядре = порядковому номеру элемента. То есть, атом с иным зарядом ядра будет представлять из себя уже другой элемент.
Определение: химический элемент – это вид атомов с одинаковым зарядом ядра.
Определение: изотопами называют разновидности одного и того же элемента с разным числом нейтронов в ядре атома.
Ответ: 3) Изотопы одного и того же химического элемента различаются числом нейтронов в ядре атома.
2. Ядро атома 27 13 Al содержит
| 1) 27 протонов и 13 нейтронов | 3) 14 протонов и 13 нейтронов |
| 2) 13 протонов и 14 нейтронов | 4) 13 протонов и 27 нейтронов |
Порядковый номер алюминия 13, значит заряд ядра = +13 = число протонов. Число нейтронов = массовое число (27) – порядковый номер (число протонов) = 27 – 13 = 14.
Ответ: 2) 13 протонов и 14 нейтронов
Чем отличаются изотопы одного элемента друг от друга
Что такое изотоп?
Хотя все атомы одного элемента имеют одинаковое число протонов, эти атомы могут отличаться числом имеющихся у них нейтронов. Такие различные атомы одного и того же элемента называются изотопами. Количество протонов, а также количество электронов у изотопа и исходного элемента совпадает. По этой причине в природе существует гораздо больше химических элементов, чем указано в таблице Менделеева, которая систематизирует элементы по числу протонов (порядковый номер).
Например, все атомы Li имеют 3 протона, но в природе существуют изотопы, содержащие от 3 до 5 нейтронов. Для обозначения изотопа, слева от символа элемента подписывают нижним индексом его порядковый номер, а верхним — массовое число. Массовое число — это суммарное число нуклонов (протонов и нейтронов) в атомном ядре, численно близкое к атомной массе элемента. Нижний индекс, обозначающий порядковый номер элемента, указывать не обязательно, так как все атомы лития имеют в своем ядре по 3 протона. Также, обсуждая эти изотопы, можно пользоваться записью «литий-6» и «литий-8».
Пример 1. Сколько протонов, нейтронов и электронов содержится в атоме урана-238? Запишите символ этого изотопа.
Решение: Порядковый номер урана (см. таблицу Менделеева) равен 92, а массовое число изотопа равно 238 (по условию). Следовательно, он содержит 92 протона, 92 электрона и 238 — 92 = 146 нейтронов. Его символ 238 U.
Методы разделения изотопов
Для изучения свойств изотопов и особенно для их применения в научных и прикладных целях требуется их получение в более или менее заметных количествах. В обычных масс-спектрометрах достигается практически полное разделение изотопов, однако количество их ничтожно мало. Поэтому усилия ученых и инженеров были направлены на поиски других возможных методов разделения изотопов. В первую очередь были освоены физико-химические методы разделения, основанные на различиях в таких свойствах изотопов одного итого же элемента, как скорости испарения, константы равновесия, скорости химических реакций и т.п. Наиболее эффективными среди них оказались методы ректификации и изотопного обмена, которые нашли широкое применение в промышленном производстве изотопов легких элементов: водорода, лития, бора, углерода, кислорода и азота.
Определение
Изотопы – это разновидность атомов какого-либо химического элемента. Электронов и протонов в любом атоме всегда равное количество. Поскольку они обладают противоположными зарядами (электроны – отрицательным, а протоны – положительным), атом всегда нейтрален (эта элементарная частица не несет заряда, он равен у нее нулю). При потере или захвате электрона атом теряет нейтральность, становясь либо отрицательным, либо положительным ионом.
Нейтроны не имеют заряда, зато их количество в атомном ядре одного и того же элемента может быть разным. Это никак не сказывается на нейтральности атома, однако влияет на его массу и свойства. Например, в любом изотопе атома водорода есть по одному электрону и протону. А количество нейтронов разное. В протии имеется всего лишь 1 нейтрон, в дейтерии – 2 нейтрона и в тритии – 3 нейтрона. Эти три изотопа заметно отличаются друг от друга по свойствам.
Особенности изотопов
Различные изотопы элементов отличаются количеством нейтронов в ядре.
Сейчас известно, что некоторые элементы (водород, бор, кадмий и т.д.) имеют свойство захватывать нейтроны и образовывать изотопы. Например, легкий водород (11Н), захватывая один нейтрон, образует тяжелый водород – дейтерий (21D), а когда захватывает еще один нейтрон – тритий (31Т).
Изотопы водорода и гелия имеют важное значение в физических исследованиях ядра. В оболочке атома водорода только один электрон, атома гелия – два электрона. Поэтому их можно сравнительно легко «сорвать», получив ядра этих элементов. Тяжелые изотопы водорода играют существенную роль в осуществлении ядерных реакций синтеза и деления. Следует отметить, что хотя молекулярные свойства вещества определяются вообще не ядром, а строением электронной оболочки, все же физические свойства тяжелых изотопов и обычного водорода заметно различаются. Например:
Важные свойства имеет тяжелая вода, то есть вода, в молекулах которой вместо атомов легкого водорода содержится дейтерий.
Однако заметные изменения свойств изотопов наблюдаются только у легких элементов. Объясняется это тем, что у тяжелых элементов отношение массы ядра к массе нейтрона гораздо больше.
Чем отличаются изотопы одного элемента друг от друга
Установлено, что каждый химический элемент, находящийся в природе – это смесь изотопов (отсюда у них дробные атомные массы). Чтобы понять, чем отличаются изотопы один от другого, необходимо детально рассмотреть строение атома. Атом образует ядро и электронное облако. На массу атома влияют электроны, движущиеся с ошеломительной скоростью по орбиталям в электронном облаке, нейтроны и протоны, входящие в состав ядра.
Что такое изотопы
Изотопы – это разновидность атомов какого-либо химического элемента. Электронов и протонов в любом атоме всегда равное количество. Поскольку они обладают противоположными зарядами (электроны – отрицательным, а протоны – положительным), атом всегда нейтрален (эта элементарная частица не несет заряда, он равен у нее нулю). При потере или захвате электрона атом теряет нейтральность, становясь либо отрицательным, либо положительным ионом.
Нейтроны не имеют заряда, зато их количество в атомном ядре одного и того же элемента может быть разным. Это никак не сказывается на нейтральности атома, однако влияет на его массу и свойства. Например, в любом изотопе атома водорода есть по одному электрону и протону. А количество нейтронов разное. В протии имеется всего лишь 1 нейтрон, в дейтерии – 2 нейтрона и в тритии – 3 нейтрона. Эти три изотопа заметно отличаются друг от друга по свойствам.
Сравнение изотопов
Чем различаются изотопы? В них разное количество нейтронов, неодинаковая масса и различные свойства. Изотопы обладают идентичным строением электронных оболочек. Это значит, что они довольно близки по химическим свойствам. Поэтому им отведено в периодической системе одно место.
В природе обнаружены изотопы стабильные и радиоактивные (нестабильные). Ядра атомов радиоактивных изотопов способны самопроизвольно превращаться в другие ядра. В процессе радиоактивного распада они испускают различные частицы.
Большинство элементов имеет свыше двух десятков радиоактивных изотопов. К тому же радиоактивные изотопы искусственно синтезированы абсолютно для всех элементов. В естественной смеси изотопов их содержание незначительно колеблется.
Существование изотопов позволило понять, почему в отдельных случаях элементы с меньшей атомной массой обладают большим порядковым номером, чем элементы с большей атомной массой. Например, в паре аргон-калий аргон включает тяжелые изотопы, а калий – легкие изотопы. Поэтому масса аргона больше, чем калия.
TheDifference.ru определил, что отличие изотопов друг от друга заключается в следующем:
Они обладают разным числом нейтронов.
Изотопы имеют разную массу атомов.
Значение массы атомов ионов влияет на их полную энергию и свойства.
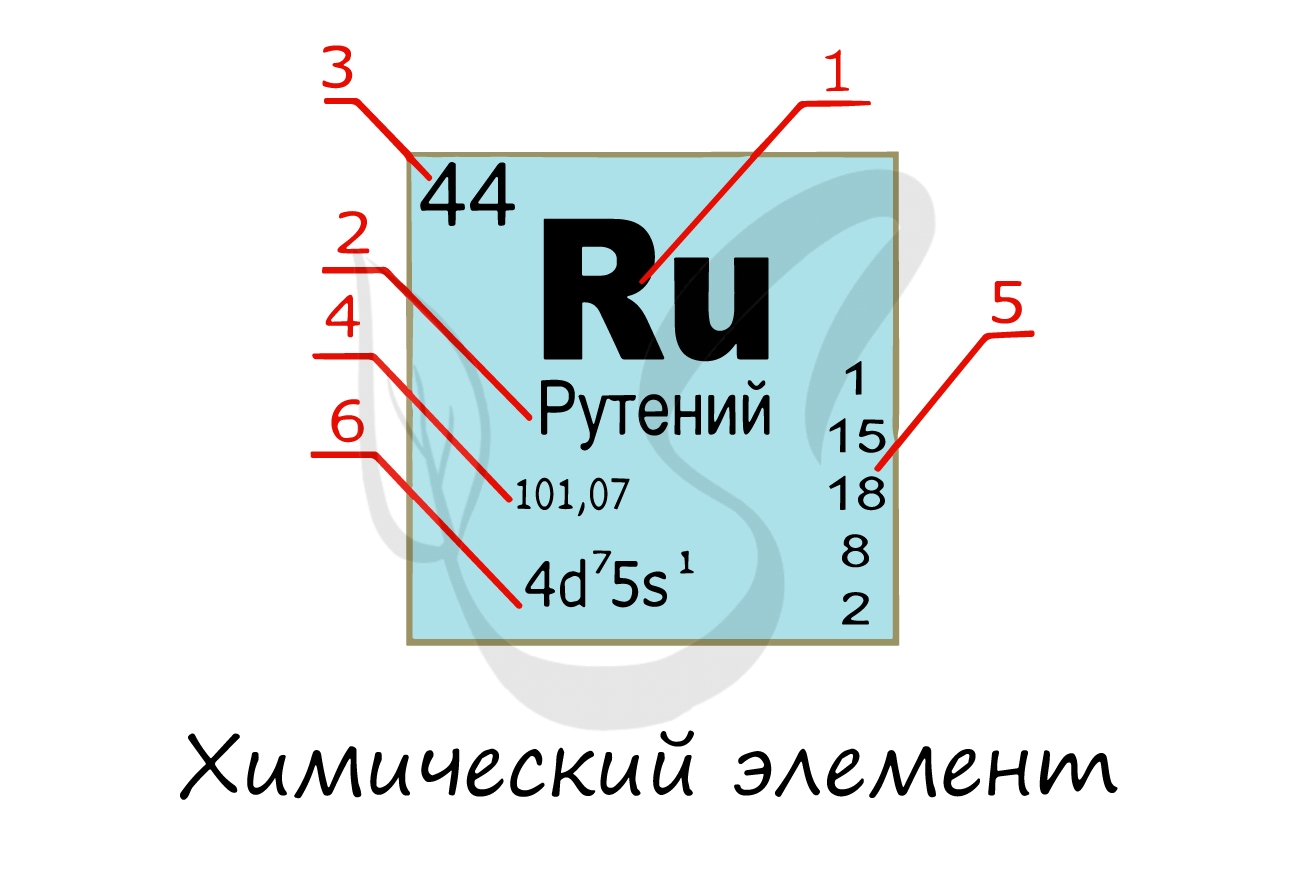
Химические элементы
Химический элемент
Надо заметить, что на экзамене часто из карточки элемента скрывают распределение электронов и конфигурацию внешнего уровня. Тем не менее, если вы успешно освоили предыдущую тему, то для вас не составит труда написать электронную конфигурацию атома зная его порядковый номер в таблице Д.И. Менделеева (номер уж точно не тронут!))
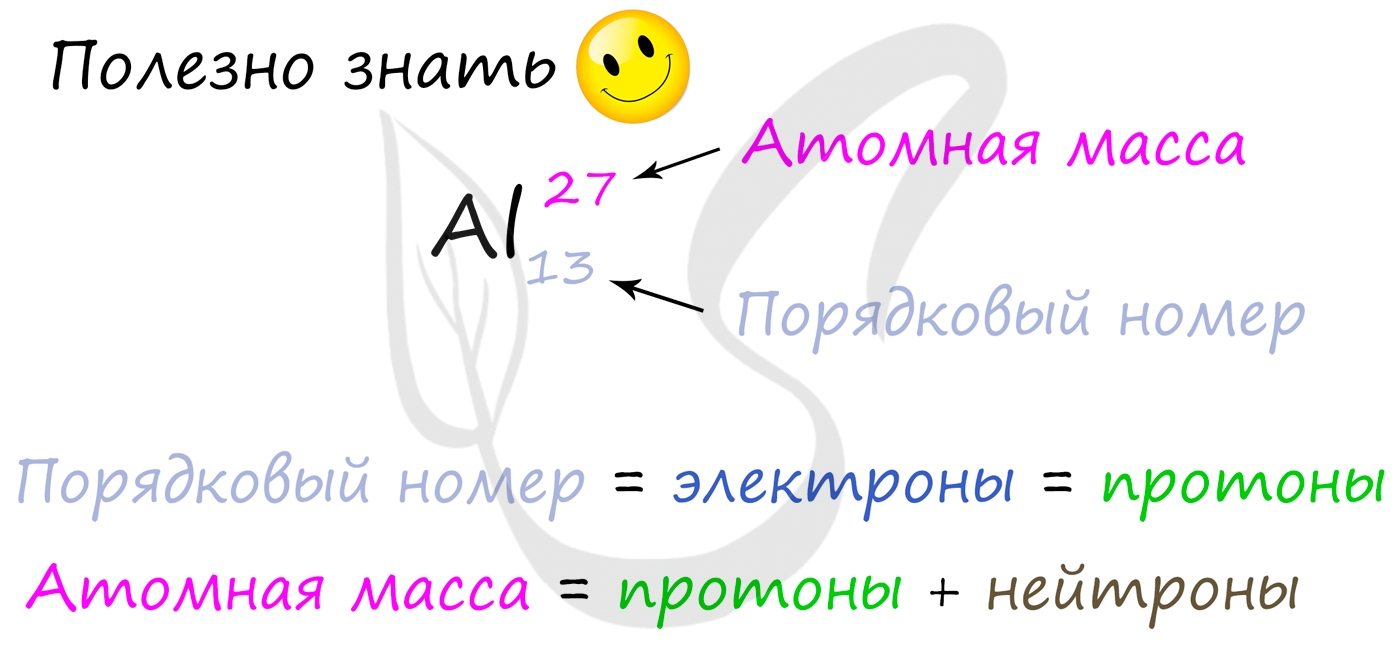
Протоны, нейтроны и электроны
Вы уже знаете, что порядковый номер элемента в периодической таблице Д.И. Менделеева равен числу протонов, а число протонов равно числу электронов.
Для того чтобы найти число нейтронов в атоме алюминия, необходимо вычесть из атомной массы число протонов:
Получается, что в атоме алюминия 14 нейтронов. Посчитайте число нейтронов, электронов и протонов самостоятельно для атомов бериллия, кислорода, меди. Решение вы найдете ниже.
Если вы поняли суть и научились считать протоны, нейтроны и электроны, самое время приступать к следующей теме.
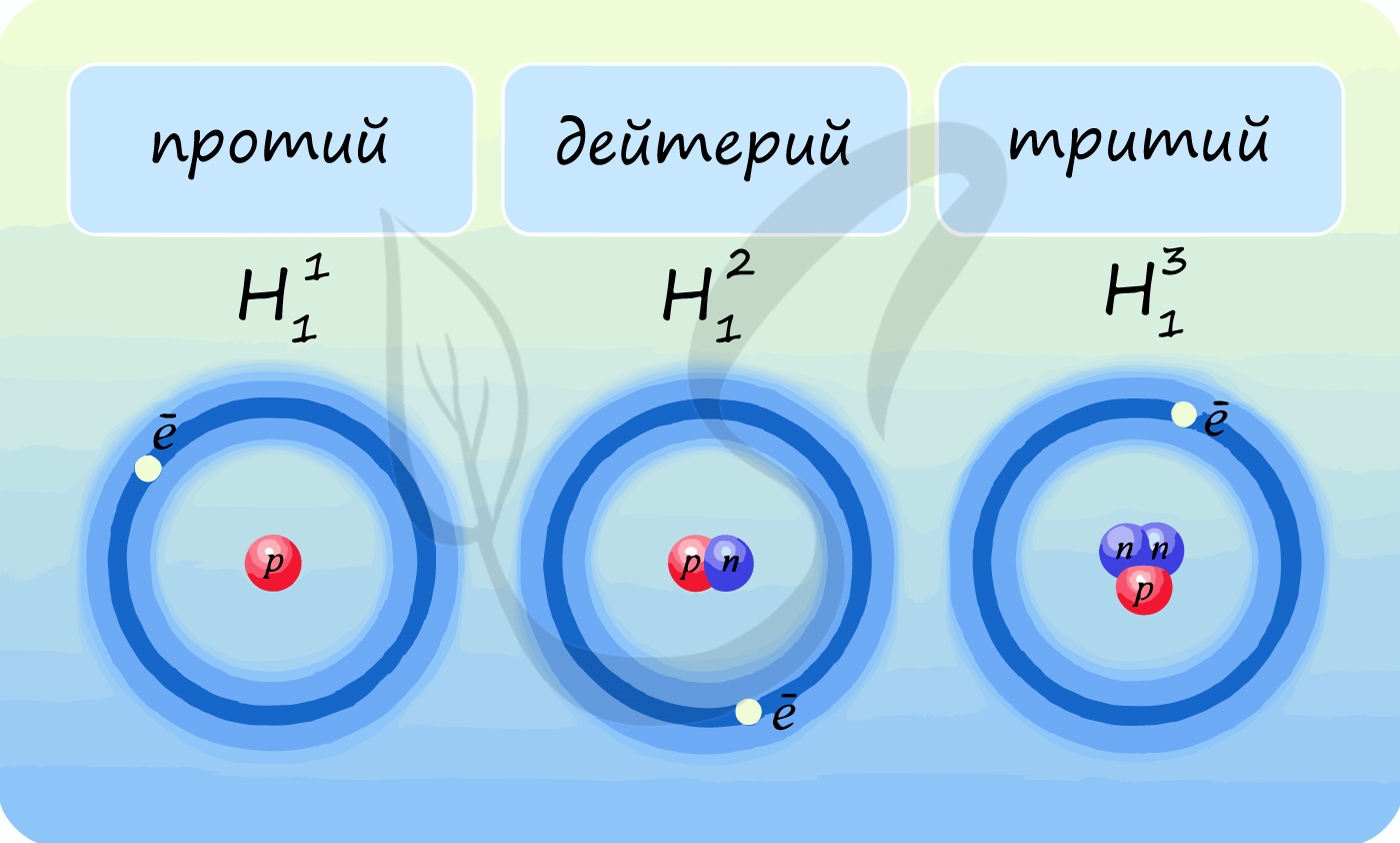
Изотопы
Лучше всего объяснить, что такое изотопы наглядным примером. Широко известны три изотопа водорода: протий, дейтерий и тритий.
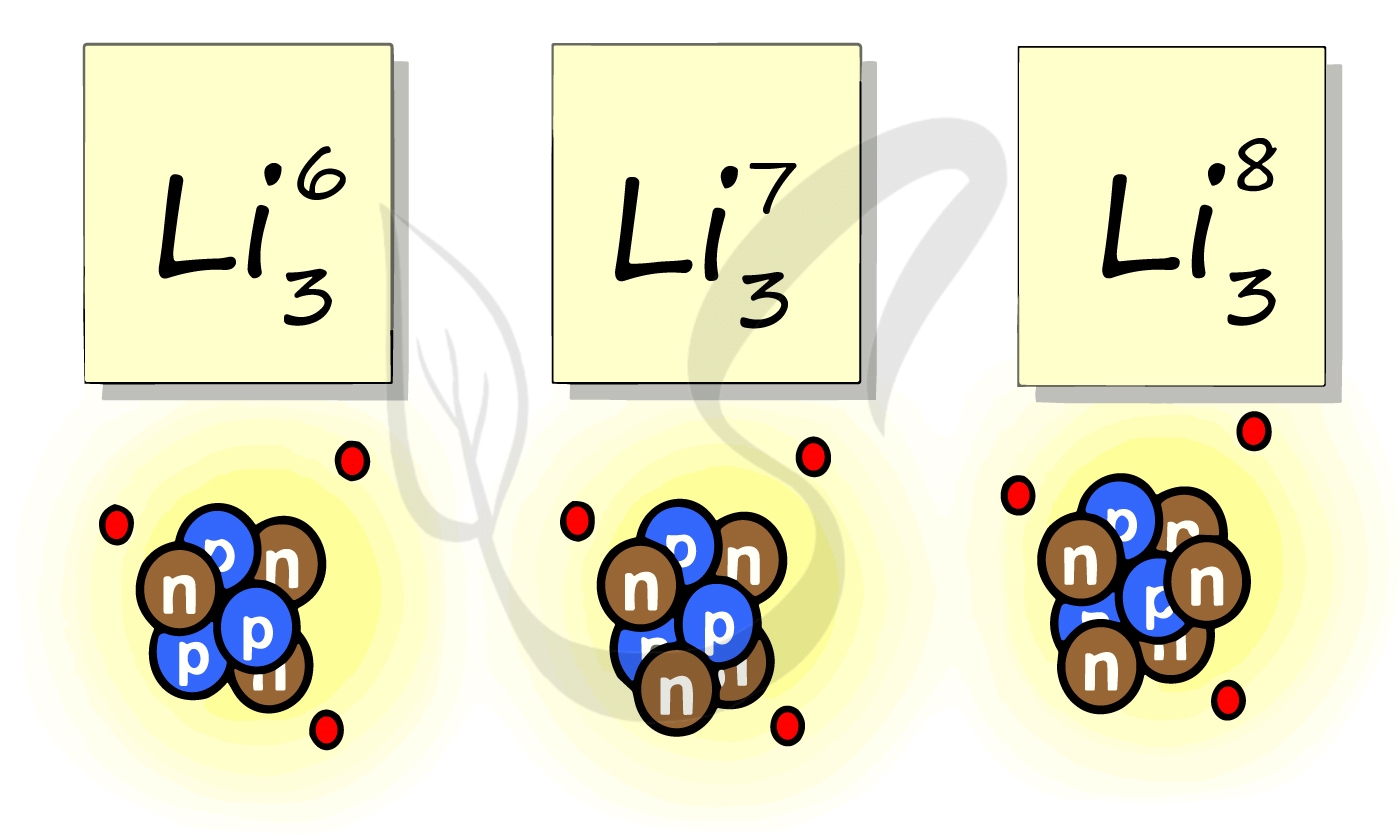
Рассмотрим пример с изотопами лития. Самостоятельно посчитайте количество нейтронов у каждого изотопа. Найдите тот, который включен в таблицу Д.И. Менделеева.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.