Чем отличается массовая с объемная с и мольная с теплоемкости
Теплоёмкость



Известно, что подвод теплоты к рабочему телу в каком-либо процессе сопровождается изменением температуры. Отношение теплоты, подведённой (отведённой) в данном процессе, к изменению температуры называется теплоёмкостью тела.
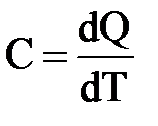
где dQ – элементарное количество теплоты
dT – элементарное изменение температуры.
Теплоёмкость численно равна количеству теплоты, которое необходимо подвести к системе, чтобы при заданных условиях повысить температуру на 1 градус. Измеряется в [Дж/К].
Количество теплоты, подведённое к рабочему телу, всегда пропорционально количеству рабочего тела. Например, количество теплоты, необходимое для нагревания на 1 градус кирпича и кирпичной стены неодинаково, поэтому для сравнения вводят удельные величины теплоёмкости, отнеся подведённую теплоту к единице рабочего тела. В зависимости от количественной единицы тела, к которому подводится теплота в термодинамике, различают массовую, объёмную и мольную теплоёмкости.
Массовая теплоёмкость – это теплоёмкость, отнесённая к единице массы рабочего тела,
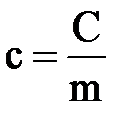
Количество теплоты, необходимое для нагревания 1 кг газа на 1 К называется массовой теплоёмкостью.
Единицей измерения массовой теплоёмкости является Дж/(кг К). Массовую теплоёмкость называют также удельной теплоёмкостью.
Объёмная теплоёмкость – теплоёмкость, отнесённая к единице объёма рабочего тела,
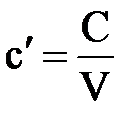
Количество теплоты, необходимое для нагревания 1 м 3 газа на 1 К называется объёмной теплоёмкостью.
Объёмная теплоёмкость измеряется в Дж/(м 3 К).
Мольная теплоёмкость – теплоёмкость, отнесённая к количеству рабочего тела,
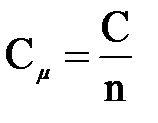
где n – количество газа в моль.
Количество теплоты, необходимое для нагревания 1 моль газа на 1 К называется мольной теплоёмкостью.
Мольную теплоёмкость измеряют в Дж/(моль×К).
Массовая и мольная теплоёмкости связаны следующим соотношением:
Теплоёмкость зависит от условий протекания процесса. Поэтому обычно в выражении для теплоёмкости указывается индекс х, который характеризует вид процесса теплообмена.
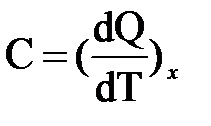
Индекс х означает, что процесс подвода (или отвода) теплоты идёт при постоянном значении какого-либо параметра, например, давления, объёма.
Среди таких процессов наибольший интерес представляют два: один при постоянном объёме газа, другой при постоянном давлении. В соответствии с этим различают теплоёмкости при постоянном объёме Cv и теплоёмкость при постоянном давлении Cp.
1) Теплоёмкость при постоянном объёме равна отношению количества теплоты dQ к изменению температуры dT тела в изохорном процессе (V = const):
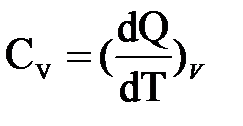
2) Теплоёмкость при постоянном давлении равна отношению количества теплоты dQ к изменению температуры dT тела в изобарном процессе (Р = const):
Для понимания сути этих процессов рассмотрим пример.
Пусть имеется два цилиндра, в которых находится по 1 кг одного и того же газа при одинаковой температуре. Один цилиндр полностью закрыт (V = const), другой цилиндр сверху закрыт поршнем, который оказывает на газ постоянное давление Р (P = const).
Подведём к каждому цилиндру такое количество тепла Q, чтобы температура газа в них повысилась от Т1 до Т2 на 1К. В первом цилиндре газ не совершил работу расширения, т.е. количество подведённого тепла будет равно
здесь индекс v – означает, что теплота подводится к газу в процессе с постоянным объёмом.
Во втором цилиндре, кроме повышения температуры на 1К, произошло ещё передвижение нагруженного поршня (газ изменил объём), т.е. была совершена работа расширения. Количество подведённого тепла в этом случае определится из выражения:
Здесь индекс р – означает, что тепло подводится к газу в процессе с постоянным давлением.
Общее количество тепла Qp будет больше Qv на величину, соответствующую работе преодоления внешних сил:
где R – работа расширения 1 кг газа при повышении температуры на 1К при Т2 – Т1 = 1К.
Если поместить в цилиндр не 1 кг газа, а 1 моль, то выражение примет вид
Это выражение носит название уравнения Майера.
Наряду с разностью Ср – Сv в термодинамических исследованиях и практических расчетах широкое применение имеет отношение теплоемкостей Ср и Сv, которое называется показателем адиабаты.
В молекулярно – кинетической теории для определения k приводится следующая формула k = 1 + 2/n,
где n – число степеней свободы движения молекул (для одноатомных газов n = 3, для двухатомных n = 5, для трёх и более атомных n = 6).
Чем отличается массовая с объемная с и мольная с теплоемкости
Теплоемкостью называется количество тепла, необходимое для изменения температуры единицы массы вещества на 1° За единицу массы вещества в технических расчетах принимают моль (килограмм-молекулу), килограмм и нормальный кубометр (для газов). В соответствии с этим применяют теплоемкость мольную, массовую и объемную. Массовая теплоемкость с равна мольной |хс, деленной на молекулярный вес данного вещества М. Объемная теплоемкость С газа равна мольной теплоемкости, деленной на объем 1 моля идеального газа в нормальных кубометрах [38], т. е. на 22,41. Следовательно, мольная, массовая и объемная теплоемкости газов связаны уравнением
Отсюда объемная теплоемкость газообразных продуктов сгорания топлива
Теплоемкость газа зависит от того, в каких условиях осуществляется его нагревание (или охлаждение) — при постоянном давлении или при постоянном объеме. При нагревании газа при постоянном давлении затрачивается энергия на расширение газа. Вследствие этого теплоемкость при постоянном давлении больше теплоемкости при постоянном объеме.
При подсчетах эффективности использования топлива в печах и котлах обычно применяют значения теплоемкости при постоянном давлении. Средняя теплоемкость — количество тепла, необходимое для изменения температуры единицы массы (или объема) вещества на 1° в заданном температурном интервале, т. е. от ty до t2.
Теплоемкость возрастает с повышением температуры, поотому при пагре — ве воздуха или топлива от температуры tx до температуры t2 истинная теплоемкость при температуре t% больше истинной теплоемкости при температура
А средняя теплоемкость от tx до t2 больше истинной теплоемкости при температуре но меньше истинной теплоемкости при температуре При охлаждении продуктов сгорания от температуры до температуры L средняя теплоемкость в интервале температур ОТ fj до t2 меньше истинной теплоемкости при начальной температуре tx и больше истинной теплоемкости при конечной температуре tz. При определении эффективности использования топлива и подсчетах располагаемого тепла продуктов сгорания обычно рименяют средние теплоемкости.
Массовая, объемная и мольная теплоемкости
Массовая, объемная и мольная теплоемкости
Очевидно, наивысшая температура точки будет в том случае, когда будут предотвращены потери тепла с обратных сторон зеркала и когда на поверхности, подверженной солнечному излучению, отсутствует теплопроводность или конвекция. Людмила Фирмаль
Так как в пространстве объемом 1 м3 в зависимости от температуры и давления помещается разное количество газа, то при установке объемной теплоемкости необходимо указать, при каких условиях будет приниматься количество газа, заполняющего 1 м3.Обычно в таблице теплоемкости указано количество газа, удовлетворяющее обычным условиям, то есть при температуре 273 К и давлении 1,01325 бар на 1 л 3.In в этом случае в размеры объемной теплоемкости вводится дополнительное обозначение, буква n C j m — град.
Интересно также вычислить, до какой температуры можно нагреть точку, расположенную в положении изображения Солнца, с помощью солнечного коллектора при оптимальных условиях. Людмила Фирмаль
Масса газа в 1 кмоль равна р кг Р-относительная молекулярная масса газа, а при нормальных условиях она принимает ID 22,4 м3 по закону Абу-хадро… pc 22,4 C Дж кмоль-град 4,7 ы Дж кг град 4.8 С 22 4 Дж Ост — 4 9 Вместо указания Cf. Name ПК используется больше often. It можно рассматривать как единичный символ молярной теплоемкости, так и как произведение молекулярной массы р и массовой теплоемкости С.
Если умножить уравнение манера 4.4 на молекулярную массу p, то получится ПЦР — и 8314 Дж кмоль-Град, 4. 10 где молярная теплоемкость газа при постоянном давлении равна J кмоль-град rg,, — молярная теплоемкость газа при постоянном объеме при j кмоль-град R-A1-Универсальная Газовая Постоянная j кмоль-в град.
Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Чем отличается массовая с объемная с и мольная с теплоемкости
Для просмотра сайта используйте Internet Explorer
Тема 2. ТЕПЛОЁМКОСТЬ ГАЗОВ
2.1.Массовая, объёмная и мольная удельные теплоёмкости
Известно, что подвод теплоты к рабочему телу или отвод теплоты от него в каком-либо процессе приводит к изменению его температуры. Отношение количества теплоты, подведенной (или отведенной) в данном процессе, к изменению температуры называется теплоемкостью тела (системы тел):



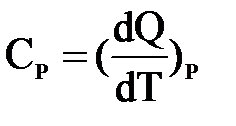






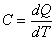 ,
,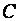 указывается индекс «x», который характеризует вид процесса теплообмена
указывается индекс «x», который характеризует вид процесса теплообмена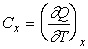 .
.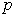 , объема
, объема 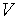 или других.
или других.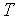 .
.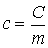 .
.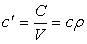 ,
,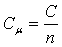 ,
,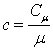
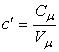
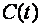 , а удельную – как
, а удельную – как 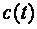 . Обычно под истинной теплоёмкостью понимают отношение элементарного количества теплоты, которое сообщается термодинамической системе в каком-либо процессе к бесконечно малому приращению температуры этой системы, вызванному сообщенной теплотой. Будем считать
. Обычно под истинной теплоёмкостью понимают отношение элементарного количества теплоты, которое сообщается термодинамической системе в каком-либо процессе к бесконечно малому приращению температуры этой системы, вызванному сообщенной теплотой. Будем считать 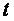 , а
, а 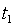 до
до 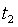 можно определить как
можно определить как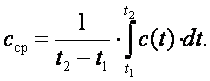
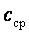 для различных интервалов температур, начинающихся с
для различных интервалов температур, начинающихся с 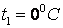 . Поэтому во всех случаях, когда термодинамический процесс проходит в интервале температур от
. Поэтому во всех случаях, когда термодинамический процесс проходит в интервале температур от 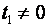 , количество удельной теплоты
, количество удельной теплоты 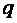 процесса определяется с использованием табличных значений средних теплоемкостей
процесса определяется с использованием табличных значений средних теплоемкостей 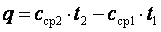 .
.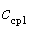 и
и 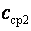 , находят по таблицам.
, находят по таблицам.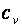 (изохорная теплоемкость, равная отношению удельного количества теплоты в изохорном процессе к изменению температуры рабочего тела dT) и при постоянном давлении
(изохорная теплоемкость, равная отношению удельного количества теплоты в изохорном процессе к изменению температуры рабочего тела dT) и при постоянном давлении 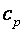 (изобарная теплоемкость, равная отношению удельного количества теплоты в изобарном процессе к изменению температуры рабочего тела dT).
(изобарная теплоемкость, равная отношению удельного количества теплоты в изобарном процессе к изменению температуры рабочего тела dT).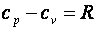 .
.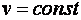 ) внешняя работа не выполняется и теплота расходуется только на изменение внутренней энергии рабочего тела, тогда как в изобарном процессе (
) внешняя работа не выполняется и теплота расходуется только на изменение внутренней энергии рабочего тела, тогда как в изобарном процессе (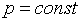 ) теплота расходуется не только на изменение внутренней энергии рабочего тела, зависящей от его температуры, но и на совершение им внешней работы.
) теплота расходуется не только на изменение внутренней энергии рабочего тела, зависящей от его температуры, но и на совершение им внешней работы.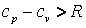 , так как при их расширении и
, так как при их расширении и 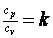 , которое носит название коэффициента Пуассона (показателя адиабаты). В табл. 2.1 приведены значения
, которое носит название коэффициента Пуассона (показателя адиабаты). В табл. 2.1 приведены значения 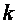 некоторых газов, полученные экспериментально при температуре 15 °С.
некоторых газов, полученные экспериментально при температуре 15 °С. — элементарное количество теплоты;
— элементарное количество теплоты;  — элементарное изменение температуры.
— элементарное изменение температуры.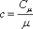

 м 3 /моль — мольный объем газа при нормальных условиях.
м 3 /моль — мольный объем газа при нормальных условиях.

 и
и  , находят по таблицам.
, находят по таблицам.