Чем определяется то или иное агрегатное состояние в другое
Агрегатные состояния вещества
Конспект по физике для 8 класса «Агрегатные состояния вещества». ВЫ УЗНАЕТЕ: Чем отличается характер движения и взаимодействия молекул вещества в различных агрегатных состояниях. Как происходит переход вещества из одного агрегатного состояния в другое.
Агрегатные состояния вещества
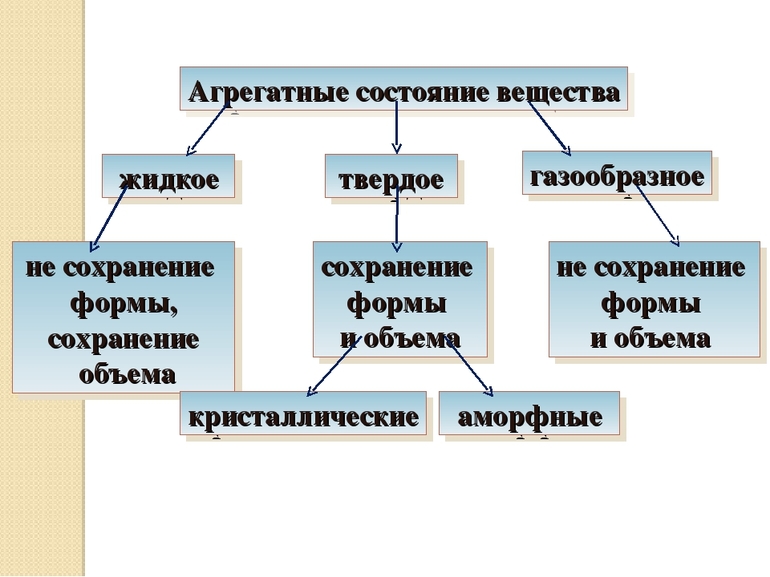
Все вещества в зависимости от условий могут находиться в трёх агрегатных состояниях: твёрдом, жидком и газообразном. Различные агрегатные состояния существуют у каждого вещества. Наглядным примером этому служат лёд, вода и водяной пар.
ЧЕМ ОПРЕДЕЛЯЕТСЯ АГРЕГАТНОЕ СОСТОЯНИЕ ВЕЩЕСТВА
Вы уже знаете, что молекулы одного и того же вещества в твёрдом, жидком и газообразном состоянии ничем не отличаются друг от друга. То или иное агрегатное состояние определяется взаимным расположением составляющих вещество молекул, а также характером их движения и взаимодействия.
В газах при атмосферном давлении расстояния между молекулами намного больше размера самих молекул. Именно поэтому притяжение между молекулами газа мало. При обычных температурах средняя кинетическая энергия молекул газа вполне достаточна для совершения работы по преодолению сил их взаимного притяжения, поэтому молекулы газа разлетаются, если газ не сдерживают стенки сосуда.
Плотности жидкостей и твёрдых тел во много раз больше плотности газа, а их молекулы расположены гораздо ближе друг к другу. В этом случае сила взаимного притяжения молекул намного больше и средней кинетической энергии молекул уже недостаточно для того, чтобы совершить работу по преодолению сил межмолекулярного притяжения. Это является причиной того, что молекулы в жидкостях и особенно в твёрдых телах не могут значительно удаляться друг от друга.
ПЕРЕХОД ВЕЩЕСТВА ИЗ ОДНОГО АГРЕГАТНОГО СОСТОЯНИЯ
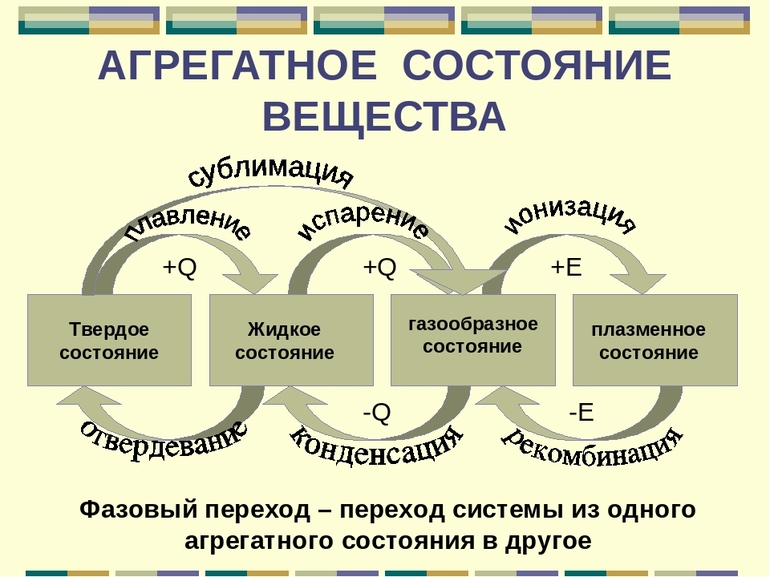
Вещества могут переходить из одного агрегатного состояния в другое. Изменение агрегатного состояния вещества всегда связано с выделением или поглощением некоторого количества теплоты.
Переход вещества из одного агрегатного состояния в другое используется для решения огромного числа практических задач. Например, в крупных городах используют снегоплавильные машины, для того чтобы грязный снег с улицы отправлять в канализацию и не загрязнять окружающую среду. На тепловых и атомных электростанциях в паровых турбинах применяют водяной пар. Сжиженный газ (фреон) используют в холодильных установках.
Всего различают шесть процессов, при которых происходит переход вещества из одного агрегатного состояния в другое.
ПЛАВЛЕНИЕ И КРИСТАЛЛИЗАЦИЯ
Переход вещества из твёрдого состояния в жидкое называется плавлением. В твёрдых телах, в отличие от жидкостей, частицы расположены упорядоченно. Поэтому, для того чтобы перевести частицы из упорядоченного состояния в неупорядоченное, нужно совершить работу по преодолению сил молекулярного притяжения. Внутренняя энергия вещества при этом увеличивается за счёт увеличения энергии взаимодействия молекул. Примерами плавления могут служить таяние льда, плавление металлов в металлургии и пр.
Обратный процесс, связанный с переходом вещества из жидкого состояния в твёрдое, называется кристаллизацией или отвердеванием. Пример кристаллизации — замерзание воды. Процесс кристаллизации сопровождается уменьшением внутренней энергии вещества за счёт уменьшения энергии взаимодействия молекул.
ПАРООБРАЗОВАНИЕ И КОНДЕНСАЦИЯ
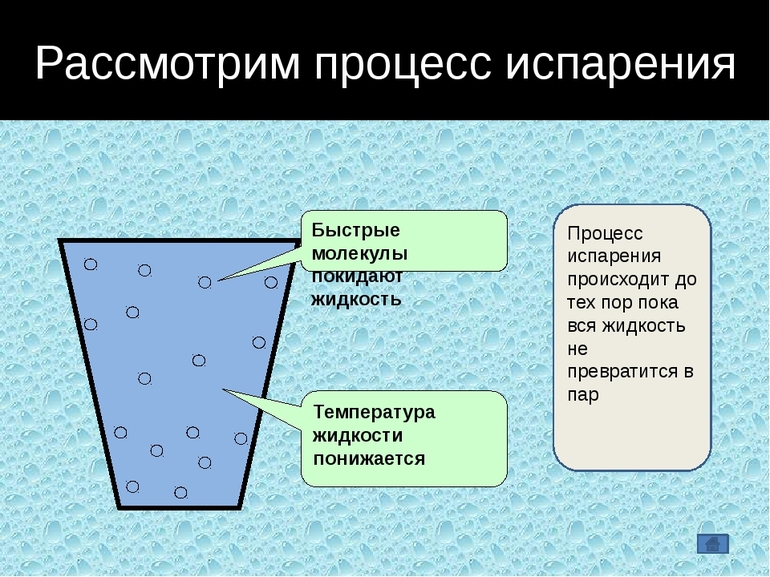
Переход вещества из жидкого состояния в газообразное называется парообразованием. Пример парообразования — испарение воды.
Обратный процесс, связанный с переходом вещества из газообразного состояния в жидкое, называется конденсацией (от лат. condense — уплотнение, сгущение). Пример конденсации — образование росы.
СУБЛИМАЦИЯ (ВОЗГОНКА) И ДЕСУБЛИМАЦИЯ
Переход вещества из твёрдого состояния в газообразное (минуя жидкое) называется сублимацией (от лат. sublimo — возношу) или возгонкой. Возгонкой объясняются также запахи, которыми обладают многие твёрдые тела. Вылетая из твёрдого тела, молекулы образуют над ним газ (или пар), который и вызывает запах. Например, разные сорта древесины имеют различный запах.
Переход вещества из газообразного состояния в твёрдое (минуя жидкое) называется десублимацией. Пример десублимации — образование на окнах зимой инея, узоров из кристалликов льда. Данный процесс десублимации может осуществляться только на внутренней поверхности оконного стекла, где молекулы паров воды превращаются в кристаллики льда.
Вы смотрели Конспект по физике для 8 класса «Агрегатные состояния вещества».
1. В каких агрегатных состояниях может находиться одно и то же вещество?
Вещество может находиться в твердом, жидком и газообразном состоянии.
2. Какое практическое значение имеют явления перехода вещества из одного агрегатного состояния в другое?
В металлургии: плавят металлы, чтобы получить из них сплавы: чугун, сталь, бронзу, латунь и др. Пар, полученный из воды при ее нагревании, используют на электростанциях в паровых турбинах.
Сжиженными газами пользуются в холодильных установках.
3. Чем определяется то или иное агрегатное состояние вещества?
Агрегатное состояние вещества определяется расположением, характером движения и взаимодействия молекул.
4. Каковы особенности молекулярного строения газов, жидкостей и твёрдых тел?
В газах при атмосферном давлении расстояние между молекулами много больше размера самых молекул. В связи с этим притяжение молекул газа мало. Средняя кинетическая энергия молекул газа вполне достоточна, чтобы совершить работу по преодолению сил молекулярного притяжения. Поэтому, если газу не мешают стенки сосуда, его молекулы разлетаются.
В жидкостях и твердых телах, плотность которых во много раз больше плотности газа, молекулы расположены ближе друг к другу. Средняя кинетическая энергия их уже недостаточна для того, чтобы совершить работу по преодолению сил молекулярного притяжения.
Поэтому молекулы в жидкостях и особенно в твердых телах не могут далеко удаляться друг от друга.
Агрегатные состояния вещества
Вещество может пребывать в твердом, жидком или газообразном состояниях, а при особых условиях также в плазменном состоянии.
Любое вещество состоит из молекул, а его физические свойства зависят от того, каким образом упорядочены молекулы и как они взаимодействуют между собой. В обычной жизни мы наблюдаем три агрегатных состояния вещества — твердое, жидкое и газообразное.
Газ расширяется, пока не заполнит весь отведенный ему объем. Если рассмотреть газ на молекулярном уровне, мы увидим беспорядочно мечущиеся и сталкивающиеся между собой и со стенками сосуда молекулы, которые, однако, практически не вступают во взаимодействие друг с другом. Если увеличить или уменьшить объем сосуда, молекулы равномерно перераспределятся в новом объеме. Молекулярно-кинетическая теория связывает молекулярные свойства газа с его макроскопическими свойствами, такими как температура и давление.
В отличие от газа жидкость при заданной температуре занимает фиксированный объем, однако и она принимает форму заполняемого сосуда — но только ниже уровня ее поверхности. На молекулярном уровне жидкость проще всего представить в виде молекул-шариков, которые хотя и находятся в тесном контакте друг с другом, однако имеют свободу перекатываться друг относительно друга, подобно круглым бусинам в банке. Налейте жидкость в сосуд — и молекулы быстро растекутся и заполнят нижнюю часть объема сосуда, в результате жидкость примет его форму, но не распространится в полном объеме сосуда.
Твердое тело имеет собственную форму, не растекается по объему контейнера и не принимает его форму. На микроскопическом уровне атомы прикрепляются друг к другу химическими связями, и их положение друг относительно друга фиксировано. При этом они могут образовывать как жесткие упорядоченные структуры — кристаллические решетки, — так и беспорядочное нагромождение — аморфные тела (именно такова структура полимеров, которые похожи на перепутанные и слипшиеся макароны в миске).
Выше были описаны три классических агрегатных состояния вещества. Имеется, однако, и четвертое состояние, которые физики склонны относить к числу агрегатных. Это плазменное состояние. Плазма характеризуется частичным или полным срывом электронов с их атомных орбит, при этом сами свободные электроны остаются внутри вещества. Таким образом, плазма, будучи ионизированной, в целом остается электрически нейтральной, поскольку число положительных и отрицательных зарядов в ней остается равным. Мы можем наблюдать как холодную и в незначительной степени ионизированную плазму (например, в люминесцентных лампах), так и полностью ионизированную горячую плазму (внутри Солнца, например).
При сверхнизких температурах скорости молекул снижаются настолько, что мы не можем точно определить их местоположение. Это происходит в силу принципа неопределенности Гейзенберга. Когда температура снижается настолько, что степень неопределенности положения атомов оказывается сопоставимой с размерами группы атомов, к которой они принадлежат, вся группа начинает вести себя, как единое целое. Такое состояние вещества называется конденсатом Бозе—Эйнштейна, и его можно считать пятым агрегатным состоянием вещества.
Статья в стиле рассказа детям на уроке природоведения.
Характеризовать агрегатное состояние по тому как вещество, находящееся в нем, заполняет предоставленный ему объем можно в рассказе второклассникам.
В жидкости друг относительно друга движутся не молекулы, а их небольшие группы.
Не показана разница между аморфными и твердыми телами.
Не выполнена главная задача любой энциклопедии: точного краткого описания с множеством ссылок на другие статьи, разъясняющих смысл всех специальных слов и понятий, встречающихся в описании, в конце концов приводящих к элементарным законам.
Состояния же материи, различимые только измерительными
ПРИБОРАМИ (тоже условный термин), возможно,
неисчислимы (и для «вещества»).
Начните измерения и окажется, что всё давно измерено и всё давно просчитано!
Прошлое движение, говорите? Возьмите настояшее движение и через мгновение оно станет прошлым! И что изменилось? где новая масса? Блин, все просчитывается известными кинематическими формулами, а вы при этом тут со своей теорией лишний. [/quote]
Если Вы не принимаете моё объяснение, то сами объясните, как рождается первичное движение? Как первичное неуловимое движение закольцовывается и в таком состоянии повторяется много раз, как и обращение Земли с повторениями лета и зимы, что мы воспринимаем массой-симбиозом движения и части пространства? Прошлое движение проявляется, материализуется через труд-инерцию, перелетающую на препятствие и изменяющее его форму и направленность движения. Настоящее движение (например, автомобиля, который своим движением перевозит груз с одного места на другое) работой переносится на объект, когда инерцией движение от одного носителя (хозяина) переходит к другому носителю (хозяину). Движения работают в момент настоящего времени, но настоящее время сменяется очередным настоящим временем, а предыдущее настоящее становится прошлым временем и его движением. Если время остановить невозможно, то движения останавливаются там, где затихает их инерция в результате торможения-передачи движения от одного тела другим телам среды.
2.5.2015г. Пивень Григорий.
Общие понятия
При нормальных внешних условия все вещества находятся в своем привычном состоянии: кислород — в газообразном, вода — в жидком, кристаллы — в твердом. Их изменение вызывает переход одного и того же вещества в разные состояния, которые называются агрегатными. Повышение или понижение температуры и/или давления окружающей среды влияет на характер взаимодействия между частицами, составляющими вещество (молекулами, атомами, ионами), и расстояние между ними.
Бывает три вида агрегатных состояний (АС):
Переход вещества из одного АС в другое называется фазовым и сопровождается скачкообразным изменением его физических и химических свойств — плотности, растворимости, кинетической и потенциальной энергии частиц и др. Всего существует шесть процессов, вызывающих изменение агрегатного состояния вещества:
Сублимированию в той или иной мере подвержены все твердые тела, но в основном количество частиц, покинувших тело, настолько мало, что процесс практически незаметен. Примеры явной сублимации — графит и сухой лед (оксид углерода). Даже сильное нагревание не приводит их в жидкое состояние, а постепенно превращает в газ. Запахи твердых тел тоже обусловлены возгонкой — отрываясь от поверхности, молекулы скапливаются в пары, обладающие ароматом (камфара, нафталин). Молекулы некоторых органических веществ, например, белков, настолько большие, что не позволяют им принять газообразную форму.
Твердые тела
При нормальных условиях находятся в стабильной форме и сохраняют свой объем. По внутреннему строению и свойствам разделяются на кристаллические и аморфные. Первые отличаются строго упорядоченным положением частиц, между которыми установлены сильные взаимосвязи — ковалентные полярные и неполярные, ионные, металлические. Тип взаимодействия определяет физические свойства твердого тела. Это, как правило, металлы и их оксиды, обладающие хорошей тепло- и электропроводностью, прочные и упругие.
Свойства аморфных тел близки к жидкостным, так как их молекулы передвигаются между хаотично расположенными условными центрами. К ним относятся разнообразные смолы, пластмассы, стекло и другие неметаллы. Нагревание кристаллических веществ приводит к нарушению упорядоченного расположения частиц, увеличению расстояний между ними и рекристаллизации. При определенной температуре, которая называется температурой плавления, перестройка молекул приводит к превращению твердого тела в жидкость. Количество теплоты, которое нужно, чтобы расплавить некоторую массу вещества, вычисляют по формуле: Q = km, где k — удельная теплота плавления этого вещества, m — его масса.
Молекулярная кинетическая энергия остается неизменной, поэтому дальнейшее нагревание вещества не приводит к повышению его температуры до тех пор, пока все оно не превратится в жидкость. Если продолжать нагрев, то с поверхности расплавленного металла начнется испарение — беспорядочный отрыв отдельных молекул, который является началом перехода в газообразное состояние. При кристаллизации, начинающейся при снижении температуры, остывающее тело само отдает тепло в атмосферу.
Опытным путем установлено, что температуры плавления и кристаллизации у каждого металла равны друг другу, а их точно известное значение отличает кристаллические тела от аморфных. В отличие от металлов, аморфные вещества не плавятся, а размягчаются. Например, стекло при нагревании сначала становится мягким, его легко согнуть или растянуть.
Дальнейшее повышение температуры приводит к тому, что оно под действием силы тяжести растекается по сосуду, который занимает. Эта масса, поначалу очень густая, постепенно приобретает консистенцию воды. Таким образом процесс перехода аморфного тела в жидкое происходит не при фиксированной температуре, как у кристаллических тел, а растягивается на все время нагревания.
Изменение жидкостей
Жидкости — это тела, занимающие весь объем, в котором находятся, образующие поверхность, но не способные удерживать упругую форму. Для них свойственно сильное межмолекулярное взаимодействие и низкая сжимаемость, что определяет их положение между газообразным и твердым АС. Жидкости изотропны, текучи и обладают удельным весом, сравнимым с тем же показателем у твердых тел.
Правильное расположение внутренних частиц распространяется на небольшие области — они не только колеблются вокруг узлов так называемой квазикристаллической решетки, но и могут перескакивать между ними. Получается сложная траектория — колебания вокруг центра, перемещающегося в пространстве. Этим объясняется текучесть тел в жидком АС. Если понизить температуру до границ кристаллизации, то различные тепловые свойства жидкостей приблизятся к показателям твердых тел.
Процесс парообразования
Некоторые молекулы жидкости могут преодолеть силы поверхностного натяжения и перейти в парообразную форму, чем объясняется явление испарения, происходящее при любой температуре. Когда она повышается, процесс становится интенсивней и распространяется на весь объем. Появляется все больше пузырьков насыщенного пара, прорывающихся из глубины на поверхность.
При температуре кипения, имеющей определенное значение для каждого жидкого тела, давление пара внутри пузырьков превышает атмосферное, и начинается интенсивный переход жидкости в газообразное АС. При пониженном атмосферном давлении температура кипения той же жидкости становится ниже.
Динамическое равновесие
Когда жидкость находится в открытой емкости, то ее количество обязательно уменьшится вследствие испарения. Но если сосуд закрыть, то этого не произойдет. Сначала начнется процесс испарения и продолжится до тех пор, пока число покинувших жидкость молекул не станет равно возвратившимся назад из паров.
Можно сказать, что замкнутая система придет в динамическое (подвижное) равновесие, так как процесс обмена молекул будет продолжаться и дальше, т. е. испарение и конденсация в замкнутой системе происходят одновременно и компенсируют друг друга. Пар, который находится в таком равновесии с соответствующей жидкостью, называется насыщенным. Изменение внутренней энергии вещества определяется по формуле: ΔU = ± mr, где m — масса тела, r — удельная теплота парообразования.
Динамическое равновесие у разных жидкостей наступает при разной плотности пара. Это зависит от силы межмолекулярного взаимодействия. Если они велики как, например, у ртути, то только незначительное число самых быстрых молекул может покидать поверхность жидкости, а равновесие наступает при малой плотности пара. У летучих жидкостей молекулы разлетаются очень быстро, поэтому нужна высокая плотность для наступления равновесия.
Газообразное состояние
При этом АС частицы химических элементов и их соединений связаны друг с другом слабо или не связаны вообще и заполняют весь предоставленный объем. Такое состояние вещества широко распространено в природе: воздушные массы атмосферы; скопления газов под землей; газообразная материя, растворенная в водах Мирового океана.
Все газы отличаются следующими свойствами:
Эти характеристики определяются большими расстояниями между молекулами и их притяжением друг к другу. Газообразное АС веществ можно рассматривать, как перегретый или ненасыщенный пар. При сверхвысоких температурах газ частично или полностью ионизируется, при этом сохраняя общую электрическую нейтральность, потому что плотности отрицательных и положительных зарядов находятся примерно на одном уровне.
Так образуется плазма, которую некоторые ученые рассматривают, как четвертый вид АС вещества. В ней взаимодействие происходит между ионами и свободными электронами с помощью электрических сил, действующих на большом расстоянии. Вещества, которые при нормальных условиях являются газами, самопроизвольно переходить в жидкое состояние не могут.
Увеличение давления и понижение температуры приводит к уменьшению расстояний между молекулами и увеличению силы взаимодействия до такой степени, что вещество из газообразного состояния переходит в жидкое, т. е. изменяет свое АС. Этот процесс называется сжижением и характеризуется критической температурой. Она определяется в точке, после которой превращение газа в жидкость невозможно ни при каком давлении.
Для каждого газообразного вещества значение этой температуры свое. Оно бывает примерно равно комнатной, как у аммиака, хлора и углекислого газа, тогда для сжижения достаточно воздействовать на газ только давлением. У водорода и гелия, например, критическая температура намного ниже комнатной. Перед сжижением их сначала охлаждают до температуры чуть ниже критической, а затем доводят до жидкого АС повышенным давлением.
Сравнительная таблица
Различие между твердыми материалами, жидкостями и газами объясняется внутренними процессами, зависящими от агрегатного состояния вещества. В таблице приведены характерные для каждого класса особенности.
| Состояние вещества | Расположение и характер движения частиц | Энергия взаимодействия | Физические свойства |
| Твердое | Расстояния между частицами, колеблющимися около положения равновесия, сопоставимы с их размерами. | Потенциальная энергия превышает кинетическую. Взаимодействие между частицами сильное. | Сохраняют собственную форму и объем. Имеют точную температуру кристаллизации и плавления. Обладают твердостью, прочностью и упругостью. |
| Жидкое | Частицы расположены вплотную и сохраняют близкий порядок упорядоченности. Могут перескакивать из одного положения равновесия в другой. | Модуль кинетической энергии почти равен потенциальной. | Сохраняют объем, но не форму. Закипают при определенной температуре. Текучи, почти не поддаются сжатию. |
| Газообразное | Частицы расположены хаотично на расстояниях, сильно превышающих их собственные размеры. Хаотичное движение частиц с довольно большими скоростями приводит к постоянным столкновениям между ними. | Кинетическая энергия по модулю намного превышает потенциальную. Легко заполняют весь предоставленный объем и сжимаются. | Принимают форму тех предметов, в которых находятся. |
Можно отметить, что переход вещества из одного АС в другое зависит от соотношения потенциальной и кинетической энергии его частиц.
Область применения
Способность металлов плавиться и поддаваться обработке в жидком состоянии широко применяется в черной и цветной металлургии. В технологиях получения соли и других химических соединений используется процесс выпаривания, при котором нужное вещество получается после испарения жидкости. В разных областях промышленности и техники распространено применение жидких газов.
Инертные газы используются в осветительных приборах, жидкий кислород — в медицине в качестве средства анестезии, при сварке металлов в смеси с ацетиленом.
Жидкий водород — это ракетное топливо, а оксид серы уничтожает плесень. В рефрижераторах и промышленных холодильниках применяют жидкий аммиак, кроме того, сжиженные газы удобней транспортировать.
Агрегатное состояние вещества определяется: а) только расположением молекул б) характером движения и взаимодействия молекул
Ответ или решение 2
Для решения данной задачи определим
Что такое агрегатное состояние вещества
Итак, чтобы понять, что такое агрегатное состояние нам необходимо рассмотреть пример. Всякое вещество, будь то вода, металл, газ могут находиться в нескольких состояниях. Проще всего это объясняется на примере воды. Все мы очень хорошо знаем что вода в холодное время года замерзает и превращается в лед так вот, вода превращенная в лед в физике называется твердым агрегатным состоянием, но в то же время многие замечали туман или что при жаркой погоде лужи высыхают. Что же с ними происходит? Все очень просто, вода переходит в газообразное состояние, испаряется, превращается в пар.
Почему решили разделить агрегатные состояния
Просто некоторым любопытным людям стало интересно:»Почему та же вода, то твердая, то жидкая, то газообразная?» И вот они стали рассматривать все вещества под разными приборами и выявили закономерности в твердых, жидких и газообразных состояниях. Оказалось, что молекулы одного и того же вещества в разных состояниях ведут себя по разному.
На основе всех своих наблюдений, изучавшие агрегатные состояния вещества, ученые пришли к выводам, что данные состояния обусловлены как раз расположением, характером движения и взаимодействия молекул. Ответ в.
В данном вопросе теста правильным является вариант В:
агрегатное состояние вещества определяется расположением молекул, характером движения и взаимодействия молекул.
В твёрдом теле атомы расположены близко друг к другу, а скорость их движения небольшая.
В жидкостях атомы расположены дальше друг от друга, чем в твёрдом теле, и скорость их перемещения также выше.
В газообразных веществах атомы расположены далеко друг от друга и перемещаются с огромной скоростью.