Чем опасна футлярная блокада осложнения
Осложнения блокады плечевого сплетения
Мигачев С.Л., Свиридов С.В.
Российский государственный медицинский университет, Москва
В последние годы в отечественной и зарубежной анестезиологии отмечается бум использования методов регионарной анестезии (РА) при операциях на верхних конечностях. В настоящее время 60-80% травматологических и ортопедических операций у взрослых пациентов выполняются под РА.
Преимущества регионарной анестезии
Увеличивающийся интерес анестезиологов к регионарным методам обезболивания обусловлен достаточно высокой эффективностью блокады плечевого сплетения (БПС) при операциях на верхних конечностях. Так, по данным литературы, процент адекватных блокад может составлять в зависимости от метода проводниковой блокады и уровня оперативного вмешательства (кисть, предплечье, плечо или надплечье) от 97,3% до 79,0% (2,5,10). Более высокая частота неадекватных анестезий отмечается при операциях в области плеча и надплечья, что обусловлено сложной иннервацией этого региона ветвями плечевого, поверхностного шейного сплетения (надключичными нервами) и межреберно-плечевым нервом. Важными преимуществами РА перед методами общей анестезии являются уменьшение выраженности послеоперационного болевого синдрома, снижение нейрогуморального ответа организма на операционную травму, уменьшение интраоперационной кровопотери, улучшение микроциркуляции в оперированной конечности [4], уменьшение количества легочных осложнений.
Выполнение регионарного блока длительно действующими местными анестетиками (бупивакаин, ропивакаин) позволяет обеспечить эффективную анальгезию на протяжении 6-18 часов после операции.
Осложнения РА плечевого сплетения
Однако, при анализе литературных данных оказывается, что частота неврологических осложнений при блокаде плечевого сплетения крайне низка. Так Фурсаев В.А. (1966) анализируя 12787 анестезий, лишь в 59 случаях (0,46%) указывает на неврологические осложнения, к тому же обратимые. Пащук А.Ю. (1987), обобщая 7554 случая проводниковых анестезий, отметил развитие постинъекционной нейропатии в 0,04 % наблюдений.
Таким образом, на сегодняшний день сложилось мнение, что осложнения БПС чаще обусловлены не травмой нервных стволов с развитием неврологического дефицита, а непреднамеренной блокадой близко расположенных нервных структур, повреждением кровеносных сосудов или купола плевры, а также системным токсическим действием МА.
Плечевое сплетение расположено в непосредственной близости от многих анатомически важных структур шеи. Так в области выхода из межпозвонковых отверстий сплетение проходит на 1-2 см медиальнее сонной артерии. Позвоночная артерия расположена в канале, образованном поперечными отростками шейных позвонков, в непосредственной близости от нервных корешков. Возвратный гортанный, диафрагмальный нервы и звездчатый ганглий расположены в том же клетчаточном пространстве, что и плечевое сплетение. Эпидуральное пространство соединяется с предпозвоночной клетчаткой, в которой располагается плечевое сплетение, через межпозвоночные отверстия [12]. В шейном отделе позвоночника в области манжет нервных корешков нередко формируются дивертикулообразные выпячивания твердой мозговой оболочки, которые через межпозвонковые (фораминарные) отверстия могут выходить за пределы позвоночного столба и располагаться в паравертебральной клетчатке. В более дистальных отделах (в надключичной области) плечевое сплетение проходит в непосредственной близости от купола плевры, в одном фасциальном футляре с подключичной артерией.
Внутрисосудистое введение МА или быстрая его адсорбция из богато васкуляризирированных областей (глубокие мышцы шеи) приводят к возникновению системного токсического эффекта, проявляющегося чаще всего симтомами нейротоксичноского действия (мышечный тремор, онемение языка, дизартрия, сомноленция, фокальный или генерализованный судорожный припадок). Кардиотоксическое действие МА в виде разнообразных аритмий (описаны случаи фибрилляции желудочков при использовании бупивакаина), снижения системного артериального давления за счет угнетения сократимости миокарда в клинической практике регистрируются достаточно редко.
Осложнения при использовании межлестничного доступа
БПС из межлестничного доступа является самым популярным методом РА при операциях на плече и плечевом суставе. При операциях на предплечье и кисти межлестничная блокада используется реже из-за высокой частоты неадекватной анестезии С7-Т1 дерматомов (зона иннервации локтевого и медиального кожного нервов предплечья). Это наиболее высокий доступ к плечевому сплетению. Технически раствор анестетика вводится в фасциальный футляр плечевого сплетения в непосредственной близости от межпозвонковых отверстий. Так как шейное и плечевое сплетения расположены в едином фасциальном футляре, при межлестничной блокаде, как правило, отмечается полная или частичная анестезия шейного сплетения.
По данным литературы и нашим собственным наблюдениям межлестничную блокаду нельзя отнести к безопасному методу РА. При её выполнении возможны многочисленные осложнения, в т.ч. жизненно-опасные, что обусловлено, главным образом, близостью многих анатомически важных структур шеи к месту выполнения регионарного блока. Так эпидуральное распространение раствора МА может привести к развитию двусторонней эпидуральной блокады шейных и верхнегрудных сегментов с появлением сенсорной и моторной блокады противоположной верхней конечности, артериальной гипотонии, брадикардии, одышки [1].
Тотальный спинальный блок развивается при субарахноидальном введении раствора МА, чаще всего при случайной пункции дивертикула твердой мозговой оболочки [13].
У 30-50% пациентов после межлестничной блокады возможно развитие синдрома Горнера в связи с блокадой звёздчатого узла и шейного симпатического ствола. Блокада возвратного гортанного нерва приводит к появлению охриплости голоса [6].
Непреднамеренное введение МА в позвоночную артерию вызывает быстрое развитие эпилептического припадка [3].
Осложнения при использовании над- и подключичного доступа
При (над-) и подключичном доступе к плечевому сплетению достигается надёжная анестезия всей верхней конечности, плечевого сустава, за исключением кожи в дельтовидной, подмышечной области, медиальной поверхности плеча. Наиболее серьезным осложнением БПС надключичным доступом (по Куленкампфу) является повреждение купола плевры и легкого с развитием пневмоторакса. Частота этого осложнения у опытных анестезиологов не превышает 2-3%. В литературе описаны случаи напряженного пневмоторакса, развившегося после БПС по Куленкампфу. По этой причине данный доступ не может быть рекомендован в амбулаторной анестезиологической практике, а также для анестезии обеих верхних конечностей.
Модификацией надключичного доступа по Куленкампфу является подключичный параваскулярный доступ по Winnie. Этот доступ приобретает все большую популярность среди анестезиологов. Принципиальная разница между этими техниками в том, что при надключичном доступе поиск плечевого сплетения осуществляется на верхней поверхности первого ребра, а при подключичном параваскулярном – в ключично-рёберном промежутке. Тем самым уменьшается вероятность повреждения плевры и лёгкого. Риск возникновения пневмоторакса при БПС по данной методике минимален.
Пункция подключичной артерии с развитием гематомы надключичной области является общим осложнением (над-) и подключичного доступов. Однако у пациентов с нормальными показателями свертываемости крови в большинстве случаев гематома не достигает значительных размеров, не приводит к компрессии сосудисто-нервного пучка и разрешается без последствий.
Характеристика клинического материала
I группу составили 65 пациентов (38 мужчин и 27 женщин), у которых была применена проводниковая анестезия плечевого сплетения подключичным параваскулярным доступом по Winnie
II группа – 54 пациента (32 мужчины и 22 женщины), которым для интраоперационного обезболивания выполнена межлестничная блокада.
Выполнение регионарного блока
Идентификация ПС осуществлялась поиском парестезий. Для анестезии использовалась смесь 2% раствора лидокаина в объёме 10 мл (200 мг) и маркаина 0,5% в объёме 20 мл (100 мг). При отсутствии противопоказаний добавлялся адреналин до концентрации 1:200.000. Данную пропись анестетиков для регионарной анестезии использовали у пациентов всех исследуемых групп.
Во всех случаях выполнялась аспирационная проба перед инъекцией МА и после введения каждых 10 мл раствора.
Время с момента выполнения РА до начала операции составляло 35±5 мин. После выполнения регионарной блокады пациентам вводился мидазолам (дормикум ® ) 1,5 – 5 мг методом титрования до состояния легкой седации. Для уменьшения психо-эмоционального и позиционного дискомфорта во время операции применяли небольшие дозы дормикума (1,5 – 2,5 мг болюсно) и фентанила (0,05 мг болюсно). Средний расход дормикума в I и II группах на 1 час операции составил 2,28±0,91мг, фентанила – 0,07±0,03 мг.
Анализ интраоперационных осложнений при выполнении регионарной анестезии
Выполнение РА плечевого сплетения подключичным параваскулярным доступом по Winnie не сопровождалось значимыми и серьезными осложнениями. Тем не менее, нами были отмечены следующие осложнения у пациентов I группы. У 2 (3,0 %) больных после введения расчетных доз МА было отмечено возникновение мышечной дрожи, онемения языка. Данные симптомы были расценены как токсическое действие МА. У 9 (13,8%) пациентов при выполнении регионарной блокады была непреднамеренно пунктирована подключичная артерия. Следует отметить, что ни у одного из пациентов не отмечалось формирование гематомы надключичной области. У 3 (4,6%) пациентов оказалась затрудненной идентификация плечевого сплетения, регионарную блокаду удалось выполнить после многократных попыток. Случаев пневмоторакса отмечено не было ( диаграмма № 1 ).
Таким образом, количество осложнений у пациентов I группы было низким, не было зарегистрировано ни одного тяжелого осложнения, что указывает на безопасность данного метода регионарной анестезии.
При анализе осложнений у пациентов II группы отмечена значительная частота побочных реакций, связанных с самой методикой межлестничной анестезии, предполагающей введение раствора МА в хорошо васкуляризированное пространство вблизи многочисленных нервных структур. Так у 3 (5,5%) пациентов отмечалось эпидуральное распространение МА с развитием блокады противоположной верхней конечности, что сопровождалось брадикардией и артериальной гипотензией. Из них у 2 (3,7%) пациентов из-за двустороннего паралича диафрагмальных нервов развилась клиника острой дыхательной недостаточности, проявляющаяся одышкой, тахипноэ, снижением сатурации артериальной крови.
У 2 (3,7%) пациентов отмечалось токсическое действие МА, проявляющееся мышечной дрожью, онемением языка, двигательным возбуждением. У 2 (3,7%) пациентов сразу после выполнения межлестничной блокады развился большой эпилептический припадок.
У одного больного через 5 минут после введения раствора МА отмечено появление желудочковой экстрасистолии, что было объяснено кардиотоксическим аритмогенным действием бупивакаина или адреналина, входящего в состав смеси МА.
У 32 (59,2%) пациентов отмечался синдром Горнера, проявляющейся птозом, миозом, энофтальмом, гиперемией коньюнктивы со стороны выполнения блокады. Клиника синдрома Горнера у всех пациентов развилась в течение 25 мин. Длительность симптомов колебалась от 8 до 18 часов.
У 17 (31,5%) пациентов после выполнения межлестничной блокады отмечено появление охриплости голоса вследствие односторонней блокады возвратного гортанного нерва.
Технические сложности при идентификации плечевого сплетения отмечались у 4 (7,4%) пациентов.
Таким образом, практически у всех пациентов при межлестничной блокаде отмечено возникновение одной или нескольких побочных реакций или осложнений ( диаграмма № 2 ), связанных с системным действием МА или сопутствующей блокадой близко расположенных нервных структур (диафрагмальный нерв, возвратный гортанный нерв, симпатическая цепочка, корешки контралатерального плечевого и шейного сплетений). Большинство осложнений межлестничной блокады можно квалифицировать как лёгкие, носящие транзиторный характер. Однако двусторонняя блокада диафрагмальных нервов с развитием клиники острой дыхательной недостаточности и большой судорожный припадок требовали неотложных лечебных мероприятий и квалифицированы нами как осложнения средней тяжести.
Наиболее типичными осложнениями межлестничной блокады являются синдром Горнера (59,2%), парез возвратного гортанного нерва (31,6%), двусторонний паралич диафрагмальных нервов (5,5%), судорожный синдром (3,7%), нейротоксическое действие местного анестетика (5,5%), проявляющееся онемением языка, мышечной дрожью, сонливостью. Вероятность развития тяжелых осложнений анестезии (тотальный спинальный блок, большой эпилептический припадок, эпидуральное распространение раствора МА с развитием клиники острой дыхательной недостаточности) требует некоторого ограничения для широкого применения межлестничной блокады при анестезиологическом обеспечении операций на верхних конечностях.
Наиболее серьезным осложнением РА плечевого сплетения надключичным доступом по Куленкампфу является пневмоторакс, обусловленный повреждением купола легкого. По этой причине данный доступ не может быть рекомендован для амбулаторной анестезиологической практики, а также для анестезии обеих верхних конечностей.
Проводниковая блокада плечевого сплетения подключичным параваскулярным доступом по Winnie является высоко безопасным методом РА при операциях на кисти и предплечье. При выполнении данной блокады риск тяжелых осложнений анестезии сводится к минимуму. При операциях на плече и плечевом суставе данная блокада должна быть дополнена проводниковой блокадой ветвей поверхностного шейного сплетения (надключичных нервов), а при хирургических манипуляциях на внутренней поверхности плеча – также блокадой межреберно-плечевого нерва.
Регионарная анестезия и лечение боли. Тематический сборник. Москва-Тверь 2004 г., стр.100-108
Блокады в позвоночник: мифы и факты
Устранение боли является актуальной задачей для современной медицины. Для борьбы с этим симптомом разработано множество методик, одной из которых является блокада в позвоночник. Процедура получила свое название из-за механизма действия: введение обезболивающих препаратов в эту область позволяет блокировать передачу нервных импульсов к участку головного мозга, который воспринимает боль. Такой способ имеет ряд преимуществ по сравнению с другими методами обезболивания, например, таблетками или внутримышечными инъекциями:
Выполнять блокады можно при широком спектре заболеваний позвоночника и защемлении отдельных нервов, для которых характерна сильная, трудно устранимая боль. Это могут быть остеохондроз, межпозвоночная грыжа (протрузия, экструзия), спондилоартроз, невралгия и др.
Несмотря на все преимущества блокады в позвоночник, не все люди соглашаются на данную процедуру по причине различных страхов. Они решают использовать менее эффективные, но при этом простые методы обезболивания, как, например, таблетки. В результате симптом никуда не уходит, качество жизни пациента падает, и он вынужден постоянно терпеть боль.
Почему не все соглашаются на блокаду в позвоночник
Каждый человек по-своему объясняет отказ от проведения процедуры. Наиболее частыми страхами являются:
Некоторые страхи оказываются настолько сильными, что избавиться от них без помощи психотерапевта оказывается непросто, однако в большинстве случаев проблему удается решить после общения с врачом, который будет проводить блокаду. Специалист подробно расскажет обо всех особенностях метода, после беседы многие предубеждения исчезнут сами собой.
Почему не нужно бояться блокады
Итак, разберем страхи.
Во время блокады используются растворы местных анестетиков, по показаниям вводят кортикостероиды или другие медикаменты. Все они обладают мощным обезболивающим эффектом – он может длиться очень долго, на протяжении нескольких дней или недель, при этом чувствительность кожи может снижаться, но лишь временно. Постоянная потеря тактильных ощущений невозможна.
Блокады в позвоночник – это хорошо проверенный метод лечения. Его применяют не первый десяток лет, и за все это время не было выявлено негативных последствий данной процедуры для здоровья, напротив, блокада признана эффективным методом купирования боли. При этом многие страхи пациентов являются необоснованными.
Как выполняются блокады в позвоночник
Перед процедурой пациента осматривает и консультирует врач. Специалист выявляет показания и подбирает вид блокады, а также препарат, который будет использоваться для инъекции, после этого переходят непосредственно к самой процедуре. Место укола предварительно обрабатывается раствором. Введение препарата может осуществляться в ткани, расположенные рядом с поясничным, шейным и грудным отделом позвоночника. После процедуры место прокола повторно обрабатывается антисептиком, на него накладывают стерильную повязку. На завершающем этапе врач дает рекомендации, которые касаются образа жизни пациента в ближайшие несколько дней.
Безопасны ли блокады
Любой метод лечения несет в себе определенные риски, и блокады не являются исключением. В небольшом проценте случаев (менее 5%) после процедуры могут развиваться осложнения :
Чтобы минимизировать эти риски, необходимо соблюдать ряд простых правил:
Общий процент осложнений после блокад в позвоночник минимален и сопоставим с рисками при других медицинских вмешательствах, в то же время данный метод отличается высокой эффективностью и обеспечивает быстрое устранение боли, поэтому продолжает активно применяться в медицине.
Как применяется блокада локтевого сустава?
Что делать, если локтевой сустав нестерпимо болит? Делать блокаду. Рассказываем всё про этот новый и простой способ купирования боли и лечения повреждений суставов.
Причин для боли в суставе локтя множество: он повреждается из-за травм и спорта, могут начаться осложнения из-за общих заболеваний, например, артрита или остеохондроза. Блокада локтевого сустава поможет избавиться от самого острого приступа боли и избежать осложнений.
Что такое лечебная блокада?
Так называют метод лечения суставов, при котором лекарство вводится непосредственно в больные участки. Врач может сделать инъекцию в разные части поражённого сустава, в окружающие мышцы и даже костную ткань. Это зависит от местоположения основного повреждения.
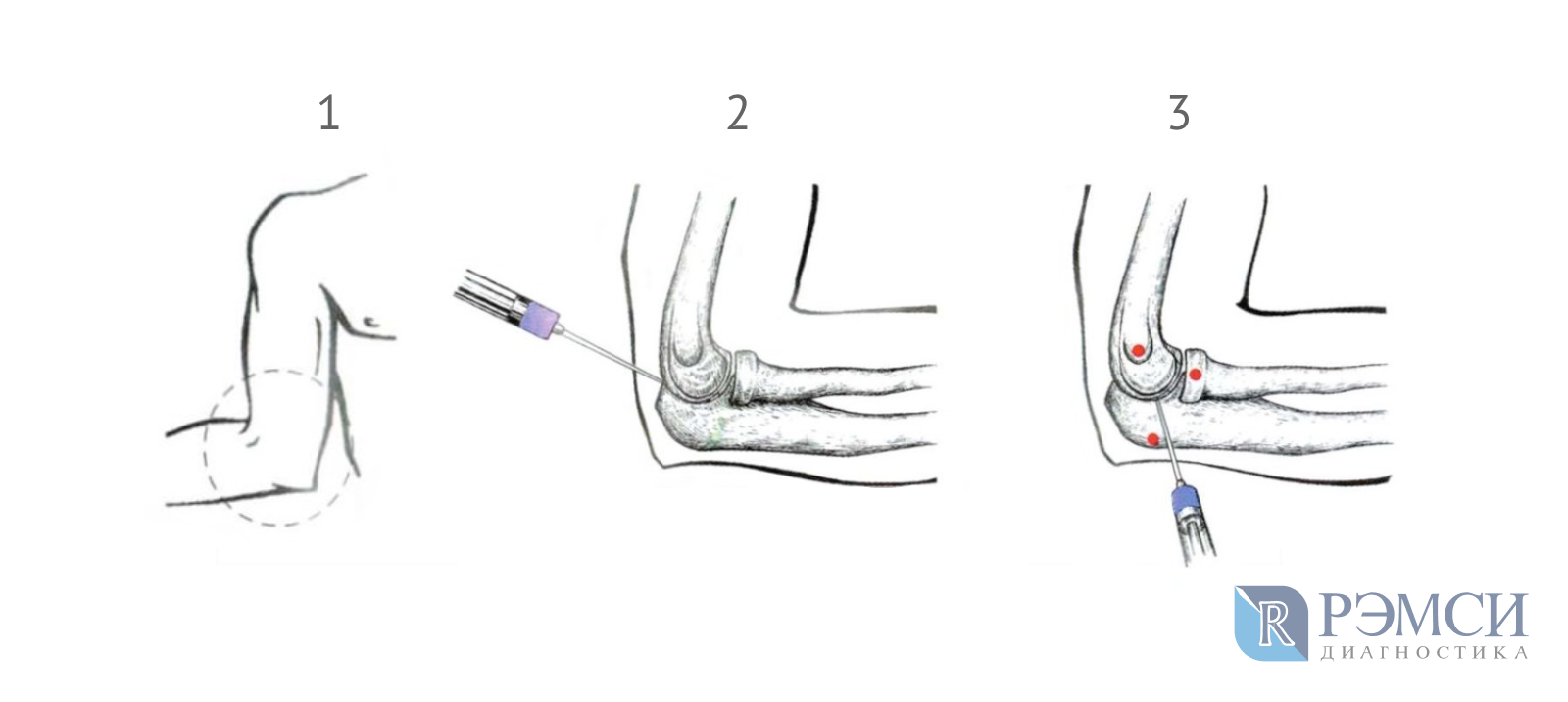
Блокада — новый способ лечения, который переносится легче оперативного вмешательства и действует эффективнее мазей и лекарств для приёма внутрь. Применяют её с двумя целями:
Благодаря такому методу в больной сустав попадает максимальная концентрация действующих веществ, что даёт наиболее быстрый результат.
Когда применяется блокада локтевого сустава
Блокаду можно применять для купирования боли в локте в самых разных случаях:
Но если боль в локте вызвана заболеваниями позвоночника, то введение блокады в локтевой сустав поможет только временно снять боль. Поэтому перед назначением процедуры врач обязательно должен выяснить причину болей и провести обследование. Оно может включать:
Только после полного осмотра и постановки диагноза специалист может назначить введение блокады в локтевой сустав. Вызвано это в том числе и необходимостью подобрать подходящее под заболевание лекарство. Однако, при нестерпимых болях, блокаду с анестезией могут применить без дополнительных обследований. Так получится ослабить симптомы и восстановить работоспособность сустава.
Как работает лечебная блокада суставов?
При блокаде локтя медицинский препарат попадает непосредственно в повреждённый сустав, что позволяет ему мгновенно воздействовать на организм. Именно поэтому её часто назначают в случаях, если традиционные способы лечения не дали результатов.
В зависимости от места инъекции, блокада локтевого сустава делится на:
Для блокады могут применять анестетики и противовоспалительные препараты различной природы — всё зависит от повреждений и причины боли.
По составу блокады делят на две группы: однокомпонентную и многокомпонентную. Если в первую входит или только обезболивающее, или только противовоспалительное, то вторая поможет и избавиться от воспаления, и снизить болевой синдром.
Дискомфорт при блокаде уходит почти мгновенно, спустя несколько секунд после введения анестетика. Для устранения острой боли (например, после перелома локтя или разрыва сухожилий) блокаду вводят один раз. Для лечения артроза, артрита, остеохондроза врач может назначить курс из нескольких инъекций.
Несмотря на практически полную трудоспособность и подвижность, постарайтесь аккуратно обращаться с больным суставом после проведения блокады. Это особенно сложно, если была повреждена ведущая рука. Но излишняя нагрузка приведёт к дальнейшему разрушению сустава. А это уже может вызвать и новые приступы боли, и серьёзные осложнения с меньшим шансом на восстановление.
Противопоказания и осложнения
Несмотря на кажущуюся простоту процедуры, у неё есть ряд противопоказаний:
Относительные противопоказания — заболевания желудочно-кишечного тракта. Связано это с тем, что применяемые в противовоспалительных препаратах глюкокортикостероидные гормоны нарушают работу желудка, кишечника и почек.
Осложнения из-за блокады проявляются редко. В основном это аллергические реакции на препарат: сыпь, покраснение, в крайне редких случаях — анафилактический шок и отёк Квинке. У части пациентов на месте введения появляются гематомы. Также внутрь может проникнуть инфекция, из-за чего начнётся более серьёзный воспалительный процесс. Однако и болезнетворные бактерии, и механические повреждения сустава после блокады встречаются очень редко. Могут проявиться токсические осложнения из-за неверно рассчитанной дозы препарата или его попадания в просвет сосудов. Чтобы этого избежать, обратитесь к опытному врачу, который точно сделает инъекцию правильно.
Несмотря на все возможные осложнения и противопоказания, лечебная блокада — одно из лучших средств для остановки воспалительных процессов в локтевом и любом другом суставе. Для успешного лечения нужно убедиться в верности диагноза и отсутствии противопоказаний, а также обратиться к опытному специалисту. Грамотно проведённая процедура сможет и избавить вас от боли, и ускорить процесс восстановления сустава.
Научная электронная библиотека
Глава 2. ОСНОВЫ МЕТОДА ВНУТРИКОСТНЫХ БЛОКАД
Под понятием лечебная медикаментозная блокада понимают введение в ткани организма лекарственных веществ, которые вызывают временную «фармакологическую невротомию» в пределах рефлекторной дуги [8, 11, 13, 14, 17].
При клинических проявлениях остеохондроза позвоночника лечебные медикаментозные блокады используются с терапевтической целью для достижения анальгезирующего, миорелаксирующего, трофостимулирующего, рассасывающего, либо иного эффекта в зависимости от вводимого лекарственного средства.
Лечебная медикаментозная блокада – это врачебная процедура, которая приравнивается к малым хирургическим вмешательствам.
Наиболее часто блокадные методы лечения применяются при болевых синдромах, возникающих при клинических проявлениях поясничного, грудного и шейного остеохондроза, радикулопатии, нейропатии, плексопатии, артралгиях, эпикондилитах, туннельных синдромах, фантомных болях. Реже – при других неврологических заболеваниях: синдром Меньера, спастико-тонические поражения мышц, трофические нарушения, сенестопатии, периферические ангиотрофоневрозы.
Противопоказанием для лечебных медикаментозных блокад являются:
1) лихорадочные состояния;
2) геморрагический синдром;
3) лекарственная непереносимость;
4) психические нарушения;
5) гнойные заболевания кожи;
6) воспалительные изменения в месте инъекции;
7) техническая невозможность проведения блокады [14, 15, 19, 33].
При проведении блокад могут наблюдаться следующие осложнения:
1) гнойные – в связи с нарушением асептики и антисептики;
2) токсические – в связи с передозировкой препарата;
3) аллергические – в связи непереносимостью вводимого лекарства;
4) травматические – в связи с травматизацией окружающих тканей (сосуды, нервы) и органов (легкие – пневмоторакс);
5) рефлекторные – в связи с местными сосудистыми и мышечными спазмами;
6) компрессионные – в связи со сдавлением нервных структур при быстром введении большого количества лекарственного вещества [14, 15, 33].
Основным действующим компонентом блокады является местный анестетик. Он проникает через биологические среды к нервным волокнам, адсорбируется на их поверхности и, благодаря взаимодействию с полярными группами фосфолипидов и фосфопротеидов, фиксируется на мембране рецептора и/или проводника. Молекулы анестетика, включенные в структуру белков и липидов мембраны, вступают в конкурентные взаимодействия с ионами кальция и нарушают обмен натрия и калия, что подавляет транспортировку натрия через мембрану и блокирует возникновение возбуждения в рецепторе и проведение его по нервному волокну [6, 8, 32].
Степень действия анестетика на нервное волокно зависит с одной стороны от физико-химических свойств анестетика, с другой – от типа нервного проводника, с третьей от точности подведения к нему раствора. Чем ближе к проводнику будет доставлен анестетик, тем меньше он будет разбавлен межтканевой жидкостью по пути диффундирования, тем меньшая начальная концентрация анестетика будет достаточна для выполнения качественного дифференциального блока, тем меньше риск токсического осложнения. С этой точки зрения блокада должна быть, по существу, «снайперским уколом».
Анестетик блокирует сначала безмиелиновые, медленные волокна – болевые и вегетативные проводники, затем миелиновые, проводящие эпикритическую чувствительность, и в последнюю очередь – двигательные волокна. Для блокирования проведения импульса по лишенным миелинового, защитного слоя проводникам достаточно воздействия анестетика пониженной концентрации. Воздействие анестетика на медленные проводники создает условия для нормализации соотношения афферентации по медленным и быстрым волокнам. Действуя преимущественно на безмиелиновые медленные проводники, анестетик блокирует и безмиелиновые эфференты – вегетативные и трофические волокна. Поэтому на время действия анестетика и длительное время после полного выведения его из организма уменьшаются патологические вегетативные реакции в виде спазма сосудов, нарушения трофики, отека и воспаления, как в местных тканях, так и в соответствующих сегментарно-метамерных зонах.
Для блокад наиболее часто применяют ксилокаин (лидокаин) – анестетик амидного типа, который в основном метаболизируется в печени, в меньшей степени, около 10 %, выводится с мочой. Ксилокаин сочетает в себе ряд положительных свойств: повышенная устойчивость в растворах и к стерилизации, малая токсичность, высокая сила действия, хорошая проницаемость, короткий скрытый период действия, выраженная глубина анестезии, практически отсутствие сосудистых и аллергических реакций [3, 4, 5, 7, 12, 18, 23, 24, 34, 40, 42].
Цитанест – один из немногих анестетиков, который обладает меньшей токсичнотью и примерно такой же длительностью анестезии, как и ксилокаин, однако, уступает последнему по степени проникновения в нервную ткань. В нем удачно сочетаются два свойства: выраженное сродство к нервной ткани, что вызывает длительную и глубокую местную анестезию, быстрый распад в печени под действием амидов, снижающий до минимума незначтельные и бысропроходящие токсичесие осложнения.
Карбокаин – токсичнее ксилокаина, в отличие от других анестетиков не расширяет сосуды, что замедляет его резорбцию и обеспечивает длительность, превосходящую ксилокаин. Карбокаин медленно инактивируется в организме, поэтому при его передозировке возможны выраженные токсические реакции.
Маркаин – самый токсичный, но и самый долго действующий анестетик. Продолжительность анестезии может достигать 16 часов. Противопоказано его внутривенное введение.
Для пролонгации анестетиков при проведении блокад наиболее часто применяют крупномолекулярные соединения: декстраны, кровезаменители, желатиноль, белковые препараты крови, аутокровь, аллогенный костный мозг. Крупные молекулы, адсорбируя на себе молекулы анестетика и других препаратов, длительно задерживаются в сосудистом русле местных тканей, тем самым, продлевая местное и уменьшая общетоксическое действие анестетика. Аутокровь выгодно отличается от других пролонгаторов. Она не вызывает аллергии, не канцерогенна, максимально доступна, обладает иммуностимулирующим и рассасывающим эффектом, уменьшает раздражающее действие препаратов на местные ткани [13, 26].
Аллогенный костный мозг, кроме того, создает дополнительные условия для усиления метаболической активности и репаративной регенерации костной ткани за счет стромальных клеток-предшественников, влияя на созревание регенерата с помощью белковых и гликозамингликановых матриц и факторов роста [10, 24, 35, 37, 41].
Для усиления терапевтического эффекта блокады наиболее часто применяют глюкокортикостероиды, в частности, дексазон 1–4 мг.
Дексаметазон является фторсодержащим глюкокортикоидным препаратом, оказывающим мощное противовоспалительное, противоотечное, десенсибилизирующее, антиаллергическое, иммунодепрессивное, противошоковое и антитоксическое действие [9, 33, 26, 29].
Внутрикожно-подкожные блокады применяются при поверхностно расположенных триггерных зонах, обусловленных нейроостеофиброзом, по зонам Захарьина-Геда при висцералгиях, по биологически активным точкам при различных заболеваниях. Используя тонкую иглу, лекарственным раствором послойно инфильтрируют кожу до образования «лимонной корочки» и подкожную клетчатку. Одновременно блокируется до 15 триггерных точек.
Миофасциальные блокады – применяются при нарушении трофики и гиподинамии в мышцах, фасциях и сухожилиях происходят дегенеративно-деструктивные изменения в виде фиброзного перерождения и атрофии. Во время проведения блокады болезненного мышечного уплотнения осуществляют его послойную и веерообразную инфильтрацию, и после получения отрицательной биологической и аспирационной проб, ввести туда основное содержимое шприца.
Периневральные блокады применяются не только в анестезиологии, но и при невритах, невралгиях, невропатиях и др. В точке выхода периферического нерва инфильтрируются окружающие ткани, затем короткая тонкая игла продвигается в канал нерва, куда медленно вводится 2–4 мл блокадной смеси.
Вегетативные блокады проводятся при вегетотрофных болевых синдромах, симпаталгиях. Отмечается место прокола кожи в соответствии с региональными анатомическими особенностями. Проводя послойную инфильтрацию, игла проводится в сагиттальной плоскости до поперечного отростка, огибая поперечный отросток, игла углубляется еще на 1,5–2 см, затем после аспирационной пробы вводится 10–15 мл блокадной смеси.
При лечении паравертебральными блокадами лечебную смесь вводят либо в паравертебральную клетчатку, либо во влагалища мышц околопозвоночной области, с расчетом, на то, что, продвигаясь периневрально, анестетик достигает начальные отделы передних ветвей нервов спинномозговых корешков, соединительных ветвей и симпатических ганглиев. Анатомической основой эффективности ПВБ является то, что фасции мышц образуют одновременно и влагалища для сосудисто-нервных пучков. При ПВБ анестетик воздействует на симпатические нервные волокна и первичные чувствительные нервные и сосудистые образования, не имеющие миелиновой оболочки [8, 11, 20, 21, 31].
Эффект обезболивания связан с временным выключением соматической и симпатической иннервации с повышением порога их возбуждения в спинном мозге. При этом лекарственный раствор воздействует на участок тканей, ограниченный пределами инфильтрата. В экперименте [8] было показано, что паравертебральное введение 10 мл анестетика на уровне Т3 позвонка, приводит к его распространению в Т2-Т6 узлах симпатической цепочки соответствующей стороны. Т1-Т5 симпатические ганглии и постганглионарные волокна идут к первичным сосудам, ответвляющимся от нисходящей аорты, межреберным артериям, сердечно-легочному комплексу и верхним конечностям.
Терапевтическая эффективность паравертебральных блокад связана с действием следующих факторов:
1) снижения возбудимости местных вегетативных центров;
2) перераспределения регионарного кровотока;
3) увеличения минутного объема крови в сегментарном пораженном органе;
4) восстановления локальной микроциркуляции,
5) местного противоотечного и противовоспалительного действия;
6) местного усиления репаративной регенерации в поврежденных инъекцией тканях (кожа, подкожная клетчатка, мышцы).
В клинике нервных болезней и нейрохирургии Российского университета дружбы народов внутрикостные блокады применяются с 1980 года. Внутрикостные блокады применяются при следующих нейроортопедических заболеваниях и синдромах: клинические проявления поясничного, грудного и шейного остеохондроза, радикулопатии, нейропатии, плексопатии, спондилогенный синдром веретбро-базилярной артериальной системы, вертебрально-кардиальный синдром, головные и лицевые боли, комплексный регионарный болевой синдром (КРБС), артралгии, эпикондилиты, туннельные синдромы, болевые синдромы при рассеянном склерозе, тазовые боли у женщин, кокцигодиния, фантомные боли, болевой синдром после операции на межпозвонковом диске и др.
При всех вышеуказанных нейроортопедических заболеваниях и синдромах внутрикостные блокады показали высокую терапевтическую эффективность.
Эта технически простая манипуляция позволяет избавить подавляющее большинство пациентов от болей в спине без операции. Внутрикостные блокады могут применяться многократно при каждом обострении клинических проявлений остеохондроза позвоночника в отличие от нейрохирургических операций. По нашему мнению, операцию на межпозвонковых дисках можно проводить только после неэффективного курса внутрикостных блокад. Исключение составляют экстренные показания к оперативному вмешательству на межпозвонковых дисках.
Следует отметить и эффективность внутрикостных блокад при лицевых болях различного происхождения, которые применяются только в нашей клинике. У 1/3 пациентов боли регрессировали полностью, у 1/3 пациентов боли уменьшились более чем на 50 %, у 1/3 пациентов боли уменьшились меньше чем на 50 %. Внутрикостные блокады можно и нужно применять у пациентов с тригеминальной невралгией, прежде чем рассматривать вопрос об оперативном лечении.
Мы также впервые в мире применили внутрикостные блокады при лечении комплексного регионарного болевого синдрома. Болевой синдром и другие клинические проявления у 80 % пациентов регрессировали более чем на 50 %.
Мы применили внутрикостные блокады для лечения болевых синдромов при рассеянном склерозе, также впервые в мире. Известно, что эти болевые синдромы трудно поддаются лечению любыми методами. Однако внутрикостные блокады показали высокую эффективность и при этой патологии. Отмечается значительный регресс не только болевого, но и спастического синдрома, а также атаксии.
Пункцию губчатой кости, обычно производят внутрикостными иглами. Существует несколько их модификаций: игла Кассирского, игла ЦИТО, игла для биопсии костного мозга и др., но специальных игл для внутрикостных блокад не разработано. В последнее время для проведения внутрикостных блокад мы используем спинальные иглы с мандреном [25].
Основным действующим компонентом блокады является местный анестетик. Для внутрикостной блокады выбор правильного анестетика принципиальный вопрос. Наиболее оптимальным анестетиком для внутрикостных блокад является лидокаин или ксилокаин. Лидокаин сильный и относительно длительно действующий анестетик.
После достижения мембраны проводника лидокаин достаточно быстро начинает блокировать проведение по нему импульса. Это очень важно при проведении внутрикостной блокады. При введении первых порций анестетика в спонгиозную ткань кости повышается внутрикостное давление и обостряется болевой синдром, пока анестетик не начал действовать как химический денервант. Применение в этом случае быстродействующего анестетика лидокаина сокращает период обострения болевого синдрома.
Лидокаин начинает блокировать проведение импульса по проводнику при концентрации 0,07 % (новокаин – 0,22 %). При введении анестетика в спонгиозную ткань он многократно разбавляется в большом объеме костного мозга, значительно в большей степени, чем при введении в мышцу. Даже при введении внутриспонгиозно низкой концентрации лидокаина (0,8–1 %) и 10-кратном его разведении в жидкой среде костного мозга сохраняется его анестезирующий эффект.
При внутривенном и внутрикостном введении 1 % лидокаина наблюдается минимальное количество токсических и сердечно-сосудистых побочных эффектов. Поэтому из всех анестетиков мы рекомендуем 0,8–1 % лидокаин – 5–10 мл для проведения различных внутрикостных блокад [2].
Из других препаратов мы применяем дексаметазон – 1–3 мг. Он является противовоспалительным, противоаллергическим, противоотечным средством. Мы не используем пролонгированные глюкокортикоиды. Повторные блокады через 1–3 дня с пролонгированным глюкокортикоидом могут привести к повышенному содержанию глюкокортикоида в крови и развитию соответствующих побочных эффектов.
При местной анестезии и паравертебральных блокадах для пролонгирования действия анестетика к нему добавляется андреналин в разведении 1:200000 или 1:400000. Введение адреналина внутрикостно даже в таких малых концентрациях противопоказано, так как это может привести к резкому повышению артериального давления и гипертоническому кризу. Это обусловлено высокой избирательной чувствительностью внутрикостных хеморецепторов к адреналину.
Нами было выполнено более 20 000 процедур внутрикостных блокад 4000 пациентам с различными хроническими болевыми синдромами и подтверждена их высокая терапевтическая эффективность и безопасность.
Мы проводим внутрикостные блокады в следующие костные выступы: остистые отростки шейных, грудных, поясничных и крестцовых позвонков, заднюю и переднюю ости крыла подвздошной кости, ость лопатки, грудину, акромион, головку плечевой кости, диафизы лучевой и локтевой кости, скуловую кость, нижнюю челюсть, вертел бедренной кости, мыщелки большеберцовой кости, головку малоберцовой кости, наружную и внутреннюю лодыжки, пяточную кость.
Блокады проводились в процедурном кабинете с соблюдением всех правил асептики и антисептики.
Внутрикостные блокады применяли в наиболее болезненные остистые отростки позвонков, а также в болезненные сегментарные костные образования в зависимости от уровня локализации неврологических проявлений остеохондроза позвоночника – ости и клювовидные отростки лопаток, головку плечевой кости, шиловидный отросток локтевой кости, грудину, гребни и задние верхние ости подвздошных костей, большой вертел бедренной кости, головки малоберцовых костей. ВКБ проводились 2–3 раза в неделю, на курс до 4–6 блокад, в зависимости от их эффективности и степени выраженности болевого синдрома.
ВКБ проводились по методике, разработанной Е.Л. Соковым (1988, 1994, 2004). После определения наиболее болезненного костного выступа 1 % раствором лидокаина инфильтрировали кожу и мягкие ткани до надкостницы. Затем через анестезированные мягкие ткани до надкостницы проводили внутрикостную иглу и внедряли ее в губчатое вещество кости на глубину 0,5 см. Правильность расположения конца иглы в губчатом веществе контролировали положительной аспирационной пробой, после чего производили ВКБ. У большинства пациентов при выполнении ВКБ в первые 15–60 секунд после начала введения лекарственной смеси в губчатое вещество кости, отмечался феномен «узнаваемой боли».
Для проведения ВКБ применялись одноразовые спинальные иглы Spinocan®, размером 0,9×88 мм/20Gx31/2˝ и 0,7×40 мм/22Gx11/2˝, лаборатории B|Braun, S.A (Brazil) [7].
Для ВКБ использовали смесь: раствор лидокаина 1 % – 8 мл, раствор дексаметазона 1–2 мг, аутологичный костный мозг – 2–3 мл. В шприц емкостью 10 мл набирали указанные препараты, иглу вводили в кость, аспирировали костный мозг, не вынимая иглы, содержимое шприца перемешивали, затем образованную смесь вводили внутрикостно.
По нашему мнению, эффективность внутрикостных блокад обусловлена следующими механизмами:
1. Адресное введение анестетика и других лекарственных препаратов непосредственно в губчатую ткань кости позволяет максимально уменьшить раздражение внутрикостных рецепторов и существенно снизить их провоцирующее влияние на процессы формирования болевого, мышечно-тонического и ангиоспастического синдромов.
2. Декомпрессивная трепанация кортикального слоя кости внутрикостной иглой приводит к снижению внутрикостной гипертензии и уменьшению раздражения внутрикостных рецепторов.
3. Дозированная альтерация кортикального слоя кости иглой с введением в губчатую ткань аутологичного костного мозга локально, но мощно стимулирует репаративную регенерацию костной ткани, усиливает ее метаболизм, а, следовательно, улучшает трофику окружающих тканей в течение длительного времени.
4. Остеоперфорация улучшает локальную микроциркуляцию и приводит к реваскуляризации сегментарных «тканей-мишеней» – мышц, связок, нервных стволов, сосудов, оболочек, хрящей.
5. Костная ткань и костный мозг являются активной рефлексогенной зоной, воздействие на которую позволяет оказывать рефлекторное влияние на различные ткани и системы организма.
6. Внутрикостное введение препаратов под повышенным давлением на длительное время восстанавливает декомпенсированный кровоток в костных сосудистых коллатералях.
7. Благодаря особенностям оттока крови от позвонков и периферических костных образований вводимые в них препараты инфильтрируют радиально пораженные окружающие сегментарные «ткани-мишени», нивелируя вторичные триггерные зоны.
Во время проведения ВКБ у 1/4 пациентов в течение 1–3 мин отмечалось легкое головокружение, металлический привкус на языке, иногда шум в ушах. Эти симптомы связаны с быстрым резорбтивным эффектом лидокаина и могут рассматриваться как признаки кратковременной вегетативно-сосудистой реакции, которые самостоятельно проходят и не требуют специальной премедикации. У двух пациентов отмечалась вегетативно-сосудистая реакция с понижением артериального давления до 80/40 мм рт.ст., которая была купирована в течение 20 мин внутримышечным введением кордиамина. Подобные сосудисто-токсические реакции наблюдаются почти во всех случаях внутрикостной анестезии, являются более выраженными и часто требуют премедикации и медикаментозной коррекции. Других реакций и осложнений в результате применения ВКБ не наблюдалось.
Надо отметить, что внутрикостные блокады, не смотря на их высокую терапевтическую эффективность, техническую простоту и экономичность за рубежом до сих пор не применяются. В нашей стране, к сожалению, они также не получили пока еще широкого применения. Такое положение объясняется несколькими причинами:
1. Роль внутрикостной сосудисто-нервной системы в патогенезе различных заболеваний изучена недостаточно.
2. Мало клинических исследований, предпринятых для изучения нейрофизиологических механизмов терапевтического действия внутрикостных блокад.
3. Опасение возможных осложнений после внутрикостной блокады.
4. Несовершенство инструментария для проведения внутрикостных блокад.
Внутрикостные блокады применяются лишь в единичных лечебных учреждениях России и Москвы, хотя пациентов, которым они могли бы помочь, великое множество. В связи с этим встает вопрос о необходимости совершенствования методов лечения больных с хроническими и часто рецидивирующими различными болевыми синдромами, важным направлением которого может быть включение метода внутрикостных блокад в медико-экономические стандарты лечения пациентов. Высокая терапевтическая эффективность применения данной медицинской технологии как в условиях поликлиники, так и суточного или дневного неврологического стационара позволяет его рекомендовать в широкое применение в практической медицине, что позволило бы существенно повысить фармакоэкономический эффект лечения значительного количества пациентов с различными болевыми синдромами.
1. Алексеев В.В., Подчуфарова Е.В., Яхно Н.Н. Алгоритмы диагностики и лечения пациентов с болевыми синдромами в пояснично-крестцовой области. Журнал Боль № 2 (11). – 2006. С. 29–37.
2. Атясов Н.И. Новые возможности использования венозного русла костей в экстремальной медицине // Актуальные вопросы медицины катастроф. – 2000. – С. 76–78.
3. Варфоломеев А.К. Лечебное действие и влияние на некоторые физиологические показатели внутрикостного введения новокаина и других лекарственных веществ. – Материалы теорет. и клин. медицины, Томск, 1973. – вып. 4. – C. 78–80.
4. Вегетативные расстройства. Под ред. А.М. Вейна. – М.: ООО «Медицинское информационное агентство», 2003. – 624 с.
5. Вейн А.М., Авруцкий М.Я. Боль и обезболивание. – М.: Медицина, 1997. – 280 с.
6. Векслер И.М. Лечение облитерирующего эндартериита внутрикостной новокаиновой блокадой. – Изв. АН ЛатвССР, 1961. – № 7. – C.79–83.
7. Джавад-Заде М.Д. Внутрикостная тазовая анестезия при операциях на простате и мочевом пузыре // Урология. – 1959. – № 5. – C. 32–39.
8. Ибатурин И.А., Тараско А.Д. Патогенетические основы действия паравертебральной новокаиновой блокады / Казанский медицинский журнал. – 1995. – т.76, № 2. – с. 93–96.
9. Ибрагимов М.В. Малоинвазивное оперативное лечение радикулярного болевого синдрома методом селективного трансфораминального введения глюкокортикостероидов и местных анестетиков под нейровизуализационным контролем. Дисс…канд.мед.наук. – Москва, 2004.
10. Ивасенко И.Н. Использование остеогенных клеток-предшественников костного мозга для репаративного остеогенеза экспериментальных животных // Бюл. эксп. биол. и мед. – 1995, т. 119, № 1. – с. 72–75.
11. Коган О.Г., Петров Б.Г., Шмидт И.Р. Лечебные медикаментозные блокады при остеохондрозе позвоночника.- Новокузнецкий государственный институт усовершенствования врачей. – Кемерово. – Кн. изд-во. – 1988. – с. 107.
12. Корнилова Л.Е. Метод внутрикостных блокад в лечении клинических проявлений поясничного, шейного и грудного остеохондроза. Дисс….д.м.н., Москва, 2007. – 264 с.
13. Красноярова Н.А., Кальменева И.М., Клипицкая Н.К., Мусабаева Ф.А. Эффективность аутогемоновокаиновых блокад при нейрогенных и соматогенных болевых синдромах // Тезисы докладов Российской научно-практической конференции с международным участием: Клинические и теоретические аспекты боли (Москва, 15–16 мая 2001 г.). – с. 78–79.
14. Лобзин B.C. Пункции и блокады в неврологии. – СПб.: Гиппократ, 1999. – 128 с.
15. Пащук А.Ю. Регионарное обезболивание. – М.: Медицина, 1987. – 155 с.
16. Поляков В.А., Сахаров Б.В. Пролонгированные внутрикостные блокады в лечении повреждений и заболеваний позвоночника. – В кн.: Актуальные вопросы позвоночника. Новосибирск, 1976. – C. 62–64.
17. Попелянский Я.Ю. Ортопедическая неврология (вертеброневрология): Руководство для врачей. – М.: МЕДпресс-информ, 2003. – 672 с.
18. Рожкова А.А. Опыт применения внутрикостной позвонковой блокады при лечении трофических язв и длительно незаживающих ран // Ортопедия, травматология и протезирование. – 1959. – № 5. – C. 16–18.
19. Руководство по реабилитации больных с двигательными нарушениями: Том 1 / Под ред. А.Н. Беловой, О.Н. Щепетовой. – М., 1998. – 224 с.
20. Смирнов Д.А. Загрудинные новокаиновые блокады в лечении тяжелых форм бронхиальной астмы и астматического статуса // Анестезиология и реаниматология. – 1990. – № 2. – с. 49–50.
21. Соков Е.Л. Внутримышечные и внутрикостные блокады в комплексном лечении неврологических проявлений поясничного остеохондроза // Журнал невропатологии и психиатрии им. С.С. Корсакова. – 1988. – № 4. – С. 57–61.
22. Соков Е.Л. Внутрикостные блокады – патогенетическое лечение выраженных неврологических проявлений поясничного остеохондроза // Терапевтический архив. – № 3. – 1994. – с.84–88.
23. Соков Л.П., Соков Е.Л., Соков С.Л. Клиническая нейротравматология и нейроортопедия: Руководство. – М.: ИД «Камерон», 2004. – 528 с.
24. Соков Л.П., Соков Е.Л., Соков С.Л. Руководство по нейроортопедии. – М. Изд-во РУДН, 2002. – 541 с.
25. Стрелков Н.С. Инструмент для внутрикостных пункций // Мед. техника. – 1999. – № 4. – С. 35–37.
27. Шуляк Г.М., Акилова А.Т. Внутрикостный метод обезболивания и его и его клиническое обоснование. – Л., 1953.
28. Bogduk, N. Management of chronic low back pain / N. Bogduk // MJA. – 2004. – Vol. 180. – P. 79–83
29. Bonneti M., Fontona A., Cotticelli B. et al Intrafopaminal 0 (2) – 0 (3) versus periradicular steroidal infiltrations in lower back pain: Randomized controlled study // Am J. Neuroradiol. – 2005. – Vol. 26 – P. 996–1042.
30. Bot S.D., van der Waal J. M., Terwee C.B. et al Incidence and prevalence of complaints of the neck and upper extremity in general practice. // Ann Rheum Dis. – 2005. – Vol. 64 – P. 118–123.
32. Deen H.G., Fenton D.S., Lamer T.J. Minimally invasive procedure for disorders of the lumbar spine // Mayo Clin Proc. Oct 2003. – Vol. 78. – N 10. – P. 1249–1256.
33. Jeong H.S., Lee J. W., Kim S.H. et al Effectiveness of transforaminal epidural steroid injection by using a preganglionic approach: A prospective randomized controlled study // Radiology. – 2007. – Vol. 245 – P. 584–590
34. Malanga G., Wolff E. Evidence – informed management of chronic low back pain with trigger point injections // Spine J. – 2008. – Vol. 8 – P. 243–252.
35. Malaval L., Modrowski D., Gupta A.K. and Aubin J.E. Cellular expression of bone-related proteins during in vitro osteogenesis in rat bone marrow stromal cell cultures // J. Cell Physiol. – 1994, vol. 158. – № 3. – p. 555–572.
36. Malliani A., Lombardi F., Pagani M. Power spectral analysis of heart rate variability: atool explore neural regulatory mechanisms // Br. Heart J. – 1994. – Vol.71. – p. 1–2.
37. Marie P.J. Cellular and molecular alterations of osteoblasts in human disorders of bone formation // Histol. Histopathol. – 1999, vol. 2. – p. 525 – 538.
39. Matsudoura K., Seichi A., KunogiJ., et al The efficacy of prostaglandin E1 derivative in patients with lumbar spinal stenosis // Spine. – 2009. – Vol. 34 – P. 115–120.
40. Purcell-Jones G, Pither CE, Justin DM: Paravertebral somatic nerve bloc: a clinical, radiographic, and computed tomographic study in chronic pain patients // Anesth. Analg. – 1988. – p. 32–68.