Чем опасен высокий ттг при беременности на ранних сроках
Тиреотропный гормон (ТТГ) при беременности
Норма ТТГ при беременности
Гормон гипофиза, ответственный за работу щитовидной железы колеблется в пределах – 0,2 – 3,5 мЕд/л у беременных.
Уровень ТТГ гормона при беременности может колебаться:
— Первый триместр: 0,1-2,5 мЕд/л
— Второй триместр 0,2-3,0 мЕд/л
— Уровень ТТГ гормона при третьем триместре беременности составляет 0,3-3,0 мЕд/л.
Расшифровка показателей ТТГ гормона при беременности
Уровень гормона ТТГ на различных этапах беременности может быть как повышен, так и незначительно понижен. Однако серьёзные колебания его концентрации говорят о необходимости дополнительных исследованиях и возможных гормональных нарушениях.
ТТГ – гормон при беременности может снижаться у 20 или 30% женщин в случае одноплодной беременности и у 100% при многоплодии. У 10% на фоне подавленной выработки ТТГ повышается уровень тироксина.
Значительное повышение ТТГ гормона при беременности (на ранних сроках) может привести к необходимости лечения L- тироксином для создания условий для нормального течения беременности.
Особенно важен контроль уровня гормонов, в том числе и ТТГ гормона до 10 недели беременности. ТТГ при беременности на этом сроке особенно влияет на развитие эндокринной и прочих систем ребёнка, поскольку щитовидная железа плода в этот период ещё не работает.
Врачи продолжают повторять, что беременность – это стресс-тест для щитовидной железы, результатом которого является гипертиреоз у женщин с йодным дефицитом или ограниченным тироидным резервом. Оценка ТТГ гормона при беременности, а также после неё важна для женщин со скрыто протекающим аутоиммунным тиреоидитом Хашимото, который до беременности мог «маскироваться» под нормальное эутиреоидное состояние.
Определение ТТГ гормона при беременности значение:
• Контроль функции щитовидной железы и йодного дефицита у женщин в разные триместры беременности;
• Выявление скрытых нарушений, в том числе и аутоиммунного поражения щитовидной железы;
• Прогноз на дальнейшее течение беременности и полноценное развитие ребёнка;
• Раннее обнаружение необходимости скорректировать уровень гормонов или восполнить недостаток йода, либо прибегнуть к другим видам терапии, для сохранения здоровья матери и ребёнка.
Где сдать кровь на ТТГ при беременности?
В LAB4U сдать кровь на ТТГ при беременности можно в любой из многочисленных клиник-партнеров. При этом, в интернет-лаборатории LAB4U высокое качество анализа крови на ТТГ сочетается с доступной ценой.
Особенности лечения заболеваний щитовидной железы у беременных
При обследовании и лечении беременных с заболеваниями щитовидной железы врачу необходимо учитывать физиологические изменения тиреоидной функции.
При обследовании и лечении беременных с заболеваниями щитовидной железы врачу необходимо учитывать физиологические изменения тиреоидной функции. Можно выделить шесть основных физиологических механизмов или факторов, которые во время беременности влияют на концентрацию тиреоидных гормонов в крови, иногда имитируя то или иное заболевание щитовидной железы.
Прежде всего, с первых недель беременности под воздействием эстрогенов увеличивается концентрация тиреоид-связывающего глобулина. Это влечет за собой увеличение общего пула тиреоидных гормонов, что не позволяет ориентироваться на их уровень как на диагностический параметр при обследовании беременных женщин.
Свободные фракции тиреоидных гормонов в норме претерпевают незначительные изменения во время беременности, оставаясь в пределах нормальных величин. В первом триместре в период пика концентрации хорионического гонадотропина отмечается повышение их уровня с постепенным снижением во втором и третьем триместрах в результате увеличения объема циркулирующей плазмы.
Во время беременности увеличивается скорость фильтрации в почках, что приводит к ускоренной экскреции йода. В результате увеличивается степень йодного дефицита. Отсутствие йодной профилактики во время беременности ведет к развитию гипотироксинемии, неблагоприятной для развития плода.
Необходимо учитывать влияние вырабатываемых в плаценте гормонов. Хорионический гонадотропин, вследствие своей структурной схожести с тиреотропным гормоном, оказывает стимулирующее влияние на щитовидную железу. Результатом этого влияния является снижение, а в ряде случаев подавление уровня тиреотропного гормона на фоне пика концентрации хорионического гонадотропина в первом триместре беременности. У 10% беременных одновременно с подавленным уровнем тиреотропного гормона выявляется повышенное количество свободного тироксина. Эти изменения не носят патологического характера, но требуют дифференциации с диффузным токсическим зобом (ДТЗ) и другими заболеваниями, сопровождающимися тиреотоксикозом.
В плаценте активно протекают процессы дейодинации, в результате которых Т3 и Т4 преобразуются в метаболически неактивные rТ3 и Т2. Образующиеся в процессе дейодинации свободные атомы йода проникают через плаценту и используются щитовидной железой плода для синтеза собственных тиреоидных гормонов. Через плаценту проникает и непосредственно тироксин, необходимый для правильного развития плода. Для восполнения потерь тиреоидных гормонов вследствие трансплацентарного переноса и активных процессов дейодинации необходимо увеличение их эндогенного синтеза или экзогенного введения в случае гипотиреоза.
Во время беременности изменяется активность иммунной системы. Точные механизмы этого процесса не установлены, но хорошо известно, что с развитием беременности происходит снижение уровня антитиреоидных антител, иногда до их полного исчезновения. Это необходимо учитывать при обследовании беременных с заболеваниями щитовидной железы. Особенно важно об этом помнить при проведении дифференциальной диагностики ДТЗ и транзиторного гестационного тиреотоксикоза (ТГТ): двух состояний, сопровождающихся тиреотоксикозом, но требующих принципиально различной тактики.
Сохранение эутиреоза на протяжении всей беременности чрезвычайно важно для сохранения беременности и правильного развития плода. Изменения тиреоидной функции как в сторону тиреотоксикоза, так и гипотиреоза сопровождаются угрозой выкидыша и преждевременных родов, а также развитием других осложнений беременности. Развитие гипотироксинемии у беременной, особенно в первом триместре, ведет к нарушению правильного формирования центральной нервной системы и отдаленным психоневрологическим нарушениям у плода. Некомпенсированный тиреотоксикоз на протяжении всей беременности приводит к развитию различных пороков у плода. Все это диктует необходимость поддержания эутиреоидного состояния у женщины на протяжении всей беременности.
Особенности ведениябеременных с диффузнымнетоксическим зобом (ДНЗ)
Вступление в беременность женщины с ДНЗ принципиально изменяет тактику ведения больной. Если вне беременности это заболевание не требует частого контроля функции щитовидной железы и, зачастую, не требует и лечения, то во время беременности эти женщины относятся к группе риска развития гипотироксинемии, которая может неблагоприятно сказаться на здоровье плода.
Нами было детально обследовано 34 беременных с ДНЗ. Среди беременных с ДНЗ, как и в группе беременных без заболеваний щитовидной железы, не было выявлено гипотироксинемии в первом триместре, даже относительной. Вероятно, в регионе легкого йододефицита, к которому относится Московская область, количество поступающего в организм беременной йода все-таки достаточно, чтобы предотвратить гипотироксинемию на ранних сроках беременности.
Во втором и третьем триместрах, когда потребность беременной в йоде существенно возрастает, частота относительной гипотироксинемии у беременных с зобом зависела от наличия и сроков начала йод-профилактики. Среди беременных, начавших прием препаратов йода только со второго триместра, отмечалась тенденция к повышению частоты относительной гипотироксинемии во втором и третьем триместрах (рис.). Среди беременных, не получавших препараты йода, к концу беременности частота гипотироксинемии была достоверно выше, чем среди получавших йод-профилактику в течение всей беременности, и встречалась в 87,5% случаев (по сравнению с 25%, р=0,04, рис.).
В нашем исследовании мы применяли 150 и 200 мкг йода. Развитие гипотироксинемии даже на фоне йодной профилактики у беременных с ДНЗ показало, что, вероятно, эта доза йода недостаточна или требуется комбинированное лечение препаратами йода и левотироксина. В 2007 г. ВОЗ рекомендовала увеличить дозу йода для беременных и женщин в период лактации до 250 мкг в сутки.
Результаты нашего исследования показали, что принципиально важна не только доза йода, но и сроки начала йодной профилактики, которая должна быть начата не позднее первого триместра беременности, а в идеальной ситуации на стадии планирования беременности.
Так как беременные с ДНЗ относятся к группе риска развития гипотироксинемии, то необходимо контролировать функцию щитовидной железы каждые 2 месяца в течение первых II триместров. Патологическое значение гипотироксинемии снижается в третьем триместре, поэтому важность контроля функции щитовидной железы в этот период уменьшается.
В случае выявления гипотироксинемии, даже относительной (т.е. снижения уровня тироксина ниже 10 перцентиля) в первом триместре показано проведение комбинированного лечения препаратами йода (Йодомарин, Йодид) и левотироксина (L-Тироксин, Эутирокс) по правилам лечения гипотиреоза. Во втором триместре опасность повреждения центральной нервной системы плода меньше, поэтому назначение левотироксина показано при развитии только явной гипотироксинемии. После родов препараты левотироксина необходимо отменить с последующим контролем функции щитовидной железы через 4–8 недель для исключения персистирующего гипотиреоза. Препараты йода женщина должна продолжать принимать весь период лактации с целью обеспечения новорожденного йодом. В дальнейшем тактика ведения определяется по общим правилам.
Особенности лечения гипотиреоза во время беременности
Гипотиреоз встречается у 2–4% беременных, при этом у части женщин заболевание не диагностировано. Так как состояние эутиреоза принципиально важно для правильного формирования плода и сохранения беременности, эндокринологическими сообществами различных стран активно обсуждается вопрос о целесообразности скрининга беременных на гипотиреоз.
Ориентироваться на клиническую картину для выделения группы риска наличия гипотиреоза чрезвычайно сложно, поскольку жалобы при гипотиреозе неспецифичны и многие из них, например слабость, сонливость, могут являться проявлениями самой беременности. Кроме этого доказано неблагоприятное влияние на течение беременности не только манифестного, но и субклинического гипотиреоза, при котором жалобы вообще отсутствуют. В связи с вышеперечисленным необходимо исследование тиреоидной функции хотя бы в группах риска, к которым относятся: 1)женщины, принимавшие левотироксин в анамнезе по любой причине; 2)женщины с аутоиммунными заболеваниями или семейным анамнезом аутоиммунных заболеваний; 3)женщины с зобом; 4)женщины, перенесшие операции на щитовидной железе или облучение шеи.
В случае выявления гипотиреоза, манифестного или субклинического, показано назначение сразу полной заместительной дозы левотироксина (L-Тироксин, Эутирокс, а не постепенное повышение дозы, как это часто принято в обычной практике. Это позволяет быстро нормализовать уровень тироксина, который, проникая через плаценту, обеспечивает нормальное развитие плода. Так как этот показатель важен для нормального развития беременности и правильного формирования плода, то и контроль компенсации гипотиреоза у беременных осуществляется не по уровню ТТГ, а по уровню свободного Т4. Уровень ТТГ является дополнительным к уровню свободного Т4 параметром, подтверждающим компенсацию гипотиреоза. Это объясняется тем, что ТТГ медленно реагирующий показатель, и для его нормализации после назначения лечения требуется 2–3 месяца в зависимости от исходных значений. Решение же о необходимости коррекции дозы левотироксина необходимо принимать гораздо быстрее, ориентируясь на уровень свободного Т4. Целевыми значениями при лечении гипотиреоза являются для ТТГ— 0,5–2,5 мЕд/л, а для свободного Т4— верхняя граница нормы.
Нами было проведено детальное обследование 13 беременных с впервые выявленным гипотиреозом. Из табл. 1 видно, что в группе беременных с гипотиреозом, выявленным в первом триместре беременности, ТТГ достиг целевых значений только в третьем триместре, что подтверждает его второстепенную роль при контроле компенсации гипотиреоза у беременных.
Контроль свободного Т4 необходимо проводить через 2 недели и повторно вместе с ТТГ через 4 недели после начала лечения. При нормальных показателях контроль в дальнейшем необходимо проводить каждые 2 месяца в течение первых двух триместров. В третьем триместре обычно достаточно однократного контроля уровня гормонов, так как в этот период уже не происходит резких изменений в уровне гормонов и патологическое значение гипотироксинемии не доказано. После родов женщинам, которым диагноз гипотиреоза был установлен во время беременности, требуется отмена лечения для того, чтобы выяснить характер нарушения функции щитовидной железы. В случае субклинического гипотиреоза вопрос о дальнейшем лечении решается индивидуально.
Часть женщин на момент наступления беременности уже получает лечение по поводу гипотиреоза. В связи с физиологическими изменениями, происходящими в организме беременной, увеличивается потребность в экзогенном левотироксине. Нами было обследовано 43 беременных с гипотиреозом, диагностированным до беременности. Декомпенсация заболевания была выявлена у 50% женщин с послеоперационным гипотиреозом и почти у 40% женщин с гипотиреозом, развившимся в результате аутоиммунного тиреоидита. В нашем исследовании декомпенсация гипотиреоза у всех беременных, за исключением одной, произошла в первом триместре беременности, однако по данным литературы декомпенсация может развиться и во втором и даже третьем триместрах беременности. Это диктует необходимость частого контроля гормонального анализа крови у беременных с гипотиреозом. Раннее развитие декомпенсации начиная с первых недель беременности требует, во-первых, планирования беременности у женщин с известным диагнозом гипотиреоза, а во-вторых, контроля гормонального анализа сразу после наступления беременности.
Так как потребность в тиреоидных гормонах увеличивается во время беременности, то требуется увеличение дозы левотироксина. В нашем исследовании было показано, что независимо от этиологии гипотиреоза увеличение дозы левотироксина на 50% предупреждало развитие гипотироксинемии у беременных на протяжении всей беременности. В случае меньшего увеличения дозы во втором и третьем триместрах возникала необходимость в дополнительной коррекции заместительной терапии.
Контроль тиреоидного статуса необходимо осуществлять 1 раз в 4 недели на протяжении первого триместра, когда особенно опасно развитие гипотироксинемии, далее 1 раз в 8 недель.
После родов в течение 4–6 недель потребность в левотироксине обычно возвращается к исходной. Но окончательное решение о дозе препарата необходимо принимать после получения результатов гормонального анализа.
Необходимо также отметить, что в регионе с дефицитом йода беременным с гипотиреозом показано проведение йодной профилактики с целью адекватного обеспечения этим микроэлементом плода. При сравнении тиреоидного статуса беременных с гипотиреозом, развившимся вследствие аутоиммунного тиреоидита, было показано, что компенсация гипотиреоза не зависела от приема препаратов йода, а применение препаратов йода сопровождалось некоторым увеличением массы тела и роста детей при рождении (3234,0±477,1 г, 50,4±2,4 см с йодопрофилактикой и 2931,1±590,2 г, 48,9±3,0 см без йодопрофилактики). В исследовании была показана прямая зависимость показателей интеллектуального развития от массы тела новорожденных, которая находилась в пределах нормальных значений. Таким образом, можно предположить благоприятное влияние йодной профилактики у беременных с гипотиреозом на развитие плода.
Особенности лечения беременных с тиреотоксикозом
Тиреотоксикоз встречается в 1–2 случаях на 1000 беременных. Хотя распространенность этого заболевания невелика, но лечение тиреотоксикоза у беременной является трудной и ответственной задачей для эндокринолога, ввиду потенциальных осложнений для беременной и плода как некомпенсированного тиреотоксикоза, так и назначаемого лечения.
В первом триместре беременности ДТЗ необходимо дифференцировать с ТГТ, так как лечебная тактика при этих состояниях различна.
ТГТ— доброкачественное состояние, не представляющее угрозы для беременной и плода, которое развивается вследствие стимулирующего влияния хорионического гонадотропина. Это состояние не требует лечения, разрешается обычно самостоятельно, но требует наблюдения и дифференциальной диагностики с ДТЗ.
Нами было проведено сравнение клинической картины у 8 беременных с впервые диагностированным тиреотоксикозом, причиной которого являлся ДТЗ, и 10 беременных с ТГТ. Из клинических проявлений достоверно чаще при диффузном токсическом зобе встречались дрожь в руках (62,5% при ДТЗ и 10% при ТГТ, р
А. В. Древаль, доктор медицинских наук, профессор Т. П. Шестакова, кандидат медицинских наук О. А. Нечаева, кандидат медицинских наук МОНИКИ им. М. Ф. Владимирского, Москва
Диагноз: гестационный гипотиреоз
Поделиться:
Кажется, лет 10 тому назад академик, доктор медицинских наук, врач-эндокринолог Галина Афанасьевна Мельниченко, известная в том числе своей просветительской интернет-деятельностью, восхищенно воскликнула: «Наконец-то гинекологи оторвали головы от промежности и обнаружили еще одну железу внутренней секреции!».
Да, это так. Большинство российских гинекологов таки вспомнило о существовании щитовидной железы, освоило современные подходы к этой проблеме и выучило нормы для беременных и готовящихся.
О связи щитовидной железы и беременности знали еще древние египтяне. В день заключения брачного союза они завязывали специальную нить вокруг шеи женщины. Когда нить разрывалась из-за увеличения размеров щитовидной железы, врачи Древнего Египта подтверждали диагноз «беременность».
Сегодня мы не хуже древних египтян знаем, что во время беременности щитовидная железа матери обязана вырабатывать тироксин «за себя и за того парня», потому что свой собственный тироксин плод начинает вырабатывать только к 16–18-й недели беременности. Дефицит этого важнейшего гормона оказывает негативное влияние как на течение беременности, так и на здоровье плода.
Гипотиреоз — заболевание, связанное со снижением выработки гормонов щитовидной железой.
Признаки гипотиреоза столь многочисленны и неспецифичны, что пропустить это заболевание легче легкого. Кого во время беременности удивит утомляемость, сонливость и/или слабость, непереносимость холода, прибавка веса, ухудшение настроения, ослабление памяти, запоры, тонкие и ломкие волосы и ногти?
Если диагноз не поставили и/или не назначили правильное лечение, такая беременность может закончиться необъяснимым выкидышем, преэклампсией, отслойкой плаценты или послеродовым кровотечением. Часто роды происходят преждевременно, дети рождаются маловесными, с незрелой легочной тканью. У таких детишек достоверно чаще встречается аутизм, синдром дефицита внимания и гиперактивности, нарушение нейроинтеллектуального развития.
Самое неприятное в этой истории то, что гипотиреоз может протекать совершенно бессимптомно, обнаруживаться совершенно случайно, но риски и угрозы бессимптомный (или субклинический) гипотиреоз создает такие же, как махровый гипотиреозище.
Именно поэтому так важно проводить тиреоидный скрининг во время беременности.
Тиреоидный скрининг: кому проводить?
Абсолютно всем беременным, заинтересованным в сохранении беременности.
За рубежом этот вопрос активно обсуждается, эксперты приходят к выводу о нецелесообразности проведения тотального скрининга, однако важно понимать, что в нашей стране до сих пор не решена проблема дефицита йода: 95 % территории России — йоддефицитные регионы. Необходимость тиреоидного скрининга у женщин с осложненным анамнезом и на йоддефицитных территориях не подлежит ни малейшему сомнению.
Как проводят скрининг?
Необходимо сдать кровь на ТТГ и Т4 свободный утром, натощак, желательно исключив стрессовое воздействие.
Кто проводит скрининг?
Назначить обследование должен врач акушер-гинеколог. К сожалению, особенности программ ОМС позволяют лишь выборочно оплачивать это исследование, поэтому в ряде регионов обследование проводится за счет собственных средств пациенток.
Читайте также:
Полное обследование
Когда проводят скрининг?
Сегодня эндокринологи говорят о том, что это анализ «первой пробирки». В идеале женщина может проводить данное обследование вместе с определением уровня ХГЧ, задолго до изучения других маркеров. Не надо приравнивать скрининг 1-го триместра на хромосомные аномалии в сроке 11–13 недель к тиреоидному скринингу. Тиреоидный скрининг — это скрининг надежды. Тут легко поставить диагноз, легко устранить дефицит гормонов и легко предупредить негативные изменения.
Зачем проводят скрининг?
Ожидалось, исследование покажет, что тиреоидный скрининг с коррекцией дефицита йода и гипотериоза во время беременности позволит получить умненьких детей. Скрининг проводили в 12 недель беременности, лечение начинали в среднем в сроке 13–14 недель. Когда детям исполнилось 3 года, психологи провели замеры IQ, сравнивая результаты с контрольной группой. Увы — никакого улучшения когнитивных функций специалисты не обнаружили.
Эндокринологов это огорчило, но акушеры-гинекологи были весьма довольны — все беременности неплохо проходили, серьезных осложнений гестации не было, детки родились в срок и с хорошим весом. Оптимисты считают, что тиреоидный скрининг проводился слишком поздно, а при таком отсроченном начале терапии «защитить интеллект» уже не получится — вмешиваться надо раньше. Новое исследование затеяно, нам остается набраться терпения и ждать обнадеживающих результатов.
Кто ставит диагноз «гипотиреоз» во время беременности?
Тот, кто нашел. Если на обследование направил акушер-гинеколог, то он и поставит диагноз. Необходимо помнить, что нормальные значения ТТГ, указанные на бланке, сильно отличаются от целевых значений во время беременности.
В 1-м триместре уровень ТТГ должен быть менее 2,5 мЕд/л. Если получилось выше, акушер-гинеколог ставит диагноз «Первичный гипотиреоз, впервые выявленный в 1-м триместре», рекомендует немедленно бежать в аптеку за йодомарином и, как можно скорее, к эндокринологу.
Кто лечит гипотиреоз?
Уточнять диагноз и проводить лечение будет врач-эндокринолог. Если попасть к специалисту быстро не получается, не будет большой беды, если лечение L-тироксином начнет акушер-гинеколог, а эндокринолог скорректирует дозировку и будет контролировать процесс.
Если небольшое повышение ТТГ на ранних сроках беременности оказалось незамеченным, не стоит огорчаться. Вероятность развития серьезных последствий для интеллектуального и физического развития развития невысока. Уровень интеллекта ребенка зависит от многих факторов. И даже при идеальной работе щитовидной железы у матери во время беременности далеко не все дети становятся медалистами в школе и в будущем — нобелевскими лауреатами.
Товары по теме: [product strict=»йодомарин»](йодомарин), [product strict=»калия йодид»](калия йодид)
Патология щитовидной железы и беременность
Опубликовано в журнале:
«Врач», 2008, №5, с. 11-16
B. Фадеев, доктор медицинских наук, профессор,
C. Перминова, кандидат медицинских наук,
Т. Назаренко, доктор медицинских наук,
М. Ибрагимова, С. Топалян,
ММА им. И. М. Сеченова, Научный центр акушерства, гинекологии и перинатологии
им. В. И. Кулакова, Москва
Заболевания щитовидной железы (ЩЖ) являются самой частой эндокринной патологией, при этом среди женщин они распространены практически в 10 раз больше и манифестируют в молодом, репродуктивном возрасте.
Важнейшей функцией тиреоидных гормонов является обеспечение развития различных органов и систем на протяжении всего эмбриогенеза, начиная с первых недель беременности. В связи с этим любые изменения функции ЩЖ, даже незначительные, несут повышенный риск нарушений развития нервной и других систем плода. Данные о распространенности тиреоидной патологии в случайной репрезентативной выборке женщин при разных сроках беременности, обратившихся для постановки на учет в женскую консультацию Москвы, представлены в табл. 1, из которой видно, что наиболее часто встречаются различные формы эутиреоидного зоба и носительство антител к тиреоидной пероксидазе (АТ-ТПО). Несколько иной спектр патологии характерен для беременных, обращающихся в специализированные эндокринологические и акушерско-гинекологические учреждения – среди них значительно больше пациенток с гипотиреозом и тиреотоксикозом.
Таблица 1. Распространенность тиреоидной патологии в случайной выборке женщин при разных сроках беременности [5]
| Патология | Количество обследованных | |
| абс. | % | |
| Число обследованных | 215 | 100 |
| Гипотиреоз: | ||
| всего | 4 | 1,86 |
| явный | 2 | 0,93 |
| субклинический | 2 | 0,93 |
| АТ-ТПО: | ||
| >35 мЕд/л | 34 | 15,8 |
| >150 мЕд/л | 21 | 9,8 |
| Тиреотоксикоз | 0 | 0 |
| Диффузный зоб* | 51 | 24,2 |
| Узловой зоб* | 8 | 3,8 |
| Примечание. * Исключая 4 женщин с гипотиреозом. | ||
Современные представления о влиянии патологии ЩЖ на репродуктивное здоровье и о принципах ее диагностики и лечения включают следующие положения:
У женщин заболевания щитовидной железы встречаются в 10 раз чаще, чем у мужчин, и манифестируют в молодом, репродуктивном возрасте
ФУНКЦИОНИРОВАНИЕ ЩЖ ВО ВРЕМЯ БЕРЕМЕННОСТИ
Изменение функционирования ЩЖ у женщины происходит уже с первых недель беременности под воздействием разных факторов, большинство из которых прямо или косвенно стимулируют ЩЖ женщины. Преимущественно это происходит в 1-й половине беременности, т.е. в период, когда у плода еще не функционирует своя ЩЖ, а весь эмбриогенез обеспечивается тиреоидными гормонами матери. В целом продукция тиреоидных гормонов во время беременности в норме увеличивается на 30–50% [8].
К физиологическим изменениям функционирования ЩЖ во время беременности относятся:
1) гиперстимуляция ЩЖ хорионическим гонадотропином (ХГ):
2) увеличение продукции тироксинсвязывающего глобу лина (ТСГ) в печени:
3) усиление экскреции йода с мочой и трансплацентарного переноса йода;
4) дейодирование тиреоидных гормонов в плаценте.
Наиболее мощным стимулятором ЩЖ во время беременности, преимущественно в 1-й ее половине, выступает ХГ, продуцируемый плацентой. По структуре он является гормоном, родственным ТТГ (одинаковые α-субъединицы, разные β-субъединицы), и в больших количествах способен оказывать ТТГ-подобные эффекты, приводя к стимуляции продукции тиреоидных гормонов. В I триместре беременности за счет эффектов ХГ происходит существенное увеличение продукции тиреоидных гормонов, что, в свою очередь, обусловливает подавление продукции ТТГ. При многоплодной беременности, когда содержание ХГ достигает очень высоких значений, уровень ТТГ в 1-й половине беременности у значительной части женщин может быть существенно понижен, а порой полностью подавлен.
Во время беременности происходит увеличение продукции эстрогенов, которые оказывают стимулирующее влияние на продукцию ТСГ в печени. Кроме того, при беременности увеличивается связывание ТСГ с сиаловыми кислотами, что приводит к существенному снижению его клиренса. В результате к 18–20-й неделе беременности уровень ТСГ удваивается. Это, в свою очередь, приводит к связыванию с ТСГ дополнительного количества свободных тиреоидных гормонов. Транзиторное снижение уровня последних вызывает дополнительную стимуляцию ЩЖ со стороны ТТГ, в результате чего свободные фракции Т4 и Т3 сохраняются на нормальном уровне, тогда как уровень общих Т4 и Т3 у всех беременных женщин в норме повышен.
Функционирование щитовидной железы изменяется под воздействием разных факторов уже с первых недель беременности
Уже в начале беременности происходит постепенное увеличение объема почечного кровотока и гломерулярной фильтрации, что приводит к росту экскреции йода с мочой и обусловливает дополнительную косвенную стимуляцию ЩЖ женщины. Кроме того, повышение потребности в йоде развивается в связи с трансплацентарным его переносом, что необходимо для синтеза тиреоидных гормонов ЩЖ плода.
Бурное развитие в последние годы вспомогательных репродуктивных технологий (ВРТ) привело к повышению частоты наступления индуцированной беременности (ИБ), а проблема ее сохранения и рождения здоровых детей приобрела особую актуальность. ИБ – беременность, наступившая в результате применения индукторов овуляции: препаратов для стимуляции функции яичников, широко используемых для восстановления фертильности при ановуляторной форме бесплодия и в программах экстракорпорального оплодотворения (ЭКО) и переноса эмбриона (ПЭ) в матку.
Стимуляция овуляции сопровождается одновременным ростом нескольких, а иногда многих фолликулов (в отличие от спонтанного цикла) и, соответственно, образованием множества желтых тел. Эти гормонально-активные структуры секретируют стероидные гормоны, концентрация которых в десятки раз превышает физиологические. Повышенная секреция половых стероидов сохраняется длительное время после отмены индуктора овуляции, что в ряде случаев приводит к существенному изменению гомеостаза в организме женщины и развитию синдрома гиперстимуляции яичников. В случае наступления беременности повышенные концентрации стероидных гормонов могут сохраняться вплоть до окончательного формирования плаценты с последующим постепенным регрессом.
Известно, что стимулированные беременности относятся к группе риска по развитию осложнений: высокой частоты ранних репродуктивных потерь, многоплодия, раннего гестоза, тяжелого синдрома гиперстимуляции яичников, фетоплацентарной недостаточности, угрозы преждевременных родов [1]. В связи с этим ведение стимулированного цикла и I триместра ИБ требует тщательного динамического наблюдения и гормонального контроля. Высокая стероидная нагрузка вследствие гиперстимуляции яичников, а также прием большого числа гормональных препаратов влияют на метаболизм тиреоидных гормонов, приводят к гиперстимуляции ЩЖ, что, в свою очередь, может усугубить неблагоприятное течение беременности и негативно отразиться на развитии плода.
ЭМБРИОЛОГИЯ И ФИЗИОЛОГИЯ ЩЖ ПЛОДА
Закладка ЩЖ происходит на 3–4-й неделе эмбрионального развития. Примерно в это же время из нервной пластинки происходит закладка центральной нервной системы (ЦНС) – начинаются процессы дендритного и аксонального роста, а также синаптогенез, нейрональная миграция и миелинизация, которые не могут адекватно развиваться без достаточного количества тиреоидных гормонов. ЩЖ плода приобретает способность захватывать йод только с 10–12-й недели беременности, а синтезировать и секретировать тиреоидные гормоны – только с 15-й недели. Таким образом, практически всю 1-ю половину беременности ЩЖ у плода еще не функционирует, а его развитие в полной мере зависит от тиреоидных гормонов беременной.
ДИАГНОСТИКА ЗАБОЛЕВАНИЙ ЩЖ ВО ВРЕМЯ БЕРЕМЕННОСТИ
Как указывалось, принципы диагностики заболеваний ЩЖ во время беременности отличаются от общепринятых:
БЕРЕМЕННОСТЬ И ЙОДОДЕФИЦИТНЫЕ ЗАБОЛЕВАНИЯ
Йододефицитными заболеваниями (ЙДЗ), по определению ВОЗ, обозначаются все патологические состояния, развивающиеся в популяции вследствие йодного дефицита, которые могут быть предотвращены при нормализации потребления йода. Спектр ЙДЗ весьма широк, при этом наиболее тяжелые из них напрямую связаны с нарушениями репродуктивной функции или развиваются перинатально (врожденные аномалии, эндемический кретинизм, неонатальный зоб, гипотиреоз, снижение фертильности).
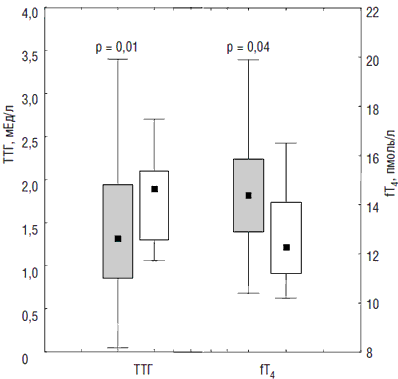
Перечисленные выше механизмы стимуляции ЩЖ беременной носят физиологический характер, обеспечивая адаптацию эндокринной системы женщины к беременности, и при наличии адекватных количеств основного субстрата синтеза тиреоидных гормонов – йода – не будут иметь каких-либо неблагоприятных последствий. Пониженное поступление йода во время беременности приводит к хронической стимуляции ЩЖ, относительной гипотироксинемии и формированию зоба как у матери, так и у плода. В ряде исследований показано, что даже в условиях легкого йодного дефицита уровень fТ4 в I триместре беременности оказывается на 10–15% ниже такового у женщин, получающих йодную профилактику [6]. По данным нашего исследования, при сравнении уровня ТТГ и fT4 в группах женщин без тиреоидной патологии, получавших и не получавших йодную профилактику, выяснилось, что к концу беременности уровень ТТГ был статистически значимо ниже, а fT4 – выше у женщин, получавших 150–200 мкг йодида калия [2] (рис. 1).
Рис. 1. Уровни ТТГ и fT в III триместре беременности у женщин, 4 получавших (темным) и не получавших (светлым) индивидуальную йодную профилактику (Me [25%, 75%], min, max) [2]
Важно отметить, что термин «относительная гестационная гипотироксинемия» сегодня имеет лишь теоретическое обоснование, поскольку конкретные диагностические критерии для него отсутствуют. Другими словами, пока это не диагноз, который может быть поставлен при гормональном обследовании беременной; под этим термином подразумевают феномен, при котором по разным причинам уровень Т4 у беременной женщины не достигает должного для этого физиологического состояния, но сохраняется в пределах нормы для здоровых вне беременности. Как уже указывалось, продукция Т4 в 1-й половине беременности для адекватного развития плода должна увеличиться на 30–50%. В ситуации, когда женщина проживает в условиях йодного дефицита, ее ЩЖ еще до беременности функционирует, в той или иной степени затрачивая свои резервные возможности, и даже использования мощных компенсаторных механизмов в ряде случаев может не хватить для обеспечения столь значительного увеличения продукции тиреоидных гормонов. В результате гиперстимуляция ЩЖ не способствует к должному результату, а приобретает патологическое значение, приводя к формированию у беременной зоба. Именно с этим феноменом и связывается патогенез нарушений психомоторного развития плода в условиях йодного дефицита.
Как уже указывалось, физиологическая гиперстимуляция ЩЖ беременной в условиях йодного дефицита оказывается мощным зобогенным фактором. Как показало проведенное нами исследование случайной выборки беременных, обращающихся для постановки на учет в женскую консультацию, у 24% из них был увеличен объем ЩЖ (см. табл. 1) [5].
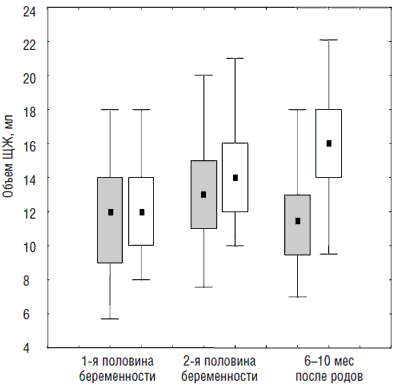
Восполнение дефицита йода с ранних сроков беременности ведет к коррекции указанных изменений. Так, в нашем исследовании, изучавшем динамику объема ЩЖ во время беременности, у женщин, получавших и не получавших йодную профилактику (рис. 2), выяснилось, что в обеих группах ко 2-й половине беременности произошло закономерное и статистически значимое увеличение объема ЩЖ, в большей степени выраженное в группе женщин, не получавших йодную профилактику. После родов в случае отсутствия йодной профилактики происходило дальнейшее увеличение объема ЩЖ, что, видимо, связано с сохранением высокой потребности в йоде в период грудного вскармливания. У женщин, получавших дополнительно 150–200 мкг йода ежедневно, на протяжении 6–10 мес после родов происходило уменьшение объема ЩЖ [2].
Рис. 2. Динамика объема ЩЖ в период беременности и после родов у женщин без патологии ЩЖ, получавших (темным) и не получавших (светлым) индивидуальную йодную профилактику (Me [25%, 75%], min, max) [2]
Для восполнения дефицита йода используются различные варианты йодной профилактики. Наиболее эффективным методом, рекомендуемым ВОЗ и другими международными организациями, является массовая (популяционная) йодная профилактика, которая заключается в йодировании пищевой соли. Поскольку беременность является периодом наибольшего риска формирования самых тяжелых ЙДЗ, уже на этапе планирования беременности женщинам целесообразно назначение индивидуальной йодной профилактики физиологическими дозами йода (200 мкг/сут. – например, одна таблетка препарата «ЙодБаланс-200» ежедневно).
ГИПОТИРЕОЗ И БЕРЕМЕННОСТЬ
Таблица 2. Осложнения некомпенсированного гипотиреоза при беременности (в %) [4]
| Осложнение | Манифестный гипотиреоз | Субклинический гипотиреоз |
| Гипертензия, преэклампсия | 22 | 15 |
| Отслойка плаценты | 5 | 0 |
| Низкая масса тела плода | 16,6 | 8,7 |
| Внутриутробная гибель | 6,6 | 1,7 |
| Пороки развития | 3,3 | 0 |
| Послеродовое кровотечение | 6,6 | 3,5 |
Заместительная терапия гипотиреоза во время беременности требует выполнения ряда условий:
БЕРЕМЕННОСТЬ И АУТОИММУННЫЙ ТИРЕОИДИТ
Аутоиммунный тиреоидит (АИТ) является основной причиной спонтанного гипотиреоза. Если диагностика последнего не вызывает особых сложностей (определение уровня ТТГ), то при отсутствии снижения функции ЩЖ диагноз АИТ зачастую носит лишь вероятностный характер. Тем не менее при АИТ, когда ЩЖ поражена аутоиммунным процессом, ее дополнительная физиологическая стимуляция, происходящая во время беременности, может не достичь своей цели; в этой ситуации, как и при йодном дефиците, у женщины не произойдет повышения продукции тиреоидных гормонов, необходимого для адекватного развития плода в 1-й половине беременности. Таким образом, АИТ во время беременности несет риск манифестации гипотиреоза у женщины и относительной гипотироксинемии у плода.
Основную сложность создает выделение среди женщин с отдельными признаками АИТ группы с максимальным риском развития гипотироксинемии. Так, распространенность носительства АТ-ТПО с уровнем выше 100 мЕд/л, как указывалось, достигает среди беременных 10%, а зоба – порой 20% (см. табл. 1). В связи с этим очевидно, что не всякое повышение уровня АТ-ТПО свидетельствует об АИТ и о существенном риске развития гипотироксинемии. При выявлении повышенного уровня АТ-ТПО без других признаков АИТ необходима динамическая оценка функции ЩЖ во время беременности (в каждом триместре).
Предложено проводить скрининг нарушений функций щитовидной железы у всех женщин на ранних сроках беременности
Как указывалось выше, в ранние сроки беременности в норме характерен низкий или даже подавленный (у 20–30% женщин) уровень ТТГ (2,5 мЕд/л на ранних сроках беременности у женщин – носительниц АТ-ТПО может косвенно свидетельствовать о снижении функциональных резервов ЩЖ и повышенном риске развития относительной гипотироксинемии [3, 7].
Возникает вопрос: каким образом выявить женщин – носительниц АТ-ТПО, а среди них – группу с повышенным риском развития гипотироксинемии, поскольку носительство АТ-ТПО не сопровождается какими-либо симптомами? Специфические клинические симптомы чаще отсутствуют и при гипотиреозе (даже манифестном, не говоря уже о субклиническом). Принимая во внимание высокую распространенность носительства АТ-ТПО и гипотиреоза в популяции, а также в силу ряда других причин, перечисленных ниже, ряд авторов и крупные эндокринологические ассоциации предложили проводить скрининг нарушений функции ЩЖ у всех женщин на ранних сроках беременности.
Аргументами в пользу проведения скрининга на нарушение функции ЩЖ и носительство АТ-ТПО у беременных являются следующие положения:
Предлагаемый скрининг базируется на определении в указанные сроки уровня ТТГ и АТ-ТПО (см. схему). В случае ИБ скрининг на нарушения функции ЩЖ целесообразно проводить в самые ранние сроки (лучше – еще во время определения β-субъединицы ХГ для констатации беременности). Если уровень ТТГ превышает 2,5 мМЕ/л, женщине показана терапия L-T4 (эутирокс).
Диагностика гипотиреоза во время беременности
| ТТГ на ранних сроках беременности (особенно при носительстве АТ-ТПО) | |
| ↓ | ↓ |
| ТТГ 2,5 мЕд/л | |
| ↓ | ↓ |
| 1. Динамическое наблюдение 2. Скрининг на тиреоидит послеродовый | L–Т4 |
АНТИТИРЕОИДНЫЕ АНТИТЕЛА И РИСК САМОПРОИЗВОЛЬНОГО ПРЕРЫВАНИЯ БЕРЕМЕННОСТИ
Многие работы показывают, что у женщин с повышенным уровнем АТ-ТПО даже без нарушений функции ЩЖ повышен риск спонтанного прерывания беременности на ранних сроках [10], патогенез которого пока не выяснен. Вряд ли есть прямая причинно-следственная связь между ним и носительством АТ-ТПО. Возможно, антитиреоидные антитела являются маркером генерализованной аутоиммунной дисфункции, в результате которой и происходит выкидыш. Таким образом, какое-либо воздействие на собственно аутоиммунный процесс в ЩЖ не приводит к снижению риска прерывания беременности и поэтому оно не требуется. Кроме того, несмотря на отсутствие каких-либо мер патогенетического воздействия на аутоиммунные процессы в ЩЖ, следует помнить о том, что носительницы АТ-ТПО входят в группу риска самопроизвольного прерывания беременности, а потому требуют специального наблюдения со стороны акушеров-гинекологов. Особенно большое значение приобретает нормальная функция ЩЖ в программах ВРТ. Результаты недавних исследований, посвященных этой проблеме, показали, что уровень ТТГ значительно выше у женщин с низким качеством ооцитов и при неудачных попытках применения программ ВРТ. Кроме того, отмечена высокая частота носительства АТ-ЩЖ у женщин с неудачными попытками ЭКО [9, 11, 13]. Все это позволяет предположить, что уровень ТТГ является одним из показателей прогноза эффективности программ ВРТ и свидетельствует о важной роли тиреоидных гормонов в физиологии ооцитов. Результаты изучения функции ЩЖ на ранних сроках ИБ после ЭКО продемонстрировали выраженное повышение концентрации ТТГ и снижение концентрации fТ4 у женщин с АТ-ТПО (по сравнению с аналогичным показателем у женщин без антител), что свидетельствует о снижении компенсаторных возможностей ЩЖ на фоне ИБ у женщин с АТ-ЩЖ [12].
Как известно, стимуляция суперовуляции, проводимая в программах ЭКО с целью получения максимального количества ооцитов, сопровождается высокими уровнями эстрогенов в крови. Гиперэстрогения за счет ряда приспособительных механизмов (повышение уровня ТСГ в печени, связывание дополнительного количества свободных тиреоидных гормонов и, как следствие, снижение уровня последних) приводит к повышению уровня ТТГ. Это способствует повышенной стимуляции ЩЖ, которая вынуждена задействовать свои резервные возможности. Поэтому у женщин с АТ-ЩЖ даже при исходно нормальной функции ЩЖ повышается риск развития относительной гипотироксинемии в ранние сроки ИБ.
Таким образом, как стимуляция суперовуляции, так и носительство АТ-ЩЖ являются факторами, снижающими нормальный функциональный ответ ЩЖ, необходимый для адекватного развития ИБ, а АТ-ЩЖ могут быть ранним маркером риска неблагоприятного прогноза беременности после ЭКО и ПЭ.
БЕРЕМЕННОСТЬ И ТИРЕОТОКСИКОЗ
Тиреотоксикоз во время беременности развивается относительно редко (в 1–2 на 1000 беременностей). Практически все случаи тиреотоксикоза у беременных женщин связаны с болезнью Грейвса (БГ). Согласно современным представлениям, выявление БГ не является показанием для прерывания беременности, поскольку в настоящее время разработаны эффективные и безопасные методы консервативного лечения токсического зоба.
Диагностика БГ в период беременности базируется на комплексе клинических данных и результатов лабораторно–инструментального исследования, при этом наибольшее число диагностических ошибок связано с дифференциальной диагностикой БГ и так называемого транзиторного гестационного гипертиреоза. Последний не требует какого-либо лечения и постепенно, с увеличением срока беременности, проходит самостоятельно.
Наибольшее число диагностических ошибок связано с дифференциальной диагностикой болезни Грейвса и транзиторного гестационного гипертиреоза
Основной целью лечения тиреостатиками БГ при беременности является поддержание уровня fT4 на верхней границе нормы или несколько выше нормы с использованием минимальных доз препаратов.
Принципы лечения БГ во время беременности таковы:
Представленный краткий обзор проблемы оставил за рамками обсуждения как большое число частных практических аспектов (например, особенности интерпретации отдельных показателей при оценке функции ЩЖ во время беременности), так и крупных проблем, среди которых – послеродовые аутоиммунные тиреопатии (послеродовый тиреоидит, послеродовая манифестация БГ), вопросы диагностики и лечения различных форм зоба (в том числе узлового) и рака ЩЖ, патология ЩЖ новорожденного, индуцированная заболеванием ЩЖ матери и ее лечением. Нашей задачей было, скорее, обозначить проблему, стоящую на стыке эндокринологии, и гинекологии и приобретающую все большую актуальность по мере развития ВРТ и совершенствования технологий, использующихся в диагностике и лечении заболеваний ЩЖ.
ЛИТЕРАТУРА
1. Назаренко Т. А., Дуринян Э. Р., Чечурова Т. Н. Эндокринное бесплодие у женщин. Диагностика и лечение. – М., 2004; 72.
2. Фадеев В. В., Лесникова С. В., Мельниченко Г. А. Функциональное состояние щитовидной железы у беременных женщин в условиях легкого йодного дефицита // Пробл. эндокринол. – 2003; 6: 23–28.
3. Фадеев В. В., Лесникова С. В., Мельниченко Г. А. Функциональное состояние щитовидной железы у беременных женщин–носительниц антител к тиреоидной пероксидазе // Пробл. эндокринол. – 2003; 5: 23–29.
4. Brent G. A. Maternal hypothyroidism: recognition and management // Thyroid. – 1999; 99: 661–665.
5. Fadeyev V., Lesnikova S., Melnichenko G. Prevalence of thyroid disorders in pregnant women with mild iodine deficiency // Gynecol. Endocrinol. – 2003; 17: 413–418.
6. Glinoer D., De Nayer P., Delange F. et al. A randomized trial for the treatment of mild iodine deficiency during pregnancy: maternal and neonatal effects // J. Clin. Endocrinol. Metab. – 1995; 80: 258–269.
7. Glinoer D., Riahi M., Gruen J. P. et al. Risk of subclinical hypothyroidism in pregnant women with asymptomatic autoimmune thyroid disorders // J. Clin. Endocrinol. Metab. – 1994; 79: 197–204.
8. Glinoer D. The regulation of thyroid function in pregnancy: pathways of endocrine adaptation from physiology to pathology // Endocr. Rev. – 1997; 18: 404–433.
9. Kim C. H., Chae H. D., Kang B. M. et al. Influence of antithyroid antiboies in euthyroid women on in vitro fertilization–embryo transfer outcome // Am. J. Reprod. Immunol. – 1998; 40 (1): 2–8.
10. Matalon S. T., Blank M., Ornoy A. et al. The association between anti– thyroid antibodies and pregnancy loss // Am. J. Reprod. Immunol. – 2001; 45 (2): 72–77.
11. Poppe K. Glinoer D. Thyroid autoimmunity and hypothyroidism before and during pregnancy // Hum. Reprod. Update. – 2003; 9 (2): 149–161.
12. Рoppe K., Glinoer D., Tournaye H. et al. Impact of ovarian hyperstimula-tion on thyroid function in women with and without thyroid autoimmunity // J. Clin. Enocrinol. Metab. – 2004; 89 (8): 3808–3812.
13. Poppe K., Velkeniers B. Female infertility and the thyroid // Best Pract. Res. Clin. Endocrinol. Metab. – 2004; 18 (2): 153–165.


 Читайте также:
Читайте также: