Чем объясняется металлический блеск металлов
Металлы
Металлы относятся к основным природным материалам используемым человечеством.
Металлургия – одна из базовых отраслей промышленности, определяющих экономический и военный потенциал страны. Создаются новые сплавы с заданными свойствами, в качестве добавок используются различные металлы.
Около 80% всех известных химических элементов ПСЭ составляют металлы. Наиболее распространенными металлами являются: Al – 8,8%; Fe – 4,0%; Ca – 3,6%; Na – 2,64%; K – 2,6%; Mg – 2,1%; Ti – 0,64%.
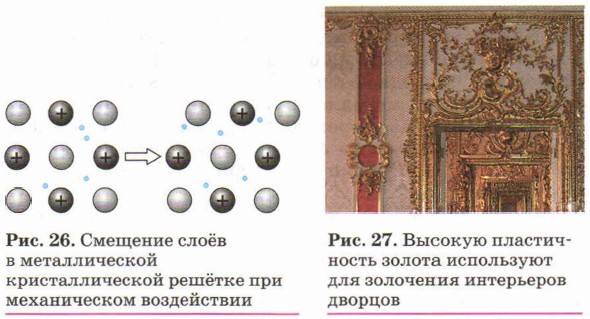
Пластичностью называется способность металлов под действием внешних сил подвергаться деформации, которая остается и после прекращения этого действия. Благодаря пластичности металлы подвергаются ковке, прокатке, штамповке. Металлы имеют различную пластичность.
Металлический блеск. Гладкая поверхность металлов отражает световые лучи. Чем меньше она эти лучи поглощает, тем больше металлический блеск. По блеску металлы можно расположить в следующий ряд: Ag, Pd, Cu, Au, Al, Fe.
На этом свойстве металлов основано производство зеркал.
С повышением температуры электропроводность уменьшается, так как усиливается колебательное движение ионов в узлах кристаллической решетки, что препятствует направленному движению электронов.
С понижением температуры электропроводность увеличивается и в области близкой к абсолютному нулю у многих металлов наблюдается сверхпроводимость.
Причиной общности физических и химических свойств металлов объясняется общностью строения их атомов и природой кристаллических решеток металлов.
Атомы металлов имеют большее, по сравнению с неметаллами размеры. Внешние электроны атомов металлов значительно удалены от ядра и связаны с ним слабо, поэтому металлы имеют низкие потенциалы ионизации (являются восстановителями).
Для металлов характерна металлическая связь (она объясняется на основе метода МО).
Физические свойства металлов.
Все металлы, за исключением ртути, при обыкновенной температуре являются твердыми веществами с характерным металлическим блеском.
Большинство металлов имеют цвет от темно-серого, до серебристо-белого. Золото и цезий имеют желтый цвет, совершенно чистая медь – светло-розовый, некоторые металлы обладают красноватым оттенком (висмут).
Плотность металлов может колебаться в широких пределах; например плотность Li = 0,53г/см3 (самый легкий), а Os является самым тяжелым металлом 22,48г/см3.
В пределах одной подгруппы аналогов величины плотностей, как правило, растут с возрастанием заряда ядра атома.
В технике металлы классифицируются по плотности: легкие, тяжелые, легкоплавкие и тугоплавкие.
Нахождение в природе.
В природе металлы встречаются как в самородном состоянии, так и в виде различных соединений. В самородном состоянии находятся только химически малоактивные металлы – Pt, Ag, Au. Химически активные металлы встречаются только в виде различных соединений – руд.
Руды бывают: окисные, сульфидные и соли.
Предварительно руду обогащают, то есть отделяют от пустой породы. Самый распространенный метод – флотационный, он основан на различной смачиваемости поверхности минералов водой.
Методы извлечения минералов из руд определяются их химическим составом. Все способы получения металлов сводятся к реакциям окисления – восстановления.
Углерод применяется для восстановления сравнительно малоактивных металлов: Fe, Cu, Zn, Pb.
При восстановлении углеродом смеси железной руды с оксидами Cr, Mo, W или Mn в промышленности получают сплавы, содержащие примерно 70% указанных металлов и очень небольшое количество углерода. Это ферросплавы, служат для получения специальных легированных сталей. Для восстановления углеродом пригодны только окиси.
Сульфидные руды (цинковые, свинцовые, медные) сначала подвергают окислительному прокаливанию:
2ZnS + 2O2 → 2ZnO + SO2
Li, Ca, Ba также, как и металлы III группы, не могут быть получены восстановлением углеродом, так как они сразу же после выделения в свободном состоянии с избытком углерода образуют карбиды.
Металлотермия. Основана на процессах вытеснения одного металла (менее активного) другим (более активным) из соответствующих окислов, хлоридов, сульфидов.
Очень хорошим восстановителем окислов металлов вследствие большого сродства к кислороду является алюминий. Процесс называется алюминотермия.
Fe2O3 + 2Al = Al2O3 + 2Fe
Алюминотермией получают и другие металлы (Mn, Cr, Ti), которые не могут быть получены в чистом виде восстановлением их окисей углем из-за образования карбидов. В алюмотермической реакции выделяется большое количество тепла за очень короткое время, вследствие чего развивается высокая температура.
Электролитическое или катодное восстановление металлов. Для трудновосстанавливаемых металлов уголь как восстановитель непригоден и в этом случае применяют катодное восстановление, то есть выделение путем электролиза. Такие металлы могут окисляться водой, поэтому их соединения подвергаются электролизу не в водных растворах, а в расплавах или растворах других растворителей.
Например, металлические Na, K, Ba, Ca, Mg, Be получают электролизом расплавов соответствующих хлоридов.
Получение металлов высокой чистоты.
В связи с бурным развитием техники потребовались металлы, обладающие очень высокой чистотой. Например, для надежной работы ядерного реактора необходимо, чтобы в расщепляющихся материалах такие примеси как бор, кадмий и др., содержались в количестве, не превышающих миллионных долей процента. Чистый цирконий – один из лучших конструкционных материалов для атомных реакторов – становится совершенно непригодным для этой цели, если в нем содержится даже ничтожная примесь гафния.
Перегонка в вакууме. Этот метод основан на различной летучести очищаемого металла и имеющихся в нем примесей. Исходный металл загружается в специальный сосуд, соединенный с вакуумным насосом и в сосуде создают вакуум, после чего нижняя часть сосуда нагревается. На холодных частях сосуда осаждаются либо примеси, либо чистый металл, в зависимости от того, что является более летучим.
1. Карбонильный процесс. Этот процесс используют в основном для получения чистого никеля и чистого железа. Металл содержащий примеси, нагревают в присутствии СО (окиси углерода) и получающийся летучий карбонил отгоняют от нелетучих примесей. Затем карбонилы разлагают при более высоких температурах с образованием высокочистых металлов.
2. Йодистый процесс дает возможность получать такие металлы, как цирконий, титан.
3. Очистка металла (обычно содержащего в качестве примесей окисел) в вакууме при нагревании его до очень высокой температуры при помощи электрической дуги.
Зонная плавка. Этот метод заключается в протягивании бруска неочищенного Германия через узкую печь; образующаяся при этом расплавленная зона, по мере продвижения бруска через нее перемещается вдоль него и уносит за собой примеси.
Многократным повторением этого процесса можно достигнуть высокой степени чистоты.
Химические свойства металлов.
У металлов отсутствует способность присоединять электроны, следовательно металлы являются восстановителями. Мерой химической активности металлов является энергия ионизации J.
Окислителями металлов могут быть: элементарные вещества, кислоты, соли менее активных металлов и т. д.
1. Взаимодействие с элементарными веществами.
2. Взаимодействие с кислотами:
а) Окислитель – ион Н+ (HCl, H2SO4 (разб.) и т. д.);
б) Окислитель анион кислоты (к таким кислотам относятся HNO3 и H2SO4 (конц.);
в) Взаимодействие с водой;
г) Взаимодействие со щелочами;
д) Взаимодействие с растворами солей.
Все атомы кислорода непосредственно связаны с атомами металла и не связаны друг с другом: Ме * О2.
Классификация оксидов металлов
Их свойства: а) взаимодействуют с кислотами; б) с кислотными оксидами; в) с водой.
Их свойства: а) взаимодействие с кислотами; б) взаимодействие со щелочами.
Кислотные – оксида малоактивных металлов в высших степенях окисления (CrO3, Mn2O7 и др.). Их свойства: а) взаимодействие с водой, образуя кислоты; б) взаимодействуют с основаниями (щелочами).
Характер изменения свойств оксидов
В пределах одного периода происходит ослабление основных свойств через амфотерные и усиление кислотных слева на право.
В группе у одного и того же элемента наблюдается такое же изменение свойств.
1. Непосредственное окисление металлов – горение.
2. Окисление сульфидов.
3. Окисление оксидами других элементов, если теплота образования получающегося оксида больше теплоты образования исходного (металлотермия).
Al + Cr2O3 = Cr + Al2O3 + Q
4. Обезвоживание соответствующих гидроксидов.
Al(OH)3 
5. Термическое разложение карбонатов, нитратов, сульфатов и других солей.
СаСО3 
Классификация: основные, амфотерные, кислотные (соответствуют оксидам).
Характер изменения свойств в природе – аналогично оксидам.
Базовые понятия. Запись 7 (физические свойства металлов)
В данной статье ознакомимся с основными физическими свойствами металлов. Вашему вниманию будут представлены пластичность, электропроводность, теплопроводность, металлический блеск, твёрдость, плотность, температура плавления.
Начнём с пластичности.
Пластичность — это свойство вещества изменять форму под внешним воздействием, не разрушаясь, и сохранять принятую форму после прекращения этого воздействия.
Почему у металлов так выходит? Это происходит из-за их строения, виновной выступает кристаллическая решётка. Она состоит из узлов и свободных электронов, которые бегают между углами, никому не принадлежа. В узлах могут быть атомы, молекулы или ионы. Электроны то присоединяются к ним, то уходят. Именно взаимосвязью между бегающими по всему веществу электронами и узлами объяснятся свойство пластичности: слои смещаются друг с другом без разрыва.
Как же определить и сравнить пластичность разных металлов? Она определяется при испытании на растяжение. Под действием нагрузки образцы разных металлов в различной степени удлиняются, а их поперечное сечение уменьшается. Чем больше способен образец удлиняться, а его поперечное сечение сужаться, тем пластичнее образец.
Существуют две единицы измерения: относительное удлинение и относительное сужение при разрыв.
По степени пластичности металлы принято подразделять следующим образом:
-высокопластичные (относительное удлинение превосходит 40 %) — металлы, составляющие основу большинства конструкционных сплавов (алюминий, медь, железо, титан, свинец) и «легкие» металлы (натрий, калий, рубидий и др.);
-пластичные (относительное удлинение лежит в диапазоне между 40 и 3%) — магний, цинк, молибден, вольфрам, висмут и др. (наиболее обширная группа);
-хрупкие (относительное удлинение меньше 3%) — хром, марганец, кобальт, сурьма.
Электропроводность — свойство проводить электрический ток.
Электрическим током зовём упорядоченное движение частиц. В нашем случае под действие некого поля начинают двигаться в одном направлении все свободные электроны в образце.
Электропроводность металлов обусловлена концентрацией электронов и их подвижностью. Чем сильнее металл нагрет, тем сильнее прыгающие узлы будут мешать электронам свободно передвигаться в выбранном направлении. Чем больше столкновений, тем сильнее нагревается металл. Данный эффект применяется в нагревательных приборах и в лампах накаливания.
Теплопроводность — свойство металлов переносить энергию от одной части тела к другой.
Оно связано с высокой подвижностью электронов: сталкиваясь с колеблющимися в узлах решётки ионами, атомами, электроны обмениваются с ними энергией. Как видим, данное свойство связано с предыдущим.
Металлический блеск — способность металлов отражать световые лучи.
Данное свойство обуславливается несколькими причинами. Во-первых, от гладкости поверхности, т.е. падающая электромагнитная волна (свет) не застревала в неровностях, а могла отразиться обратно.
Во-вторых, свет попадает на металл, поглощается электронами и через некое малое время излучается обратно, при этом количество энергии, которое может уйти на нагревание, небольшое. Отражённую волну воспринимает наш глаз, цвет волны определяется из величины «длина волны».
Твёрдость — свойство твёрдого тела сопротивляться проникновению в него другого тела.
Если хотите много теории по данному свойству, то прошу сюда:
Оценка металла по шкале Мооса берёт за основу то, насколько легко образец может быть поцарапан другими металлами. Например, коэффициент твердости золота — 2,5-3, что значительно ниже коэффициента твердости большинства других материалов. В то время как графит и некоторые виды пластика стоят на одном конце шкалы, имея значение 1, то на другой её конец ставится алмаз, одно из самых твердых веществ на Земле. Он оценивается в 10 баллов.
Олово: 1.5
Цинк: 2.5
Золото: 2.5-3
Серебро: 2.5-3
Алюминий: 2.5-3
Медь: 3
Медь: 3
Бронза: 3
Никель: 4
Платина: 4-4.5
Сталь: 4-4.5
Железо: 4.5
Палладий: 4.75
Родий: 6
Титан: 6
Укрепленная сталь: 7-8
Вольфрам: 7.5
Карбид вольфрама: 8.5-9
Плотность — это отношение массы на объём.
Тяжело расшифровать определение, но я попробую. Оно значит, что при равном объёме разные металлы будут проявлять разную инерцию. Конечно, если и стало понятнее, то на чуток.
-лёгкие (плотность не более 5 г/см 3 ) — магний, алюминий, титан и др.:
-тяжёлые — (плотность от 5 до 10 г/см 3 ) — железо, никель, медь, цинк, олово и др. (это наиболее обширная группа);
-очень тяжёлые (плотность более 10 г/см 3 ) — молибден, вольфрам, золото, свинец и др.
Таблицы с плотностями:
Температура плавления — температура, при которой осуществляется процесс перехода вещества из твёрдого состояния в жидкое.
При увеличении внутренней энергии начинают сильнее колебаться узлы, решётка теряет свою структуру, нарушаются связи. Примерно такой процесс можно назвать переходом в жидкое состоянии.
Делят металлы на несколько групп:
-легкоплавкие (температура плавления не превышает 600 o С) — цинк, олово, свинец, висмут и др.;
-среднеплавкие (от 600 o С до 1600 o С) — к ним относятся почти половина металлов, в том числе магний, алюминий, железо, никель, медь, золото;
-тугоплавкие ( более 1600 o С) — вольфрам, молибден, титан, хром и др.
§ 9. Физические свойства металлов
Из курса химии 9 класса вы уже имеете представление о природе химической связи, существующей в кристаллах металлов, — металлической связи. Напомним, что в узлах металлических кристаллических решёток располагаются атомы и положительные ионы металлов, связанные посредством обобществлённых внешних электронов, принадлежащих всему кристаллу. Эти электроны компенсируют силы электростатического отталкивания между положительными ионами и тем самым связывают их, обеспечивая устойчивость металлической решётки.
Металлическая связь обусловливает все важнейшие физические свойства металлов: пластичность, электро- и теплопроводность, металлический блеск и другие свойства, характерные для этого класса простых веществ.
Пластичность — это свойство вещества изменять форму под внешним воздействием и сохранять принятую форму после прекращения этого воздействия.
Способность расплющиваться от удара или вытягиваться в проволоку под действием силы составляет важнейшее механическое свойство металлов. Оно лежит в основе такой уважаемой большинством народов мира профессии, как профессия кузнеца. Недаром покровителем кузнечного дела у разных народов был бог огня: у греков — Гефест, у римлян — Вулкан, у славян — Сварог.
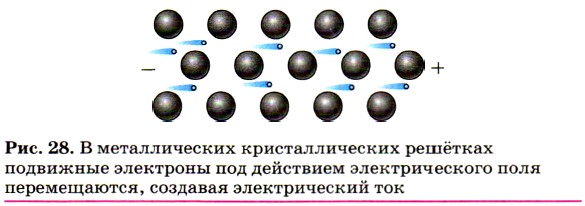
Пластичность металлов обусловлена способностью одних слоёв атом-ионов в кристаллах под внешним воздействием легко смещаться (как бы скользить) по отношению к другим слоям без разрыва связей между ними (рис. 26). Наиболее пластичны золото, серебро и медь. Например, из золота можно изготовить «золотую фольгу» толщиной 0,003 мм, которую используют для золочения изделий (рис. 27).
Высокая электропроводность большинства металлов обусловлена присутствием в их кристаллических решётках подвижных электронов, которые направленно перемещаются под действием электрического поля (рис. 28).
При нагревании колебательные движения ионов в кристалле усиливаются, что затрудняет направленное движение электронов и ведёт к снижению электрической проводимости. При охлаждении электропроводность металлов увеличивается и вблизи абсолютного нуля переходит в сверхпроводимость. Наибольшую электропроводность имеют серебро и медь, наименьшую — марганец, свинец, ртуть и вольфрам.
Такое свойство, как теплопроводность металлов, также связано с высокой подвижностью свободных электронов: сталкиваясь с колеблющимися в узлах решётки ионами, электроны обмениваются с ними энергией. С повышением температуры колебания ионов при посредстве электронов передаются другим ионам, и температура всего металлического предмета быстро выравнивается.
Для гладкой поверхности металлов характерен металлический блеск — результат отражения световых лучей. В порошкообразном состоянии большинство металлов теряет блеск, приобретая чёрную или серую окраску, и только алюминий и магний сохраняют блеск в порошке. Из алюминия, серебра и палладия, обладающих наиболее высокой отражательной способностью, изготовляют зеркала, в том числе и применяемые в прожекторах.
Для большинства металлов характерен белый или серый цвет. Золото и медь окрашены соответственно в жёлтый и жёлто-красный цвет. Из других физических свойств металлов наибольший практический интерес представляют твёрдость, плотность и температура плавления.
Для большинства металлов характерен белый или серый цвет. Золото и медь окрашены соответственно в жёлтый и жёлто-красный цвет.
Из других физических свойств металлов наибольший практический интерес представляют твёрдость, плотность и температура плавления.
Для всех металлов (кроме ртути) при обычных условиях характерно твёрдое агрегатное состояние. Однако твёрдость их различна. Наиболее твёрдые — металлы побочной подгруппы VI группы (VIB группы) Периодической системы Д. И. Менделеева. Так, хром по твёрдости приближается к алмазу. Самые мягкие — металлы главной подгруппы I группы (IA группы) Периодической системы Д. И. Менделеева — щелочные металлы. Например, натрий и калий легко режутся ножом.
По плотности металлы делят на лёгкие (плотность меньше 5 г/см 3 ) и тяжёлые (плотность больше 5 г/см 3 ). К лёгким относят щелочные, щёлочноземельные металлы и алюминий. Из переходных металлов сюда включают скандий, иттрий и титан. Эти металлы, благодаря лёгкости и тугоплавкости, всё шире применяют в различных областях техники.
Самый лёгкий металл — это литий (р = 0,53 г/см 3 ). Самый тяжёлый — осмий (р = 22,6 г/см 3 ).
Лёгкие металлы обычно легкоплавки, галлий может плавиться уже на ладони руки, а тяжёлые металлы — тугоплавки. Наибольшей температурой плавления, которая равна 3380 °С, обладает вольфрам. Это свойство вольфрама используют для изготовления ламп накаливания (рис. 29, 2). Кроме него в конструкцию лампы входят ещё семь металлов.
В Российской Федерации в настоящее время, как и ранее в Евросоюзе и США, на государственном уровне принято решение о замене привычных ламп накаливания на более экономичные и долговечные современные лампы, например галогенные, люминесцентные и светодиодные. Галогенная лампа (рис. 29, 2) — это та же лампа накаливания с вольфрамовой нитью, заполненная инертными газами с добавкой паров галогенов (брома или иода).
Люминесцентные (рис. 29, 3) — это хорошо знакомые вам лампы дневного света, имеющие один существенный недостаток — они содержат ртуть, а потому нуждаются в соблюдении особых правил утилизации на специальных пунктах приёма. Светодиодные лампы (рис. 29, 4) — самые экономичные и самые долговечные (срок работы до 100 тыс. ч), но пока и самые дорогие из ламп.
В технике, как вы уже знаете, металлы делят на чёрные (железо и его сплавы) и цветные (все остальные, более подробно о них будет рассказано в следующем параграфе) (рис. 30). Золото, серебро, платину и некоторые другие металлы относят к драгоценным металлам (рис. 31). 1
1. Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
2. Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и слово-сочетаниям следующего параграфа.
1. Назовите самый легкоплавкий металл.
2. Какие физические свойства металлов используют в технике?
3. Фотоэффект, т. е. свойство металлов испускать электроны под действием лучей света, характерен для щелочных металлов, например для цезия. Почему? Где это свойство находит применение?
4. Какие физические свойства вольфрама лежат в основе его применения в лампах накаливания?
Физические свойства металлов
Физические свойства металлов
Металлическая связь и особенности кристаллического строения обуславливают особые физические свойства металлов.
Металлическая связь основана на обобществлении электронов, входящих в состав атомов металла. Все электроны на внешних энергетических уровнях атомов металлов обобществленные, т.е. принадлежат всем атомам вещества. И эти электроны легко отрываются и попадают на энергетические уровни таких же атомов металлов. Постоянно перемещаясь по кристаллической решетке, электроны компенсируют силы электростатического отталкивания между положительно заряженными ионами и тем самым связывают их в устойчивую металлическую решетку.
Содержимое разработки
9. Физические свойства металлов
Металлическая связь и особенности кристаллического строения обуславливают особые физические свойства металлов.
Металлическая связь основана на обобществлении электронов, входящих в состав атомов металла. Все электроны на внешних энергетических уровнях атомов металлов обобществленные, т.е. принадлежат всем атомам вещества. И эти электроны легко отрываются и попадают на энергетические уровни таких же атомов металлов. Постоянно перемещаясь по кристаллической решетке, электроны компенсируют силы электростатического отталкивания между положительно заряженными ионами и тем самым связывают их в устойчивую металлическую решетку.
Металлическая связь – это связь в металлах и сплавах между атом-ионами посредством обобществленных электронов.
Разобраться в том, какой электрон принадлежал какому атому, просто невозможно, так как все оторвавшиеся электроны становятся общими, соединяясь с ионами. Эти электроны временно образуют атомы, потом снова отрываются и соединяются с другим ионом. Этот процесс продолжается бесконечно. Таким образом, в металлических соединениях атомы непрерывно превращаются в ионы и наоборот.
Именно строением металлической связи обусловлены физические свойства металлов.
К физическим свойствам металлов относятся:
Электропроводность и теплопроводность.
Высокая плотность и температура плавления.
Рассмотрим каждое из свойств более подробно.
Металлический блеск обусловлен металлической связью между атомами, для которой свойственны обобществленные электроны. Они как раз и испускают под воздействием света свои, вторичные волны излучения, которые мы воспринимаем как металлический блеск.
В порошкообразном состоянии большинство металлов теряют металлический блеск и приобретают серую или черную окраску.
Металлический блеск в порошкообразном состоянии сохраняют алюминий и магний.
Прекрасно отражают свет палладий Pd, ртуть Hg, серебро Ag, медь Cu.
Из алюминия, серебра и палладия, основываясь на их отражательной способности, изготавливают зеркала, в том числе и применяемые в прожекторах.
Электропроводность и теплопроводность.
Все металлы хорошо проводят электрический ток и имеют высокую теплопроводность, также благодаря наличию металлической связи. При нагревании металла, увеличивается скорость движения электронов. Быстро движущиеся по кристаллической решетке электроны выравнивают температуру по всей поверхности металла, проводя тепло. Высокая теплопроводность металлов используется для изготовления из них посуды.
Высокая электропроводность металлов обусловлена направленным движением электронов в кристаллической решетке при воздействии электрического тока. Серебро Ag, медь Cu, золото Au и алюминий Al обладают наибольшей электропроводностью, поэтому медь Cu и алюминий Al используют в качестве материала для изготовления электрических проводов.
Наименьшей электропроводностью обладают марганец Mn, свинец Pb, ртуть Hg и вольфрам W.
Пластичность – это физической свойство вещества изменять форму под внешним воздействием и сохранять принятую форму после прекращения этого воздействия.
Большинство металлов пластично, так как слои атом-ионов металлов легко смещаются относительно друг друга и между ними не происходит разрыва связи.
Наиболее пластичные металлы – золото Au, серебро Ag, медь Cu. Из золота Au можно изготовить тонкую фольгу толщиной 0,003 мм, которую используют для золочения изделий.
Именно на пластичности металлов основано кузнечное дело и возможность изготавливать различные предметы с помощью механического воздействия на металл.
Все металлы (кроме ртути) при нормальных условиях представляют собой твердые вещества. Твердость металлов различна. Наиболее твердыми являются металлы побочной подгруппы шестой группы Периодической системы Д.И. Менделеева. Наименее твердыми являются щелочные металлы.
Температура плавления металлов находится в диапазоне от 39 (ртуть Hg) до 3410 о С (вольфрам W). Температура плавления большинства металлов высока, однако некоторые металлы, например, олово Sn и свинец Pl, можно расплавить на электрической плите.
Физические свойства металлов и в настоящее время широко используются в промышленности и электронике.
В технике все металлы делятся на черные, к ним относятся железо и его сплавы, и цветные.
Изделия из различных видов металлов используются повсеместно благодаря их пластичности, но чаще всего в сплавах.
К драгоценным металлам относят золото, серебро, платину и некоторые другие редко встречающиеся металлы.