Чем нейтрализовать перекись водорода в организме
Чем нейтрализовать перекись водорода в организме
В 1900 г. перекисью водорода в США было обусловлено 8177 отравлений. Чаще всего речь шла о растворе «бытовой» крепости (3 %), и обычно исход был благоприятным. Прием внутрь препаратов крепче 10 % чреват тяжелыми последствиями, однако летальные исходы редки.
б) Применение перекиси водорода. Перекись водорода — эффективное дезинфицирующее средство, которое применяют также для удаления уплотненного мекония, выявления ректовагинальных свищей и лечения запора или каловых завалов. Рентгенологи используют Н2О2 для удаления газа из кишечника при рентгеноскопии брюшной полости и в смеси с барием для флюороскопической идентификации места желудочно-кишечного кровотечения, поскольку при контакте с перекисью водорода кровь образует пузырьки.
Это средство рекомендуется для дезинфекции тонометрических наконечников, офтальмологических инструментов и пробных контактных линз с целью предупреждения передачи вирусов, особенно ВИЧ.
Растворы низкой концентрации (3—9 %) используются для лечения воспалений наружного слухового прохода, а также для полоскания рта и горла. Перекисью водорода дезинфицируют корневые каналы зубов и другие полости, очищенные от зубной пульпы. Она используется как раствор для орошения влагалища. Более концентрированными препаратами (20—30 %) отбеливают волосы и зубы. Раствор крепостью 90 % применяется для химического синтеза, отбеливания текстиля и бумаги и в составе ракетного топлива.
Управление FDA указывает, что перекись водорода промышленной крепости нелегально распространяется как «35 % пищевая перекись» для разведения и использования в «гипероксигенационной терапии» СПИДа, рака и других болезней. Эту жидкость закупают оптом на химических предприятиях Техаса и Мексики, а затем разливают в мелкие емкости для розничной продажи. В некоторых лавках «здоровой пищи» ее можно встретить под названиями «Biowater» и «Н2О2». Эта концентрация не утверждена FDA для терапевтического применения в США.
в) Лекарственные формы перекиси водорода. В продаже имеются концентрат для наружного применения 30,5 % по массе, 1,5 % гель (Peroxyl Oral Spot Treatment) и раствор крепостью 1,5 (полоскание для рта Peroxyl mouth rinse с 6 % спирта) и 3 %.
г) Токсичная доза. Ингаляция 90 % перекиси водорода вызывает воспаление легких у животных. У людей, случайно вдохнувших пары 90 % Н2О2, отмечаются слюнотечение, першение в глотке и воспаление дыхательных путей. Серьезное поражение легких у человека при экспозиции к белому дыму, выделяемому 90 % Н2О2 при контакте с тяжелым металлом или его солью, маловероятно.
У одного взрослого, хронически вдыхавшего аэрозоль Н2О2 в концентрации 41 мэкв/м3 (средневзвешенная по времени ПДК NIOSH/OSHA равна 1 млн-1, или 1,41 мг/м3), развилась хроническая диффузная интерстициальная болезнь легких.
д) Механизм действия перекиси водорода:
— Повреждение клеток. На клеточном уровне индуцированное перекисью водорода повреждение ДНК, по-видимому, обусловлено связанными с ДНК ионами переходных металлов, которые могут взаимодействовать с Н2О2 с образованием высокореактивного радикала, скорее всего ОН. Этот радикал, оказавшись рядом с ДНК, реагирует с ней, что приводит к появлению пуриновых и пиримидиновых продуктов, аналогичных обнаруживаемым в водном растворе ДНК после воздействия на него ионизирующей радиации.
— Клинические проявления на макроскопическом уровне. «Белоснежный» вид ободочной слизистой оболочки (побеление и образование пены), наблюдаемый после ее обработки перекисью водорода, объясняется проникновением этого вещества в интерстициальные пространства эпителия и капилляры с образованием микроскопических пузырьков молекулярного кислорода. Кровь выталкивается из интрамуральных сосудов и замещается кислородом в результате реакции с участием тканевой каталазы.
е) Клиника отравления перекисью водорода:
— Промывание ран под давлением. Перекись водорода расщепляется на воду и кислород. При использовании в замкнутом пространстве под давлением (как 3 % Н2О2) высвобождающемуся кислороду некуда деваться. Возможны кислородная эмболизация и послеоперационная эмфизема. Cina и соавт. описали факторы, которые надо учитывать при диагностике перорального отравления перекисью водорода.
• Возрастная группа риска: 1—3 года (старше при умственной отсталости).
• Анамнез: пациент обнаружен рядом с открытой емкостью из-под перекиси водорода; белая пена изо рта, носа и/или заднего прохода; промывание раны перекисью или недавно сделанная перекисная клизма.
• Принятое внутрь количество: вероятно, более 2—4 унций (60—120 мл) 3 % раствора.
• «Клинический» диагноз: шок, острая коронарная недостаточность, синдром внезапной детской смерти, остановка дыхания, эпилептический статус, инсульт или сепсис.
• Рентгенологическая картина: газ в системах брыжеечных, желудочных, селезеночной или воротной вен с расширением желудка и двенадцатиперстной кишки или без него, с газом в нижней полой вене (НПВ) и правом желудочке или без него.
• Макроскопические данные: расширение желудка; «иней» на желудочно-кишечной слизистой оболочке; гастрит, дуоденит и/или колит; пенистая кровь в воротной вене, НПВ, правом желудочке и/или шейных венах; крепитация печени; внутренностная гиперемия; петехии тимуса, эпикарда и, возможно, других внутренних органов или отек мозга.
• Микроскопические данные: гастрит, дуоденит и/или колит, острая внутренностная гиперемия; прозрачные вакуоли в подслизистой основе желудочно-кишечного тракта; прозрачные вакуоли в желудочно-кишечных венах, лимфатических сосудах, брыжеечных лимфатических узлах или связанной со слизистой оболочкой лимфоидной ткани либо вакуолизация других органов (газовые эмболы).
• Токсикологический анализ: в крови, желудочном содержимом и найденной при пострадавшем емкости токсичных веществ не обнаружено.
• Микробиологические данные: патогены не обнаружены. Описан пневморетроперитонеум.
— Промывание ободочной и подвздошной кишок. Кислородная эмболизация вен и лимфатических сосудов тонкой кишки может произойти при промывании подвздошной кишки 1 % перекисью водорода. Пузырьки воздуха появляются при начале ее инстилляции и сохраняются в течение примерно 30 мин. Перекись водорода (1%), использованная для промывания кишечника у одного младенца по поводу закупорки меконием, вызвала газовую эмболизацию брыжеечных и воротной вен с летальным исходом.
Клизмы с перекисью водорода могут привести к язвенному колиту, который иногда имитирует псевдомембранозный колит. Наблюдался также «перекисный» проктит.
— Изъязвление полости рта. Избыточное применение 3 % перекиси водорода вместе с бикарбонатом натрия и поваренной солью или без них для полоскания рта чревато эрозией мягких тканей десен.
— Поражение роговицы — дезинфекция мягких контактных линз. Применение 3 % перекиси водорода для дезинфекции мягких контактных линз может обусловить жжение, слезотечение, гиперемию, блефароспазм, отек и даже необратимое повреждение роговицы. Этим же чревато прикладывание к глазу наконечника тонометра, смоченного раствором Н2О2.
— Перекись водорода в замкнутых полостях тела. Введение через канюлю 20 мл перекиси водорода и одновременное использование пропитанных ею тампонов при полной артропластике тазобедренного сустава привели к тяжелому циркуляторному коллапсу и остановке сердца.
— Пероральное отравление перекисью водорода «бытовой» концентрации (3—9 %). Прием внутрь слабого раствора перекиси водорода приводит к умеренному раздражению слизистых оболочек и чреват спонтанной рвотой или небольшим вздутием живота.
— Промышленная концентрация (более 10 %). Прием внутрь перекиси водорода промышленной концентрации чреват тяжелыми ожогами ротоглотки и пищеварительного тракта с возможным разрывом полых органов в результате выделения кислорода. Пена может вызвать закупорку дыхательных путей и механическую асфиксию. Предполагается, что именно дыхательная недостаточность была причиной летальных исходов после приема внутрь перекиси водорода концентрацией выше 10 %.
ж) Лечение отравления перекисью водрода:
— Стабилизация состояния:
1. Крайне важно как можно быстрее восстановить проходимость дыхательных путей, поскольку ранней причиной смерти, по-видимому, являются нарушение и остановка дыхания.
2. При доставке в отделение неотложной медицинской помощи необходимо немедленно обеспечить доступ в вену, к кислороду и кардиомонитору. Надо определить газовый состав артериальной крови. По показаниям проводят эндотрахеальную интубацию, кислородотерапию, аппаратную вентиляцию и массаж сердца.
3. Надо быть готовым к быстрому развитию припадков.
4. Начинают инфузионную терапию, следя за количеством вводимой и выводимой жидкости и не допуская перегрузки ею организма, иначе пациент может умереть от дыхательной недостаточности и остановки дыхания.
— Очистка пищеварительного тракта. Можно сделать промывание желудка ледяным солевым раствором при эндотрахеальном лаваже. При перораль-ном приеме перекиси водорода промышленной крепости польза активированного угля, слабительных средств и других способов очистки кишечника не доказана.
— Усиление выведения. Процедуры, усиливающие выведение перекиси водорода из кровотока, за исключением хирургического вмешательства при вызванной ею закупорке сосудов, не известны.
— Антидоты перекиси водорода. Антидотов не существует.
— Поддерживающая терапия. Отравление перекисью водорода обычно лечат симптоматическими и поддерживающими мерами.
Припадки. При рецидивировании припадков внутривенно вводят диазепам и фенитоин. Проводят компьютерно-томографическое сканирование головного мозга.
Кома. Обычные назначения при коме: налоксон, тиамин, 50 % раствор декстрозы.
Метаболический ацидоз. Вводят бикарбонат натрия внутривенно.
Эзофа гогастродуоденоскопия. Делают вскоре после поступления пациента в стационар и еще раз через 48 ч. В зависимости от мнения гастроэнтеролога при ожогах желудка после эндоскопии можно назначить антациды.
Лапаротомия. Может потребоваться при симптомах скопления воздуха в желудочно-кишечном тракте.
Мониторинг внутричерепного давления. По показаниям назначают гипервентиляцию.
Рентгеноскопия брюшной полости. Выявляют наличие воздуха в области печени.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Отравление перекисью водорода
Отравление перекисью водорода — это патологическое состояние, возникающее при приеме токсиканта внутрь, его внутривенном введении или наружном использовании средства с высокой концентрацией. Клиническая картина включает чувство жжения и распирания в желудке, боль за грудиной, тошноту. Возможно появление признаков химического ожога, газовой эмболии. Патология диагностируется на основании анамнеза, данных ФГДС, результатов коагулограммы, контрастной рентгенографии органов живота. Лечение предусматривает удаление яда, противоотечную и инфузионную терапию, обезболивание, антибиотики, седативные медикаменты.
МКБ-10
Общие сведения
Отравление перекисью водорода происходит при неправильном применении 3% или 6% раствора, а также пергидроля (27% или 31%). На его долю приходится около 5% всех поражений прижигающими ядами. 3% жидкость становится причиной тяжелых патологических состояний только при внутривенном вливании. Средства с более высокой концентрацией вызывают химический ожог при приеме внутрь или нанесении на кожные покровы. Патология часто встречается у детей 4-7 лет, стариков, людей, практикующих нетрадиционные методы лечения. Повреждения ЖКТ, связанные с пероральным приемом перекиси, чаще встречаются на территории стран с низким уровнем медицинской грамотности населения.
Причины
Распространенная причина патологии — случайный прием средства через рот. Подобное становится возможным при нарушении правил хранения вещества, нахождении его в емкостях из-под продуктов, напитков. Поражение обычно бывает тяжелым, так как медикамент не обладает резко выраженным вкусом. Человек успевает сделать 2-3 глотка до момента, когда понимает, что жидкость не является пищевой. Другие ситуации, в которых происходит отравление перекисью водорода:
Патогенез
Патогенез перекисных экзотоксикозов имеет несколько механизмов. Высококонцентрированные жидкости приводят к образованию колликвационного некроза. Происходит своеобразное расплавление тканей, повергшихся воздействию токсиканта. Они становятся дряблыми, размягченными. Вокруг формируется воспалительный валик. Очаг инфильтрирован нейтрофилами, макрофагами и гистиоцитами. Существует риск присоединения вторичной инфекции. При правильном лечении рана заживает вторичным натяжением через 3-4 недели.
Синтезирующийся при приеме перекиси внутрь кислород способен проникать в кровь путем диффузии. В сосудистом русле образуются пузырьки газа, которые закупоривают его и ограничивают кровоснабжение определенных участков тела. Наиболее опасна ишемия тканей ЦНС, миокарда, легких. Возможно поражение менее значимых структур: почек, печени, кишечника, скелетной мускулатуры. H2O2 снижает активность каталазы и пероксидазы. Это приводит к развитию гемолиза. Отмечается метгемоглобинобразующее влияние, которое обусловлено окислением железа до трехвалентного состояния.
Симптомы
Отравление перекисью водорода сопровождается развитием клинической картины, которая напрямую зависит от концентрации и количества препарата, пути его введения в организм. После попадания в желудок 3% раствора больные жалуются на чувство вздутия, умеренную болезненность, тошноту, обильную отрыжку. После употребления 6% вещества или пергидроля определяются признаки химического повреждения: резкая болезненность, видимые ожоги кожи белого цвета около рта, на слизистой оболочке губ, щек, неба и языка. Отмечается снижение АД, психомоторное возбуждение, шок.
Симптоматика газовой эмболии определяется поражением того или иного органа. При ишемии участка головного мозга формируется очаговая неврологическая картина: парез конечностей, нарушения зрения и слуха, асимметрия лица, изменения речи и координации движений, головная боль. Вовлечение в процесс мышечной стенки сердца сопровождается возникновением сжимающей боли за грудиной, страхом смерти, ухудшением гемодинамики. При окклюзии легочных артерий определяется одышка, цианоз верхней части тела, шум жернова над проекцией сердца, признаки шока.
Локальные ожоги выглядят как белые, будто присыпанные пудрой участки. Выраженная болезненность отсутствует. Могут образовываться пузыри, наполненные серозным содержимым. Они окружены воспалительным валом, близлежащие ткани гиперемированы, отечны. На практике встречаются повреждения 1 и 2 степени. Более глубокие травмы обычно не возникают. По мере заживления пузыри лопаются, некротизированные слои эпидермиса отшелушиваются, пораженная зона покрывается здоровой кожей.
Осложнения
Наиболее опасным осложнением является формирование участков некроза миокарда или головного мозга. Развивается в 35-37% случаев газовой окклюзии. Отмирание большого количества кардиомиоцитов становится причиной кардиогенного шока, остановки сердца. Если пациент выживает, в толще сердечной стенки образуется рубец, сократительная функция органа снижается. Повреждение структур ЦНС оканчивается необратимыми или частично обратимыми нарушениями моторных возможностей, мыслительных способностей, тех или иных внутренних систем.
Ожоги пищеварительного тракта вторично инфицируются у 20% больных. Это замедляет регенеративные процессы, способствует усилению общетоксического синдрома. При отсутствии адекватной терапии развивается нагноение ран. Существует риск возникновения инфекционного шока. Бактериальное обсеменение наружных травм повреждений оканчивается значимыми осложнениями. В 1-2% случаев выявляются подкожные нагноения, которые легко устраняются путем хирургической санации с последующим наложением антисептических мазей.
Диагностика
Предварительный диагноз выставляет врач скорой помощи, прибывший на место происшествия. Для подтверждения требуется ряд обследований, которые проводят токсиколог и реаниматолог, по показаниям – гастроэнтеролог или комбустиолог. К работе привлекают специалистов лаборатории. Патологию следует отличать от поражений, вызванных другими ядами сходного действия, термических ожогов. Используются следующие способы диагностики:
Лечение отравления перекисью водорода
Лечение осуществляется поэтапно. Выбор метода зависит от особенностей клинического течения патологии и способа проникновения яда. Во всех случаях, за исключением поверхностных травм небольшой площади, необходима госпитализация пострадавшего. При внутренних химических ожогах больного транспортируют в реанимацию. Отравление без признаков эмболии является показанием для размещения в общем токсикологическом отделении.
Первая помощь
Консервативная терапия
Консервативное стационарное лечение требует введения антибиотиков, стероидных гормонов, холинолитиков, спазмолитиков. На поздних этапах рекомендованы гемостатические средства. Обезболивание осуществляют с применением наркотиков или нейролептанальгезии (фентанил и дроперидол). Необходима объемная инфузионная терапия, предназначенная для восстановления ОЦК, удаления продуктов гемолиза, коррекции гематокрита. Используются коллоидные и солевые растворы (до 10 литров/сутки). Далее выполняются вливания диуретиков. При повреждении почек показан гемодиализ.
При наличии симптомов газовой эмболии проводится гипербарическая оксигенация. Продолжительность сеанса — 45 минут, курс — 5-12 процедур. Давление составляет 2-3 атмосферы. Возможна управляемая гипотермия, при которой тело пациента охлаждают до 34° C. Метод способствует улучшению растворимости газов крови. Помимо сказанного назначается стандартная терапия, которая зависит от вида поражения: сердечные ЛС при окклюзии коронарных сосудов, ноотропные — при ишемическом инсульте.
Хирургическое лечение
Пищеводные и желудочные кровотечения устраняются эндоскопическим путем. С помощью манипулятора, оснащенного иглой и видеокамерой, место повреждения обкалывают раствором адреналина с антибиотиками, восстанавливают целостность слизистой оболочки специальным синтетическим клеем или прижигают лазером. Массивное разрушение тканей требует открытой оперативной реконструкции. После заживления ожогов больному может быть показано бужирование пищевода, поскольку рубцы способствуют формированию стриктур. Удаление газовых эмболов осуществляется путем аспирации катетером.
Реабилитация
Восстановительные мероприятия проводятся как в условиях стационара, так и при амбулаторном долечивании пострадавшего. Срок госпитализации при легких ожогах составляет 10 суток, при средних — 20 суток. Тяжелые повреждения требуют пребывания в ЛПУ до 1-2 месяцев. Полный курс реабилитации может достигать 2-4 месяцев. Основным условием является соблюдение диеты. Первую неделю применяется стол №1а по Певзнеру. Далее пациент получает пищу, соответствующую диете №1 или 1б.
На протяжении 1-2 дней с момента получения травмы рекомендован голод или парентеральное питание. Затем больному дают жидкие блюда: бульон, молоко, кисель. Еда должна быть охлажденной. Позднее допускается потребление яиц всмятку, творога, протертого мяса. Через 2-4 недели разрешено есть слизистые супы, каши из мягких круп. Запрещены консервы, хлеб, цельный отварной и жареный картофель, чипсы, твердые сыры, кусковое мясо. Необходим полный отказ от употребления спиртных напитков. Чай и кофе разрешены только в охлажденном до комнатной температуры виде.
Прогноз и профилактика
Прогноз благоприятный при отсутствии газовой эмболии, поверхностных ожогах рта и пищевода. Выживаемость близка к 100%. Глубокие химические травмы ЖКТ в 8-10% случаев провоцируют развитие осложнений, несовместимых с жизнью. Летальность при закупорке кровеносных сосудов зависит от органа, подвергшегося ишемии, и объема поврежденных тканей. Трансмуральные инфаркты приводят к гибели пациента в 40-50% случаев, ОИМ небольшого размера завершаются смертью в 3-5% ситуаций. Эмболия крупных легочных сосудов также имеет высокую летальность.
Чтобы предотвратить отравление перекисью водорода, следует хранить медикамент в закрытых шкафах, недоступных детям и пожилым людям. Недопустимо переливать средство в емкости из-под питьевой воды, лимонадов, алкоголя. Люди, страдающие психическими заболеваниями, не должны оставаться дома одни. Перед обработкой ран необходимо проверить концентрацию используемого препарата. Введение перекиси в вену не допускается. Следует помнить, что подобные методы оксигенации не относятся к классической доказательной медицине.
Свободнорадикальное окисление и сердечно-сосудистая патология: коррекция антиоксидантами
В основе ведущих метаболических процессов человека лежат окислительно-восстановительные реакции. Среди них особую роль играют свободнорадикальные реакции, при которых в результате метаболических процессов образуются перекисные соединения. Инициатором обр
В основе ведущих метаболических процессов человека лежат окислительно-восстановительные реакции. Среди них особую роль играют свободнорадикальные реакции, при которых в результате метаболических процессов образуются перекисные соединения. Инициатором образования таких соединений обычно являются свободные радикалы — молекулы или фрагменты молекул, имеющие в одном из атомов кислорода неспаренный электрон. Активные формы кислорода чаще всего представлены супероксидным (О2 о ) и гидроксипероксидным (НО2 о ) радикалами.
Одним из основных субстратов для свободнорадикальных реакций служат липиды, в первую очередь молекулы полиненасыщенных жирных кислот (ЖК), липидные компоненты липопротеидов низкой и очень низкой плотности (ЛОНП и ЛНП). В результате окисления ЖК образуются гидроперекиси (диеновые конъюгаты), которые затем метаболизируются во вторичные — малоновый диальдегид (МДА) и третичные продукты перекисного окисления липидов (ПОЛ) — шиффовы основания. Процессы ПОЛ протекают во всех клетках, однако наиболее мощным генератором свободных радикалов служат лейкоциты и тромбоциты, а также гепатоциты [3].
Физиологическая роль свободных радикалов достаточно велика. Большая часть свободных радикалов генерируются фагоцитами, Т-лимфоцитами при воспалительных реакциях и выполняют защитную роль, лизируя патогенные микроорганизмы, мутировавшие (раковые) клетки. Свободнорадикальные процессы лежат в основе синтеза циклических и алифатических гидроперекисей, служащих интермедиаторами ферментативного синтеза простагландинов и лейкотриенов. Важнейшую физиологическую роль выполняет генерируемый в эндотелии сосудов оксид азота NO (эндотелий-зависимый релаксирующий фактор), обеспечивающий расслабление гладкой мускулатуры сосудистой стенки и регулирующий уровень артериального давления, коронарный и органный кровоток, а также предотвращающий агрегацию тромбоцитов.
Сами по себе свободные радикалы, перекиси крайне токсичны. Они окисляют фосфолипиды и белки клеточных мембран, нарушая их целостность, инактивируют клеточные и мембранные ферменты.
В противовес свободнорадикальным процессам в организме существует антиоксидантая система, представленная в первую очередь системой антиоксидантных ферментов: супероксиддимутазой (СОД), связывающей активные формы кислорода с образованием перекиси водорода; каталазой, деструктирующей перекиси в липидные гидропероксиды, глютатионпероксидазой (ГПО), редуцирующей липидные гидропероксиды за счет окисления глютатиона, глютатионредуктазой, восстанавливающей глютатион путем окисления НАДФН, последний восстанавливается через цитохромную цепь и систему природных антиоксидантов — α-токоферол, аскорбиновая кислота, флавоноиды.
Таким образом, про- и антиоксидантная системы находятся в состоянии динамического равновесия, что поддерживается определенной организацией плазменных и клеточных липидов, динамической системой обмена мембранных фосфолипидов и холестерина, определяющих исходный уровень жесткости и окисляемости клеточных мембран.
Чрезмерная активация свободнорадикальных процессов влечет за собой целый каскад негативных реакций и патологических процессов, лежащих в основе ряда заболеваний. Среди наиболее изученных на сегодняшний день свободнорадикальных патологий являются атеросклероз, ишемическая болезнь сердца, артериальная гипертония, в развитии которых большое значение приобретает неконтролируемая генерация пероксидов. Исходная активация свободнорадикальных процессов при атеросклерозе обусловлена снижением активности естественных антиоксидантных ферментов и дефицитом природных антиоксидантов, а также наличием дислипидемии, при которой содержащиеся в высокой концентрации в крови атерогенные липиды служат легким субстратом для перекисного окисления.
В последнее время, говоря о механизмах атерогенеза, многие авторы придают большое значение перекисной модификации липопротеидов низкой плотности (ЛНП) — липидно-белковых комплексов, обеспечивающих транспорт холестерина в эндотелиальные клетки. У модифицированных липопротеидов низкой плотности замедляется катаболизм, что становится причиной развития дислипидемии. Они приобретают способность быстрее связываться с эндотелиальными рецепторами и транспортировать в эндотелий больше холестерина. Накопление в эндотелиальных клетках перекисно модифицированных ЛП, в состав которых входит окисленный ХС, а также хемотаксическое действие тромбина и ряда других факторов свертывания, активированных липопероксидами, стимулируют миграцию в эндотелий из кровяного русла моноцитов и захват холестерина. Проникшие через межклеточные пространства макрофаги начинают интенсивно захватывать модифицированные ЛП, при этом модифицированные ЛП захватываются в десятки раз быстрее, чем обычные. Пересыщенные ХС макрофаги превращаются в пенистые клетки, подавляющая часть которых быстро погибает, в результате чего в интиму изливается накопленный ЭХС, НЭХС, кристаллы моногидрата ХС, формируется липидная инфильтрация артериальной стенки. Гибели пенистых клеток способствуют перекиси, нарушающие структурную целостность клеточной и плазматических мембран. Накопившиеся в интиме липопероксиды, ХС, тромбоцитарные и фибробластные факторы роста стимулируют миграцию гладкомышечных клеток из медии с последующей их пролиферацией, что в итоге приводит к формированию атеросклеротической бляшки. Доказательством главенствующей роли перекисно модифицированных ЛНП в развитии атеросклероза служит тот факт, что в экспериментальных работах на культуре клеток in vitro инактивация окисления ЛНП с помощью природных или синтетических антиоксидантов предотвращала миграцию макрофагов в интиму, задерживала формирование атеросклеротической бляшки. Применение антиоксидантов (пробукола) у кроликов линии Watanabe с гиперхолестеринемией также препятствовало развитию атеросклероза, при этом ПОЛ инактивировалось как в гепатоцитах, так и в интиме сосудов. У больных атеросклерозом применение антиоксиданта пробукола предотвращало развитие рестенозов после ангиопластики [3].
При стенокардии активация перекисных процессов обусловлена частыми ангинальными приступами, вызывающими гиперкатехоламинемию, стимулирующую липолиз, в результате которого увеличивается содержание свободных жирных кислот, являющихся доступным субстратом для окисления. При гипоксии (ишемии) миокарда окислительные процессы в митохондриях кардиомиоцитов нарушаются (как бы не доходят до конца), в результате чего накапливаются промежуточные метаболиты цикла Кребса, крайне легко подверженные восстановлению с образованием свободных радикалов и перекисных соединений, угнетающих систему антиоксидантной защиты. В конечном итоге создается парадоксальная ситуация — уменьшение кислорода в клетке приводит к увеличению кислородных радикалов. Развивающаяся после каждого эпизода транзиторной ишемии реперфузия миокарда также сопровождается значительной активацией (в сотни раз) свободнорадикальных процессов и выбросом липопероксидов в кровоток. Выраженная активация процессов свободнорадикального окисления и следующая за ним реакция тканей и систем организма получили название оксидативного стресса.
Активация свободнорадикальных процессов при артериальной гипертензии ведет к уменьшению синтеза эндогенного NO, связывает NO при реакции липидными радикалами, тем самым снижает эндотелий-зависимую вазодилатацию, уменьшает эффективность многих классов гипотензивных препаратов, так как они реализуют свою фармакологическую активность через систему эндогенного NO.
Одна из популярных в настоящее время гипотез старения основана на положении о накоплении клеточных повреждений, вызванных воздействием свободных радикалов, что косвенно подтверждается угасанием активности антиоксидантной системы организма с возрастом.
Как показали клинико-экспериментальные исследования, проведенные за последние 10 лет в этой области, коррекция прооксидантных нарушений в проантиоксидантной системе при атеросклерозе, различных формах ишемической болезни сердца, артериальной гипертонии значительно улучшает клиническое течение нестабильной стенокардии, инфаркта миокарда, артериальной гипертензии, уменьшает прогрессирование атеросклероза.
Основной группой препаратов, способной противостоять оксидативному стрессу, являются антиоксидантные средства, инактивирующие свободные радикалы и препятствующие их образованию, участвующие в восстановлении антиоксидантов, или препараты, обладающие опосредованной антиоксидантной активностью. Последние непосредственно не являются антиоксидантами, но способны либо активировать антиоксидантную систему, либо повышать эффективность природных антиоксидантов, либо препятствовать окислению потенциальных субстратов.
Как указывалось выше, система антиоксидантной защиты имеет несколько «эшелонов обороны» и включает целый комплекс ферментативных систем и природных соединений, позволяющих утилизировать свободные радикалы, предотвратив их негативное воздействие на организм. Однако терапевтическое использование таких соединений на практике для лечения пациентов во многих случаях нереально либо по причине их нестойкости, либо из-за того, что они не усваиваются организмом. Кроме того, некоторые антиоксиданты идеально эффективны в биохимическом плане как утилизаторы пероксидов в экспериментах in vitro, но при парентеральном или пероральном применении вызывают серьезные побочные эффекты, исключающие их применение в клинической практике.
Недостаточная популярность антиоксидантных средств и отсутствие традиций их широкого применения в практической медицине обусловлены рядом причин: недостаточной изученностью этого вопроса, сложностью адекватной оценки состояния параметров перекисного окисления в организме, отсутствием эффективных медикаментозных средств, обладающих антиоксидантной активностью и способных быстро уменьшить последствия оксидативного стресса.
К сожалению, в настоящее время не существует общепринятой классификации антиоксидантных препаратов. Как правило, антиоксиданты разделяют на природные и синтетические. К природным антиоксидантам относятся α-токоферол (витамин Е), β-каротин. Их применение уменьшает риск развития и прогрессирования атеросклероза, несколько снижает высокий уровень липопероксидов в крови больных хроническими формами ИБС, артериальной гипертонии. Однако для достижения эффекта их применение должно быть достаточно долгим (месяцы), в связи с чем указанные средства представляют интерес только в качестве профилактических препаратов.
Определенными антиоксидантными свойствами обладает аскорбиновая кислота. Она способна восстанавливать окисленные α-токоферольные радикалы, возвращая α-токоферолу его антиоксидантные свойства, а также непосредственно связывать супероксидионы и активные радикалы. Однако ее антиоксидантная активность невелика и проявляется лишь в малых концентрациях. В высоких концентрациях она выступает как прооксидант. Указанные свойства аскорбиновой кислоты позволяют использовать ее преимущественно как профилактическое средство.
В последние годы довольно активно стали использоваться в качестве пищевых добавок или в составе витаминных комплексов ионы металлов с переменной валентностью (селен, марганец, медь, цинк), которые входят в состав активных центров ряда природных антиоксидантных ферментов (супероксиддисмутаз) и потому способны существенно увеличивать их активность. Особую значимость использование таких препаратов приобретает в географических зонах с низким содержанием указанных элементов в воде и пище.
К другим природным антиоксидантным соединениям относятся флавоноиды, в большом количестве содержащиеся в виноградных косточках, ягодах черники, листьях гинкго билобы, сухом красном вине. Флавоноиды тормозят свободнорадикальные процессы на уровне инициации, взаимодействуя с активными радикалами. Однако в настоящее время доказана их эффективность только in vitro, убедительных данных о доминирующей антиоксидантной активности флавоноидов in vivo пока не получено.
Определенную антиоксидантную активность имеют SH-содержащие аминокислоты (цистеин, цистин, метионин), при этом SH-группы выступают как конкурирующие с другими субстратами объекты окисления, не дающие свободных радикалов и фактически гасящие цепную реакцию свободнорадикального окисления. SH-содержащие соединения способны пролонгировать продолжительность «жизни» молекулы NO. Однако терапевтическое применение соединений, содержащих SH-группы (глютатион, тиоловая кислота, N-ацетилцистеин), ограничивается из-за невысокой их проницаемости через цитоплазматические мембраны, где они могут являться защитниками от внутриклеточного оксидативного стресса, а также из-за способности активировать перекисные реакции во внеклеточной среде.
Умеренной антиоксидантной активностью обладают женские половые гормоны (эстрадиол, эстрагон, эстриол), чем, вероятно, обусловлена нераспространенность атеросклероза у женщин в детородном возрасте. Описана опосредованная антиоксидантная активность у мелатонина. Однако клиническое использование гормональных средств в качестве антиоксидантов представляется весьма проблематичным.
В последние годы предпринимаются небезуспешные попытки клинического использования коэнзима Q (убихинона) — одного из самых распространенных соединений в клетках бактерий и животных, сходного по химической структуре с α-токоферолом. Однако возможности, которыми обладает коэнзим Q, и целесообразность его применения служат в настоящее время предметом изучения.
Большой интерес представляют в клиническом плане синтетические антиоксиданты или препараты, обладающие антиоксидантной активностью. Наибольшей эффективностью, отсутствием токсичности и минимальными побочными эффектами характеризуются производные 3-оксипиридина — эмоксипин, мексикор. Эмоксипин является, пожалуй, одним из первых синтетических антиоксидантных средств, вошедших в широкую клиническую практику. Опыт применения раствора эмоксипина у больных с острым инфарктом миокарда на фоне традиционной терапии показал, что препарат существенно улучшал клиническое течение болезни, снижал частоту фатальных осложнений, увеличивал выживаемость больных в острый и подострый период инфаркта.
Мексикор, сходный с эмоксипином по механизмам действия, обладает значительно большей антиоксидантной активностью, выпускается в разрешенной к клиническому применению капсулированной (для перорального приема) и водорастворимой инъекционной форме для парентерального введения. Это позволяет использовать препарат в любых фазах инфаркта и при нестабильной стенокардии, а также сохранить преемственность терапии, переходя с инъекционных форм (на острой стадии болезни) на капсулированную форму (в последующий подострый период или период стабилизации).
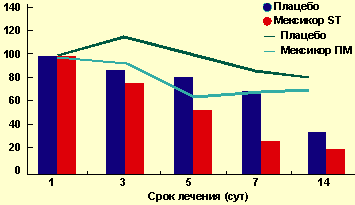
Рандомизированное плацебо-контролируемое исследование мексикора у больных с нестабильной стенокардией показало, что пероральное применение препарата в дозе 6 мг/кг/сут на фоне комплексной традиционной терапии антикоагулянтами, антиагрегантами и антиангинальными средствами, в сравнении с контрольной группой, значительно ускоряло стабилизацию стенокардии, снижало частоту и продолжительность периодов ишемии, а также суммарный интеграл суточного смещения сегмента ST (рисунок 1) и, кроме того, сокращало частоту желудочковых нарушений ритма по результатам холтеровского мониторирования. Указанные изменения сопровождались быстрой нормализацией концентрации продуктов перекисного окисления липидов в крови.
| Рисунок 1. Изменения интеграла смещения ST и отношения болевых/безболевых периодов ишемии у больных нестабильной стенокардией на фоне терапии мексикором. |
 |
Как показали экспериментальные исследования на изолированных сегментах артерий собак, мексикор существенно усиливал вазодилатирующие эффекты нитроглицерина, а при экспериментальной модели окклюзионного инфаркта миокарда у собак повышал объемную скорость коронарного кровотока, сохраняя положительное действие на его фазовую структуру.
Клинические исследования подтверждают способность мексикора увеличивать антиангинальную эффективность пролонгированных нитратов у больных стабильной стенокардией II—III функционального класса: применение мексикора в дозе 0,3-0,4 г/сут. в течение двух месяцев на фоне неизменной дозы пролонгированных нитратов позволило повысить пороговую мощность при велоэргометрическом тесте через один месяц (рисунок 2).
| Рисунок 2. Изменения величины пороговой мощности ВЭМ на фоне терапии мексикором и нитратами больных стабильной стенокардией. |
 |
Открытое рандомизированное исследование инъекционной формы мексикора (6 мг/кг/сут в течение двух недель с последующим переходом на капсулированную форму до одного месяца) у больных острым инфарктом миокарда показало, что мексикор существенно ускорял, в сравнении с контролем, восстановление диастолической функции левого желудочка (оценка производилась по параметрам трансмитрального потока). Мексикор улучшал сегментарную сократимость левого желудочка, ускоряя переход отдельных сегментов миокарда левого желудочка в периинфарктной зоне из состояния акинеза в гипокинез, гипокинеза — в нормокинез (рисунок 3).
| Рисунок 3. Число зон акинезии у больных острым инфарктом на фоне терапии мексикором. |
 |
Мексикор уменьшал частоту и продолжительность эпизодов желудочковых аритмий в острый период инфаркта, а также существенно ускорял нормализацию содержания липопероксидов в крови. Применение мексикора улучшало клиническое течение инфаркта, снижало частоту пролонгированного и рецидивирующего течения болезни, достоверно уменьшало госпитальную и отдаленную (в течение шести месяцев) летальность.
Клиническое использование мексикора в комплексной терапии артериальной гипертонии с кризовым течением позволяет сократить сроки стабилизации давления, уменьшить частоту рецидивирования кризов на постгоспитальном этапе, повысить эффективность гипотензивной терапии.
Преимущество мексикора как средства выбора при лечении острой сердечно-сосудистой патологии, наряду с высокой эффективностью, обусловлено наличием парентеральной формы препарата, применение которой позволяет быстро создать терапевтическую концентрацию и получить клинический эффект.
Определенной опосредованной антиоксидантной активностью обладают некоторые гипохолестеринемические препараты — статины (симвастатин), противоишемический препарат триметазидин, некоторые ингибиторы АПФ, а также β-адреноблокаторы. Механизм действия последних обусловлен ограничением катехоламинемии, снижением интенсивности липолиза и уменьшением содержания в крови легко окисляемых свободных жирных кислот. Однако позитивные антиоксидантные эффекты указанных средств, хотя и позволяют отдать им предпочтение при выборе лекарств у больных с атеросклерозом и артериальной гипертонией, все же являются второстепенными, что следует учитывать при назначении этих лекарственных средств по основным показаниям.
Пробукол долгое время считался перспективным антиоксидантным препаратом, однако отсутствие инъекционной формы, позднее развитие антиоксидантного эффекта (месяцы), наличие осложнений (удлинение интервала QT) не позволили использовать этот препарат достаточно широко.
Следует также помнить, что позитивная фармакодинамика кардиопротективных и противоишемических лекарственных средств (триметазидин, милдронат) лишь в некоторой степени связана с подавлением в ишемизированных тканях свободнорадикальных процессов, все-таки основной точкой приложения этих препаратов является оптимизация клеточного энергетического обмена, уменьшение потребности ишемизированной ткани в кислороде.
Таким образом, имеющийся на сегодняшний день клинический опыт и результаты экспериментальных исследований свидетельствуют о важной роли оксидативного стресса в формировании и прогрессировании сердечно-сосудистой патологии и необходимости его ранней, планомерной и комплексной антиоксидантной коррекции.
Литература
А. П. Голиков, доктор медицинских наук, профессор, академик РАМН
С. А. Бойцов, доктор медицинских наук, профессор
В. П. Михин, доктор медицинских наук, профессор
В. Ю. Полумисков, кандидат медицинских наук, доцент
НИИ СП им. Н. В. Склифосовского, Государственный медицинский центр, Медицинский центр УД Президента РФ (Москва), Курский ГМУ


